Kovalent bağ, ametaller arasında elektron ortaklaşması ile oluşan bir kimyasal... Daha fazla göster
TYT Kimya - Lewis Yapısı ve Kimyasal Türler Arası Etkileşimler

Kovalent Bağın Temel Yapısı
Kovalent bağ, ametal atomları (H, C, N, O, F, Cl, Br, I, P, S, Se) arasında elektronların ortaklaşa kullanılmasıyla oluşur. Bu ortaklaşma sayesinde atomlar kararlı hale gelir ve molekülleri oluşturur.
Ortaklaşa kullanılan elektron çiftlerine bağlayıcı elektron çifti veya ortaklanmış elektron çifti adı verilir. Örneğin, H + H → H:H tepkimesinde, iki hidrojen atomu bir elektron çifti paylaşır. Bağ oluşumuna katılmayan elektronlar ise ortaklanmamış elektron çiftleri olarak adlandırılır.
Kovalent bağlar, molekül formüllerinde çizgi (-) ile gösterilir. Örneğin H-Cl bağında, elektronlar iki atom arasında paylaşılır. Kovalent bağlar temelde iki tipe ayrılır: Polar kovalent bağ ve apolar kovalent bağ.
⚠️ Dikkat: Polar kovalent bağda elektronlar eşit paylaşılmaz ve atomların birinde kısmi (+δ), diğerinde kısmi (-δ) yük oluşur. H-Cl bağında, elektronlar Cl tarafına daha fazla çekilir.
Polar kovalent bağ, farklı tür ametal atomları arasında oluşur (HCl, H₂O, BH₃, NH₃, CH₄, CO₂ gibi). Apolar kovalent bağ ise aynı tür ametal atomları arasında oluşur (H₂, N₂, O₂, Cl₂ gibi).
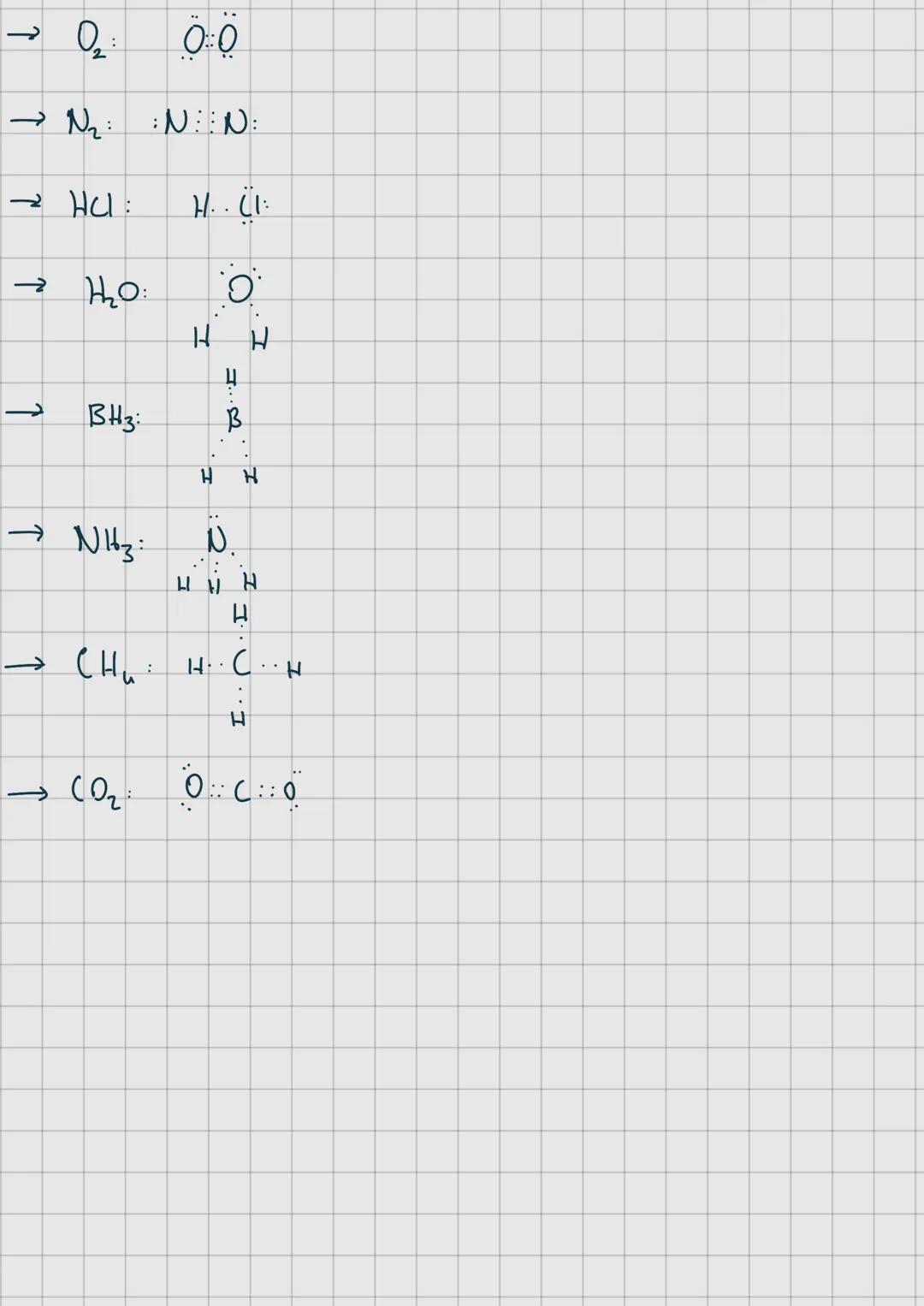
Moleküllerin Lewis Yapıları
Moleküllerin kimyasal davranışını anlamak için Lewis yapıları çok önemlidir. Bu yapılar, moleküldeki atomlar arasındaki bağları ve ortaklanmamış elektron çiftlerini gösterir.
Diatomik moleküllerde (iki atomlu) Lewis yapısı çizimi oldukça basittir. Örneğin, O₂ molekülünde iki oksijen atomu arasında çift bağ (O::O) bulunur. N₂ molekülünde ise üç bağ (N:::N) vardır. Bu şekilde, aynı tür atomlar arasındaki bağlar apolar kovalent bağ olarak adlandırılır.
Farklı atomlu moleküllerde, elektronlar elektronegativitesi yüksek olan atoma doğru kayar. Örneğin HCl'de elektronlar Cl'ye doğru çekilir. Daha karmaşık moleküllerde, merkez atoma bağlanan atomların dizilişi önemlidir. H₂O'da oksijen merkezdedir ve iki hidrojen atomuna bağlıdır. CH₄'te ise karbon merkezdedir ve dört hidrojen atomuna bağlanmıştır.
💡 İpucu: Bir molekülün Lewis yapısını çizerken, önce her atomun değerlik elektronlarını belirleyin, sonra ortak kullanılan elektronları çizerek bağları oluşturun.
CO₂ gibi birden fazla bağ içeren moleküllerde, karbon atomunun oksijen atomlarına çift bağla bağlandığını (O::C::O) görebilirsiniz. Bu yapı, molekülün doğrusal şekilde düzenlendiğini gösterir.
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Lewis Structures
2Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
TYT Kimya - Lewis Yapısı ve Kimyasal Türler Arası Etkileşimler
Kovalent bağ, ametaller arasında elektron ortaklaşması ile oluşan bir kimyasal bağ türüdür. Bu bağlar, elementlerin elektron paylaşarak kararlı yapıya kavuşmasını sağlar. Günlük hayatta karşılaştığımız birçok molekül, kovalent bağlar sayesinde bir arada durur.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Kovalent Bağın Temel Yapısı
Kovalent bağ, ametal atomları (H, C, N, O, F, Cl, Br, I, P, S, Se) arasında elektronların ortaklaşa kullanılmasıyla oluşur. Bu ortaklaşma sayesinde atomlar kararlı hale gelir ve molekülleri oluşturur.
Ortaklaşa kullanılan elektron çiftlerine bağlayıcı elektron çifti veya ortaklanmış elektron çifti adı verilir. Örneğin, H + H → H:H tepkimesinde, iki hidrojen atomu bir elektron çifti paylaşır. Bağ oluşumuna katılmayan elektronlar ise ortaklanmamış elektron çiftleri olarak adlandırılır.
Kovalent bağlar, molekül formüllerinde çizgi (-) ile gösterilir. Örneğin H-Cl bağında, elektronlar iki atom arasında paylaşılır. Kovalent bağlar temelde iki tipe ayrılır: Polar kovalent bağ ve apolar kovalent bağ.
⚠️ Dikkat: Polar kovalent bağda elektronlar eşit paylaşılmaz ve atomların birinde kısmi (+δ), diğerinde kısmi (-δ) yük oluşur. H-Cl bağında, elektronlar Cl tarafına daha fazla çekilir.
Polar kovalent bağ, farklı tür ametal atomları arasında oluşur (HCl, H₂O, BH₃, NH₃, CH₄, CO₂ gibi). Apolar kovalent bağ ise aynı tür ametal atomları arasında oluşur (H₂, N₂, O₂, Cl₂ gibi).
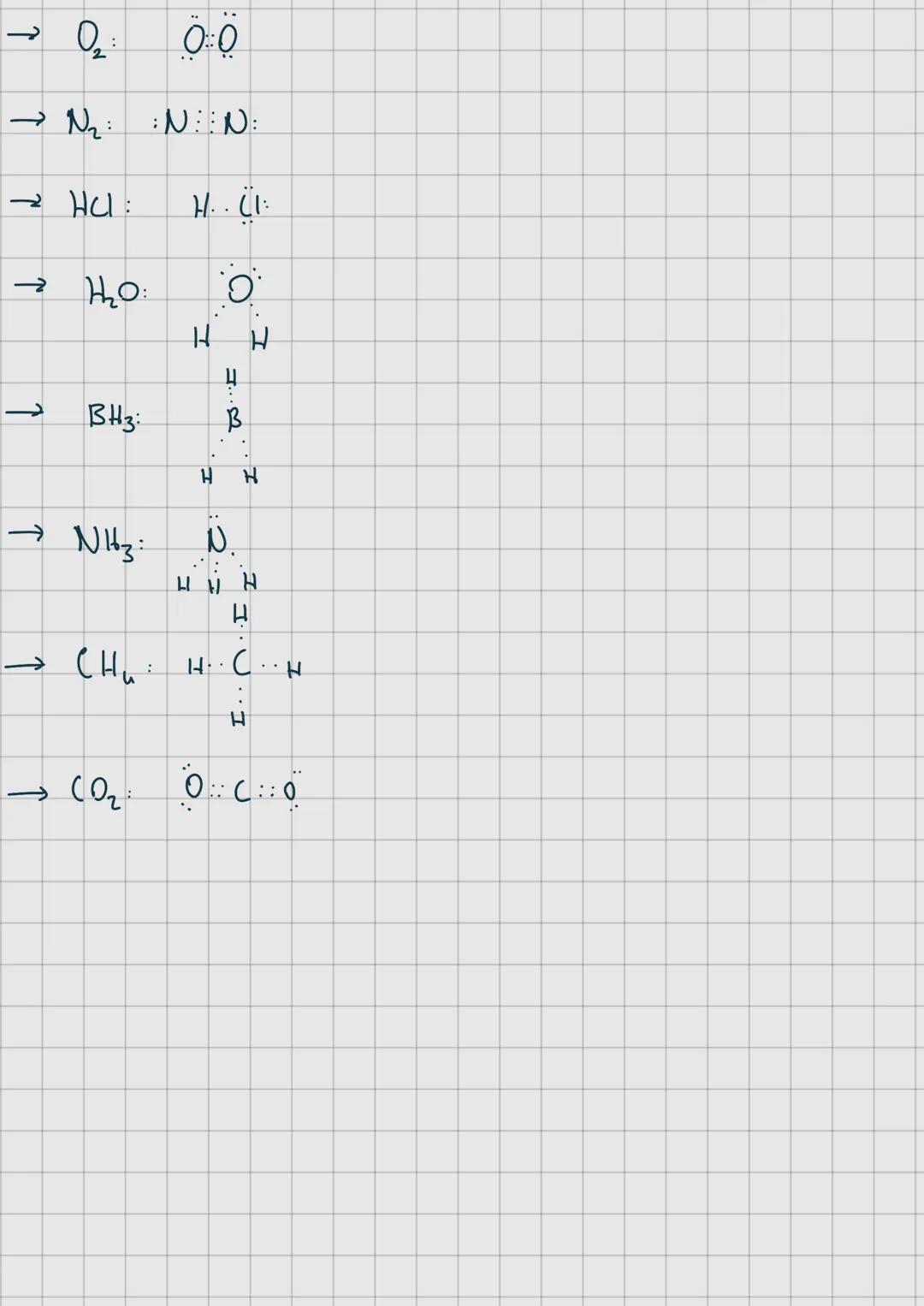
Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Moleküllerin Lewis Yapıları
Moleküllerin kimyasal davranışını anlamak için Lewis yapıları çok önemlidir. Bu yapılar, moleküldeki atomlar arasındaki bağları ve ortaklanmamış elektron çiftlerini gösterir.
Diatomik moleküllerde (iki atomlu) Lewis yapısı çizimi oldukça basittir. Örneğin, O₂ molekülünde iki oksijen atomu arasında çift bağ (O::O) bulunur. N₂ molekülünde ise üç bağ (N:::N) vardır. Bu şekilde, aynı tür atomlar arasındaki bağlar apolar kovalent bağ olarak adlandırılır.
Farklı atomlu moleküllerde, elektronlar elektronegativitesi yüksek olan atoma doğru kayar. Örneğin HCl'de elektronlar Cl'ye doğru çekilir. Daha karmaşık moleküllerde, merkez atoma bağlanan atomların dizilişi önemlidir. H₂O'da oksijen merkezdedir ve iki hidrojen atomuna bağlıdır. CH₄'te ise karbon merkezdedir ve dört hidrojen atomuna bağlanmıştır.
💡 İpucu: Bir molekülün Lewis yapısını çizerken, önce her atomun değerlik elektronlarını belirleyin, sonra ortak kullanılan elektronları çizerek bağları oluşturun.
CO₂ gibi birden fazla bağ içeren moleküllerde, karbon atomunun oksijen atomlarına çift bağla bağlandığını (O::C::O) görebilirsiniz. Bu yapı, molekülün doğrusal şekilde düzenlendiğini gösterir.
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Lewis Structures
2Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅