Kimya, çevremizdeki maddeleri ve değişimleri inceleyen temel bir bilim dalıdır.... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
149
•
Güncellendi May 16, 2026
•
Duru Karaburun
@durukaraburun
Kimya, çevremizdeki maddeleri ve değişimleri inceleyen temel bir bilim dalıdır.... Daha fazla göster






Kimya, sistematik bilgi birikimi içeren ve bilimsel yöntemleri kullanan önemli bir bilim dalıdır. Teorik bilgileriyle hayatımızın neredeyse her alanına dokunur.
Kimya birçok alanda uygulama alanı bulur. Petrokimya, gübre, tekstil, ilaç ve boya üretimi bunların başında gelir. Ayrıca gıda, enerji, temizlik, nanoteknoloji ve madencilik sektörleri de kimya biliminden yararlanır.
Kimyanın ana alt dalları arasında anorganik kimya, organik kimya, analitik kimya, biyokimya, polimer kimyası ve fizikokimya bulunur. Bu alt dallar, farklı madde gruplarını veya özellikleri inceler.
Unutma! Kimya bilgisi, kimyager ve kimya mühendisliği dışında eczacılık, metalurji, malzeme mühendisliği ve kimya öğretmenliği gibi pek çok mesleğin temelini oluşturur.
Kimyasalların temel uyarı özellikleri de bilinmelidir: yanıcı, yakıcı, korozif, patlayıcı, tahriş edici, zehirli (toksik), radyoaktif ve çevreye zararlı özellikler taşıyabilirler. Bu özellikleri tanımak, güvenliğimiz için çok önemlidir!
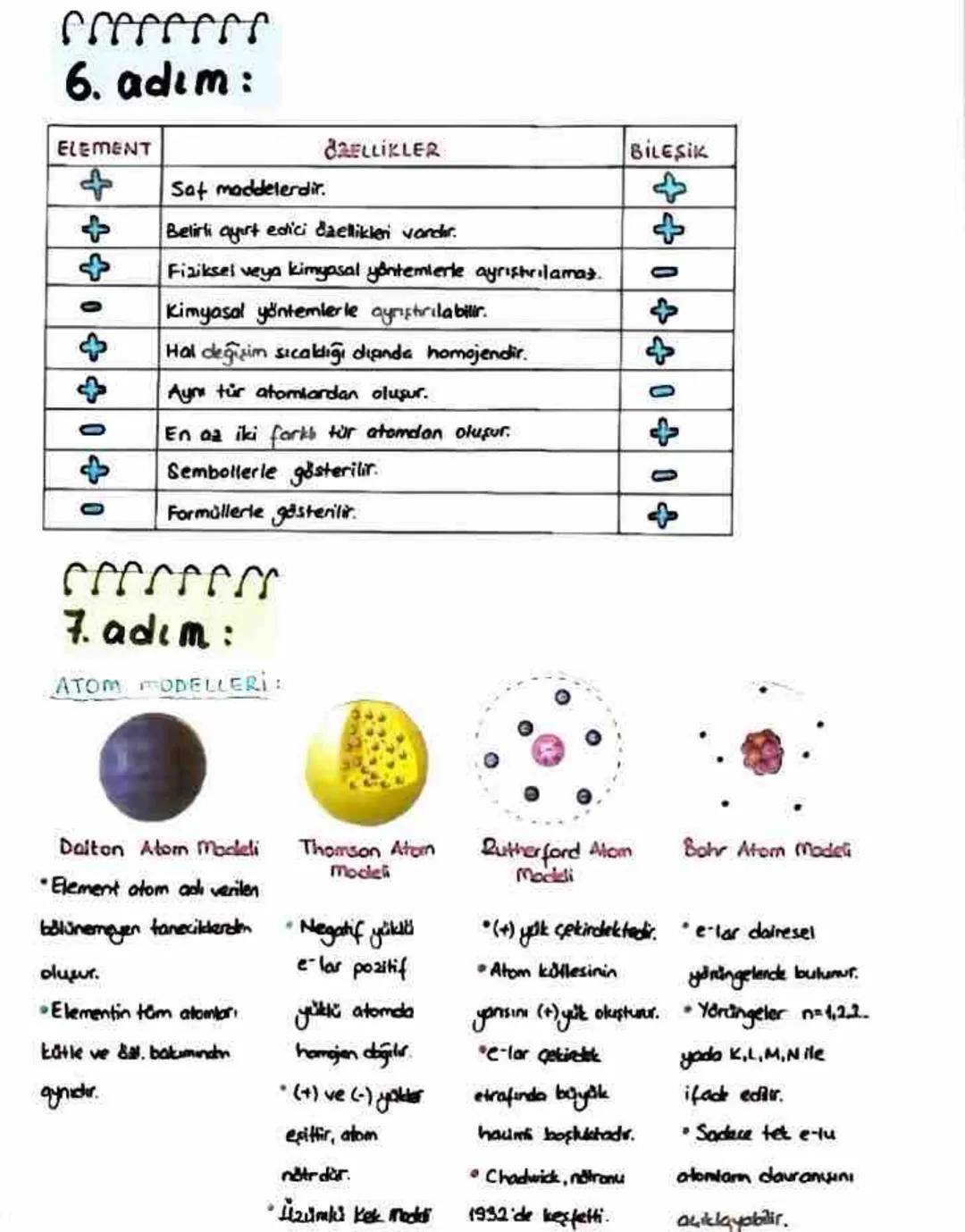
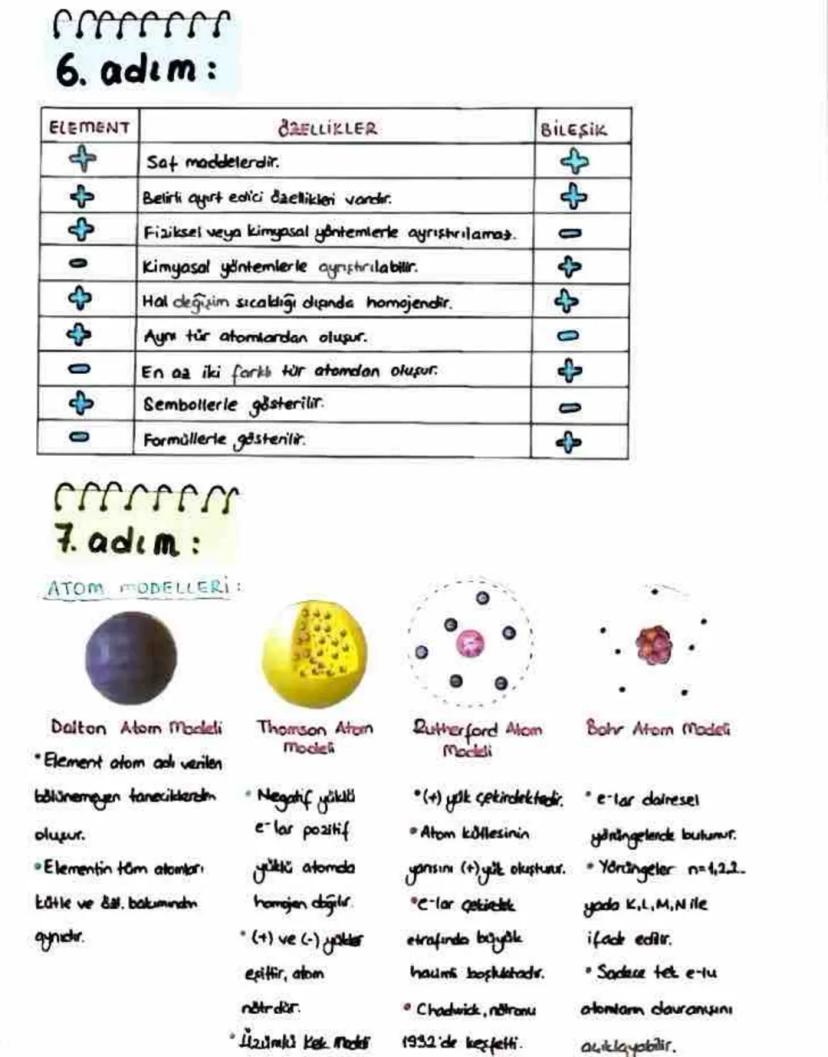
Elementler ve bileşikler arasındaki farkları anlamak kimyanın temelidir. Elementler saf maddelerdir ve aynı tür atomlardan oluşur. Fiziksel veya kimyasal yöntemlerle daha basit maddelere ayrıştırılamazlar ve sembollerle gösterilirler.
Bileşikler ise en az iki farklı tür atomdan oluşur ve formüllerle gösterilirler. Kimyasal yöntemlerle ayrıştırılabilirler. Elementler gibi bileşikler de hal değişim sıcaklığı dışında homojen özellik gösterirler.
Atomun yapısını anlamak için bilim insanları çeşitli modeller geliştirmiştir. Dalton modeli atomu bölünemeyen tanecikler olarak tanımlarken, Thomson modeli atomu pozitif yüklü bir küre içinde negatif elektronların bulunduğu "üzümlü kek" olarak tarif etmiştir.
İlginç bilgi: Rutherford atom modelinde pozitif yük çekirdektedir ve elektronlar çekirdek etrafındaki büyük boşlukta bulunur. Nötronu ise Chadwick 1932'de keşfetmiştir!
Bohr atom modeli elektronların belirli dairesel yörüngelerde bulunduğunu öne sürer. Bu yörüngeler n=1, 2... veya K, L, M, N harfleriyle ifade edilir. Ancak bu model sadece tek elektronlu atomların davranışını açıklayabilmektedir.

Atom kavramını anlamak için "izo" kavramlarını bilmek gerekir. İzotop atomlar proton sayıları aynı, nötron sayıları farklı atomlardır. İzoton atomlar nötron sayıları aynı, atom numaraları farklı atomlardır. İzobar atomlar kütle numaraları aynı, proton sayıları farklı atomlardır. İzoelektron atomlar ise elektron sayıları ve dizilişleri aynı, proton sayıları farklı atomlardır.
Bir atomun kütle numarası nötron ve proton sayılarının toplamına eşittir. Proton sayısı, atom numarasına eşittir ve çekirdek yükünü belirtir. Nötr atomda elektron sayısı proton sayısına eşitken, iyonlarda bu durum değişir.
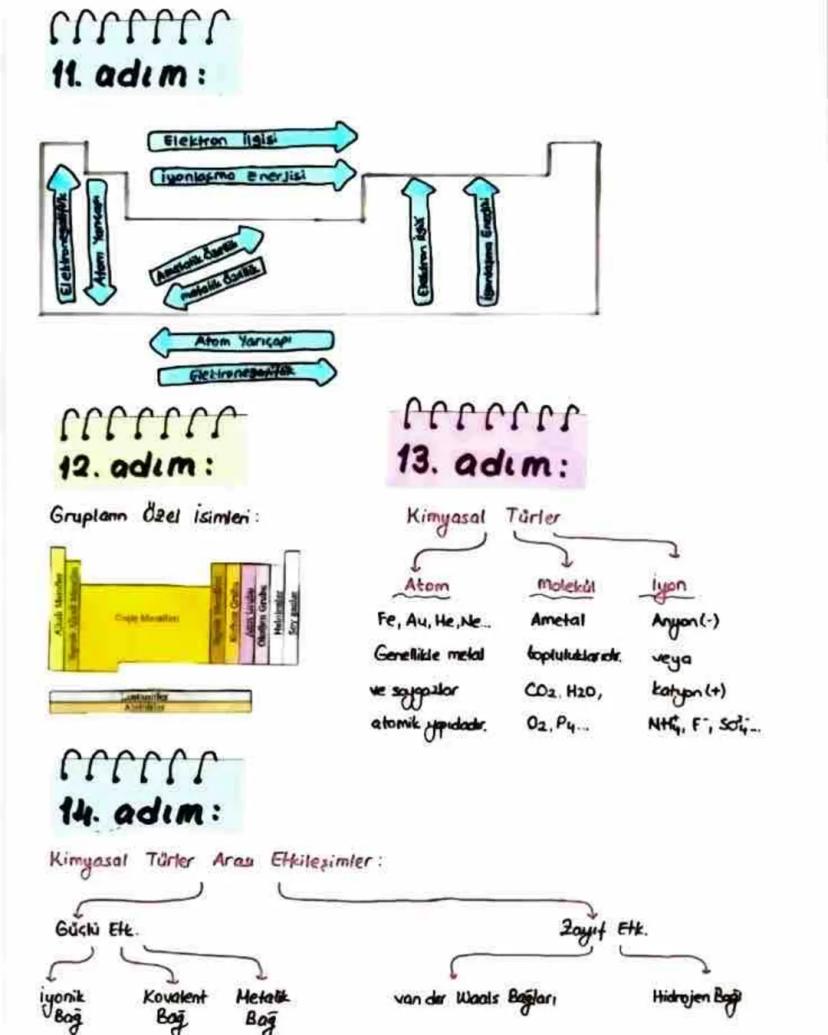
Periyodik özellikler atomların davranışlarını anlamamızı sağlar. Atom yarıçapı genellikle periyotta soldan sağa azalır, grupta yukarıdan aşağı artar. İyonlaşma enerjisi ise periyotta soldan sağa artma eğilimindedir (1A<3A<2A<4A<6A<5A<7A<8A).
Dikkat! Elektronegatiflik, bir atomun bağ elektronlarını kendine çekme yeteneğidir ve periyodik tabloda en yüksek değere sahip element flordur. Elektron ilgisi ise en yüksek olan element klordur.
Atom yarıçapı, elektronegatiflik, iyonlaşma enerjisi ve elektron ilgisi gibi özellikler, periyodik tablodaki elementlerin kimyasal davranışlarını belirler. Bu özellikleri anlamak, kimyasal bağları ve tepkimeleri kavramak için çok önemlidir.
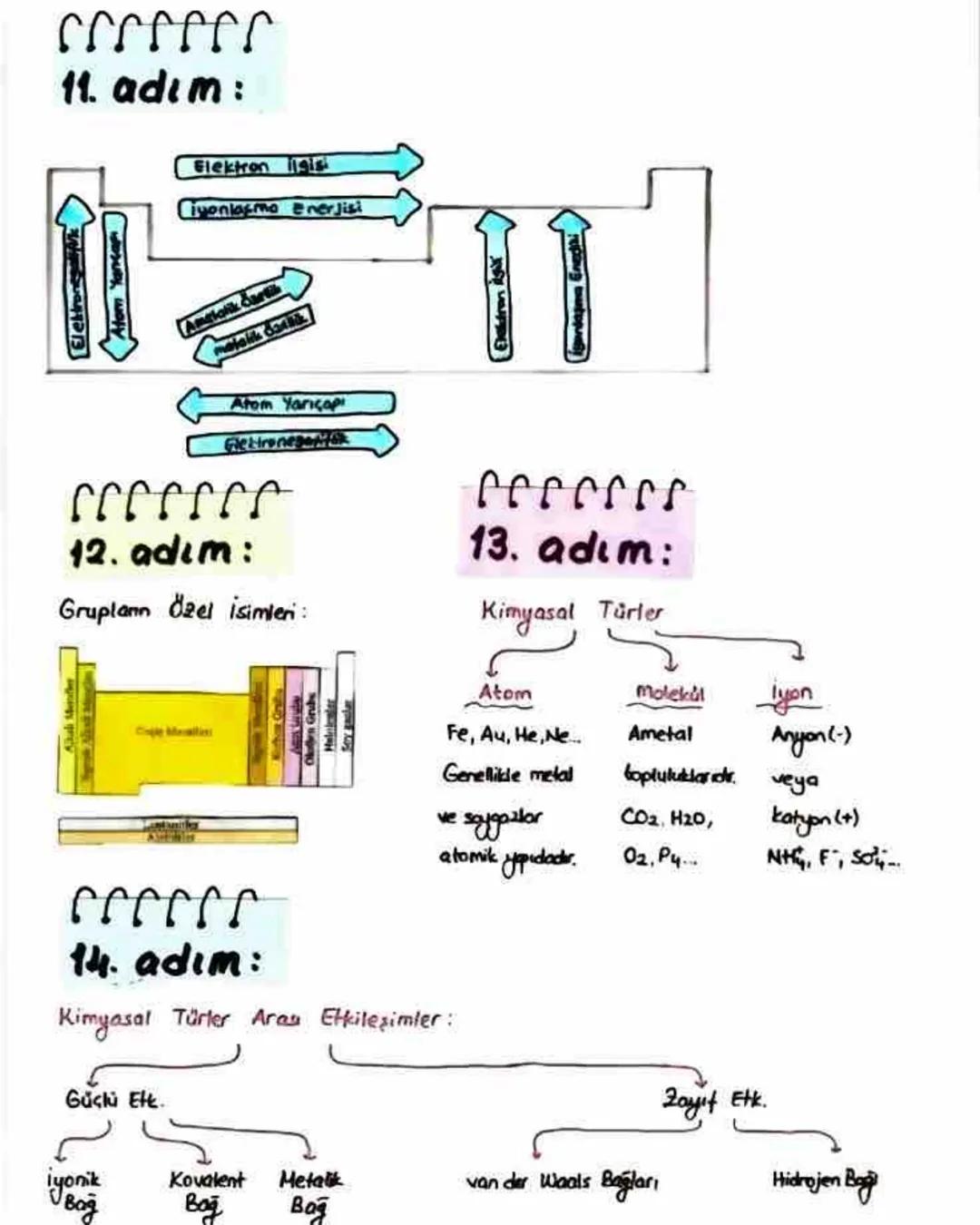
Periyodik tabloda elementlerin gruplarının özel isimleri vardır. Örneğin, 1A grubu alkali metaller, 7A grubu halojenler, 8A grubu ise soy gazlar olarak adlandırılır. Bu gruplardaki elementler benzer özellikler gösterir.
Kimyasal türler başlıca atom, molekül ve iyon olarak sınıflandırılır. Atomlar genellikle metal ve soy gazlardır (Fe, Au, He, Ne). Moleküller ametallerden oluşur (CO₂, H₂O, O₂). İyonlar ise pozitif yüklü katyon (genellikle metal) veya negatif yüklü anyon (genellikle ametal) olabilir.
Kimyasal türler arasındaki etkileşimler güçlü ve zayıf olarak ikiye ayrılır. Güçlü etkileşimler arasında iyonik bağ , kovalent bağ ve metalik bağ yer alır.
Merak et! İyonik bağlar metal ve ametal arasında elektron alışverişiyle oluşurken, kovalent bağlarda elektronlar paylaşılır. Bu fark, maddelerin fiziksel ve kimyasal özelliklerini nasıl etkiliyor?
Zayıf etkileşimler ise van der Waals bağları ve hidrojen bağıdır. Hidrojen bağı, hidrojenin flor, oksijen veya azot atomlarıyla oluşturduğu özel bir etkileşimdir. Bu zayıf etkileşimler, maddelerin hal değişimleri ve çözünürlük gibi özelliklerini belirler.
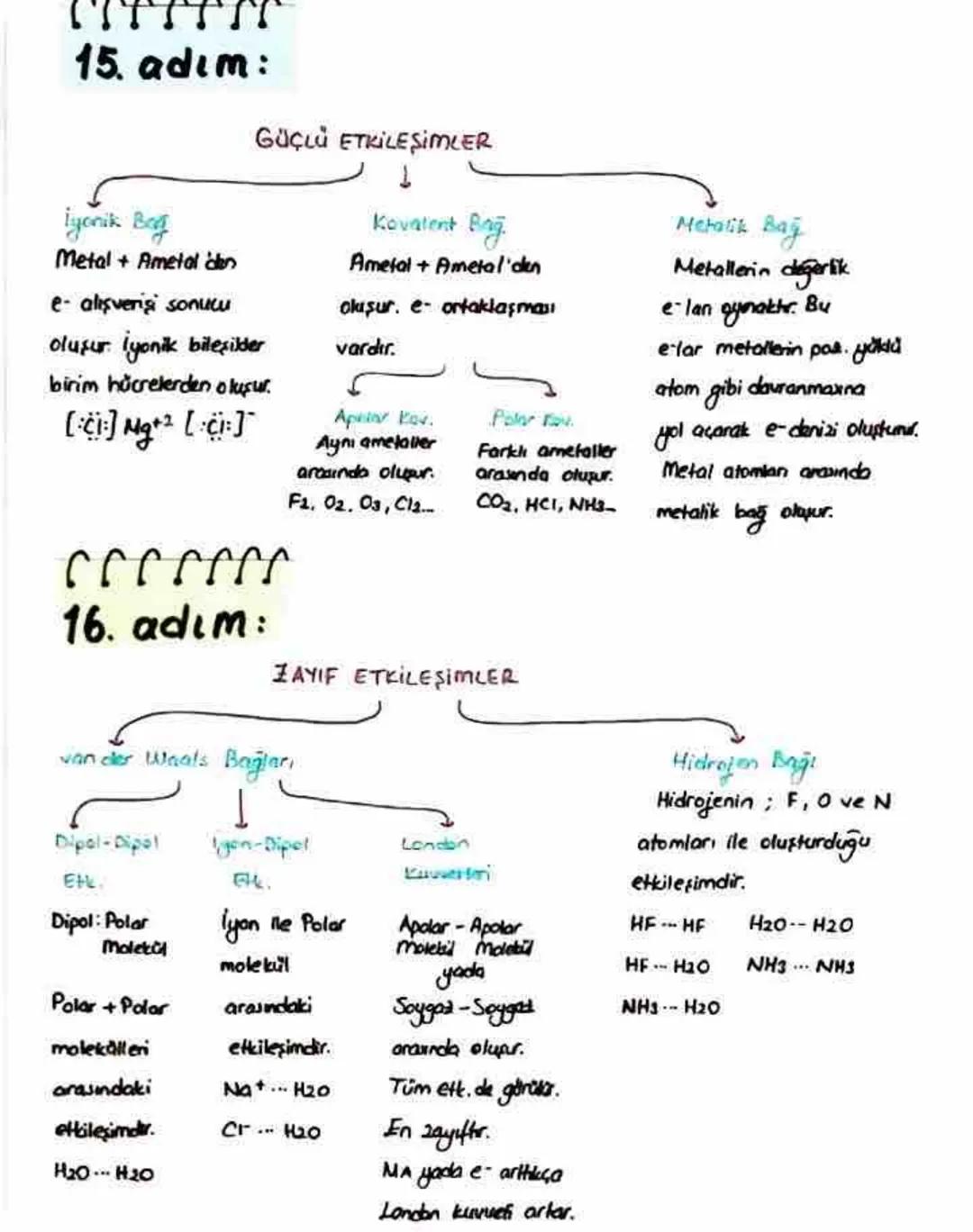
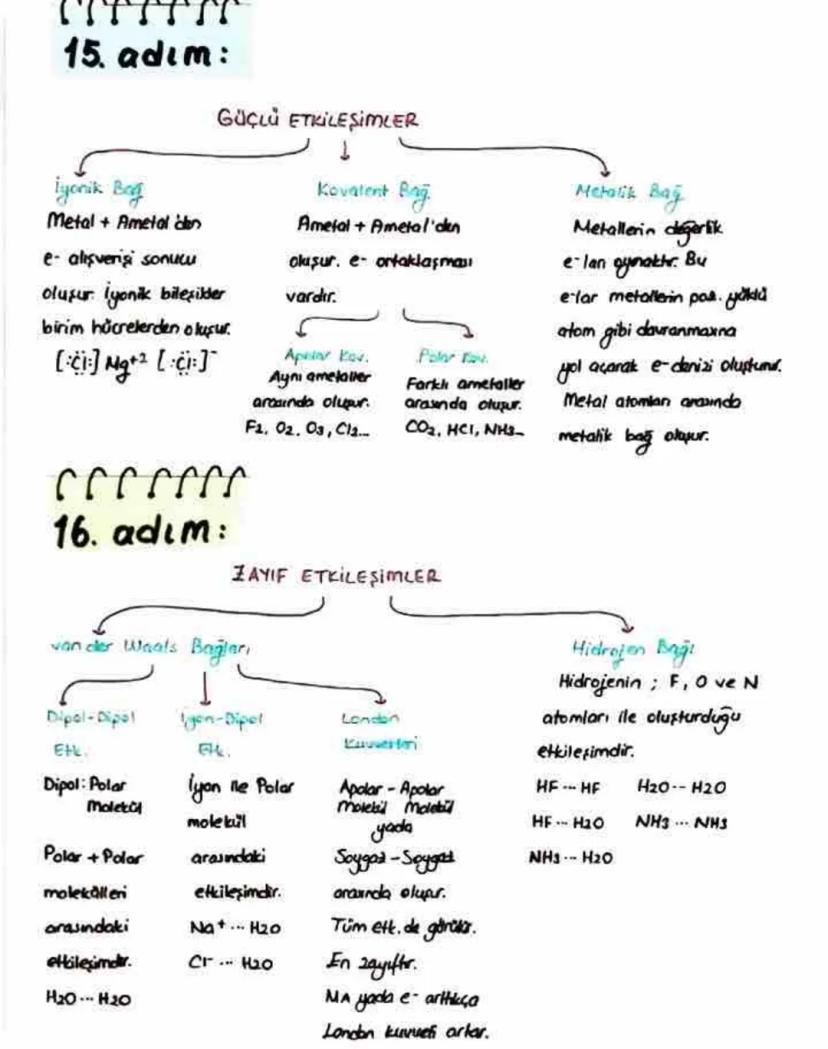
Güçlü etkileşimler maddelerin temel yapı taşlarını bir arada tutar. İyonik bağ metal ve ametal arasında elektron alışverişi sonucu oluşur ve Mg²⁺Cl⁻ gibi iyonik bileşikler birim hücrelerden oluşur.
Kovalent bağ ise ametaller arasında elektron ortaklaşması ile oluşur. Aynı ametaller arasında oluşursa (F₂, O₂, O₃, Cl₂) apolar kovalent bağ, farklı ametaller arasında oluşursa (CO₂, HCl, NH₃) polar kovalent bağ olarak adlandırılır.
Metalik bağ metallerin değerlik elektronlarının serbestçe hareket etmesiyle oluşur. Bu elektronlar adeta bir "elektron denizi" oluşturarak metal atomlarını bir arada tutar. Bu bağ, metallerin elektrik iletkenliği gibi özelliklerini açıklar.
Harika! Su, alkol, DNA gibi birçok önemli molekülde hidrojen bağı bulunur ve bu bağlar maddelerin özelliklerini belirler. Örneğin suyun kaynama noktasının yüksek olması hidrojen bağları sayesindedir!
Zayıf etkileşimler arasında en önemlilerinden biri hidrojen bağıdır. Bu bağ, hidrojen ile F, O veya N atomları arasında oluşur (HF...HF, H₂O...H₂O, NH₃...NH₃). Diğer zayıf etkileşimler arasında dipol-dipol (polar moleküller arasında), iyon-dipol (iyon ile polar molekül arasında) ve tüm etkileşimlerde görülen en zayıf bağ olan London kuvvetleri bulunur.
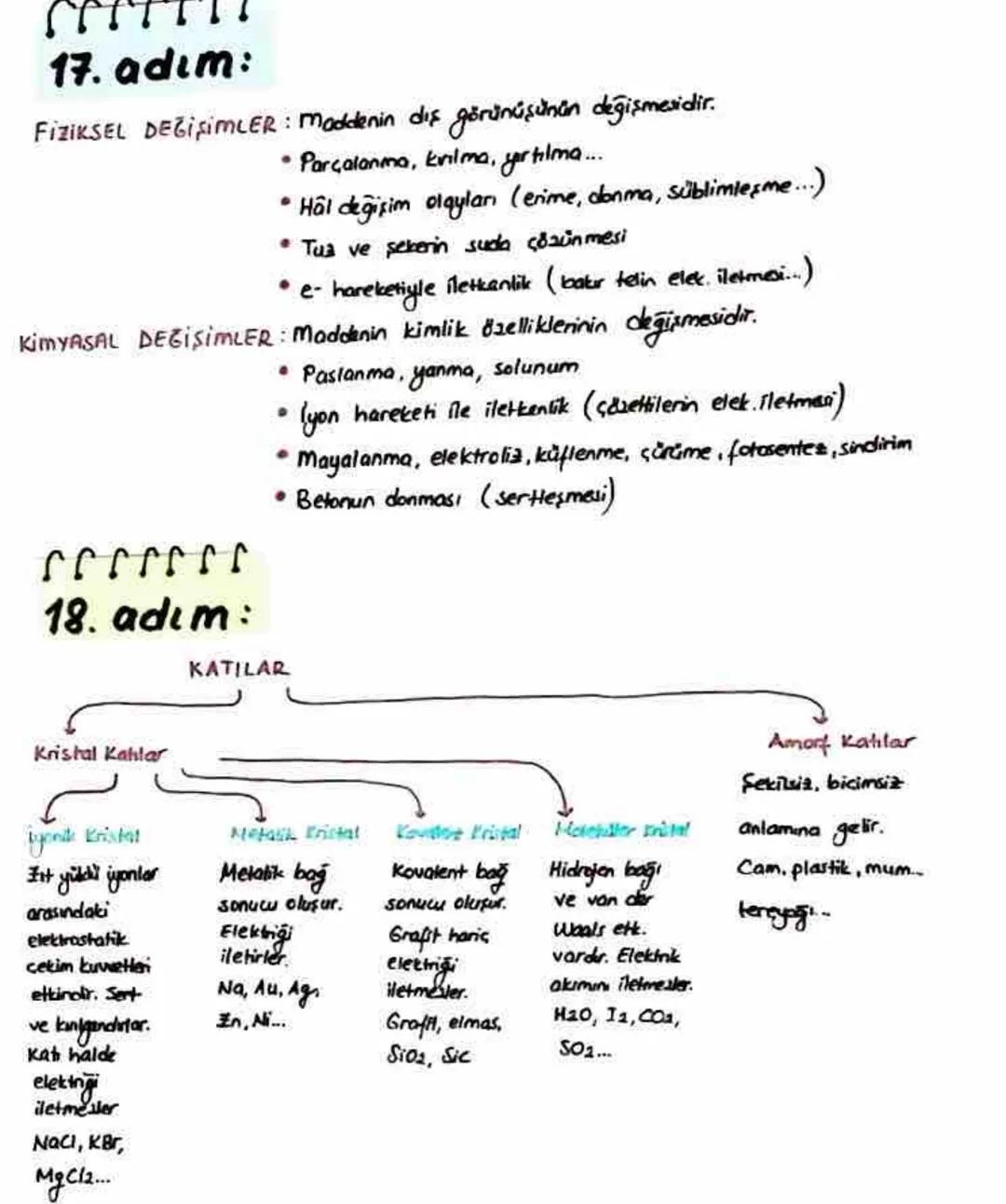
Maddeler fiziksel ve kimyasal olmak üzere iki tür değişim gösterir. Fiziksel değişim maddenin sadece dış görünüşünü değiştirir. Parçalanma, kırılma, hal değişimi (erime, donma, süblimleşme) ve tuz/şekerin suda çözünmesi buna örnektir. Elektron hareketiyle iletkenlik de fiziksel değişimdir.
Kimyasal değişim ise maddenin kimlik özelliklerinin değişmesidir. Paslanma, yanma, solunum, mayalanma, elektroliz ve küflenme buna örnek verilebilir. İyon hareketi ile iletkenlik ve betonun sertleşmesi de kimyasal değişimlerdir.
Katı maddeler kristal ve amorf yapıda olabilir. Kristal katılar düzenli bir yapıya sahiptir ve dört çeşittir: İyonik kristaller (NaCl, KBr), metalik kristaller (Na, Au), kovalent kristaller (grafit, elmas) ve moleküler kristaller (H₂O, I₂).
Bunu bilmek işine yarayacak! İyonik kristaller katı halde elektrik iletmezken, erimiş halde veya sulu çözeltide iletkendir. Grafit hariç kovalent kristaller de elektriği iletmez.
Amorf katılar ise düzensiz yapıya sahiptir ve "şekilsiz, biçimsiz" anlamına gelir. Cam, plastik, mum ve tereyağı amorf katılara örnektir. Bu tür katılar genellikle belirli bir erime noktasına sahip değildir ve ısıtıldıklarında yavaş yavaş yumuşarlar.
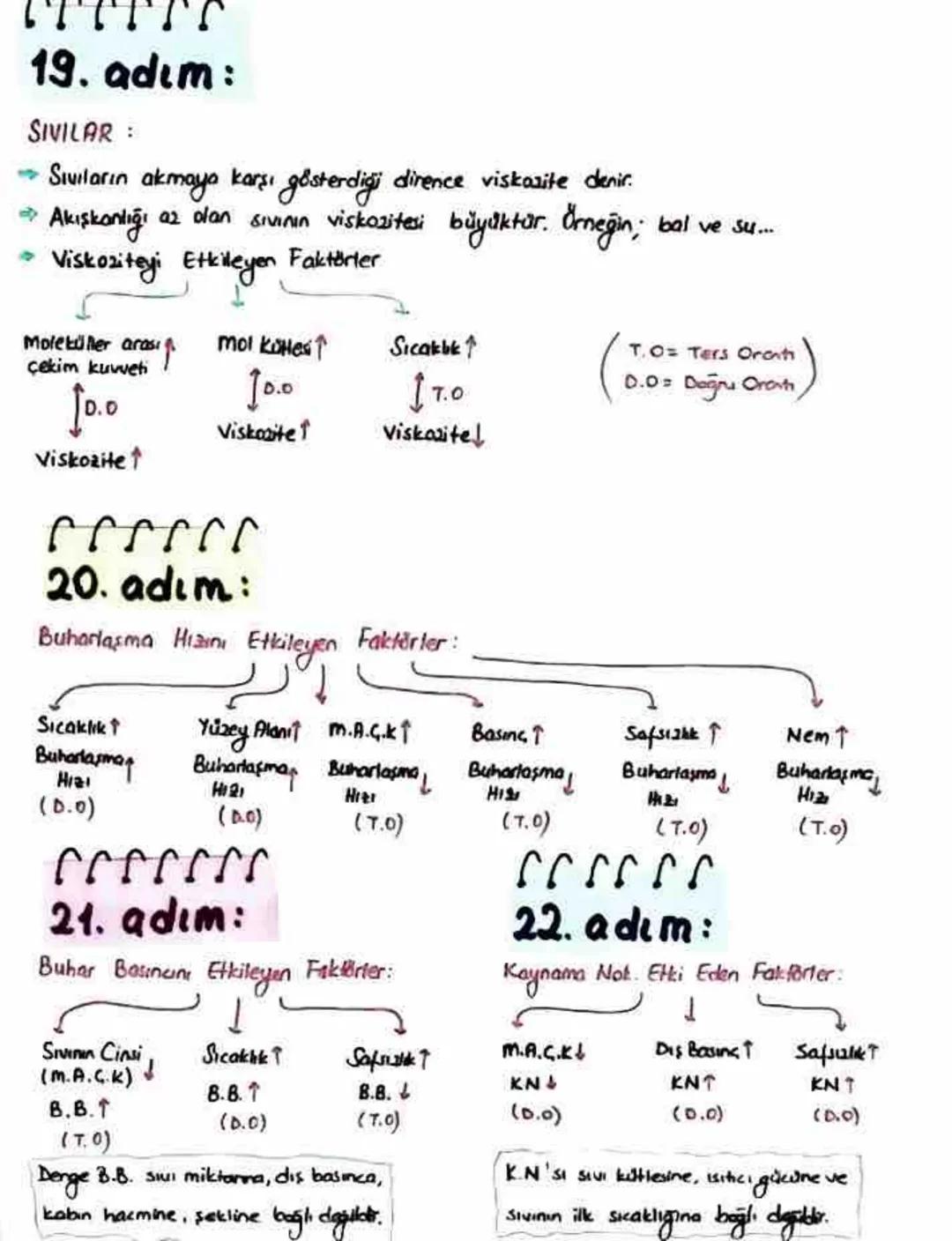
Sıvıların akmaya karşı gösterdiği dirence viskozite denir. Akışkanlığı az olan sıvının viskozitesi büyüktür. Örneğin balın viskozitesi sudan yüksektir. Viskozite, moleküller arası çekim kuvveti ve molekül kütlesi arttıkça artar, sıcaklık arttıkça azalır.
Buharlaşma hızını etkileyen faktörleri bilmek önemlidir. Sıcaklık ve yüzey alanı arttıkça buharlaşma hızı artar. Ancak moleküller arası çekim kuvveti, basınç, safsızlık ve nem arttıkça buharlaşma hızı azalır.
Buhar basıncı sıcaklık ve saflık arttıkça artar, moleküller arası çekim kuvveti arttıkça azalır. Buhar basıncı sıvı miktarına, dış basınca, kabın hacmine ve şekline bağlı değildir.
İpucu! Kaynama, buhar basıncının dış basınca eşit olduğu sıcaklıkta gerçekleşir. Bu yüzden dağ başında su daha düşük sıcaklıkta kaynar!
Kaynama noktasını etkileyen faktörlere gelince, dış basınç ve moleküller arası çekim kuvveti arttıkça kaynama noktası artar, saflık arttıkça azalır. Kaynama noktası sıvı kütlesine, ısıtıcının gücüne ve sıvının ilk sıcaklığına bağlı değildir. Hal değişimleri sırasında madde ısı alır (erime, buharlaşma, süblimleşme) veya ısı verir .

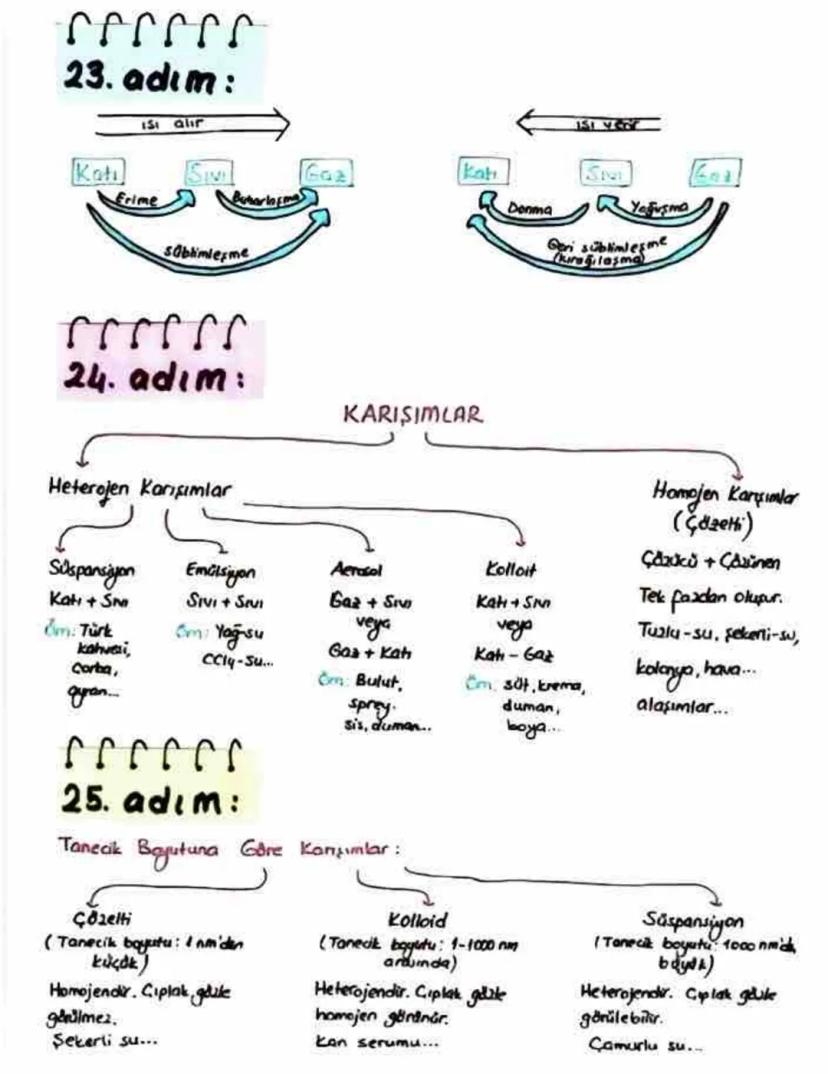
Karışımlar heterojen ve homojen olmak üzere ikiye ayrılır. Heterojen karışımlar farklı fazlardan oluşurken, homojen karışımlar (çözeltiler) tek fazdan oluşur.
Heterojen karışımların çeşitleri vardır: Süspansiyonlar , emülsiyonlar , aerosoller ve kolloitler . Bu karışımlarda farklı fazlar gözle veya mikroskopla görülebilir.
Homojen karışımlar (çözeltiler) ise çözücü ve çözünenden oluşur. Tuzlu su, şekerli su, kolonya, hava ve alaşımlar buna örnektir. Çözeltilerde tek bir faz vardır ve bileşenler gözle ayırt edilemez.
Örnek ver! Tanecik boyutuna göre karışımları günlük hayattan örneklerle hatırlayabilirsin: Şekerli su (çözelti), süt (kolloit) ve çamurlu su (süspansiyon).
Tanecik boyutuna göre karışımlar üç grupta incelenir: Çözeltiler (tanecik boyutu 1 nm'den küçük) homojendir ve çıplak gözle görülmez. Kolloitler aslında heterojendir ama homojen görünür. Süspansiyonlar (tanecik boyutu 1000 nm'den büyük) heterojendir ve çıplak gözle görülebilir.

Karışımları ayırmak için çeşitli yöntemler kullanılır. Bu yöntemler karışımdaki maddelerin özelliklerine göre seçilir. Tanecik boyutu farkı ile ayırma yöntemleri arasında ayıklama, eleme, süzme ve diyaliz bulunur.
Çözünürlük farkı ile ayırma yöntemleri ayrımsal kristallendirme ve ekstraksiyon (özütleme) şeklindedir. Yoğunluk farkı ile ayırma için ayırma hunisi, çöktürme, aktarma (dekantasyon) ve yüzdürme (flokasyon) teknikleri kullanılır. Kaynama noktası farkı ile ayırmada ise damıtma ve ayrımsal damıtma yöntemleri uygulanır.
"Benzer benzeri çözer" ilkesi çözünürlükte temeldir. Polar yapılı maddeler polar çözücülerde, apolar maddeler apolar çözücülerde daha iyi çözünür. İyonik kristaller (tuz gibi) genellikle su gibi polar çözücülerde çözünür. C ve H'den oluşan hidrokarbonlar apolar yapıdadır.
Pratik bilgi: Çözünürlük hesaplamalarında kütlece yüzde derişim, hacimce yüzde derişim ve ppm (milyonda bir parça) birimleri kullanılır. Bu hesaplamalar laboratuvar ve endüstride çok önemlidir!
Çözeltilerin derişimini ifade etmek için çeşitli birimler kullanılır. Kütlece yüzde derişim, çözünenin kütlesinin çözelti kütlesine oranının yüzde olarak ifadesidir. Hacimce yüzde derişim ise çözünenin hacminin çözelti hacmine oranının yüzdesidir. ppm ise çözünenin mg cinsinden kütlesinin çözeltinin g cinsinden kütlesine oranıdır.
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Duru Karaburun
@durukaraburun
Kimya, çevremizdeki maddeleri ve değişimleri inceleyen temel bir bilim dalıdır. Bu ders notlarında kimyanın çalışma alanları, temel kavramları ve madde özellikleri ele alınmaktadır. Günlük hayatta karşılaştığımız birçok olay kimyanın konusudur.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimya, sistematik bilgi birikimi içeren ve bilimsel yöntemleri kullanan önemli bir bilim dalıdır. Teorik bilgileriyle hayatımızın neredeyse her alanına dokunur.
Kimya birçok alanda uygulama alanı bulur. Petrokimya, gübre, tekstil, ilaç ve boya üretimi bunların başında gelir. Ayrıca gıda, enerji, temizlik, nanoteknoloji ve madencilik sektörleri de kimya biliminden yararlanır.
Kimyanın ana alt dalları arasında anorganik kimya, organik kimya, analitik kimya, biyokimya, polimer kimyası ve fizikokimya bulunur. Bu alt dallar, farklı madde gruplarını veya özellikleri inceler.
Unutma! Kimya bilgisi, kimyager ve kimya mühendisliği dışında eczacılık, metalurji, malzeme mühendisliği ve kimya öğretmenliği gibi pek çok mesleğin temelini oluşturur.
Kimyasalların temel uyarı özellikleri de bilinmelidir: yanıcı, yakıcı, korozif, patlayıcı, tahriş edici, zehirli (toksik), radyoaktif ve çevreye zararlı özellikler taşıyabilirler. Bu özellikleri tanımak, güvenliğimiz için çok önemlidir!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Elementler ve bileşikler arasındaki farkları anlamak kimyanın temelidir. Elementler saf maddelerdir ve aynı tür atomlardan oluşur. Fiziksel veya kimyasal yöntemlerle daha basit maddelere ayrıştırılamazlar ve sembollerle gösterilirler.
Bileşikler ise en az iki farklı tür atomdan oluşur ve formüllerle gösterilirler. Kimyasal yöntemlerle ayrıştırılabilirler. Elementler gibi bileşikler de hal değişim sıcaklığı dışında homojen özellik gösterirler.
Atomun yapısını anlamak için bilim insanları çeşitli modeller geliştirmiştir. Dalton modeli atomu bölünemeyen tanecikler olarak tanımlarken, Thomson modeli atomu pozitif yüklü bir küre içinde negatif elektronların bulunduğu "üzümlü kek" olarak tarif etmiştir.
İlginç bilgi: Rutherford atom modelinde pozitif yük çekirdektedir ve elektronlar çekirdek etrafındaki büyük boşlukta bulunur. Nötronu ise Chadwick 1932'de keşfetmiştir!
Bohr atom modeli elektronların belirli dairesel yörüngelerde bulunduğunu öne sürer. Bu yörüngeler n=1, 2... veya K, L, M, N harfleriyle ifade edilir. Ancak bu model sadece tek elektronlu atomların davranışını açıklayabilmektedir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Atom kavramını anlamak için "izo" kavramlarını bilmek gerekir. İzotop atomlar proton sayıları aynı, nötron sayıları farklı atomlardır. İzoton atomlar nötron sayıları aynı, atom numaraları farklı atomlardır. İzobar atomlar kütle numaraları aynı, proton sayıları farklı atomlardır. İzoelektron atomlar ise elektron sayıları ve dizilişleri aynı, proton sayıları farklı atomlardır.
Bir atomun kütle numarası nötron ve proton sayılarının toplamına eşittir. Proton sayısı, atom numarasına eşittir ve çekirdek yükünü belirtir. Nötr atomda elektron sayısı proton sayısına eşitken, iyonlarda bu durum değişir.
Periyodik özellikler atomların davranışlarını anlamamızı sağlar. Atom yarıçapı genellikle periyotta soldan sağa azalır, grupta yukarıdan aşağı artar. İyonlaşma enerjisi ise periyotta soldan sağa artma eğilimindedir (1A<3A<2A<4A<6A<5A<7A<8A).
Dikkat! Elektronegatiflik, bir atomun bağ elektronlarını kendine çekme yeteneğidir ve periyodik tabloda en yüksek değere sahip element flordur. Elektron ilgisi ise en yüksek olan element klordur.
Atom yarıçapı, elektronegatiflik, iyonlaşma enerjisi ve elektron ilgisi gibi özellikler, periyodik tablodaki elementlerin kimyasal davranışlarını belirler. Bu özellikleri anlamak, kimyasal bağları ve tepkimeleri kavramak için çok önemlidir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Periyodik tabloda elementlerin gruplarının özel isimleri vardır. Örneğin, 1A grubu alkali metaller, 7A grubu halojenler, 8A grubu ise soy gazlar olarak adlandırılır. Bu gruplardaki elementler benzer özellikler gösterir.
Kimyasal türler başlıca atom, molekül ve iyon olarak sınıflandırılır. Atomlar genellikle metal ve soy gazlardır (Fe, Au, He, Ne). Moleküller ametallerden oluşur (CO₂, H₂O, O₂). İyonlar ise pozitif yüklü katyon (genellikle metal) veya negatif yüklü anyon (genellikle ametal) olabilir.
Kimyasal türler arasındaki etkileşimler güçlü ve zayıf olarak ikiye ayrılır. Güçlü etkileşimler arasında iyonik bağ , kovalent bağ ve metalik bağ yer alır.
Merak et! İyonik bağlar metal ve ametal arasında elektron alışverişiyle oluşurken, kovalent bağlarda elektronlar paylaşılır. Bu fark, maddelerin fiziksel ve kimyasal özelliklerini nasıl etkiliyor?
Zayıf etkileşimler ise van der Waals bağları ve hidrojen bağıdır. Hidrojen bağı, hidrojenin flor, oksijen veya azot atomlarıyla oluşturduğu özel bir etkileşimdir. Bu zayıf etkileşimler, maddelerin hal değişimleri ve çözünürlük gibi özelliklerini belirler.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Güçlü etkileşimler maddelerin temel yapı taşlarını bir arada tutar. İyonik bağ metal ve ametal arasında elektron alışverişi sonucu oluşur ve Mg²⁺Cl⁻ gibi iyonik bileşikler birim hücrelerden oluşur.
Kovalent bağ ise ametaller arasında elektron ortaklaşması ile oluşur. Aynı ametaller arasında oluşursa (F₂, O₂, O₃, Cl₂) apolar kovalent bağ, farklı ametaller arasında oluşursa (CO₂, HCl, NH₃) polar kovalent bağ olarak adlandırılır.
Metalik bağ metallerin değerlik elektronlarının serbestçe hareket etmesiyle oluşur. Bu elektronlar adeta bir "elektron denizi" oluşturarak metal atomlarını bir arada tutar. Bu bağ, metallerin elektrik iletkenliği gibi özelliklerini açıklar.
Harika! Su, alkol, DNA gibi birçok önemli molekülde hidrojen bağı bulunur ve bu bağlar maddelerin özelliklerini belirler. Örneğin suyun kaynama noktasının yüksek olması hidrojen bağları sayesindedir!
Zayıf etkileşimler arasında en önemlilerinden biri hidrojen bağıdır. Bu bağ, hidrojen ile F, O veya N atomları arasında oluşur (HF...HF, H₂O...H₂O, NH₃...NH₃). Diğer zayıf etkileşimler arasında dipol-dipol (polar moleküller arasında), iyon-dipol (iyon ile polar molekül arasında) ve tüm etkileşimlerde görülen en zayıf bağ olan London kuvvetleri bulunur.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Maddeler fiziksel ve kimyasal olmak üzere iki tür değişim gösterir. Fiziksel değişim maddenin sadece dış görünüşünü değiştirir. Parçalanma, kırılma, hal değişimi (erime, donma, süblimleşme) ve tuz/şekerin suda çözünmesi buna örnektir. Elektron hareketiyle iletkenlik de fiziksel değişimdir.
Kimyasal değişim ise maddenin kimlik özelliklerinin değişmesidir. Paslanma, yanma, solunum, mayalanma, elektroliz ve küflenme buna örnek verilebilir. İyon hareketi ile iletkenlik ve betonun sertleşmesi de kimyasal değişimlerdir.
Katı maddeler kristal ve amorf yapıda olabilir. Kristal katılar düzenli bir yapıya sahiptir ve dört çeşittir: İyonik kristaller (NaCl, KBr), metalik kristaller (Na, Au), kovalent kristaller (grafit, elmas) ve moleküler kristaller (H₂O, I₂).
Bunu bilmek işine yarayacak! İyonik kristaller katı halde elektrik iletmezken, erimiş halde veya sulu çözeltide iletkendir. Grafit hariç kovalent kristaller de elektriği iletmez.
Amorf katılar ise düzensiz yapıya sahiptir ve "şekilsiz, biçimsiz" anlamına gelir. Cam, plastik, mum ve tereyağı amorf katılara örnektir. Bu tür katılar genellikle belirli bir erime noktasına sahip değildir ve ısıtıldıklarında yavaş yavaş yumuşarlar.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Sıvıların akmaya karşı gösterdiği dirence viskozite denir. Akışkanlığı az olan sıvının viskozitesi büyüktür. Örneğin balın viskozitesi sudan yüksektir. Viskozite, moleküller arası çekim kuvveti ve molekül kütlesi arttıkça artar, sıcaklık arttıkça azalır.
Buharlaşma hızını etkileyen faktörleri bilmek önemlidir. Sıcaklık ve yüzey alanı arttıkça buharlaşma hızı artar. Ancak moleküller arası çekim kuvveti, basınç, safsızlık ve nem arttıkça buharlaşma hızı azalır.
Buhar basıncı sıcaklık ve saflık arttıkça artar, moleküller arası çekim kuvveti arttıkça azalır. Buhar basıncı sıvı miktarına, dış basınca, kabın hacmine ve şekline bağlı değildir.
İpucu! Kaynama, buhar basıncının dış basınca eşit olduğu sıcaklıkta gerçekleşir. Bu yüzden dağ başında su daha düşük sıcaklıkta kaynar!
Kaynama noktasını etkileyen faktörlere gelince, dış basınç ve moleküller arası çekim kuvveti arttıkça kaynama noktası artar, saflık arttıkça azalır. Kaynama noktası sıvı kütlesine, ısıtıcının gücüne ve sıvının ilk sıcaklığına bağlı değildir. Hal değişimleri sırasında madde ısı alır (erime, buharlaşma, süblimleşme) veya ısı verir .

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Karışımlar heterojen ve homojen olmak üzere ikiye ayrılır. Heterojen karışımlar farklı fazlardan oluşurken, homojen karışımlar (çözeltiler) tek fazdan oluşur.
Heterojen karışımların çeşitleri vardır: Süspansiyonlar , emülsiyonlar , aerosoller ve kolloitler . Bu karışımlarda farklı fazlar gözle veya mikroskopla görülebilir.
Homojen karışımlar (çözeltiler) ise çözücü ve çözünenden oluşur. Tuzlu su, şekerli su, kolonya, hava ve alaşımlar buna örnektir. Çözeltilerde tek bir faz vardır ve bileşenler gözle ayırt edilemez.
Örnek ver! Tanecik boyutuna göre karışımları günlük hayattan örneklerle hatırlayabilirsin: Şekerli su (çözelti), süt (kolloit) ve çamurlu su (süspansiyon).
Tanecik boyutuna göre karışımlar üç grupta incelenir: Çözeltiler (tanecik boyutu 1 nm'den küçük) homojendir ve çıplak gözle görülmez. Kolloitler aslında heterojendir ama homojen görünür. Süspansiyonlar (tanecik boyutu 1000 nm'den büyük) heterojendir ve çıplak gözle görülebilir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Karışımları ayırmak için çeşitli yöntemler kullanılır. Bu yöntemler karışımdaki maddelerin özelliklerine göre seçilir. Tanecik boyutu farkı ile ayırma yöntemleri arasında ayıklama, eleme, süzme ve diyaliz bulunur.
Çözünürlük farkı ile ayırma yöntemleri ayrımsal kristallendirme ve ekstraksiyon (özütleme) şeklindedir. Yoğunluk farkı ile ayırma için ayırma hunisi, çöktürme, aktarma (dekantasyon) ve yüzdürme (flokasyon) teknikleri kullanılır. Kaynama noktası farkı ile ayırmada ise damıtma ve ayrımsal damıtma yöntemleri uygulanır.
"Benzer benzeri çözer" ilkesi çözünürlükte temeldir. Polar yapılı maddeler polar çözücülerde, apolar maddeler apolar çözücülerde daha iyi çözünür. İyonik kristaller (tuz gibi) genellikle su gibi polar çözücülerde çözünür. C ve H'den oluşan hidrokarbonlar apolar yapıdadır.
Pratik bilgi: Çözünürlük hesaplamalarında kütlece yüzde derişim, hacimce yüzde derişim ve ppm (milyonda bir parça) birimleri kullanılır. Bu hesaplamalar laboratuvar ve endüstride çok önemlidir!
Çözeltilerin derişimini ifade etmek için çeşitli birimler kullanılır. Kütlece yüzde derişim, çözünenin kütlesinin çözelti kütlesine oranının yüzde olarak ifadesidir. Hacimce yüzde derişim ise çözünenin hacminin çözelti hacmine oranının yüzdesidir. ppm ise çözünenin mg cinsinden kütlesinin çözeltinin g cinsinden kütlesine oranıdır.
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
2
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı