Kimya laboratuvarında güvenliğin en önemli kuralı, tehlike sembollerini tanımak! Bu... Daha fazla göster
TYT Kimya Konuları ve İçerikleri














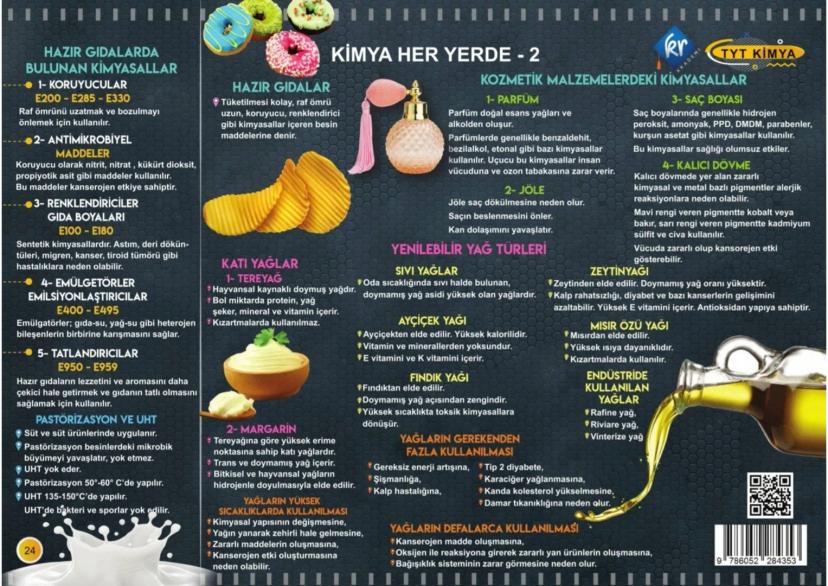

Tehlike Sembolleri ve Güvenlik
Kimya laboratuvarında karşılaştığın tehlike sembolleri hayat kurtarıcı! Her sembol, o maddenin nasıl davranacağını ve hangi önlemleri alman gerektiğini gösteriyor.
Yanıcı maddeler (alkol, aseton gibi) ateş ve kıvılcımdan uzak tutulmalı. Patlayıcı maddeler ise en tehlikeli grup - LPG ve asetilen gibi gazlar çarpma ve ısıya karşı son derece hassas.
Korozif maddeler derini ve metalları eritebilir. H₂SO₄ gibi asitlerle çalışırken mutlaka koruyucu ekipman kullan. Toksik maddeler zehirlenmeye neden olurken, radyoaktif maddeler kanserojen etki yapar.
💡 Önemli İpucu: Her kimyasal maddenin etiketi üzerindeki semboller, o maddeyle güvenli çalışmanın yol haritası!
Kimyagerler sadece laboratuvarda değil; ilaç, gıda, enerji, boya gibi birçok sektörde çalışıyor. Eczacı, kimya mühendisi ya da öğretmen olmak istiyorsan, bu temel güvenlik kuralları kariyerinin başlangıcı!

Kimyanın Sembolik Dili ve Elementler
Kimya evrensel bir dil! Dünyanın her yerinde element sembolleri aynı şekilde yazılıyor. H hidrojen, O oksijen, Au altın demek - bu semboller sayesinde Çinli bir kimyager de Türk bir kimyager de aynı dili konuşuyor.
Elementler doğadaki en basit maddeler. Fiziksel ya da kimyasal yöntemlerle daha basit maddelere ayrışmazlar. Atomik halde (Na, Cu gibi) ya da moleküler halde (H₂, O₂ gibi) bulunabilirler.
Her elementin ayırt edici özellikleri sabit: erime noktası, kaynama noktası, özkütle gibi. Bu özellikler o elementin kimlik kartı gibi!
💡 Tarihsel Not: Berzelius'un 1814'teki sembol önerisi sayesinde bugün tüm dünyada ortak kimya dili konuşabiliyoruz!
Elementleri metaller, ametaller, yarı metaller ve soy gazlar olarak sınıflandırıyoruz. Bu sınıflandırma, elementlerin davranışlarını tahmin etmeni sağlıyor.

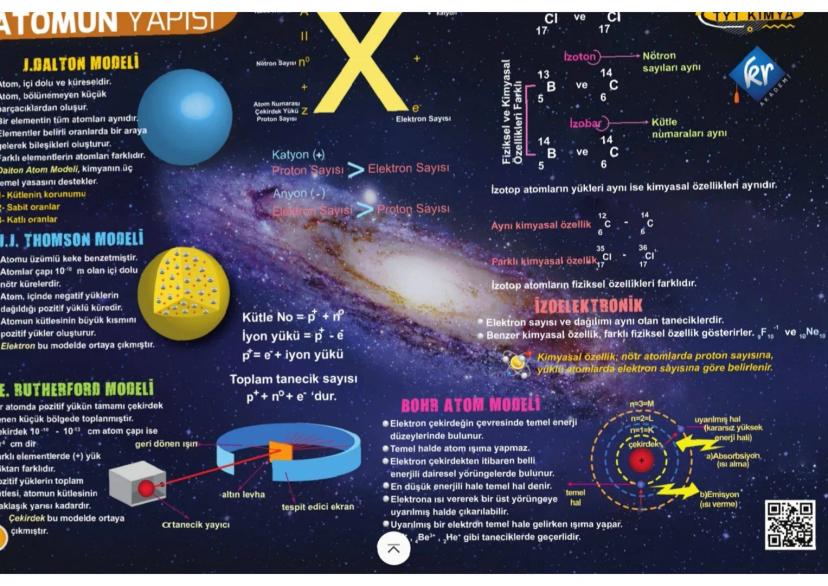
Atomun Yapısı ve Modeller
Atomun yapısını anlamak için bilim insanları farklı atom modelleri geliştirdi. Dalton atomu bölünmez küre olarak görürken, Thomson "üzümlü kek" modeli ile elektronları keşfetti.
Rutherford modeli devrim yarattı: Atomun merkezinde küçücük bir çekirdek var ve tüm pozitif yük burada toplanmış! Çekirdek atom çapının 10.000'de 1'i kadar küçük ama kütlenin yarısını barındırıyor.
Modern atomda proton sayısı = atom numarası eşitliği temel kural. İyonlar proton-elektron dengesizliğinden oluşuyor: fazla elektron (-) iyon, eksik elektron (+) iyon yapıyor.
İzotop, izoton, izobar kavramları sınav favorisi! İzotoplar aynı element ama farklı nötron sayısı. C-12 ve C-14 gibi izotopların kimyasal özellikleri aynı ama fiziksel özellikleri farklı.
💡 Sınav İpucu: İzoelektronik tanecikler (F⁻ ve Ne gibi) aynı elektron sayısına sahip ama farklı çekirdek yüküne sahip!
Bohr modeli elektronların belirli yörüngelerde döndüğünü söylüyor. Elektron enerji alınca üst yörüngeye çıkıyor, enerji verince alt yörüngeye iniyor ve ışık çıkarıyor.

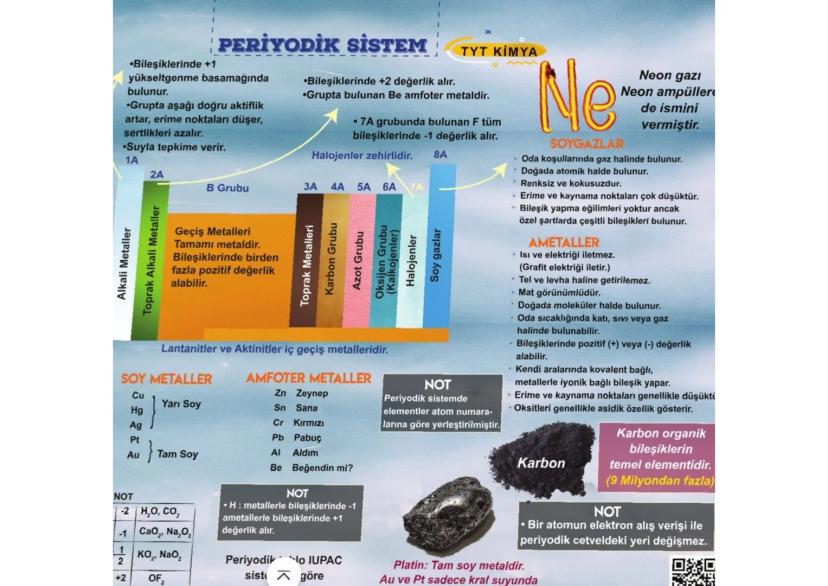
Periyodik Sistem ve Element Grupları
Periyodik sistem kimyanın haritası! Elementler atom numaralarına göre dizilmiş ve benzer özelliklere sahip olanlar aynı grupta yer alıyor. Bu düzenleme sayesinde elementlerin özelliklerini tahmin edebiliyorsun.
1A grubu (alkali metaller) çok aktif! Suyla tepkime verirler ve aşağı doğru aktiflik artar. 2A grubu (toprak alkali metaller) +2 değerlik alırken, 7A grubu (halojenler) -1 değerlik alıyor.
Geçiş metalleri B grubunda bulunuyor ve birden fazla değerlik alabiliyorlar. Soy gazlar ise en kararlı elementler - bileşik yapmak istemiyorlar çünkü elektron dizilimleri mükemmel!
💡 Önemli Kural: Amfoter metaller (Zn, Al, Cr, Pb, Sn, Be) hem asit hem baz gibi davranabilir!
Soy metaller (Au, Pt, Ag, Cu, Hg) paslanmaya dayanıklı. Altın ve platin sadece kral suyunda çözünüyor! Ametaller ise genellikle elektriği iletmiyor (grafit hariç) ve moleküler halde bulunuyor.

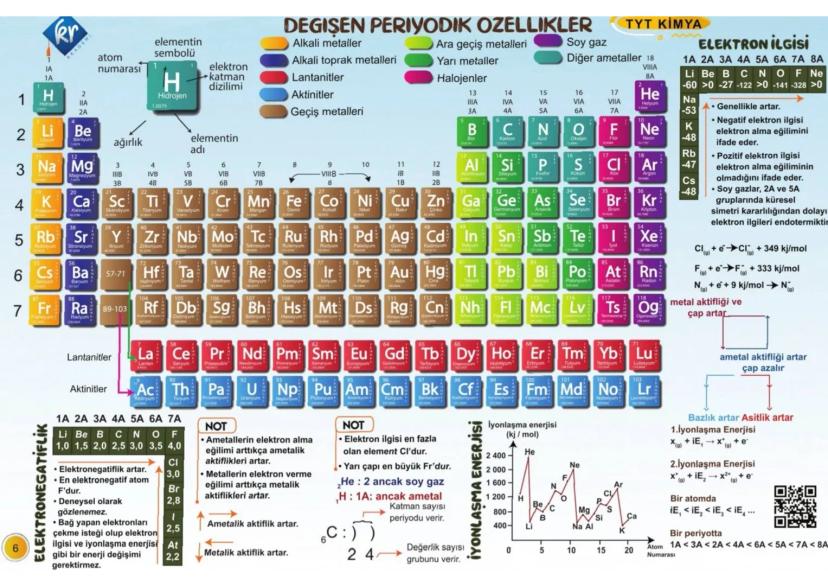
Periyodik Özellikler
Periyodik sistemde düzenli değişen özellikler var ki bunları bilmen sınavlar için kritik! Soldan sağa doğru atom çapı küçülürken, iyonlaşma enerjisi artıyor.
İyonlaşma enerjisi elektronunu koparmak için gereken enerji. Soldan sağa artar çünkü çekirdek yükü artıyor. Yukarıdan aşağı azalır çünkü elektron çekirdekten uzaklaşıyor.
Elektronegatiflik bağdaki elektronları çekme gücü. En elektronegatif element flor (F)! Elektronegatiflik farkı büyükse bağ iyonik, küçükse kovalent oluyor.
Elektron ilgisi genellikle endotermik bir süreç. 7A grubu elementleri elektron almayı çok seviyor çünkü soy gaz yapısına ulaşıyorlar.
💡 Sınav Taktiği: Periyodik özellikler için "soldan sağa artar, yukarıdan aşağı azalır" kuralını ezberle!
Metalik aktiflik soldan sağa azalırken, ametalik aktiflik artıyor. Bu yüzden franciyum en aktif metal, flor en aktif ametal!

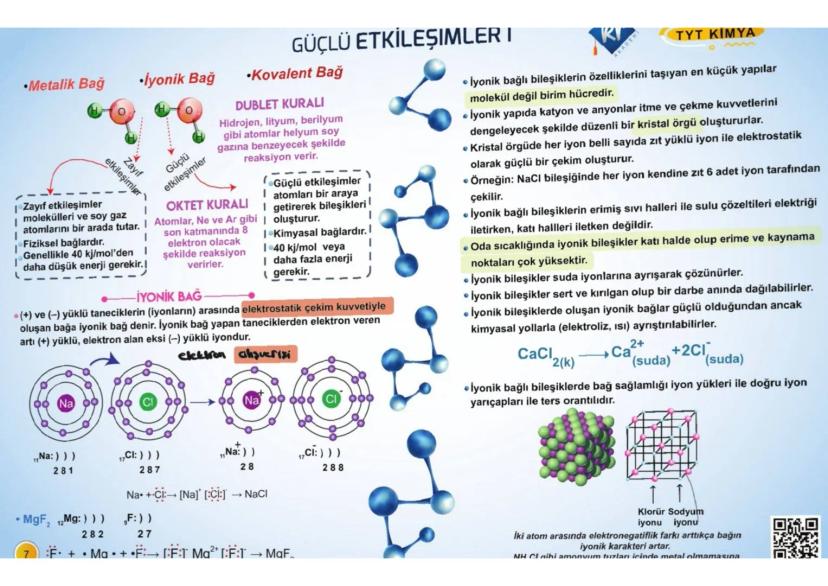
Kimyasal Bağlar - Güçlü Etkileşimler
Atomlar neden bağ yapar? Oktet kuralı gereği! Atomlar son katmanlarında 8 elektron olacak şekilde (hidrojen için 2) bağ kurarak kararlı hale gelmeye çalışıyor.
İyonik bağ metal ile ametal arasında elektron alış-verişi ile oluşuyor. Na'dan bir elektron gidip Cl'ye geçince Na⁺Cl⁻ iyonik bileşiği oluşuyor. Bu bileşikler kristal örgü yapısında düzenleniyor.
İyonik bileşiklerin özellikleri çok karakteristik: Katı halde elektrik iletmiyor ama suda çözününce iletiyor. Erime noktaları yüksek, sert ama kırılgan yapıdalar.
Metalik bağ metal atomları arasında oluşuyor. Pozitif metal iyonları ile negatif elektron denizi arasındaki çekim kuvveti. Bu bağ sayesinde metaller elektrik iletiyor ve tel haline getirilebiliyor.
💡 Bağ Sağlamlığı: İyon yükleri arttıkça bağ güçleniyor, iyon çapları arttıkça zayıflıyor!
Kovalent bağ ametal atomları arasında elektron ortaklaşması ile kuruluyor. H-F bağında elektron çifti paylaşılıyor ve her atom kararlı hale ulaşıyor.

Kovalent Bağ ve Lewis Gösterimleri
Kovalent bağ ametallar arasında elektron paylaşımı ile oluşuyor. Elektronegatiflik farkına göre polar ya da apolar kovalent bağ kurulabiliyor.
Lewis gösterimleri atomların değerlik elektronlarını görsel olarak gösteriyor. Nokta ve çizgilerle hangi atomun kaç elektronu olduğunu ve nasıl bağ kurduğunu rahatlıkla görebiliyorsun.
Bağlanmamış elektron çiftleri molekülün şeklini etkiliyor. NH₃ molekülünde azotun üzerindeki yalnız elektron çifti, molekülü polar yapıyor.
Metalik bağın kuvveti değerlik elektron sayısı ile doğru, atom çapı ile ters orantılı. Bu yüzden periyodik sistemde soldan sağa metalik bağ güçleniyor, erime noktaları yükseliyor.
💡 Pratik İpucu: Lewis yapısı çizerken önce toplam elektron sayısını bul, sonra bağları kur, kalan elektronları yalnız çiftler halinde dağıt!
Kovalent bağlarda çoklu bağlar da olabiliyor. O₂ molekülünde çift bağ , N₂ molekülünde üçlü bağ (N≡N) bulunuyor.

Bileşiklerin Adlandırılması
İyonik bileşikler metal-ametal, metal-kök veya kök-kök kombinasyonları ile oluşuyor. Sodyum klorür (NaCl), kalsiyum sülfat (CaSO₄) gibi örnekler günlük hayatta da karşına çıkıyor.
Değişken değerlik alan metaller için Roma rakamları kullanılıyor. FeCl₃ için "demir (III) klorür" diyoruz çünkü demir +3 değerlik alıyor.
Kovalent bileşikler Latin sayılarının ön ekleri ile adlandırılıyor. CO₂ karbon dioksit, N₂O₅ diazot pentaoksit oluyor. İlk elementi "mono" ile başlamıyoruz!
Katyonlar ve anyonlar tablosunu ezberlemen gerekiyor. NH₄⁺ amonyum, SO₄²⁻ sülfat gibi çok atomlu iyonlar özellikle önemli.
💡 Adlandırma Kuralı: İlk element sayı+isim, ikinci element sayı+anyon ismi şeklinde okunuyor!
Bazı özel durumlar var: NH₄ bileşikleri metal içermemesine rağmen iyonik bağlı, oksijen ilk elementse "oksijen" ikinci elementse "oksit" oluyor.

Zayıf Etkileşimler
Kimyasal bağlardan farklı olarak zayıf etkileşimler maddenin fiziksel halini belirliyor. Bu kuvvetler sayesinde su 100°C'de kaynıyor, yoksa çok daha düşük sıcaklıkta kaynar!
Hidrojen bağı en güçlü zayıf etkileşim. H₂O, NH₃, HF gibi moleküllerde H atomu F, O, N atomlarından birine bağlı olmalı. Su moleküleri arasında 4 hidrojen bağı kurulabiliyor.
Dipol-dipol etkileşimi polar moleküller arasında oluşuyor. HCl gibi moleküllerde δ+ ve δ- yüklü uçlar birbirini çekiyor.
London kuvvetleri tüm moleküller arasında bulunuyor ama apolar moleküllerde tek etkileşim türü. Molekül ağırlığı arttıkça kuvvet artıyor: I₂ > Br₂ > Cl₂ > F₂ sırası.
💡 Çözünürlük Kuralı: "Benzer benzeri çözer" - polar maddeler polarda, apolar maddeler apolarda çözünüyor!
İyon-dipol etkileşimi tuz suda çözünürken görülüyor. NaCl suda çözününce Na⁺ ve Cl⁻ iyonları su moleküllerinin dipolleri tarafından çevreleniyor.










Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Salts
1Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
TYT Kimya Konuları ve İçerikleri
Kimya laboratuvarında güvenliğin en önemli kuralı, tehlike sembollerini tanımak! Bu sembollerin her biri, o maddeyle nasıl çalışman gerektiğini söylüyor. Ayrıca kimyanın evrensel dili olan semboller ve atomun yapısı da kimyayı anlamanın temelidir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Tehlike Sembolleri ve Güvenlik
Kimya laboratuvarında karşılaştığın tehlike sembolleri hayat kurtarıcı! Her sembol, o maddenin nasıl davranacağını ve hangi önlemleri alman gerektiğini gösteriyor.
Yanıcı maddeler (alkol, aseton gibi) ateş ve kıvılcımdan uzak tutulmalı. Patlayıcı maddeler ise en tehlikeli grup - LPG ve asetilen gibi gazlar çarpma ve ısıya karşı son derece hassas.
Korozif maddeler derini ve metalları eritebilir. H₂SO₄ gibi asitlerle çalışırken mutlaka koruyucu ekipman kullan. Toksik maddeler zehirlenmeye neden olurken, radyoaktif maddeler kanserojen etki yapar.
💡 Önemli İpucu: Her kimyasal maddenin etiketi üzerindeki semboller, o maddeyle güvenli çalışmanın yol haritası!
Kimyagerler sadece laboratuvarda değil; ilaç, gıda, enerji, boya gibi birçok sektörde çalışıyor. Eczacı, kimya mühendisi ya da öğretmen olmak istiyorsan, bu temel güvenlik kuralları kariyerinin başlangıcı!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Kimyanın Sembolik Dili ve Elementler
Kimya evrensel bir dil! Dünyanın her yerinde element sembolleri aynı şekilde yazılıyor. H hidrojen, O oksijen, Au altın demek - bu semboller sayesinde Çinli bir kimyager de Türk bir kimyager de aynı dili konuşuyor.
Elementler doğadaki en basit maddeler. Fiziksel ya da kimyasal yöntemlerle daha basit maddelere ayrışmazlar. Atomik halde (Na, Cu gibi) ya da moleküler halde (H₂, O₂ gibi) bulunabilirler.
Her elementin ayırt edici özellikleri sabit: erime noktası, kaynama noktası, özkütle gibi. Bu özellikler o elementin kimlik kartı gibi!
💡 Tarihsel Not: Berzelius'un 1814'teki sembol önerisi sayesinde bugün tüm dünyada ortak kimya dili konuşabiliyoruz!
Elementleri metaller, ametaller, yarı metaller ve soy gazlar olarak sınıflandırıyoruz. Bu sınıflandırma, elementlerin davranışlarını tahmin etmeni sağlıyor.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Atomun Yapısı ve Modeller
Atomun yapısını anlamak için bilim insanları farklı atom modelleri geliştirdi. Dalton atomu bölünmez küre olarak görürken, Thomson "üzümlü kek" modeli ile elektronları keşfetti.
Rutherford modeli devrim yarattı: Atomun merkezinde küçücük bir çekirdek var ve tüm pozitif yük burada toplanmış! Çekirdek atom çapının 10.000'de 1'i kadar küçük ama kütlenin yarısını barındırıyor.
Modern atomda proton sayısı = atom numarası eşitliği temel kural. İyonlar proton-elektron dengesizliğinden oluşuyor: fazla elektron (-) iyon, eksik elektron (+) iyon yapıyor.
İzotop, izoton, izobar kavramları sınav favorisi! İzotoplar aynı element ama farklı nötron sayısı. C-12 ve C-14 gibi izotopların kimyasal özellikleri aynı ama fiziksel özellikleri farklı.
💡 Sınav İpucu: İzoelektronik tanecikler (F⁻ ve Ne gibi) aynı elektron sayısına sahip ama farklı çekirdek yüküne sahip!
Bohr modeli elektronların belirli yörüngelerde döndüğünü söylüyor. Elektron enerji alınca üst yörüngeye çıkıyor, enerji verince alt yörüngeye iniyor ve ışık çıkarıyor.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Periyodik Sistem ve Element Grupları
Periyodik sistem kimyanın haritası! Elementler atom numaralarına göre dizilmiş ve benzer özelliklere sahip olanlar aynı grupta yer alıyor. Bu düzenleme sayesinde elementlerin özelliklerini tahmin edebiliyorsun.
1A grubu (alkali metaller) çok aktif! Suyla tepkime verirler ve aşağı doğru aktiflik artar. 2A grubu (toprak alkali metaller) +2 değerlik alırken, 7A grubu (halojenler) -1 değerlik alıyor.
Geçiş metalleri B grubunda bulunuyor ve birden fazla değerlik alabiliyorlar. Soy gazlar ise en kararlı elementler - bileşik yapmak istemiyorlar çünkü elektron dizilimleri mükemmel!
💡 Önemli Kural: Amfoter metaller (Zn, Al, Cr, Pb, Sn, Be) hem asit hem baz gibi davranabilir!
Soy metaller (Au, Pt, Ag, Cu, Hg) paslanmaya dayanıklı. Altın ve platin sadece kral suyunda çözünüyor! Ametaller ise genellikle elektriği iletmiyor (grafit hariç) ve moleküler halde bulunuyor.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Periyodik Özellikler
Periyodik sistemde düzenli değişen özellikler var ki bunları bilmen sınavlar için kritik! Soldan sağa doğru atom çapı küçülürken, iyonlaşma enerjisi artıyor.
İyonlaşma enerjisi elektronunu koparmak için gereken enerji. Soldan sağa artar çünkü çekirdek yükü artıyor. Yukarıdan aşağı azalır çünkü elektron çekirdekten uzaklaşıyor.
Elektronegatiflik bağdaki elektronları çekme gücü. En elektronegatif element flor (F)! Elektronegatiflik farkı büyükse bağ iyonik, küçükse kovalent oluyor.
Elektron ilgisi genellikle endotermik bir süreç. 7A grubu elementleri elektron almayı çok seviyor çünkü soy gaz yapısına ulaşıyorlar.
💡 Sınav Taktiği: Periyodik özellikler için "soldan sağa artar, yukarıdan aşağı azalır" kuralını ezberle!
Metalik aktiflik soldan sağa azalırken, ametalik aktiflik artıyor. Bu yüzden franciyum en aktif metal, flor en aktif ametal!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Kimyasal Bağlar - Güçlü Etkileşimler
Atomlar neden bağ yapar? Oktet kuralı gereği! Atomlar son katmanlarında 8 elektron olacak şekilde (hidrojen için 2) bağ kurarak kararlı hale gelmeye çalışıyor.
İyonik bağ metal ile ametal arasında elektron alış-verişi ile oluşuyor. Na'dan bir elektron gidip Cl'ye geçince Na⁺Cl⁻ iyonik bileşiği oluşuyor. Bu bileşikler kristal örgü yapısında düzenleniyor.
İyonik bileşiklerin özellikleri çok karakteristik: Katı halde elektrik iletmiyor ama suda çözününce iletiyor. Erime noktaları yüksek, sert ama kırılgan yapıdalar.
Metalik bağ metal atomları arasında oluşuyor. Pozitif metal iyonları ile negatif elektron denizi arasındaki çekim kuvveti. Bu bağ sayesinde metaller elektrik iletiyor ve tel haline getirilebiliyor.
💡 Bağ Sağlamlığı: İyon yükleri arttıkça bağ güçleniyor, iyon çapları arttıkça zayıflıyor!
Kovalent bağ ametal atomları arasında elektron ortaklaşması ile kuruluyor. H-F bağında elektron çifti paylaşılıyor ve her atom kararlı hale ulaşıyor.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Kovalent Bağ ve Lewis Gösterimleri
Kovalent bağ ametallar arasında elektron paylaşımı ile oluşuyor. Elektronegatiflik farkına göre polar ya da apolar kovalent bağ kurulabiliyor.
Lewis gösterimleri atomların değerlik elektronlarını görsel olarak gösteriyor. Nokta ve çizgilerle hangi atomun kaç elektronu olduğunu ve nasıl bağ kurduğunu rahatlıkla görebiliyorsun.
Bağlanmamış elektron çiftleri molekülün şeklini etkiliyor. NH₃ molekülünde azotun üzerindeki yalnız elektron çifti, molekülü polar yapıyor.
Metalik bağın kuvveti değerlik elektron sayısı ile doğru, atom çapı ile ters orantılı. Bu yüzden periyodik sistemde soldan sağa metalik bağ güçleniyor, erime noktaları yükseliyor.
💡 Pratik İpucu: Lewis yapısı çizerken önce toplam elektron sayısını bul, sonra bağları kur, kalan elektronları yalnız çiftler halinde dağıt!
Kovalent bağlarda çoklu bağlar da olabiliyor. O₂ molekülünde çift bağ , N₂ molekülünde üçlü bağ (N≡N) bulunuyor.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Bileşiklerin Adlandırılması
İyonik bileşikler metal-ametal, metal-kök veya kök-kök kombinasyonları ile oluşuyor. Sodyum klorür (NaCl), kalsiyum sülfat (CaSO₄) gibi örnekler günlük hayatta da karşına çıkıyor.
Değişken değerlik alan metaller için Roma rakamları kullanılıyor. FeCl₃ için "demir (III) klorür" diyoruz çünkü demir +3 değerlik alıyor.
Kovalent bileşikler Latin sayılarının ön ekleri ile adlandırılıyor. CO₂ karbon dioksit, N₂O₅ diazot pentaoksit oluyor. İlk elementi "mono" ile başlamıyoruz!
Katyonlar ve anyonlar tablosunu ezberlemen gerekiyor. NH₄⁺ amonyum, SO₄²⁻ sülfat gibi çok atomlu iyonlar özellikle önemli.
💡 Adlandırma Kuralı: İlk element sayı+isim, ikinci element sayı+anyon ismi şeklinde okunuyor!
Bazı özel durumlar var: NH₄ bileşikleri metal içermemesine rağmen iyonik bağlı, oksijen ilk elementse "oksijen" ikinci elementse "oksit" oluyor.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Zayıf Etkileşimler
Kimyasal bağlardan farklı olarak zayıf etkileşimler maddenin fiziksel halini belirliyor. Bu kuvvetler sayesinde su 100°C'de kaynıyor, yoksa çok daha düşük sıcaklıkta kaynar!
Hidrojen bağı en güçlü zayıf etkileşim. H₂O, NH₃, HF gibi moleküllerde H atomu F, O, N atomlarından birine bağlı olmalı. Su moleküleri arasında 4 hidrojen bağı kurulabiliyor.
Dipol-dipol etkileşimi polar moleküller arasında oluşuyor. HCl gibi moleküllerde δ+ ve δ- yüklü uçlar birbirini çekiyor.
London kuvvetleri tüm moleküller arasında bulunuyor ama apolar moleküllerde tek etkileşim türü. Molekül ağırlığı arttıkça kuvvet artıyor: I₂ > Br₂ > Cl₂ > F₂ sırası.
💡 Çözünürlük Kuralı: "Benzer benzeri çözer" - polar maddeler polarda, apolar maddeler apolarda çözünüyor!
İyon-dipol etkileşimi tuz suda çözünürken görülüyor. NaCl suda çözününce Na⁺ ve Cl⁻ iyonları su moleküllerinin dipolleri tarafından çevreleniyor.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Salts
1Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅