Asit ve bazların kuvveti hayatımızda çok önemli bir konu -... Daha fazla göster
Sulu Çözeltide Asit Baz Dengesi Nedir?



















Kuvvetli Asit ve Bazlar
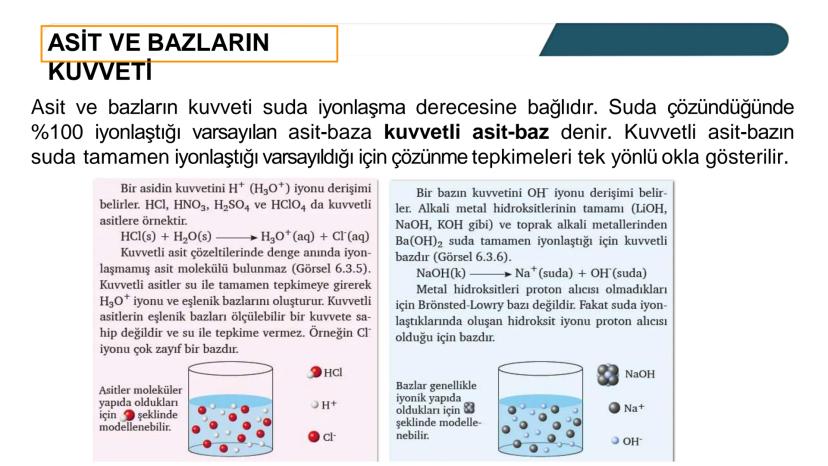
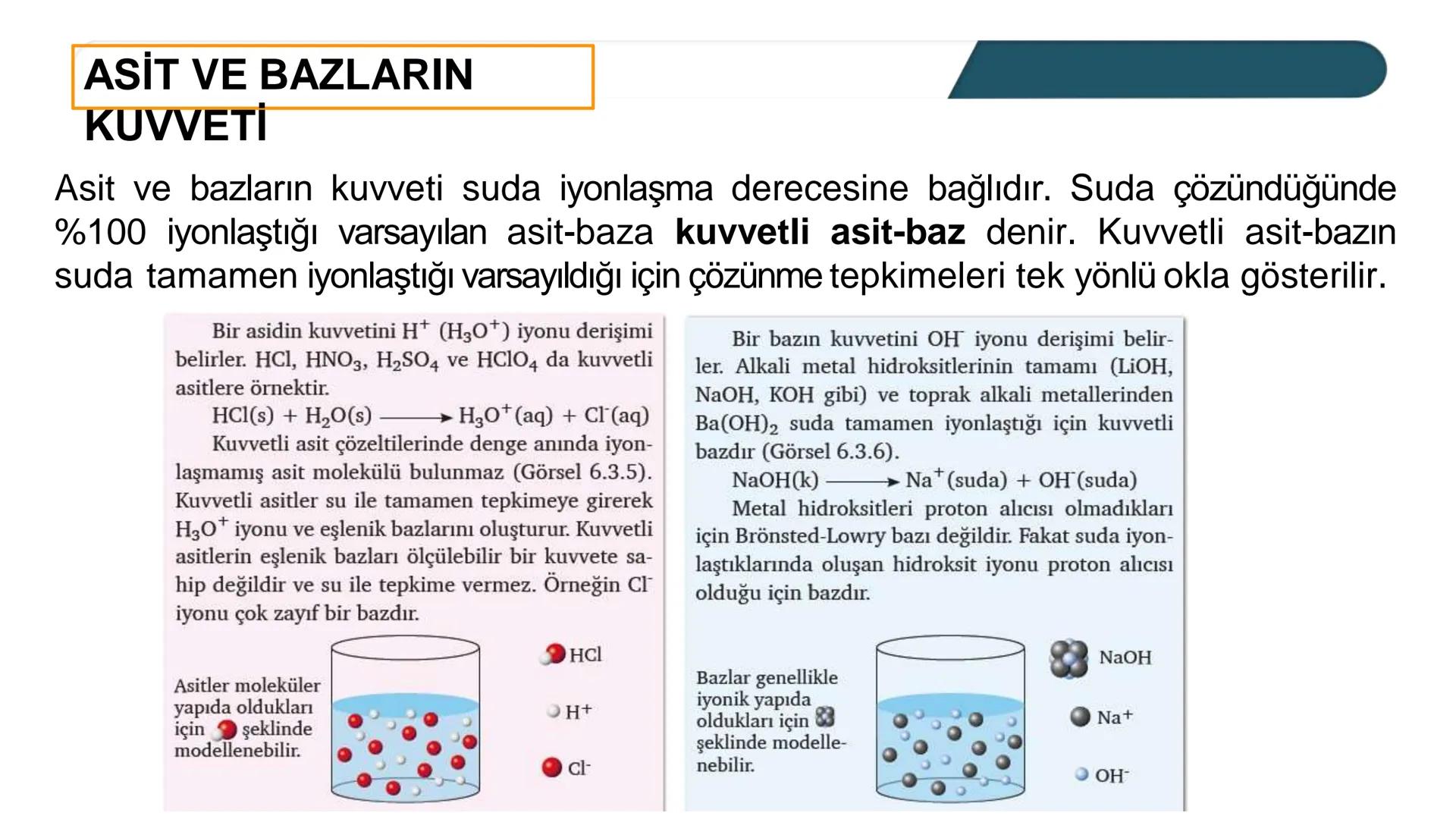
Kuvvetli asit ve bazlar suda %100 iyonlaşan maddelerdir - yani çözündüklerinde tamamen parçalanıp iyon haline geçerler. Bu yüzden tepkimelerini tek yönlü okla yazıyoruz çünkü geri dönüş yok!
Asidin gücünü H⁺ (H₃O⁺) iyonu derişimi belirler. HCl, HNO₃, H₂SO₄ gibi asitler kuvvetli asit örnekleridir. Mesela HCl suda tamamen çözünür: HCl + H₂O → H₃O⁺ + Cl⁻
Bazın gücünü ise OH⁻ iyonu derişimi belirler. NaOH, KOH gibi alkali metal hidroksitleri ve Ba(OH)₂ kuvvetli bazlardır. Bunlar da suda tamamen iyonlaşır.
Önemli: Kuvvetli asitlerin eşlenik bazları çok zayıftır ve pratikte hiç etki etmezler!

Zayıf Asit ve Bazlar
Zayıf asit ve bazlar suda kısmen iyonlaştığı için çok daha karmaşık davranırlar. Tepkimelerini çift yönlü okla yazıyoruz çünkü sürekli denge halindeler.
Zayıf asitlerin çözeltilerinde aynı anda üç şey bulunur: iyonlaşmamış asit molekülleri, H₃O⁺ iyonları ve eşlenik bazlar. CH₃COOH (sirke asidi), HF, HCN gibi asitler zayıf asittir.
Zayıf bazlarda da benzer durum var. NH₃ (amonyak) sudan proton alarak NH₄⁺ ve OH⁻ oluşturur: NH₃ + H₂O ⇌ NH₄⁺ + OH⁻
Dikkat: Asit ne kadar zayıfsa, eşlenik bazı o kadar kuvvetlidir - bu çok önemli bir kural!

Asit Gibi Davranan Katyonlar
Bazı katyonlar suda çözündüklerinde asit gibi davranır ve çözeltiyi asidik yaparlar. Bu biraz şaşırtıcı olabilir ama gayet mantıklı!
Zayıf bazların eşlenik asitleri (NH₄⁺ gibi) su ile tepkimeye girip proton verirler: NH₄⁺ + H₂O ⇌ NH₃ + H₃O⁺. Bu yüzden amonyum tuzları asidik çözeltiler oluşturur.
Çapı küçük, yükü büyük metal katyonları (Fe³⁺, Cr³⁺, Cu²⁺) su moleküllerini kendilerine çeker ve onları parçalar. Sonuçta H₃O⁺ iyonları oluşur ve çözelti asidik olur.
Pratik bilgi: Bu durum, bazı metal tuzlarının neden asidik çözelti verdiğini açıklıyor!

Baz Gibi Davranan Anyonlar
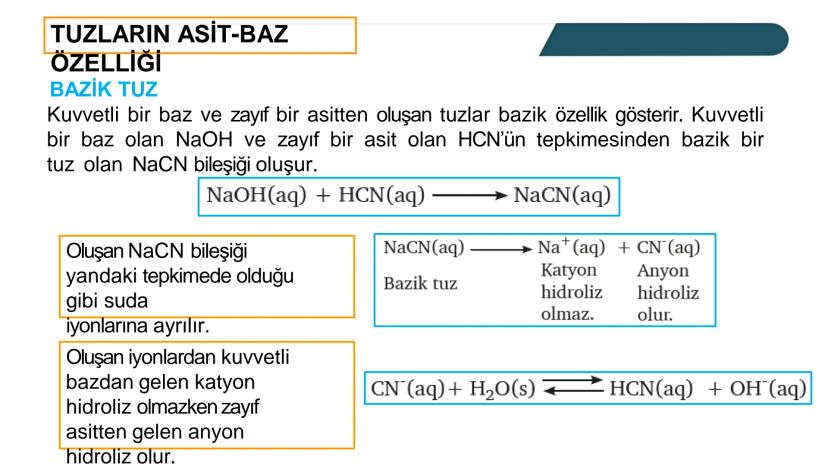
Zayıf asitlerin eşlenik bazları olan anyonlar su ile tepkimeye girip baz gibi davranırlar. Bu da çok mantıklı çünkü proton almaya meyilliler.
CN⁻, F⁻, NO₂⁻, CH₃COO⁻ gibi anyonlar sudan proton alıp OH⁻ iyonu oluştururlar. Mesela: CN⁻ + H₂O ⇌ HCN + OH⁻
Bu anyonlar zayıf asitlerin eşlenik bazları oldukları için ölçülebilir bazik kuvvete sahipler. Yani çözeltilerinin pH'ını 7'nin üzerine çıkarabilirler.
Hatırla: Zayıf asitlerin tuzları genellikle bazik çözelti verir!

Uygulama Soruları
Bu tür sorularda anyon ve katyonların kökenine bakman gerekiyor. Zayıf asitten mi, zayıf bazdan mı geliyorlar?
F⁻ anyonu: HF zayıf bir asidin eşlenik bazıdır, dolayısıyla baz gibi davranır: F⁻ + H₂O ⇌ HF + OH⁻
PO₄³⁻ anyonu: H₃PO₄ zayıf asidin eşlenik bazı olduğu için bazik özellik gösterir.
Fe³⁺ katyonu: Çapı küçük, yükü büyük metal katyonu olduğu için asit gibi davranır: Fe³⁺ + H₂O → Fe(OH)³ + H₃O⁺
İpucu: Anyon mu baz, katyon mu asit - bu genelleme çoğu zaman işe yarar!

Asit ve Bazların Ayrışma Dengesi
Zayıf asit ve bazlar için denge sabitlerini yazmak zorundayız çünkü tamamen iyonlaşmıyorlar. Bu sabitler asit ve bazların kuvvetini karşılaştırmamızı sağlıyor.
Zayıf bir asit HA için: HA + H₂O ⇌ H₃O⁺ + A⁻. Asitlik sabiti (Ka) şöyle yazılır: Ka = [H₃O⁺][A⁻]/[HA]
Ka değeri ne kadar büyükse asit o kadar kuvvetlidir. Çünkü daha çok iyonlaştığı anlamına gelir. Bu mantık çok basit: çok iyonlaşan = kuvvetli asit.
Suda iyonlaşma tepkimesinde su derişimi sabittir, bu yüzden denge ifadesine yazmıyoruz.
Önemli: Ka büyük = kuvvetli asit, Ka küçük = zayıf asit!

Bazların Ayrışma Dengesi
Zayıf bazlar için de bazlık sabiti (Kb) tanımlanır. Mantık aynen asitlerde olduğu gibi çalışır.
Zayıf baz MOH için: MOH ⇌ M⁺ + OH⁻. Bazlık sabiti şöyle yazılır: Kb = [M⁺][OH⁻]/[MOH]
Kb değeri büyük olan bazlar daha kuvvetlidir çünkü daha çok iyonlaşırlar. NH₃ gibi bazlar için de aynı mantık geçerli.
Pratik kural: Kb arttıkça bazın kuvveti artar. Bu sayede farklı bazları kolayca karşılaştırabilirsin.
Not: Denge sabitlerini ezberlemene gerek yok, her zaman soruda veriliyor!

NH₃ Çözeltisi Hesaplama Örneği
Bu tür problemlerde iyonlaşma yüzdesi isteniyor. NH₃'ın bazlık sabiti Kb = 1,8×10⁻⁵, derişim 0,02 M.
NH₃ + H₂O ⇌ NH₄⁺ + OH⁻ tepkimesi için denge tablosu kurman gerekiyor. Başlangıçta [NH₃] = 0,02 M, diğerleri sıfır.
α iyonlaşma yüzdesini temsil ederse, [OH⁻] = [NH₄⁺] = 0,02α ve [NH₃] = 0,02(1-α) olur. Kb ifadesine yerleştir ve α'yı çöz.
İpucu: α çok küçükse (α << 1) payda yaklaşık 0,02 alınabilir ve işlem basitleşir!

HNO₂ Asidi Hesaplama Örneği
Nitröz asit için Ka = 4,5×10⁻⁴, derişim 2 M veriliyor. Iyonlaşma yüzdesini bulmak için aynı yöntemi kullanıyoruz.
HNO₂ + H₂O ⇌ H₃O⁺ + NO₂⁻ tepkimesi için [H₃O⁺] = [NO₂⁻] = 2α ve [HNO₂] = 2(1-α) yazabilirsin.
Ka ifadesine yerleştirince: 4,5×10⁻⁴ = (2α)²/[2(1-α)] elde edersin. Bu denklemi çözdükten sonra α değerini yüzde olarak ifade et.
Dikkat: Bu örnekte α değeri büyük olabilir, o zaman paydada (1-α) yaklaşımı kullanma!











Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Acid-base Equilibria
1Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
Sulu Çözeltide Asit Baz Dengesi Nedir?
Asit ve bazların kuvveti hayatımızda çok önemli bir konu - çünkü vücudumuzdan günlük temizlik ürünlerine kadar her yerde karşılaştığımız maddelerin özelliklerini anlamamızı sağlıyor. Bu konuyu öğrendikten sonra neden bazı temizlik ürünlerinin çok güçlü olduğunu ya da midemizde neler olup bittiğini... Daha fazla göster

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Kuvvetli Asit ve Bazlar
Kuvvetli asit ve bazlar suda %100 iyonlaşan maddelerdir - yani çözündüklerinde tamamen parçalanıp iyon haline geçerler. Bu yüzden tepkimelerini tek yönlü okla yazıyoruz çünkü geri dönüş yok!
Asidin gücünü H⁺ (H₃O⁺) iyonu derişimi belirler. HCl, HNO₃, H₂SO₄ gibi asitler kuvvetli asit örnekleridir. Mesela HCl suda tamamen çözünür: HCl + H₂O → H₃O⁺ + Cl⁻
Bazın gücünü ise OH⁻ iyonu derişimi belirler. NaOH, KOH gibi alkali metal hidroksitleri ve Ba(OH)₂ kuvvetli bazlardır. Bunlar da suda tamamen iyonlaşır.
Önemli: Kuvvetli asitlerin eşlenik bazları çok zayıftır ve pratikte hiç etki etmezler!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Zayıf Asit ve Bazlar
Zayıf asit ve bazlar suda kısmen iyonlaştığı için çok daha karmaşık davranırlar. Tepkimelerini çift yönlü okla yazıyoruz çünkü sürekli denge halindeler.
Zayıf asitlerin çözeltilerinde aynı anda üç şey bulunur: iyonlaşmamış asit molekülleri, H₃O⁺ iyonları ve eşlenik bazlar. CH₃COOH (sirke asidi), HF, HCN gibi asitler zayıf asittir.
Zayıf bazlarda da benzer durum var. NH₃ (amonyak) sudan proton alarak NH₄⁺ ve OH⁻ oluşturur: NH₃ + H₂O ⇌ NH₄⁺ + OH⁻
Dikkat: Asit ne kadar zayıfsa, eşlenik bazı o kadar kuvvetlidir - bu çok önemli bir kural!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Asit Gibi Davranan Katyonlar
Bazı katyonlar suda çözündüklerinde asit gibi davranır ve çözeltiyi asidik yaparlar. Bu biraz şaşırtıcı olabilir ama gayet mantıklı!
Zayıf bazların eşlenik asitleri (NH₄⁺ gibi) su ile tepkimeye girip proton verirler: NH₄⁺ + H₂O ⇌ NH₃ + H₃O⁺. Bu yüzden amonyum tuzları asidik çözeltiler oluşturur.
Çapı küçük, yükü büyük metal katyonları (Fe³⁺, Cr³⁺, Cu²⁺) su moleküllerini kendilerine çeker ve onları parçalar. Sonuçta H₃O⁺ iyonları oluşur ve çözelti asidik olur.
Pratik bilgi: Bu durum, bazı metal tuzlarının neden asidik çözelti verdiğini açıklıyor!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Baz Gibi Davranan Anyonlar
Zayıf asitlerin eşlenik bazları olan anyonlar su ile tepkimeye girip baz gibi davranırlar. Bu da çok mantıklı çünkü proton almaya meyilliler.
CN⁻, F⁻, NO₂⁻, CH₃COO⁻ gibi anyonlar sudan proton alıp OH⁻ iyonu oluştururlar. Mesela: CN⁻ + H₂O ⇌ HCN + OH⁻
Bu anyonlar zayıf asitlerin eşlenik bazları oldukları için ölçülebilir bazik kuvvete sahipler. Yani çözeltilerinin pH'ını 7'nin üzerine çıkarabilirler.
Hatırla: Zayıf asitlerin tuzları genellikle bazik çözelti verir!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Uygulama Soruları
Bu tür sorularda anyon ve katyonların kökenine bakman gerekiyor. Zayıf asitten mi, zayıf bazdan mı geliyorlar?
F⁻ anyonu: HF zayıf bir asidin eşlenik bazıdır, dolayısıyla baz gibi davranır: F⁻ + H₂O ⇌ HF + OH⁻
PO₄³⁻ anyonu: H₃PO₄ zayıf asidin eşlenik bazı olduğu için bazik özellik gösterir.
Fe³⁺ katyonu: Çapı küçük, yükü büyük metal katyonu olduğu için asit gibi davranır: Fe³⁺ + H₂O → Fe(OH)³ + H₃O⁺
İpucu: Anyon mu baz, katyon mu asit - bu genelleme çoğu zaman işe yarar!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Asit ve Bazların Ayrışma Dengesi
Zayıf asit ve bazlar için denge sabitlerini yazmak zorundayız çünkü tamamen iyonlaşmıyorlar. Bu sabitler asit ve bazların kuvvetini karşılaştırmamızı sağlıyor.
Zayıf bir asit HA için: HA + H₂O ⇌ H₃O⁺ + A⁻. Asitlik sabiti (Ka) şöyle yazılır: Ka = [H₃O⁺][A⁻]/[HA]
Ka değeri ne kadar büyükse asit o kadar kuvvetlidir. Çünkü daha çok iyonlaştığı anlamına gelir. Bu mantık çok basit: çok iyonlaşan = kuvvetli asit.
Suda iyonlaşma tepkimesinde su derişimi sabittir, bu yüzden denge ifadesine yazmıyoruz.
Önemli: Ka büyük = kuvvetli asit, Ka küçük = zayıf asit!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Bazların Ayrışma Dengesi
Zayıf bazlar için de bazlık sabiti (Kb) tanımlanır. Mantık aynen asitlerde olduğu gibi çalışır.
Zayıf baz MOH için: MOH ⇌ M⁺ + OH⁻. Bazlık sabiti şöyle yazılır: Kb = [M⁺][OH⁻]/[MOH]
Kb değeri büyük olan bazlar daha kuvvetlidir çünkü daha çok iyonlaşırlar. NH₃ gibi bazlar için de aynı mantık geçerli.
Pratik kural: Kb arttıkça bazın kuvveti artar. Bu sayede farklı bazları kolayca karşılaştırabilirsin.
Not: Denge sabitlerini ezberlemene gerek yok, her zaman soruda veriliyor!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
NH₃ Çözeltisi Hesaplama Örneği
Bu tür problemlerde iyonlaşma yüzdesi isteniyor. NH₃'ın bazlık sabiti Kb = 1,8×10⁻⁵, derişim 0,02 M.
NH₃ + H₂O ⇌ NH₄⁺ + OH⁻ tepkimesi için denge tablosu kurman gerekiyor. Başlangıçta [NH₃] = 0,02 M, diğerleri sıfır.
α iyonlaşma yüzdesini temsil ederse, [OH⁻] = [NH₄⁺] = 0,02α ve [NH₃] = 0,02(1-α) olur. Kb ifadesine yerleştir ve α'yı çöz.
İpucu: α çok küçükse (α << 1) payda yaklaşık 0,02 alınabilir ve işlem basitleşir!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
HNO₂ Asidi Hesaplama Örneği
Nitröz asit için Ka = 4,5×10⁻⁴, derişim 2 M veriliyor. Iyonlaşma yüzdesini bulmak için aynı yöntemi kullanıyoruz.
HNO₂ + H₂O ⇌ H₃O⁺ + NO₂⁻ tepkimesi için [H₃O⁺] = [NO₂⁻] = 2α ve [HNO₂] = 2(1-α) yazabilirsin.
Ka ifadesine yerleştirince: 4,5×10⁻⁴ = (2α)²/[2(1-α)] elde edersin. Bu denklemi çözdükten sonra α değerini yüzde olarak ifade et.
Dikkat: Bu örnekte α değeri büyük olabilir, o zaman paydada (1-α) yaklaşımı kullanma!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Acid-base Equilibria
1Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅