Avogadro sayısı ve mol kavramı, kimyanın en temel konuları arasında... Daha fazla göster
Mol Kavramı Nedir? Açıklaması ve Örnekler











































Avogadro Sayısı ve Mol Kavramına Giriş
Günlük hayatta bazen maddeleri tek tek saymak yerine toplu olarak ifade etmeyi tercih ederiz. Nasıl ki 30 yumurtayı "1 koli yumurta", 12 silgiyi "1 düzine silgi" veya 10 kalemi "1 deste kalem" olarak ifade ediyoruz, benzer bir yaklaşımı atomlar için de kullanıyoruz.
Kimyada da çok küçük tanecikleri saymak için özel bir birime ihtiyaç duyarız. Çünkü atomlar ve moleküller o kadar küçüktür ki normal yollarla sayılamaz ve tartılamazlar.
⚠️ Dikkat: Nasıl buğdayı kile ile, çiviyi kilo ile ifade ediyorsak, atom ve molekül gibi mikroskobik tanecikleri de "mol" adı verilen özel bir birimle ifade ederiz.

Mol Kavramı ve Tanımı
Atomlar ve moleküller gözle göremeyeceğimiz ve normal yöntemlerle sayamayacağımız kadar küçük taneciklerdir. Bu yüzden onları tek tek saymak yerine mol kavramını kullanırız.
Bir mol, tam olarak 12 gram karbon-12 (12C) izotopunda bulunan atom sayısı kadar taneciği ifade eder. Bu rakam inanılmaz büyüktür ve bilimsel çalışmalarda kullanılması pratik değildir.
Günlük hayatta düzine, kilo, deste gibi kavramları kullanmamız gibi, kimya dünyasında da mol kavramı bize büyük kolaylık sağlar. Çok küçük tanecikleri anlamlı miktarlarda ifade etmemizi mümkün kılar.

Avogadro Sayısı
Avogadro sayısı, bir moldeki tanecik sayısını ifade eder ve NA ile gösterilir. Değeri 6,02214179 × 1023 mol-1'dir, ancak hesaplamalarda genellikle 6,02 × 1023 mol-1 olarak yuvarlatılır.
"mol-1" birimi, bir mol maddedeki tanecik sayısını gösterir. Bu sayı evrendeki en büyük sabit sayılardan biridir ve maddenin cinsinden bağımsızdır.
Buna göre 1 mol karbon, 6,02 × 1023 tane karbon atomu içerir ve kütlesi 12,011 gramdır. Benzer şekilde, 1 mol oksijen, 6,02 × 1023 tane oksijen atomu içerir ve kütlesi 15,9994 gramdır.
💡 İpucu: Mol sayısı ile atom/molekül sayısı arasındaki ilişkiyi anlaman, kimyada sayısal hesaplamaları kolaylıkla yapabilmeni sağlayacaktır.

Avogadro Sayısının Büyüklüğü
Avogadro sayısı (6,02 × 1023) hayal edilemeyecek kadar büyük bir sayıdır. Bu sayının büyüklüğünü anlamak için birkaç örnek düşünelim.
Eğer bir fasulye tanesinin hacmi 0,1 cm³ olsa, bir mol fasulye (yani 6,02 × 1023 adet fasulye) Türkiye'nin yüzeyini yaklaşık 72 km kalınlığında bir tabaka şeklinde kaplayacak kadardır!
Hatta 100 yıl yaşayan bir insan, saniyede bir sayı sayarak doğumundan ölümüne kadar ancak 3,15 × 109 sayısına kadar sayabilir. Dünyadaki 7 milyar insanın hepsi aynı işi yapsa bile, hep birlikte sadece 2,8 × 1019 sayısına kadar ulaşabilirler - ki bu, Avogadro sayısının çok altındadır.
Bu örnekler, Avogadro sayısının ne kadar büyük olduğunu ve atomların/moleküllerin ne kadar küçük olduklarını göstermektedir.

Moleküller ve Mol Kavramı
Elementlerin yapı taşları atomlardır. Buna göre 6,02 × 1023 tane atom, 1 mol elementi oluşturur. Örneğin, 6,02 × 1023 tane Zn atomu, 1 mol Zn elementine karşılık gelir.
Bileşiklerin ve moleküler elementlerin (H2, O2, P4 gibi) yapı taşları ise moleküllerdir. 6,02 × 1023 tane molekül, 1 mol bileşik veya 1 mol moleküler element demektir.
Örneğin:
- 6,02 × 1023 tane H2O molekülü = 1 mol su molekülü
- 6,02 × 1023 tane P4 molekülü = 1 mol P4 elementi
🔍 Unutma: 1 mol her zaman 6,02 × 1023 tanecik anlamına gelir, ancak bu taneciklerin ne olduğu (atom, molekül, iyon vb.) duruma göre değişir.

Tanecik Sayısı ve Mol Hesaplamaları
Tanecik sayısı verilen bir maddenin mol sayısını hesaplamak için şu formülü kullanabilirsin:
n = N / NA
Burada:
- n: Mol sayısı
- N: Verilen tanecik sayısı
- NA: Avogadro sayısı (6,02 × 1023)
Örneğin, 9,03 × 1023 tane CH4 molekülünün kaç mol olduğunu hesaplarsak: n = 9,03 × 1023 / 6,02 × 1023 = 1,5 mol
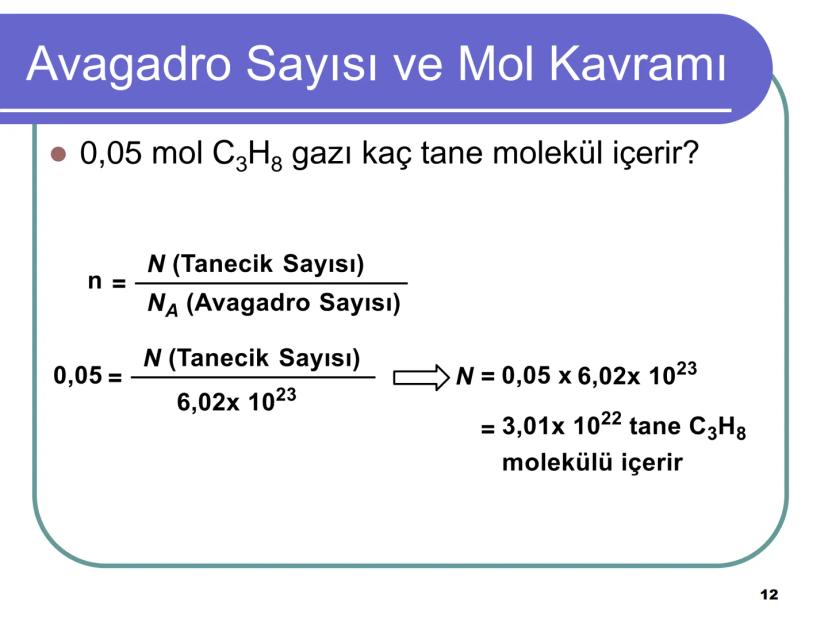
Tam tersi olarak, 0,05 mol C3H8 gazının kaç molekül içerdiğini bulmak için: N = n × NA = 0,05 × 6,02 × 1023 = 3,01 × 1022 tane C3H8 molekülü
Bu hesaplamalar, kimyasal maddelerin miktar ilişkilerini anlamamızı sağlar.

Formül ve Molekül Kütlesi
Formül kütlesi iyonik bileşikler için, molekül kütlesi (veya mol kütlesi) ise moleküler bileşikler için kullanılan terimlerdir. Her ikisi de benzer şekilde hesaplanır.
Bir bileşiğin formül veya molekül kütlesini bulmak için, o bileşiğin formülündeki her elementin atom sayısı ile atom kütlesi çarpılır ve bu değerler toplanır. Sonuç, akb (atom kütlesi birimi) veya g/mol olarak ifade edilir.
Örneğin, yangın söndürücü olarak kullanılan halotan (C2HBrClF3) molekülünün kütlesini hesaplayalım:
- C: 2 × 12 = 24 g/mol
- H: 1 × 1 = 1 g/mol
- Br: 1 × 80 = 80 g/mol
- Cl: 1 × 35,5 = 35,5 g/mol
- F: 3 × 19 = 57 g/mol
- Toplam: 197,5 g/mol
📝 Not: Molekül kütlesi hesaplamaları, kimyasal tepkimelerdeki kütle ilişkilerini anlamak için temel oluşturur.

Mol Sayısı ve Kütle İlişkisi
Bir maddenin mol sayısı ile kütlesi arasında şu ilişki vardır:
n = m / MA
Burada:
- n: Mol sayısı
- m: Verilen kütle (g)
- MA: Mol kütlesi
Örnek: 1 gram CaCO3 kaç moldür? Önce CaCO3'ün mol kütlesini hesaplayalım: CaCO3: (1 × 40) + (1 × 12) + (3 × 16) = 100 g/mol
Şimdi formülü uygulayalım: n = 1 g / 100 g/mol = 0,01 mol
Başka bir örnek: 23,3 g Zn kaç moldür? Zn'nin atom kütlesi 65,39 g/mol olduğuna göre: n = 23,3 g / 65,39 g/mol = 0,356 mol
Bu hesaplamalar laboratuvarda maddelerin ölçülmesi için çok önemlidir.

Kimyasal Formülden Yüzde Bileşim Hesabı
Bir bileşiğin yüzde bileşimi, o bileşiği oluşturan elementlerin kütlece yüzde oranlarını ifade eder. Formülden yüzde bileşimi hesaplamak için şu adımları izleyebilirsin:
- Bileşiğin mol kütlesini hesapla
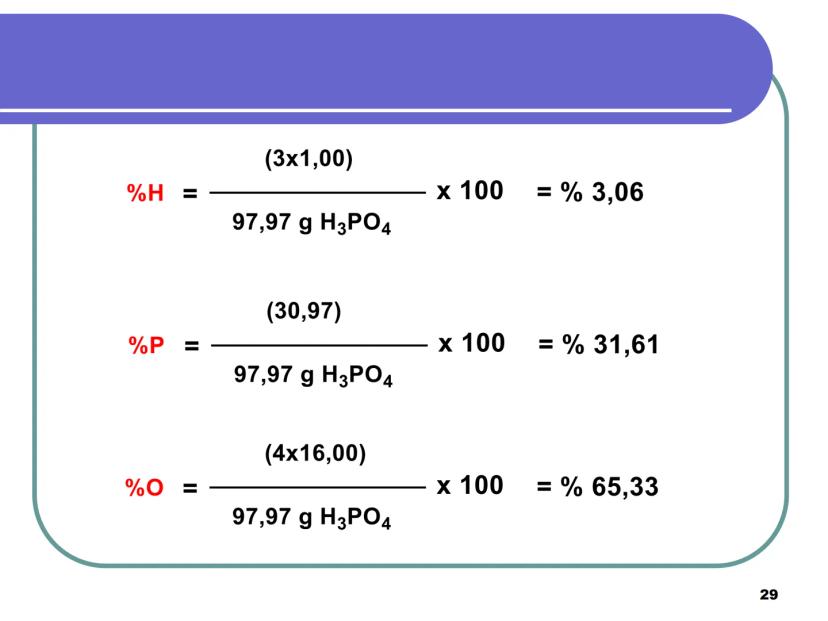
- Her elementin toplam kütlesini bul (atom kütlesi × atom sayısı)
- Her elementin kütlesini toplam mol kütlesine böl ve 100 ile çarp
Örneğin, C2HBrClF3'ün yüzde bileşimini hesaplayalım:
- Mol kütlesi: 197,5 g/mol
- % C = [(2 × 12) / 197,5] × 100 = %12,15
- % H = [1,0 / 197,5] × 100 = %0,51
- % Br = [80 / 197,5] × 100 = %40,50
- % Cl = [35,5 / 197,5] × 100 = %17,98
- % F = [(3 × 19) / 197,5] × 100 = %28,86
💯 İpucu: Yüzdelerin toplamı her zaman %100 olmalıdır. Hesaplarını kontrol etmek için bu yöntemi kullanabilirsin!

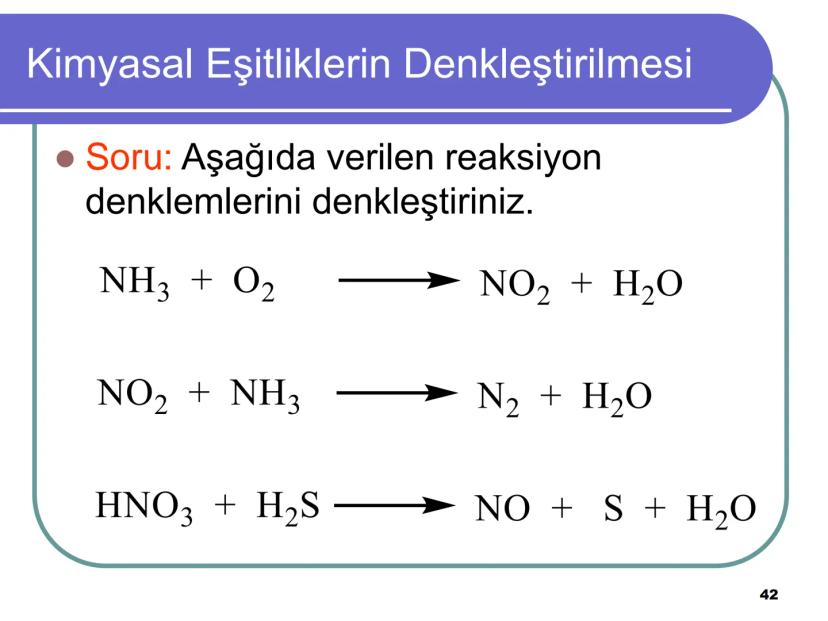
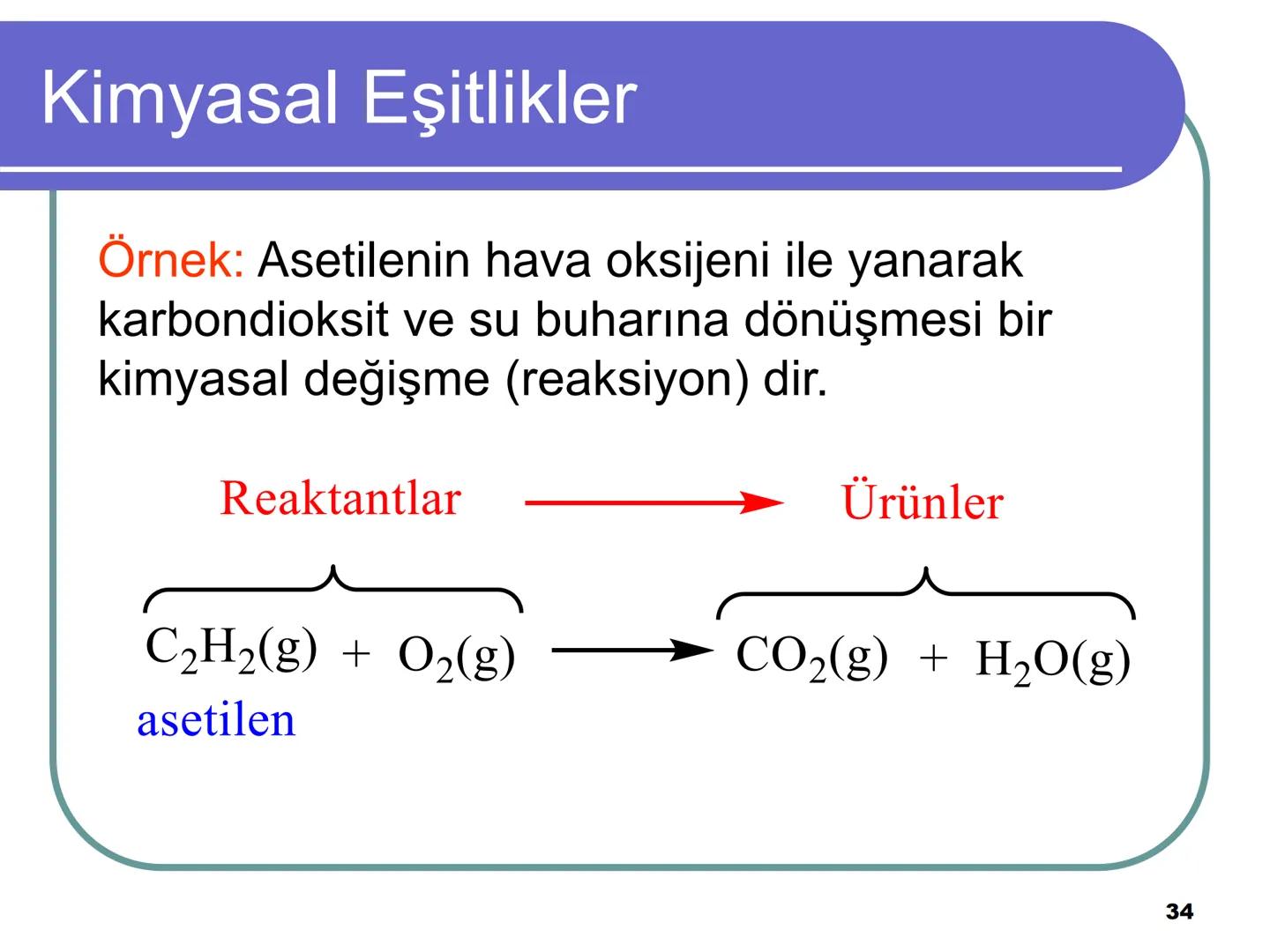
Kimyasal Reaksiyonlar
Kimyasal reaksiyon (tepkime), kimyasal maddelerdeki değişme olayıdır. Bu süreçte maddeler birbirleriyle etkileşerek yeni ürünler oluştururlar.
Günlük hayatta birçok kimyasal reaksiyon örneği görürüz:
- Gümüşün kararması
- Doğal gazın yanarak enerji üretmesi
- Üzüm suyunun sirkeye dönüşmesi
Bir kimyasal reaksiyonun gerçekleştiğini anlamak için şu belirtilere dikkat edebilirsin:
- Renk değişimi
- Katı oluşumu (çökelme)
- Gaz çıkışı (kabarcıklar)
- Isı enerjisi açığa çıkması veya soğurulması
Kimyasal reaksiyonlar, maddenin iç yapısının değiştiği olaylar olduğu için fiziksel değişimlerden farklıdır.


































Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Mole
910 sınıf kimya mol kavramı
Mol kavramı özellikleri kavramlar ve örnek sorular konu anlatım ders notu
Mol Kavramı
Mol Kavramı
Mol kavramı
mol kavramı konu anlatımı ve çözümlü örnekler
Mol kavramı
Mol kavramı ve hesaplamalarını anlatır
Kimya mol kavramı
10 sınıf kimya dersinde mol kavramı konusunda konu anlatımı
Mol kavramı
Mol kavramını burdan öğrenebilirsiniz
MOL KAVRAMI 10 SINIF KIMYA
Kimya 10 sinif
Mol kavramı
10. sınıf kimya mol kavramı ve kütle hacim ilişkileri
Mol Kavramı
Mol Kavramı
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
Mol Kavramı Nedir? Açıklaması ve Örnekler
Avogadro sayısı ve mol kavramı, kimyanın en temel konuları arasında yer alır ve maddelerin tanecik düzeyinde anlaşılmasını sağlar. Bu konular, günlük hayatta kullandığımız sayma yöntemlerinden farklı olarak, gözle göremediğimiz atomları ve molekülleri saymak için kullanılan özel birimlerdir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Avogadro Sayısı ve Mol Kavramına Giriş
Günlük hayatta bazen maddeleri tek tek saymak yerine toplu olarak ifade etmeyi tercih ederiz. Nasıl ki 30 yumurtayı "1 koli yumurta", 12 silgiyi "1 düzine silgi" veya 10 kalemi "1 deste kalem" olarak ifade ediyoruz, benzer bir yaklaşımı atomlar için de kullanıyoruz.
Kimyada da çok küçük tanecikleri saymak için özel bir birime ihtiyaç duyarız. Çünkü atomlar ve moleküller o kadar küçüktür ki normal yollarla sayılamaz ve tartılamazlar.
⚠️ Dikkat: Nasıl buğdayı kile ile, çiviyi kilo ile ifade ediyorsak, atom ve molekül gibi mikroskobik tanecikleri de "mol" adı verilen özel bir birimle ifade ederiz.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Mol Kavramı ve Tanımı
Atomlar ve moleküller gözle göremeyeceğimiz ve normal yöntemlerle sayamayacağımız kadar küçük taneciklerdir. Bu yüzden onları tek tek saymak yerine mol kavramını kullanırız.
Bir mol, tam olarak 12 gram karbon-12 (12C) izotopunda bulunan atom sayısı kadar taneciği ifade eder. Bu rakam inanılmaz büyüktür ve bilimsel çalışmalarda kullanılması pratik değildir.
Günlük hayatta düzine, kilo, deste gibi kavramları kullanmamız gibi, kimya dünyasında da mol kavramı bize büyük kolaylık sağlar. Çok küçük tanecikleri anlamlı miktarlarda ifade etmemizi mümkün kılar.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Avogadro Sayısı
Avogadro sayısı, bir moldeki tanecik sayısını ifade eder ve NA ile gösterilir. Değeri 6,02214179 × 1023 mol-1'dir, ancak hesaplamalarda genellikle 6,02 × 1023 mol-1 olarak yuvarlatılır.
"mol-1" birimi, bir mol maddedeki tanecik sayısını gösterir. Bu sayı evrendeki en büyük sabit sayılardan biridir ve maddenin cinsinden bağımsızdır.
Buna göre 1 mol karbon, 6,02 × 1023 tane karbon atomu içerir ve kütlesi 12,011 gramdır. Benzer şekilde, 1 mol oksijen, 6,02 × 1023 tane oksijen atomu içerir ve kütlesi 15,9994 gramdır.
💡 İpucu: Mol sayısı ile atom/molekül sayısı arasındaki ilişkiyi anlaman, kimyada sayısal hesaplamaları kolaylıkla yapabilmeni sağlayacaktır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Avogadro Sayısının Büyüklüğü
Avogadro sayısı (6,02 × 1023) hayal edilemeyecek kadar büyük bir sayıdır. Bu sayının büyüklüğünü anlamak için birkaç örnek düşünelim.
Eğer bir fasulye tanesinin hacmi 0,1 cm³ olsa, bir mol fasulye (yani 6,02 × 1023 adet fasulye) Türkiye'nin yüzeyini yaklaşık 72 km kalınlığında bir tabaka şeklinde kaplayacak kadardır!
Hatta 100 yıl yaşayan bir insan, saniyede bir sayı sayarak doğumundan ölümüne kadar ancak 3,15 × 109 sayısına kadar sayabilir. Dünyadaki 7 milyar insanın hepsi aynı işi yapsa bile, hep birlikte sadece 2,8 × 1019 sayısına kadar ulaşabilirler - ki bu, Avogadro sayısının çok altındadır.
Bu örnekler, Avogadro sayısının ne kadar büyük olduğunu ve atomların/moleküllerin ne kadar küçük olduklarını göstermektedir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Moleküller ve Mol Kavramı
Elementlerin yapı taşları atomlardır. Buna göre 6,02 × 1023 tane atom, 1 mol elementi oluşturur. Örneğin, 6,02 × 1023 tane Zn atomu, 1 mol Zn elementine karşılık gelir.
Bileşiklerin ve moleküler elementlerin (H2, O2, P4 gibi) yapı taşları ise moleküllerdir. 6,02 × 1023 tane molekül, 1 mol bileşik veya 1 mol moleküler element demektir.
Örneğin:
- 6,02 × 1023 tane H2O molekülü = 1 mol su molekülü
- 6,02 × 1023 tane P4 molekülü = 1 mol P4 elementi
🔍 Unutma: 1 mol her zaman 6,02 × 1023 tanecik anlamına gelir, ancak bu taneciklerin ne olduğu (atom, molekül, iyon vb.) duruma göre değişir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Tanecik Sayısı ve Mol Hesaplamaları
Tanecik sayısı verilen bir maddenin mol sayısını hesaplamak için şu formülü kullanabilirsin:
n = N / NA
Burada:
- n: Mol sayısı
- N: Verilen tanecik sayısı
- NA: Avogadro sayısı (6,02 × 1023)
Örneğin, 9,03 × 1023 tane CH4 molekülünün kaç mol olduğunu hesaplarsak: n = 9,03 × 1023 / 6,02 × 1023 = 1,5 mol
Tam tersi olarak, 0,05 mol C3H8 gazının kaç molekül içerdiğini bulmak için: N = n × NA = 0,05 × 6,02 × 1023 = 3,01 × 1022 tane C3H8 molekülü
Bu hesaplamalar, kimyasal maddelerin miktar ilişkilerini anlamamızı sağlar.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Formül ve Molekül Kütlesi
Formül kütlesi iyonik bileşikler için, molekül kütlesi (veya mol kütlesi) ise moleküler bileşikler için kullanılan terimlerdir. Her ikisi de benzer şekilde hesaplanır.
Bir bileşiğin formül veya molekül kütlesini bulmak için, o bileşiğin formülündeki her elementin atom sayısı ile atom kütlesi çarpılır ve bu değerler toplanır. Sonuç, akb (atom kütlesi birimi) veya g/mol olarak ifade edilir.
Örneğin, yangın söndürücü olarak kullanılan halotan (C2HBrClF3) molekülünün kütlesini hesaplayalım:
- C: 2 × 12 = 24 g/mol
- H: 1 × 1 = 1 g/mol
- Br: 1 × 80 = 80 g/mol
- Cl: 1 × 35,5 = 35,5 g/mol
- F: 3 × 19 = 57 g/mol
- Toplam: 197,5 g/mol
📝 Not: Molekül kütlesi hesaplamaları, kimyasal tepkimelerdeki kütle ilişkilerini anlamak için temel oluşturur.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Mol Sayısı ve Kütle İlişkisi
Bir maddenin mol sayısı ile kütlesi arasında şu ilişki vardır:
n = m / MA
Burada:
- n: Mol sayısı
- m: Verilen kütle (g)
- MA: Mol kütlesi
Örnek: 1 gram CaCO3 kaç moldür? Önce CaCO3'ün mol kütlesini hesaplayalım: CaCO3: (1 × 40) + (1 × 12) + (3 × 16) = 100 g/mol
Şimdi formülü uygulayalım: n = 1 g / 100 g/mol = 0,01 mol
Başka bir örnek: 23,3 g Zn kaç moldür? Zn'nin atom kütlesi 65,39 g/mol olduğuna göre: n = 23,3 g / 65,39 g/mol = 0,356 mol
Bu hesaplamalar laboratuvarda maddelerin ölçülmesi için çok önemlidir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Kimyasal Formülden Yüzde Bileşim Hesabı
Bir bileşiğin yüzde bileşimi, o bileşiği oluşturan elementlerin kütlece yüzde oranlarını ifade eder. Formülden yüzde bileşimi hesaplamak için şu adımları izleyebilirsin:
- Bileşiğin mol kütlesini hesapla
- Her elementin toplam kütlesini bul (atom kütlesi × atom sayısı)
- Her elementin kütlesini toplam mol kütlesine böl ve 100 ile çarp
Örneğin, C2HBrClF3'ün yüzde bileşimini hesaplayalım:
- Mol kütlesi: 197,5 g/mol
- % C = [(2 × 12) / 197,5] × 100 = %12,15
- % H = [1,0 / 197,5] × 100 = %0,51
- % Br = [80 / 197,5] × 100 = %40,50
- % Cl = [35,5 / 197,5] × 100 = %17,98
- % F = [(3 × 19) / 197,5] × 100 = %28,86
💯 İpucu: Yüzdelerin toplamı her zaman %100 olmalıdır. Hesaplarını kontrol etmek için bu yöntemi kullanabilirsin!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Kimyasal Reaksiyonlar
Kimyasal reaksiyon (tepkime), kimyasal maddelerdeki değişme olayıdır. Bu süreçte maddeler birbirleriyle etkileşerek yeni ürünler oluştururlar.
Günlük hayatta birçok kimyasal reaksiyon örneği görürüz:
- Gümüşün kararması
- Doğal gazın yanarak enerji üretmesi
- Üzüm suyunun sirkeye dönüşmesi
Bir kimyasal reaksiyonun gerçekleştiğini anlamak için şu belirtilere dikkat edebilirsin:
- Renk değişimi
- Katı oluşumu (çökelme)
- Gaz çıkışı (kabarcıklar)
- Isı enerjisi açığa çıkması veya soğurulması
Kimyasal reaksiyonlar, maddenin iç yapısının değiştiği olaylar olduğu için fiziksel değişimlerden farklıdır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Mole
910 sınıf kimya mol kavramı
Mol kavramı özellikleri kavramlar ve örnek sorular konu anlatım ders notu
Mol Kavramı
Mol Kavramı
Mol kavramı
mol kavramı konu anlatımı ve çözümlü örnekler
Mol kavramı
Mol kavramı ve hesaplamalarını anlatır
Kimya mol kavramı
10 sınıf kimya dersinde mol kavramı konusunda konu anlatımı
Mol kavramı
Mol kavramını burdan öğrenebilirsiniz
MOL KAVRAMI 10 SINIF KIMYA
Kimya 10 sinif
Mol kavramı
10. sınıf kimya mol kavramı ve kütle hacim ilişkileri
Mol Kavramı
Mol Kavramı
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅