Mol kavramı, kimyasal hesaplamaların temelini oluşturan ve madde miktarını anlamak... Daha fazla göster
Mol Kavramı Nedir? Kolay Anlatım





















Mol Kavramı Nedir?
Mol, Latince "büyük yığın" anlamına gelen ve küçük maddelerin oluşturduğu grupları tanımlamaya yarayan bir ölçü birimidir. Günlük hayatta düzine (12 tane) veya deste (10 tane) gibi grup adları kullanırız, kimyada ise 1 mol = 6,02×10²³ tane olarak tanımlanır.
Bu sayı Avogadro sayısı olarak bilinir ve kısaca Na veya No ile gösterilir. Avogadro sayısı o kadar büyüktür ki, atomlar ve moleküller gibi gözle göremediğimiz çok küçük tanecikleri pratik şekilde sayabilmemizi sağlar.
Not: Mol kavramı, nasıl ki 1 düzine her zaman 12 tane ise, 1 mol de her zaman 6,02×10²³ tanecik içerir. Bu sayı tanecik türünden bağımsızdır.

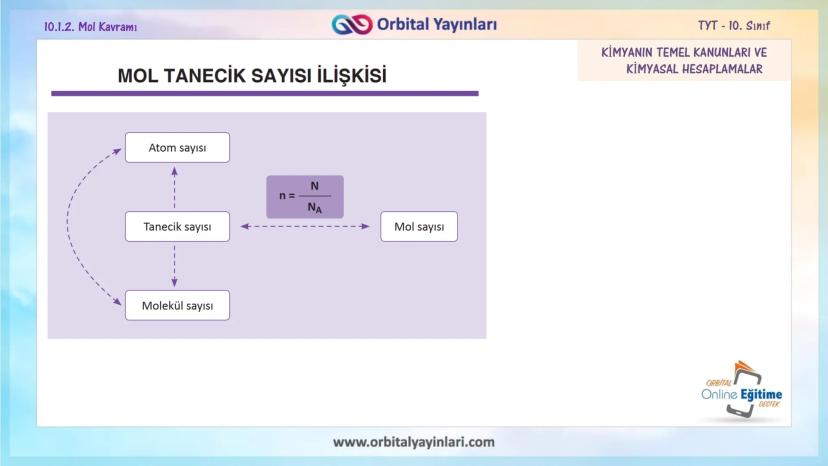
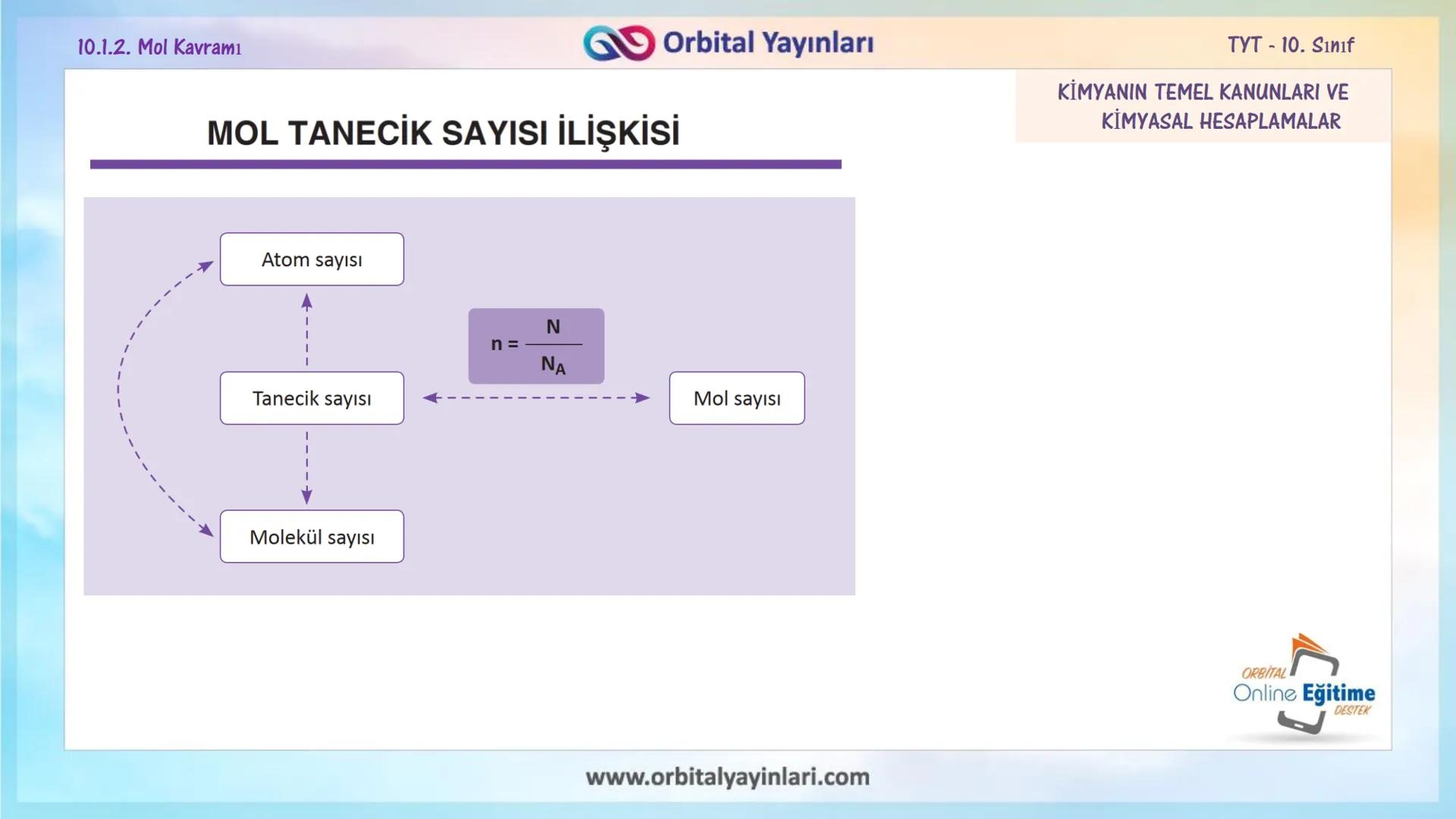
Mol-Tanecik Sayısı İlişkisi
Mol ile tanecik sayısı arasında doğrudan bir bağlantı vardır. Örneğin:
- 1 mol Fe elementi = 6,02×10²³ tane Fe atomu
- 2 mol He elementi = 12,04×10²³ tane He atomu
- 1 mol H₂O bileşiği = 6,02×10²³ tane H₂O molekülü
Mol sayısı ile tanecik sayısı arasında şöyle bir matematiksel ilişki vardır:
n = N/Nₐ
Burada;
- n: Mol sayısı
- N: Tanecik sayısı
- Nₐ: Avogadro sayısı (6,02×10²³)
1 molekül CO₂ ile 1 mol CO₂ arasındaki fark önemlidir. Birincisi tek bir molekülü, ikincisi ise 6,02×10²³ tane CO₂ molekülünü ifade eder.

Bileşiklerde Mol Hesaplamaları
Bileşiklerdeki atom sayıları, formüldeki atom sayılarıyla mol sayısı çarpılarak bulunur. Örneğin:
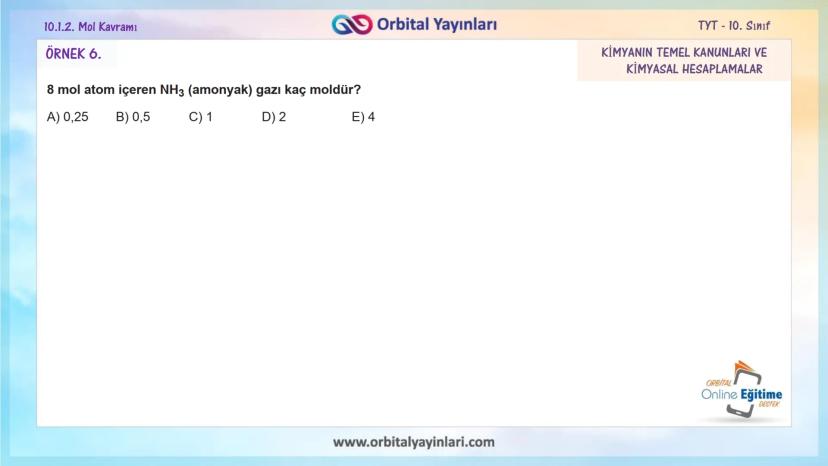
1 mol H₃PO₄ bileşiğinde:
- 3 mol H atomu
- 1 mol P atomu
- 4 mol O atomu Toplam: 8 mol atom bulunur
0,2 mol H₃PO₄ bileşiğinde ise:
- 0,6 mol H atomu (0,2 × 3)
- 0,2 mol P atomu (0,2 × 1)
- 0,8 mol O atomu (0,2 × 4) Toplam: 1,6 mol atom bulunur
Önemli: Bir bileşiğin içerdiği toplam atom sayısını bulmak için, formüldeki her elementin atom sayısını toplayıp, mol sayısıyla çarpmanız gerekir.

Mol-Kütle İlişkisi
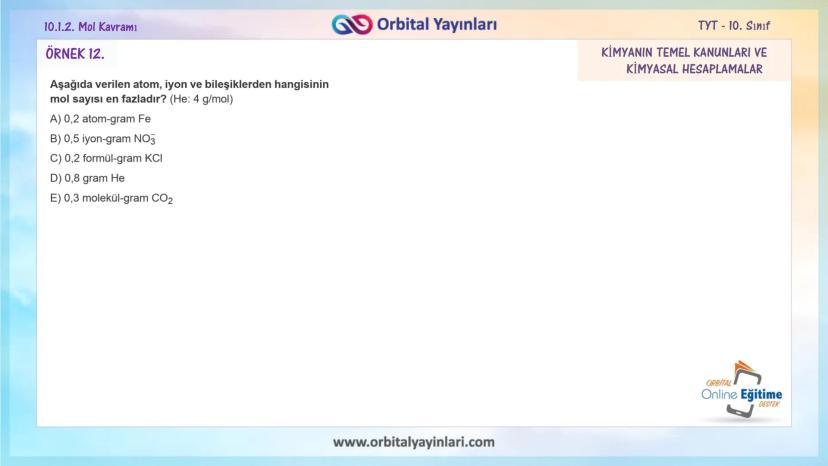
Bir elementin 1 mol atomunun gram cinsinden kütlesine o elementin mol kütlesi (atom kütlesi, Mₐ) denir. Örneğin, He elementinin mol kütlesi 4 g/mol'dür.
Bu bilgiyle:
- 1 mol He elementi = 4 gram
- 2 mol He elementi = 8 gram
- 0,2 mol He elementi = 0,8 gram
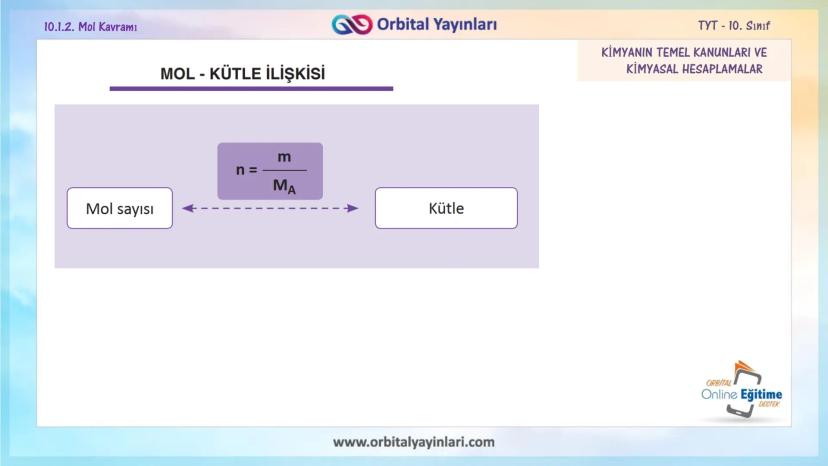
Kütle ile mol sayısı arasındaki matematiksel ilişki şöyledir:
n = m/Mₐ
Burada;
- n: Mol sayısı
- m: Kütle (gram)
- Mₐ: Mol kütlesi
Kolaylaştırıcı İpucu: Eğer bir elementin kaç mol olduğunu bulmak istiyorsanız, kütlesini (g) mol kütlesine bölmeniz yeterlidir.

Bileşiklerin Mol Kütlesi
Bir bileşiğin mol kütlesi, onu oluşturan elementlerin atom kütlelerinin toplamıdır. Örneğin:
H₂O bileşiğinin mol kütlesi = (2 × 1) + (1 × 16) = 18 g/mol
CaCO₃ bileşiğinde:
- 1 mol Ca = 40 g
- 1 mol C = 12 g
- 3 mol O = 48 g Toplam: 100 g/mol
Bu bilgiler, kimyasal hesaplamalarda çok işinize yarayacak. Örneğin, 18 gram su yaklaşık 1 mol H₂O molekülü içerir ve bu da 6,02×10²³ tane su molekülü demektir.
Sınavlarda hesaplamalarınızı doğru yapabilmeniz için element atom kütleleri genellikle sorularda verilir.
Mol-Hacim İlişkisi
Gazlarla çalışırken bilmeniz gereken önemli bir bilgi: Normal koşullarda (0°C ve 1 atm basınçta) 1 mol gaz 22,4 litre hacim kaplar. Bu değer, gazın türünden bağımsızdır!
Örneğin:
- NK'da 1 mol He gazı = 22,4 L
- NK'da 2 mol He gazı = 44,8 L
- NK'da 1 mol CO₂ gazı = 22,4 L
- NK'da 0,5 mol CO₂ gazı = 11,2 L
Normal koşullarda gazların hacmi ile mol sayısı arasındaki matematiksel ilişki şöyledir:
n = V/22,4
Burada;
- n: Mol sayısı
- V: Hacim (litre)
Bu bilgi, gaz hacmi ve mol sayısı arasında dönüşüm yapmanıza olanak sağlar.

Atomik Kütle Birimi (akb)
1 atomik kütle birimi (akb), 1 tane ¹²C izotopunun kütlesinin 1/12'sine eşittir ve çok küçük bir kütle birimidir. Elementlerin akb türünden kütlelerine bağıl atom kütlesi denir.
Kütle birimleri arasındaki ilişki:
- 1 ton = 1000 kg
- 1 kg = 1000 g
- 1 g = 6,02×10²³ akb
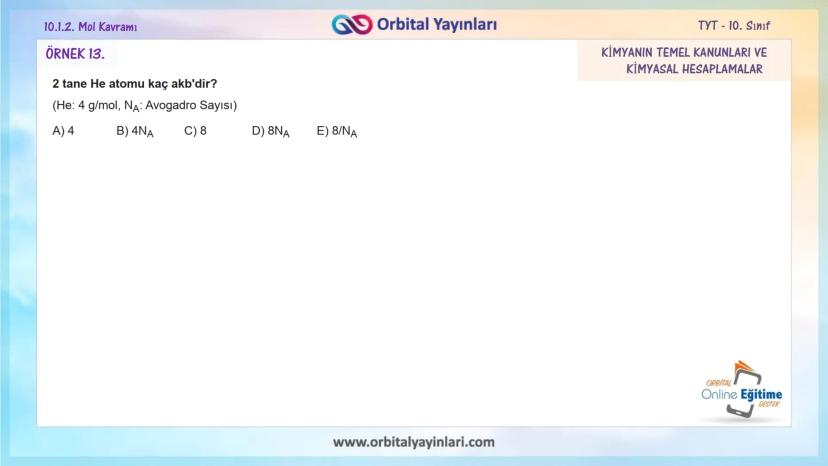
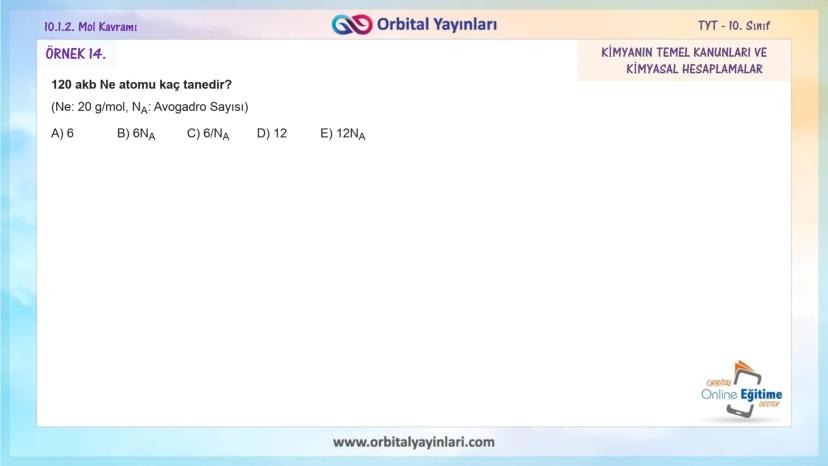
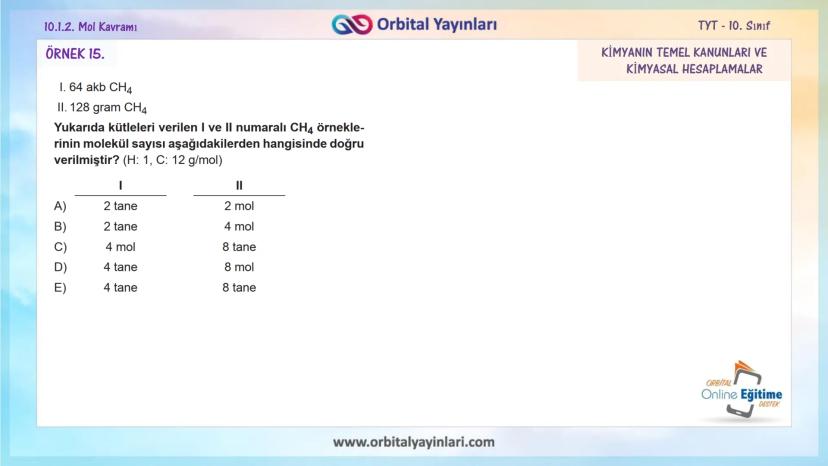
Tek bir atomun kütlesi çok küçük olduğundan, akb ile ifade edilir. Örneğin:
- 1 mol C (12 gram) = 6,02×10²³ tane C atomu (her biri 12 akb)
- 1 mol H₂O (18 gram) = 6,02×10²³ tane H₂O molekülü (her biri 18 akb)
Hatırlatma: 1 akb aynı zamanda 1 tane protonun kütlesine eşit kabul edilir. Akb sayısal değer olarak mol kütlesiyle aynıdır .
Mol Kavramında Formüller Özeti
Mol kavramıyla ilgili tüm hesaplamalarda kullanabileceğiniz temel formüller:
-
Mol-Tanecik Sayısı İlişkisi: n = N/Nₐ (n: mol sayısı, N: tanecik sayısı, Nₐ: Avogadro sayısı)
-
Mol-Kütle İlişkisi: n = m/Mₐ (n: mol sayısı, m: kütle (g), Mₐ: mol kütlesi)
-
Mol-Hacim İlişkisi (NK'da Gazlar için): n = V/22,4 (n: mol sayısı, V: hacim (L))
Bu formüller arasında dönüşüm yapabilmek, kimyasal hesaplamalarda size büyük kolaylık sağlayacaktır. Herhangi birini bildiğinizde, diğer niceliklerini kolayca hesaplayabilirsiniz.
Örnek: 4 gram CH₄ gazı kaç moldür? Kaç molekül içerir? NK'da hacmi nedir?
Mol Kavramı Uygulama Örnekleri
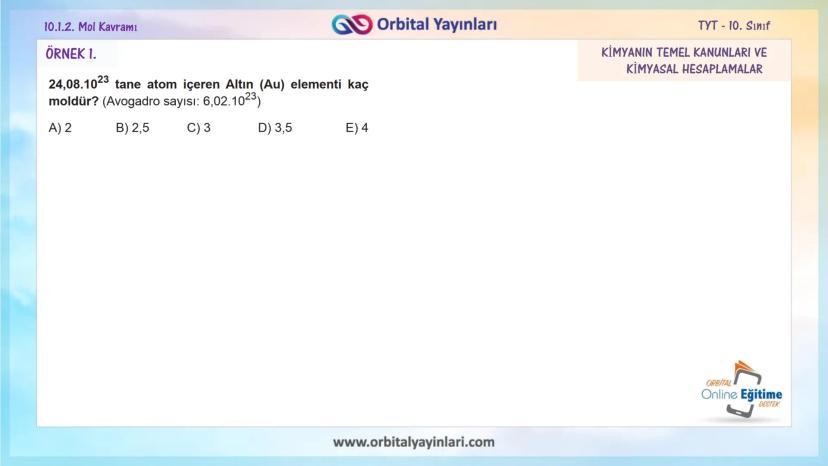
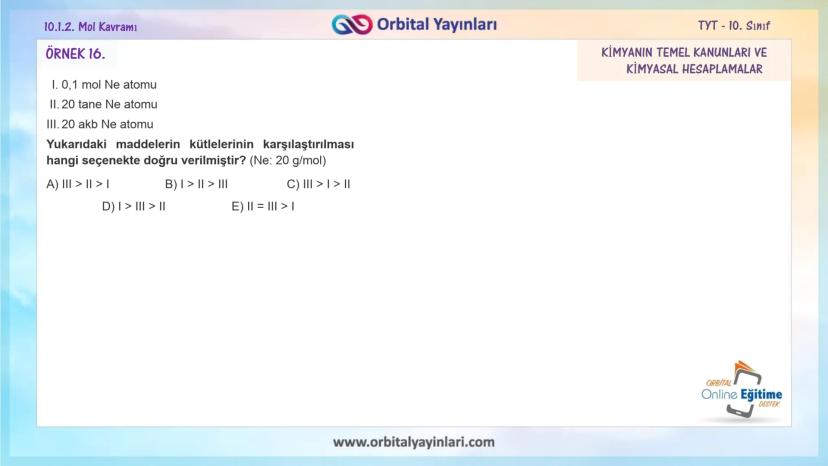
Örnek 1: 24,08×10²³ tane atom içeren Altın (Au) elementi kaç moldür?
- n = N/Nₐ = 24,08×10²³ / 6,02×10²³ = 4 mol
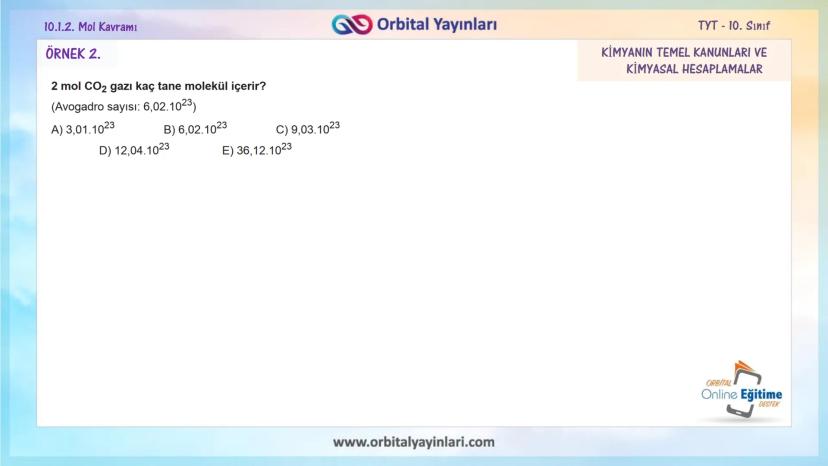
Örnek 2: 2 mol CO₂ gazı kaç tane molekül içerir?
- N = n × Nₐ = 2 × 6,02×10²³ = 12,04×10²³ molekül
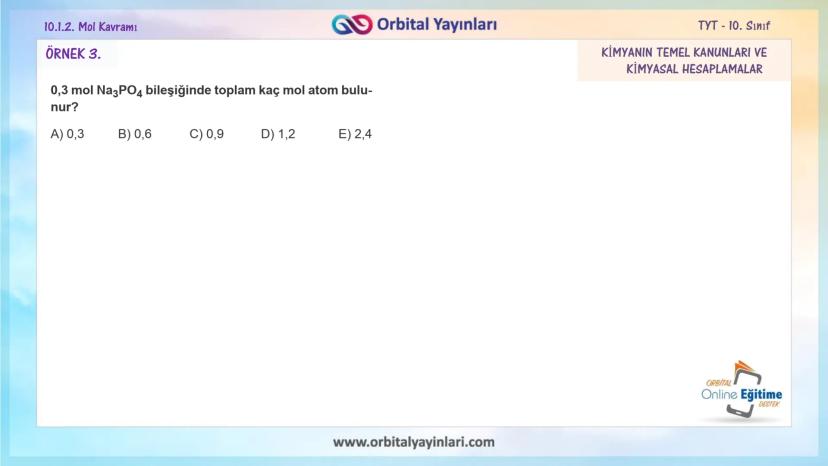
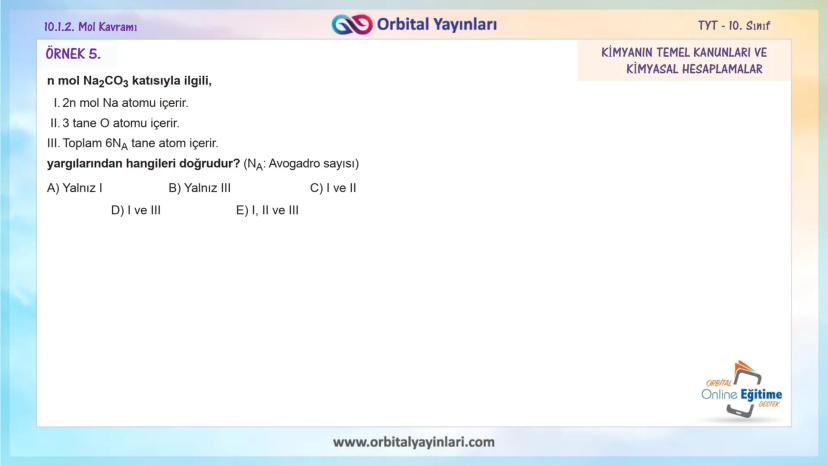
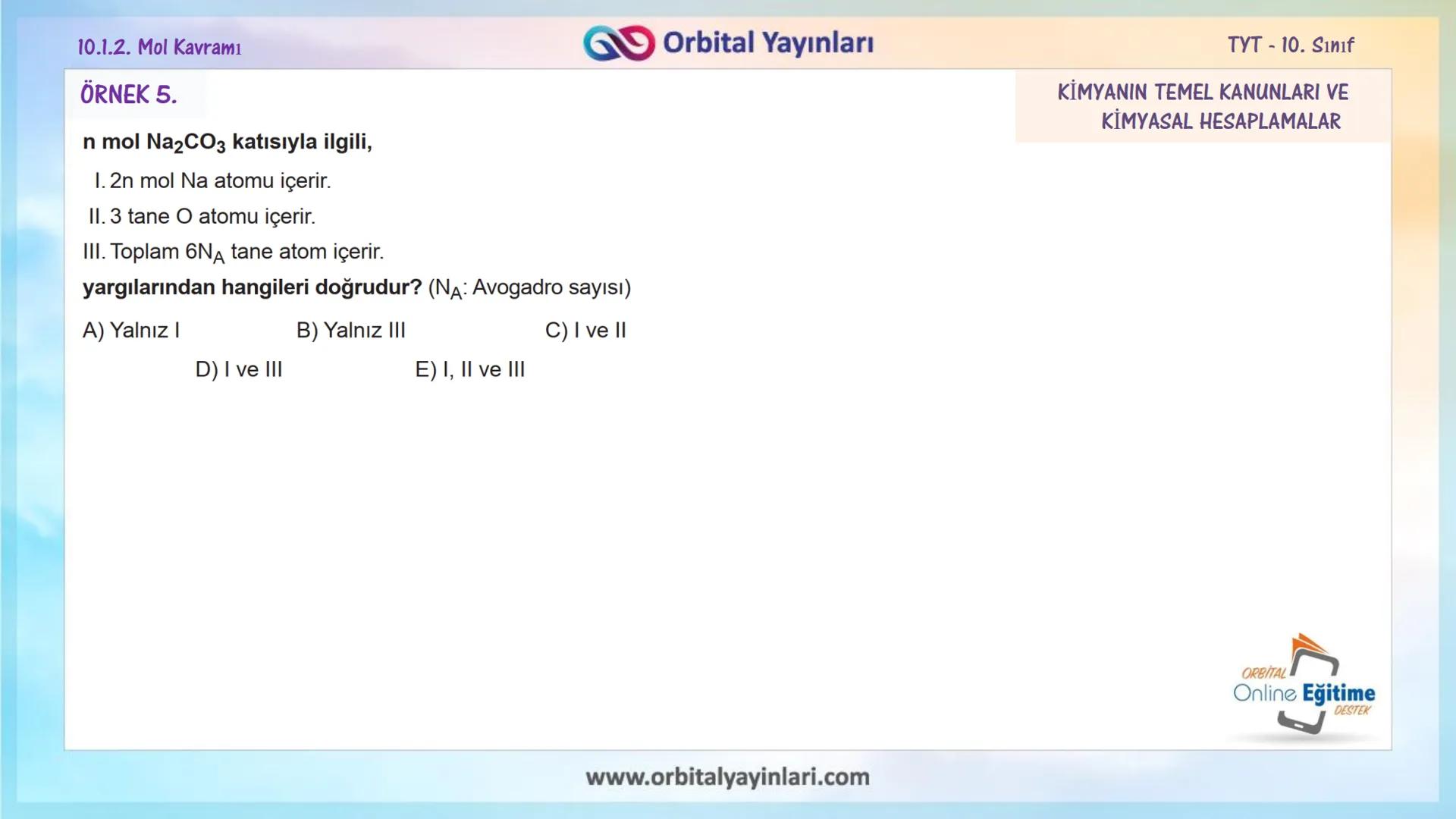
Örnek 3: 0,3 mol Na₃PO₄ bileşiğinde toplam kaç mol atom bulunur?
- Na₃PO₄'te toplam atom sayısı: 3 + 1 + 4 = 8
- Toplam mol atom: 0,3 × 8 = 2,4 mol atom
Örnek 4: 0,25 mol H₂CrO₄ bileşiğinde kaç tane oksijen atomu vardır?
- O atomu sayısı: 4 (formülden)
- O atomu mol sayısı: 0,25 × 4 = 1 mol
- O atomu tanecik sayısı: 1 × 6×10²³ = 6×10²³ tane
Sınav İpucu: Sınavlarda bu tür hesaplamalar sıkça sorulur. Formülü dikkatlice inceleyip, içerdiği her elementin atom sayısını doğru belirlemeniz çok önemlidir!

Gaz Hesaplamaları ve Karışımlar
Örnek 1: NK'da 11,2 L hacim kaplayan SO₂ gazı için hangisi doğrudur?
- Mol sayısı: n = V/22,4 = 11,2/22,4 = 0,5 mol
- Kütlesi: m = n × Mₐ = 0,5 × (32 + 2×16) = 0,5 × 64 = 32 gram
Örnek 2: NK'da hacimleri eşit olan C₃H₈ ve CO₂ gazları için hangi nicelikler eşittir?
- Hacimleri eşitse mol sayıları da eşittir
- Mol sayıları eşitse molekül sayıları da eşittir
- Ancak kütleleri farklıdır çünkü molekül ağırlıkları farklıdır
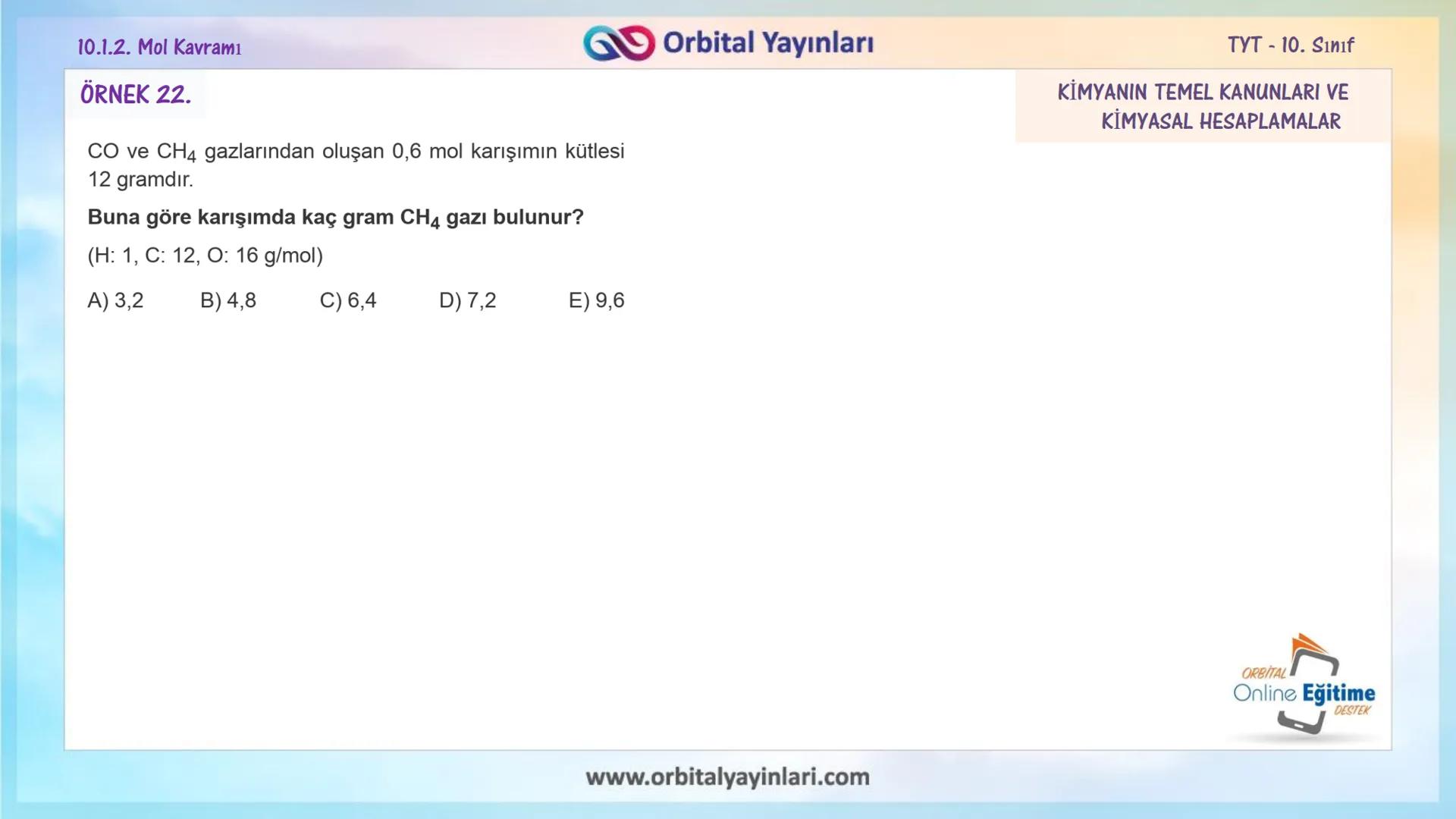
Örnek 3: CO ve CH₄ gazlarından oluşan 0,6 mol karışımın kütlesi 12 gramdır. Karışımda kaç gram CH₄ gazı vardır?
Bu tür karışım problemlerinde denklem kurarak çözüm yapmanız gerekir. Böyle karmaşık soruları çözerken şu adımları izleyin:
- Bilinenleri yazın
- Bilinmeyenleri x, y gibi değişkenlerle gösterin
- Mol sayısı ve kütle denklemlerini oluşturun
- Denklem sistemini çözün




















Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Mole
910 sınıf kimya mol kavramı
Mol kavramı özellikleri kavramlar ve örnek sorular konu anlatım ders notu
Mol Kavramı
Mol Kavramı
Mol kavramı
mol kavramı konu anlatımı ve çözümlü örnekler
Mol kavramı
Mol kavramı ve hesaplamalarını anlatır
Kimya mol kavramı
10 sınıf kimya dersinde mol kavramı konusunda konu anlatımı
MOL KAVRAMI 10 SINIF KIMYA
Kimya 10 sinif
Mol kavramı
10. sınıf kimya mol kavramı ve kütle hacim ilişkileri
Mol kavramı
Mol kavramı detaylı
Mol Kavramı
Mol Kavramı
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
Mol Kavramı Nedir? Kolay Anlatım
Mol kavramı, kimyasal hesaplamaların temelini oluşturan ve madde miktarını anlamak için kullanılan önemli bir ölçü birimidir. Atomlar ve moleküller gibi çok küçük tanecikleri büyük gruplar halinde ifade etmemizi sağlar. 6,02×10²³ taneciğe karşılık gelen 1 mol, kimya derslerinde karşınıza sıkça çıkacak... Daha fazla göster

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Mol Kavramı Nedir?
Mol, Latince "büyük yığın" anlamına gelen ve küçük maddelerin oluşturduğu grupları tanımlamaya yarayan bir ölçü birimidir. Günlük hayatta düzine (12 tane) veya deste (10 tane) gibi grup adları kullanırız, kimyada ise 1 mol = 6,02×10²³ tane olarak tanımlanır.
Bu sayı Avogadro sayısı olarak bilinir ve kısaca Na veya No ile gösterilir. Avogadro sayısı o kadar büyüktür ki, atomlar ve moleküller gibi gözle göremediğimiz çok küçük tanecikleri pratik şekilde sayabilmemizi sağlar.
Not: Mol kavramı, nasıl ki 1 düzine her zaman 12 tane ise, 1 mol de her zaman 6,02×10²³ tanecik içerir. Bu sayı tanecik türünden bağımsızdır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Mol-Tanecik Sayısı İlişkisi
Mol ile tanecik sayısı arasında doğrudan bir bağlantı vardır. Örneğin:
- 1 mol Fe elementi = 6,02×10²³ tane Fe atomu
- 2 mol He elementi = 12,04×10²³ tane He atomu
- 1 mol H₂O bileşiği = 6,02×10²³ tane H₂O molekülü
Mol sayısı ile tanecik sayısı arasında şöyle bir matematiksel ilişki vardır:
n = N/Nₐ
Burada;
- n: Mol sayısı
- N: Tanecik sayısı
- Nₐ: Avogadro sayısı (6,02×10²³)
1 molekül CO₂ ile 1 mol CO₂ arasındaki fark önemlidir. Birincisi tek bir molekülü, ikincisi ise 6,02×10²³ tane CO₂ molekülünü ifade eder.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Bileşiklerde Mol Hesaplamaları
Bileşiklerdeki atom sayıları, formüldeki atom sayılarıyla mol sayısı çarpılarak bulunur. Örneğin:
1 mol H₃PO₄ bileşiğinde:
- 3 mol H atomu
- 1 mol P atomu
- 4 mol O atomu Toplam: 8 mol atom bulunur
0,2 mol H₃PO₄ bileşiğinde ise:
- 0,6 mol H atomu (0,2 × 3)
- 0,2 mol P atomu (0,2 × 1)
- 0,8 mol O atomu (0,2 × 4) Toplam: 1,6 mol atom bulunur
Önemli: Bir bileşiğin içerdiği toplam atom sayısını bulmak için, formüldeki her elementin atom sayısını toplayıp, mol sayısıyla çarpmanız gerekir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Mol-Kütle İlişkisi
Bir elementin 1 mol atomunun gram cinsinden kütlesine o elementin mol kütlesi (atom kütlesi, Mₐ) denir. Örneğin, He elementinin mol kütlesi 4 g/mol'dür.
Bu bilgiyle:
- 1 mol He elementi = 4 gram
- 2 mol He elementi = 8 gram
- 0,2 mol He elementi = 0,8 gram
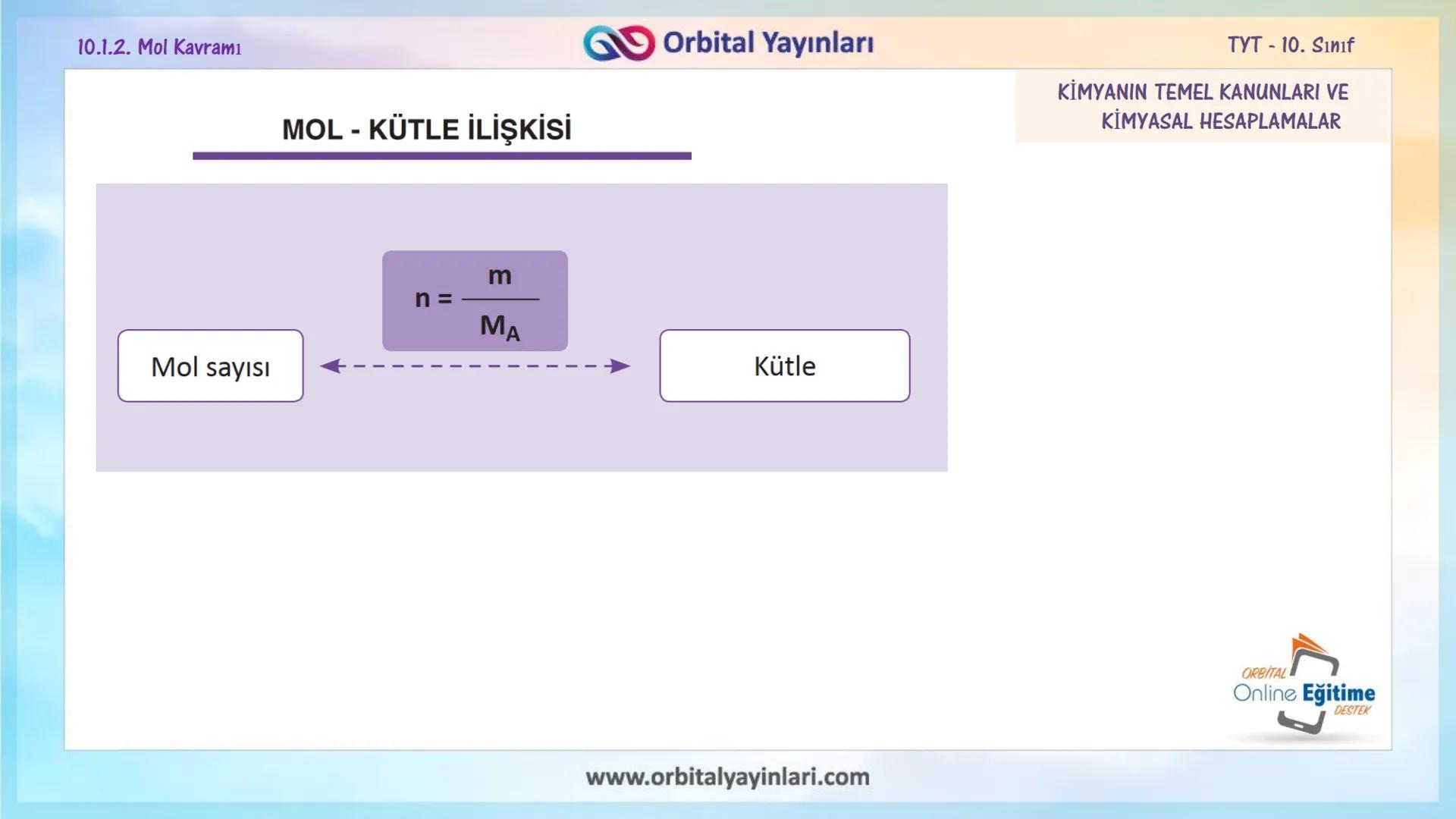
Kütle ile mol sayısı arasındaki matematiksel ilişki şöyledir:
n = m/Mₐ
Burada;
- n: Mol sayısı
- m: Kütle (gram)
- Mₐ: Mol kütlesi
Kolaylaştırıcı İpucu: Eğer bir elementin kaç mol olduğunu bulmak istiyorsanız, kütlesini (g) mol kütlesine bölmeniz yeterlidir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Bileşiklerin Mol Kütlesi
Bir bileşiğin mol kütlesi, onu oluşturan elementlerin atom kütlelerinin toplamıdır. Örneğin:
H₂O bileşiğinin mol kütlesi = (2 × 1) + (1 × 16) = 18 g/mol
CaCO₃ bileşiğinde:
- 1 mol Ca = 40 g
- 1 mol C = 12 g
- 3 mol O = 48 g Toplam: 100 g/mol
Bu bilgiler, kimyasal hesaplamalarda çok işinize yarayacak. Örneğin, 18 gram su yaklaşık 1 mol H₂O molekülü içerir ve bu da 6,02×10²³ tane su molekülü demektir.
Sınavlarda hesaplamalarınızı doğru yapabilmeniz için element atom kütleleri genellikle sorularda verilir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Mol-Hacim İlişkisi
Gazlarla çalışırken bilmeniz gereken önemli bir bilgi: Normal koşullarda (0°C ve 1 atm basınçta) 1 mol gaz 22,4 litre hacim kaplar. Bu değer, gazın türünden bağımsızdır!
Örneğin:
- NK'da 1 mol He gazı = 22,4 L
- NK'da 2 mol He gazı = 44,8 L
- NK'da 1 mol CO₂ gazı = 22,4 L
- NK'da 0,5 mol CO₂ gazı = 11,2 L
Normal koşullarda gazların hacmi ile mol sayısı arasındaki matematiksel ilişki şöyledir:
n = V/22,4
Burada;
- n: Mol sayısı
- V: Hacim (litre)
Bu bilgi, gaz hacmi ve mol sayısı arasında dönüşüm yapmanıza olanak sağlar.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Atomik Kütle Birimi (akb)
1 atomik kütle birimi (akb), 1 tane ¹²C izotopunun kütlesinin 1/12'sine eşittir ve çok küçük bir kütle birimidir. Elementlerin akb türünden kütlelerine bağıl atom kütlesi denir.
Kütle birimleri arasındaki ilişki:
- 1 ton = 1000 kg
- 1 kg = 1000 g
- 1 g = 6,02×10²³ akb
Tek bir atomun kütlesi çok küçük olduğundan, akb ile ifade edilir. Örneğin:
- 1 mol C (12 gram) = 6,02×10²³ tane C atomu (her biri 12 akb)
- 1 mol H₂O (18 gram) = 6,02×10²³ tane H₂O molekülü (her biri 18 akb)
Hatırlatma: 1 akb aynı zamanda 1 tane protonun kütlesine eşit kabul edilir. Akb sayısal değer olarak mol kütlesiyle aynıdır .

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
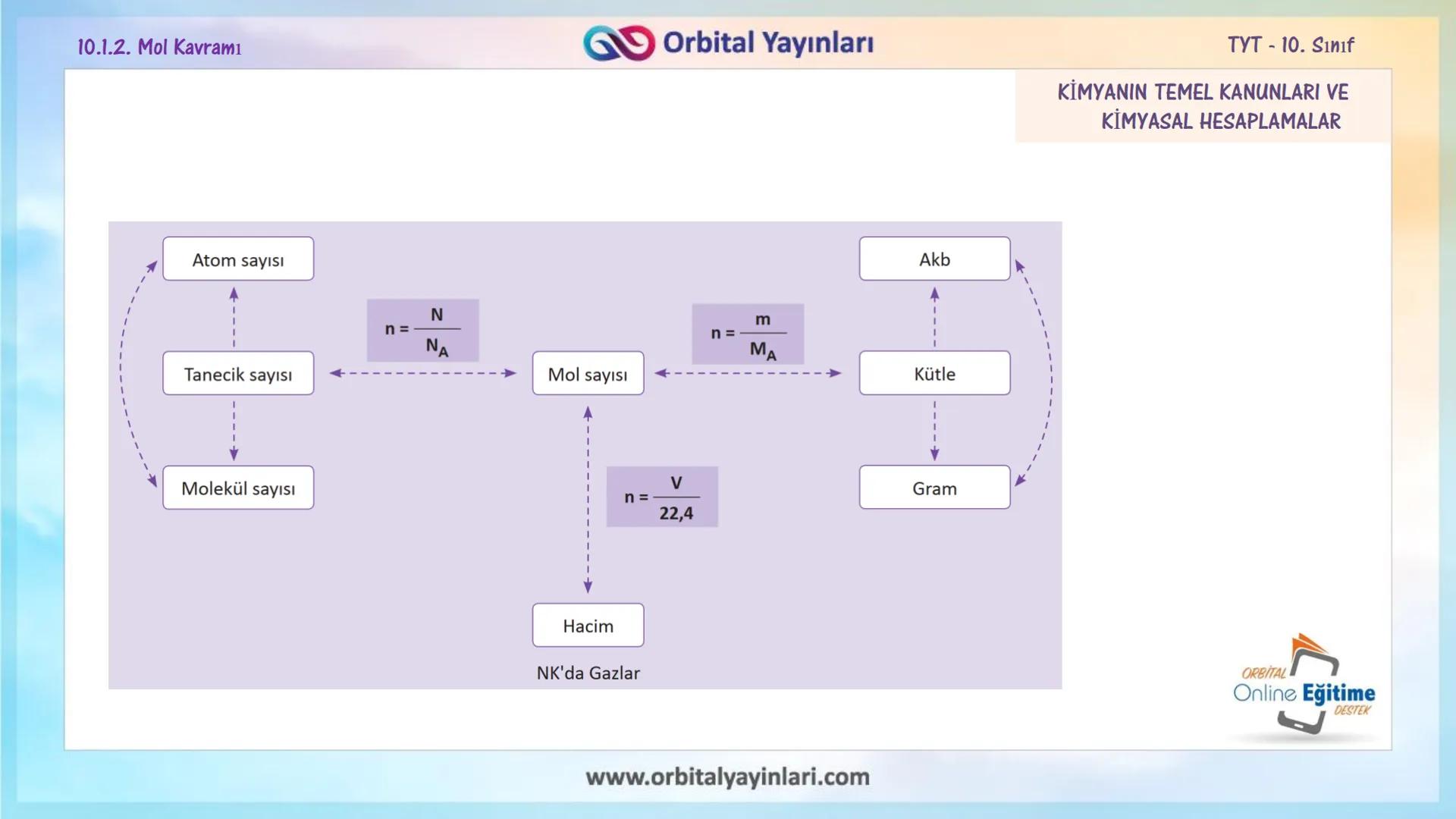
Mol Kavramında Formüller Özeti
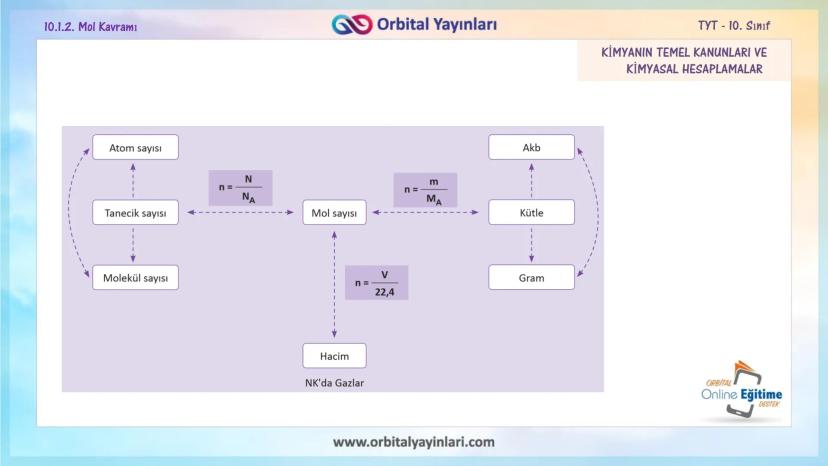
Mol kavramıyla ilgili tüm hesaplamalarda kullanabileceğiniz temel formüller:
-
Mol-Tanecik Sayısı İlişkisi: n = N/Nₐ (n: mol sayısı, N: tanecik sayısı, Nₐ: Avogadro sayısı)
-
Mol-Kütle İlişkisi: n = m/Mₐ (n: mol sayısı, m: kütle (g), Mₐ: mol kütlesi)
-
Mol-Hacim İlişkisi (NK'da Gazlar için): n = V/22,4 (n: mol sayısı, V: hacim (L))
Bu formüller arasında dönüşüm yapabilmek, kimyasal hesaplamalarda size büyük kolaylık sağlayacaktır. Herhangi birini bildiğinizde, diğer niceliklerini kolayca hesaplayabilirsiniz.
Örnek: 4 gram CH₄ gazı kaç moldür? Kaç molekül içerir? NK'da hacmi nedir?

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Mol Kavramı Uygulama Örnekleri
Örnek 1: 24,08×10²³ tane atom içeren Altın (Au) elementi kaç moldür?
- n = N/Nₐ = 24,08×10²³ / 6,02×10²³ = 4 mol
Örnek 2: 2 mol CO₂ gazı kaç tane molekül içerir?
- N = n × Nₐ = 2 × 6,02×10²³ = 12,04×10²³ molekül
Örnek 3: 0,3 mol Na₃PO₄ bileşiğinde toplam kaç mol atom bulunur?
- Na₃PO₄'te toplam atom sayısı: 3 + 1 + 4 = 8
- Toplam mol atom: 0,3 × 8 = 2,4 mol atom
Örnek 4: 0,25 mol H₂CrO₄ bileşiğinde kaç tane oksijen atomu vardır?
- O atomu sayısı: 4 (formülden)
- O atomu mol sayısı: 0,25 × 4 = 1 mol
- O atomu tanecik sayısı: 1 × 6×10²³ = 6×10²³ tane
Sınav İpucu: Sınavlarda bu tür hesaplamalar sıkça sorulur. Formülü dikkatlice inceleyip, içerdiği her elementin atom sayısını doğru belirlemeniz çok önemlidir!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Gaz Hesaplamaları ve Karışımlar
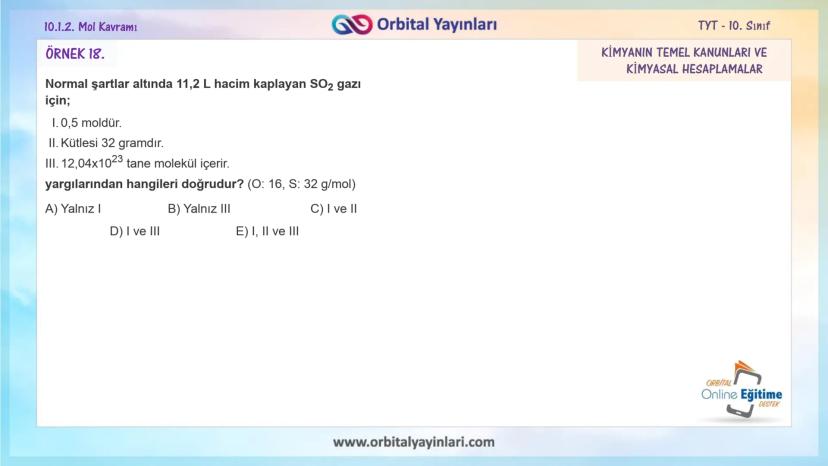
Örnek 1: NK'da 11,2 L hacim kaplayan SO₂ gazı için hangisi doğrudur?
- Mol sayısı: n = V/22,4 = 11,2/22,4 = 0,5 mol
- Kütlesi: m = n × Mₐ = 0,5 × (32 + 2×16) = 0,5 × 64 = 32 gram
Örnek 2: NK'da hacimleri eşit olan C₃H₈ ve CO₂ gazları için hangi nicelikler eşittir?
- Hacimleri eşitse mol sayıları da eşittir
- Mol sayıları eşitse molekül sayıları da eşittir
- Ancak kütleleri farklıdır çünkü molekül ağırlıkları farklıdır
Örnek 3: CO ve CH₄ gazlarından oluşan 0,6 mol karışımın kütlesi 12 gramdır. Karışımda kaç gram CH₄ gazı vardır?
Bu tür karışım problemlerinde denklem kurarak çözüm yapmanız gerekir. Böyle karmaşık soruları çözerken şu adımları izleyin:
- Bilinenleri yazın
- Bilinmeyenleri x, y gibi değişkenlerle gösterin
- Mol sayısı ve kütle denklemlerini oluşturun
- Denklem sistemini çözün

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Mole
910 sınıf kimya mol kavramı
Mol kavramı özellikleri kavramlar ve örnek sorular konu anlatım ders notu
Mol Kavramı
Mol Kavramı
Mol kavramı
mol kavramı konu anlatımı ve çözümlü örnekler
Mol kavramı
Mol kavramı ve hesaplamalarını anlatır
Kimya mol kavramı
10 sınıf kimya dersinde mol kavramı konusunda konu anlatımı
MOL KAVRAMI 10 SINIF KIMYA
Kimya 10 sinif
Mol kavramı
10. sınıf kimya mol kavramı ve kütle hacim ilişkileri
Mol kavramı
Mol kavramı detaylı
Mol Kavramı
Mol Kavramı
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅