Atomların iç yapısını anlamak için Bohr'dan günümüze kadar geliştirilen atom... Daha fazla göster
Modern Atom Teorisi PDF İndir
















Bohr Atom Modeli ve Temelleri
Atomları gerçekten anlayabilmek için önce Bohr'un ne söylediğine bakalım. 1913'te Niels Bohr, atomları güneş sistemi gibi düşündü: çekirdek merkezde, elektronlar etrafında dairesel yörüngelerde dönüyor.
Bohr modeli üç temel özellik öne sürdü. İlk olarak, elektronlar belirli dairesel yörüngelerde hareket eder. İkinci olarak, her yörüngenin sabit bir enerjisi vardır (1, 2, 3 rakamları ya da K, L, M harfleriyle gösterilebilir). Son olarak, atomlar enerji aldıklarında uyarılır ve bu enerjiyi geri verirken ışın yayar.
Bu model sadece tek elektronlu atomları açıklayabildi. Çok elektronlu atomlarda işe yaramadı çünkü elektronların gerçekte tanecik ve dalga özelliği birlikte göstermesi nedeniyle, yerini ve hızını aynı anda belirlemek mümkün değil (Heisenberg Belirsizlik İlkesi).
Hatırla: Bohr modeli güneş sistemi gibi - çekirdek güneş, elektronlar gezegen gibi düşünülür!

Modern Atom Teorisi ve Kuantum Modeli
Günümüzde kullandığımız kuantum modeli çok daha gerçekçi. Bu modelde elektronların tam yerini bilemeyiz ama bulunma olasılığının yüksek olduğu bölgeleri tanımlayabiliriz. İşte bu bölgelere orbital denir.
Yörünge ile orbital arasındaki fark çok önemli. Yörünge dairesel ve düz bir yolken, orbital üç boyutlu elektron bulutu şeklinde. Bir orbital en fazla 2 elektron alabilir, yörüngede ise bu sınır yoktu.
Modern atom teorisinde dört kuantum sayısı var: baş kuantum sayısı (n), açısal momentum kuantum sayısı (ℓ), manyetik kuantum sayısı (mℓ) ve spin kuantum sayısı (ms). Bu sayılar elektronların kimliğini tamamen belirler.
Baş kuantum sayısı (n) 1, 2, 3, 4... değerlerini alır ve elektron kabuğunu gösterir. Açısal momentum kuantum sayısı (ℓ) ise orbital türünü belirler: ℓ=0 için s, ℓ=1 için p, ℓ=2 için d, ℓ=3 için f orbitali.
İpucu: Kuantum sayıları elektronun kimlik kartı gibi - her elektron farklı kombinasyona sahip!

Orbital Türleri ve Şekilleri
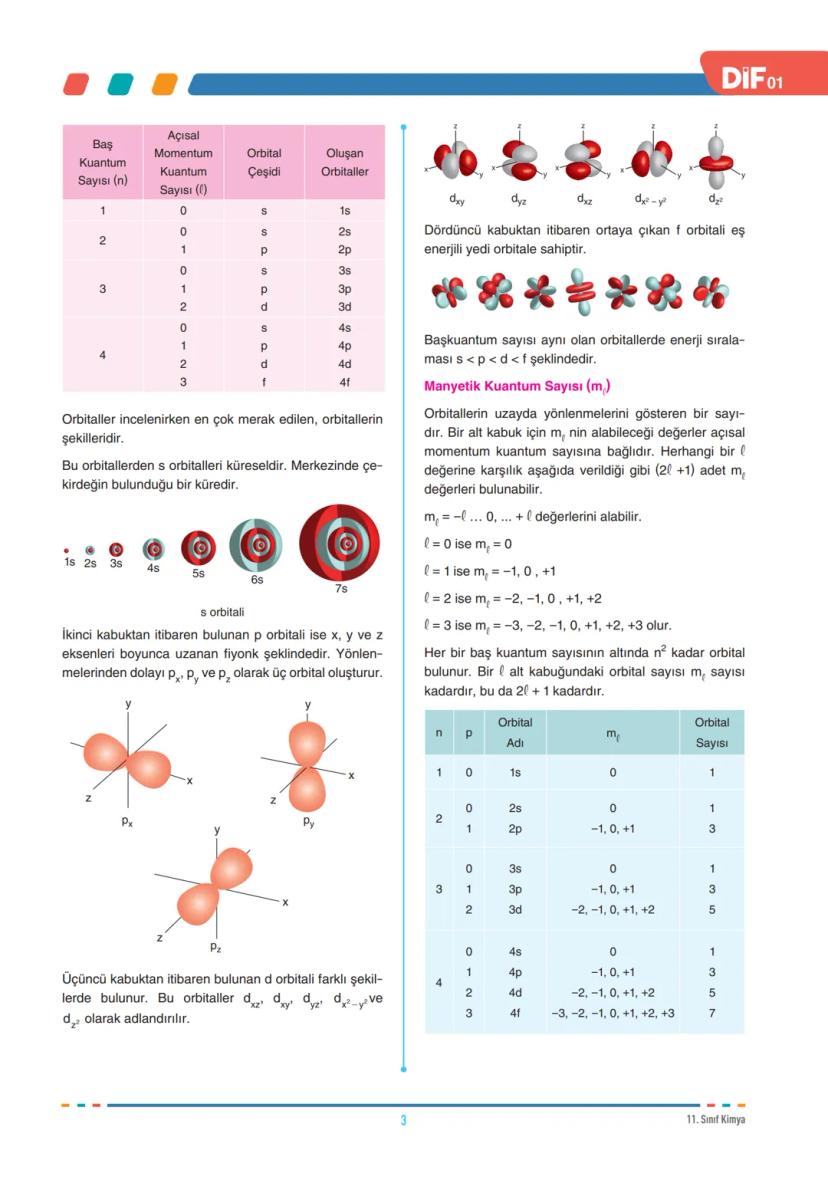
Orbitallerin şekilleri çok karakteristik. s orbitali küresel, p orbitali fiyonk şeklinde (px, py, pz olmak üzere üç tanesi var). d orbitali beş farklı şekle sahip, f orbitali ise yedi farklı yönelime sahip.
Manyetik kuantum sayısı (mℓ) orbitallerin uzayda nasıl yönlendiğini gösterir. ℓ değerine bağlı olarak -ℓ ile +ℓ arasında (2ℓ+1) farklı değer alır. Örneğin, ℓ=1 için mℓ = -1, 0, +1 değerlerini alır.
Orbital sayıları şu şekilde hesaplanır: s orbitalinden 1 tane, p orbitalinden 3 tane, d orbitalinden 5 tane, f orbitalinden 7 tane bulunur. Her bir baş kuantum sayısının altında n² kadar orbital vardır.
Enerji sıralaması aynı kabukta s < p < d < f şeklindedir. Bu bilgi elektron dizilimleri yazarken çok işinize yarayacak.
Çabuk Hatırla: s küre, p fiyonk, d beş şekil, f yedi şekil!

Elektron Dizilimi Kuralları ve İlkeleri
Elektron dizilimi yazarken üç temel kural var. Aufbau ilkesine göre elektronlar en düşük enerjili orbitalden başlayarak doldurulur. Hund kuralına göre eş enerjili orbitallere önce birer elektron yerleşir. Pauli ilkesine göre aynı orbitalde bulunan elektronlar zıt spinli olmalı.
Küresel simetri atomlara kararlılık kazandırır. Tam dolu (s², p⁶, d¹⁰, f¹⁴) ya da yarı dolu orbitaller özel kararlılık gösterir. Bu yüzden Cr ve Cu atomları beklenmedik elektron dizilimine sahip.
₂₄Cr: 4s¹3d⁵ (yarı dolu d orbitali için) ₂₉Cu: 4s¹3d¹⁰ (tam dolu d orbitali için)
Bu "istisna durumlar" sınavlarda çok soruluyor çünkü atomlar daha kararlı olmak için normal kuralları çiğneyebilir.
Sınav İpucu: Cr ve Cu'nun elektron dizilimleri ezber değil, kararlılık arayışının sonucu!

İyonların Elektron Dizilimi ve Değerlik Elektronları
Anyon oluştururken (negatif iyon) nötr atoma elektron eklenir. Katyon oluştururken (pozitif iyon) en yüksek enerji düzeyinden elektron koparılır - önce s sonra d orbitalinden.
Değerlik elektronları atomun en dış kabuğundaki elektronlardır ve kimyasal özellikleri belirler. Elektron dizilimi s ile bitiyorsa sadece s orbitalindeki elektronlar, p ile bitiyorsa s+p orbitalindeki elektronlar değerlik elektronu sayılır.
d bloku elementlerde hem s hem de d orbitali değerlik orbitali olarak kabul edilir. Örneğin ₂₆Fe için 4s²3d⁶ diziliminde 8 değerlik elektronu var.
Önemli nokta: İyon elektron dizilimi yazarken, metal katyonlarda önce s sonra d orbitalinden elektron koparılır. Bu sınavlarda çok karışan bir konu!
Pratik Bilgi: Değerlik elektronları = kimyasal davranış, aynı grup elementleri benzer değerlik elektronuna sahip!











Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Quantum Numbers
7Atomun Kuantum Modeli
atomun kuantum modeli detaylı özet
Modern ve Bohr Atom Teorisi
Benzerlik ve Farklılıklar
Kimya
Orbital türleri
Kuantum sayıları
Kuantum sayıları, maddeler halinde
11. sinif atomun kuantum modeli
modern atom teorisi
Atomun Kuamtum Modeli
Bu konu hakkında kısa bir özet yapıp detaylı bilgiler vermeye çalıştım umarım hepinize yardımcı olabiliyorumdur☺️🫠💗🫠
Modern atom teorisi
Orbital çeşitleri ve kuantum sayıları konu anlatımı
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
Modern Atom Teorisi PDF İndir
Atomların iç yapısını anlamak için Bohr'dan günümüze kadar geliştirilen atom modelleri üzerinden gidelim. Modern atom teorisi ve kuantum mekaniği sayesinde elektronların atomlardaki davranışlarını daha doğru anlayabiliyoruz.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Bohr Atom Modeli ve Temelleri
Atomları gerçekten anlayabilmek için önce Bohr'un ne söylediğine bakalım. 1913'te Niels Bohr, atomları güneş sistemi gibi düşündü: çekirdek merkezde, elektronlar etrafında dairesel yörüngelerde dönüyor.
Bohr modeli üç temel özellik öne sürdü. İlk olarak, elektronlar belirli dairesel yörüngelerde hareket eder. İkinci olarak, her yörüngenin sabit bir enerjisi vardır (1, 2, 3 rakamları ya da K, L, M harfleriyle gösterilebilir). Son olarak, atomlar enerji aldıklarında uyarılır ve bu enerjiyi geri verirken ışın yayar.
Bu model sadece tek elektronlu atomları açıklayabildi. Çok elektronlu atomlarda işe yaramadı çünkü elektronların gerçekte tanecik ve dalga özelliği birlikte göstermesi nedeniyle, yerini ve hızını aynı anda belirlemek mümkün değil (Heisenberg Belirsizlik İlkesi).
Hatırla: Bohr modeli güneş sistemi gibi - çekirdek güneş, elektronlar gezegen gibi düşünülür!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Modern Atom Teorisi ve Kuantum Modeli
Günümüzde kullandığımız kuantum modeli çok daha gerçekçi. Bu modelde elektronların tam yerini bilemeyiz ama bulunma olasılığının yüksek olduğu bölgeleri tanımlayabiliriz. İşte bu bölgelere orbital denir.
Yörünge ile orbital arasındaki fark çok önemli. Yörünge dairesel ve düz bir yolken, orbital üç boyutlu elektron bulutu şeklinde. Bir orbital en fazla 2 elektron alabilir, yörüngede ise bu sınır yoktu.
Modern atom teorisinde dört kuantum sayısı var: baş kuantum sayısı (n), açısal momentum kuantum sayısı (ℓ), manyetik kuantum sayısı (mℓ) ve spin kuantum sayısı (ms). Bu sayılar elektronların kimliğini tamamen belirler.
Baş kuantum sayısı (n) 1, 2, 3, 4... değerlerini alır ve elektron kabuğunu gösterir. Açısal momentum kuantum sayısı (ℓ) ise orbital türünü belirler: ℓ=0 için s, ℓ=1 için p, ℓ=2 için d, ℓ=3 için f orbitali.
İpucu: Kuantum sayıları elektronun kimlik kartı gibi - her elektron farklı kombinasyona sahip!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Orbital Türleri ve Şekilleri
Orbitallerin şekilleri çok karakteristik. s orbitali küresel, p orbitali fiyonk şeklinde (px, py, pz olmak üzere üç tanesi var). d orbitali beş farklı şekle sahip, f orbitali ise yedi farklı yönelime sahip.
Manyetik kuantum sayısı (mℓ) orbitallerin uzayda nasıl yönlendiğini gösterir. ℓ değerine bağlı olarak -ℓ ile +ℓ arasında (2ℓ+1) farklı değer alır. Örneğin, ℓ=1 için mℓ = -1, 0, +1 değerlerini alır.
Orbital sayıları şu şekilde hesaplanır: s orbitalinden 1 tane, p orbitalinden 3 tane, d orbitalinden 5 tane, f orbitalinden 7 tane bulunur. Her bir baş kuantum sayısının altında n² kadar orbital vardır.
Enerji sıralaması aynı kabukta s < p < d < f şeklindedir. Bu bilgi elektron dizilimleri yazarken çok işinize yarayacak.
Çabuk Hatırla: s küre, p fiyonk, d beş şekil, f yedi şekil!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektron Dizilimi Kuralları ve İlkeleri
Elektron dizilimi yazarken üç temel kural var. Aufbau ilkesine göre elektronlar en düşük enerjili orbitalden başlayarak doldurulur. Hund kuralına göre eş enerjili orbitallere önce birer elektron yerleşir. Pauli ilkesine göre aynı orbitalde bulunan elektronlar zıt spinli olmalı.
Küresel simetri atomlara kararlılık kazandırır. Tam dolu (s², p⁶, d¹⁰, f¹⁴) ya da yarı dolu orbitaller özel kararlılık gösterir. Bu yüzden Cr ve Cu atomları beklenmedik elektron dizilimine sahip.
₂₄Cr: 4s¹3d⁵ (yarı dolu d orbitali için) ₂₉Cu: 4s¹3d¹⁰ (tam dolu d orbitali için)
Bu "istisna durumlar" sınavlarda çok soruluyor çünkü atomlar daha kararlı olmak için normal kuralları çiğneyebilir.
Sınav İpucu: Cr ve Cu'nun elektron dizilimleri ezber değil, kararlılık arayışının sonucu!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
İyonların Elektron Dizilimi ve Değerlik Elektronları
Anyon oluştururken (negatif iyon) nötr atoma elektron eklenir. Katyon oluştururken (pozitif iyon) en yüksek enerji düzeyinden elektron koparılır - önce s sonra d orbitalinden.
Değerlik elektronları atomun en dış kabuğundaki elektronlardır ve kimyasal özellikleri belirler. Elektron dizilimi s ile bitiyorsa sadece s orbitalindeki elektronlar, p ile bitiyorsa s+p orbitalindeki elektronlar değerlik elektronu sayılır.
d bloku elementlerde hem s hem de d orbitali değerlik orbitali olarak kabul edilir. Örneğin ₂₆Fe için 4s²3d⁶ diziliminde 8 değerlik elektronu var.
Önemli nokta: İyon elektron dizilimi yazarken, metal katyonlarda önce s sonra d orbitalinden elektron koparılır. Bu sınavlarda çok karışan bir konu!
Pratik Bilgi: Değerlik elektronları = kimyasal davranış, aynı grup elementleri benzer değerlik elektronuna sahip!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Quantum Numbers
7Atomun Kuantum Modeli
atomun kuantum modeli detaylı özet
Modern ve Bohr Atom Teorisi
Benzerlik ve Farklılıklar
Kimya
Orbital türleri
Kuantum sayıları
Kuantum sayıları, maddeler halinde
11. sinif atomun kuantum modeli
modern atom teorisi
Atomun Kuamtum Modeli
Bu konu hakkında kısa bir özet yapıp detaylı bilgiler vermeye çalıştım umarım hepinize yardımcı olabiliyorumdur☺️🫠💗🫠
Modern atom teorisi
Orbital çeşitleri ve kuantum sayıları konu anlatımı
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅