Modern Atom Teorisi ve Periyodik Özellikler konusu, elementlerin elektron dizilimlerini... Daha fazla göster
Çağdaş Atom Teorisi ve Öne Çıkan İlkeleri













































Modern Atom Teorisi - Periyodik Özellikler
Periyodik tablo, elementlerin atom numaralarına göre sıralandığı ve benzer özellikler gösterenlerin aynı gruplarda toplandığı bilimsel bir düzenlemedir. Modern atom teorisi, elektronların atomda nasıl dizildiğini ve bu dizilimin elementlerin özelliklerini nasıl belirlediğini açıklar.
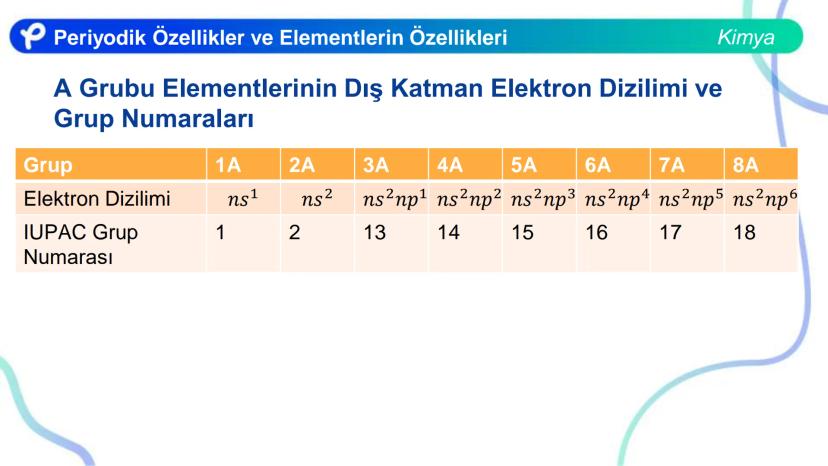
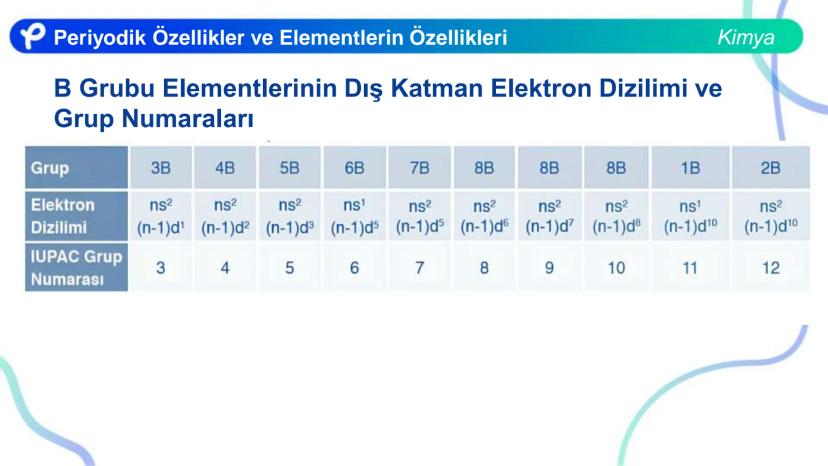
Periyodik sistemde elementler, elektron dizilimlerine göre sınıflandırılmıştır. Bu dizilimler, elementlerin fiziksel ve kimyasal davranışlarını belirler.
Not: Periyodik tabloyu anlamak, kimyasal reaksiyonları tahmin etmede ve elementlerin özelliklerini kavramada büyük kolaylık sağlar!

İyonların Elektron Dizilimi
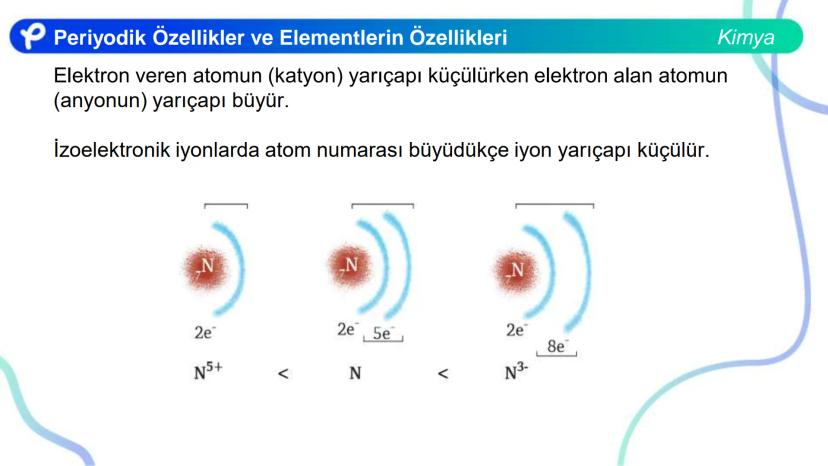
İyonlar, atomların elektron kazanması veya kaybetmesiyle oluşur. Pozitif iyonlar (katyonlar) elektron kaybederek, negatif iyonlar (anyonlar) ise elektron kazanarak oluşur.
Örneğin:
- N atomu (1s² 2s² 2p³) → N³⁻ iyonu (1s² 2s² 2p⁶)
- Ca atomu (1s² 2s² 2p⁶ 3s² 3p⁶ 4s²) → Ca²⁺ iyonu (1s² 2s² 2p⁶ 3s² 3p⁶)
- Fe atomu (1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d⁶) → Fe²⁺ iyonu (1s² 2s² 2p⁶ 3s² 3p⁶ 3d⁶)
Metal atomları genellikle elektron vererek pozitif iyon oluştururken, ametal atomları elektron alarak negatif iyon oluşturur.

İzoelektronik Tanecikler
İzoelektronik tanecikler, proton sayıları farklı olmasına rağmen aynı elektron sayısına ve elektron dizilimine sahip olan taneciklerdir.
Örnek olarak:
- Na⁺ (11 proton, 10 elektron)
- O²⁻ (8 proton, 10 elektron)
- F⁻ (9 proton, 10 elektron)
Bu taneciklerin hepsi 10 elektrona sahiptir ve [1s² 2s² 2p⁶] elektron dizilimini gösterir.
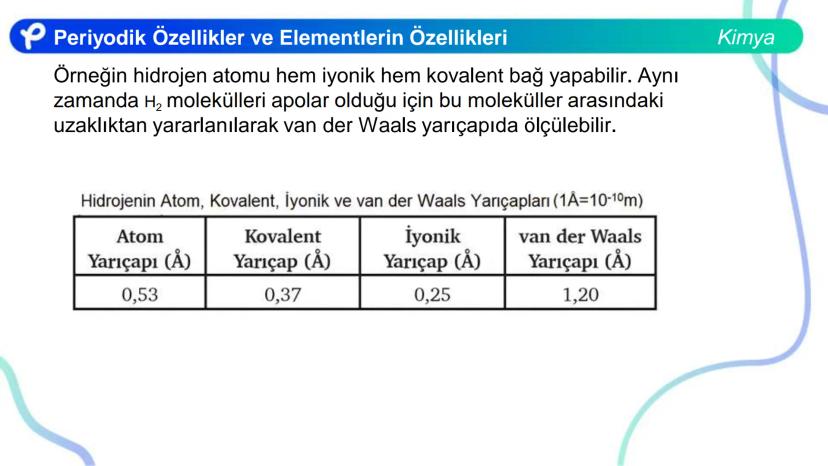
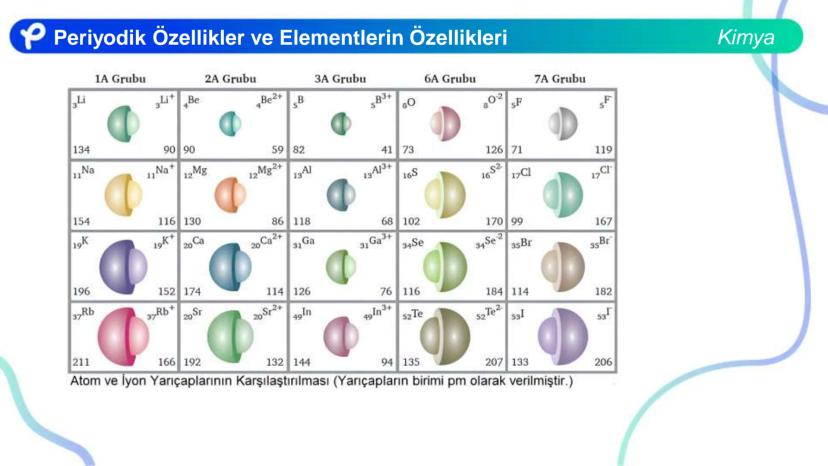
İzoelektronik taneciklerde, proton sayısı arttıkça iyon yarıçapı küçülür çünkü daha fazla proton aynı sayıda elektronu daha güçlü çeker.

Elektronların Yerleşim Kuralları
Elektronlar atomda belirli kurallar çerçevesinde orbitallere yerleşir. Bu kurallar:
Aufbau Kuralı: Elektronlar öncelikle düşük enerjili orbitallerden başlayarak yerleşir. Yani önce 1s, sonra 2s, 2p, 3s... şeklinde dolar.
Hund Kuralı: Elektronlar enerjisi aynı olan orbitallere önce birer birer, daha sonra ikinciler zıt spinli olarak yerleşir.
Pauli İlkesi: Bir orbitalde zıt spinli en fazla iki elektron bulunabilir.
İpucu: Bu kuralları şöyle hatırlayabilirsin: Aufbau "inşa etmek" demektir, yani atomu tabandan inşa ederiz. Hund "köpek" demektir, köpekler tek başına olmayı sever. Pauli ise "çift" anlamında düşünülebilir, en fazla bir çift!

İyonların ve Atomların Karşılaştırılması
₂₉X²⁺ iyonu ve ₂₇Y atomu karşılaştırıldığında:
- X (Cu) atomu [Ar]4s¹3d¹⁰ → X²⁺ iyonu [Ar]3d⁹ olur
- Y (Co) atomu [Ar]4s²3d⁷ şeklindedir
Bu durumda:
- s orbitallerindeki elektron sayıları farklıdır (X²⁺'da 0, Y'de 2)
- İzoelektronik değillerdir (X²⁺'da 27, Y'de 27 elektron)
- Yarı dolu orbital sayıları farklıdır (X²⁺'da 1, Y'de 3)
Atom ve iyonların karşılaştırılması, elementlerin kimyasal davranışlarını anlamada önemli ipuçları verir.

Küresel Simetri
Küresel simetri, atomun elektronlarının uzayda her yönde eşit dağıldığı durumu ifade eder. Bu durum, tam dolu veya yarı dolu orbitallere sahip atomlarda görülür.
Verilen seçeneklerden 24Cr elementi küresel simetri gösterir çünkü elektron dizilimi [Ar]4s¹3d⁵ şeklindedir ve 3d orbitallerinin hepsi yarı doludur.
Diğer elementlerin elektron dizilimleri:
- 6C: 1s²2s²2p² (yarı dolu değil)
- 9F: 1s²2s²2p⁵ (tam dolu değil)
- 16S: 1s²2s²2p⁶3s²3p⁴ (ne tam dolu ne yarı dolu)
- 21Sc: 1s²2s²2p⁶3s²3p⁶4s²3d¹ (ne tam dolu ne yarı dolu)

Uyarılmış Atom
Atomlar enerji aldıklarında, elektronlarının bazıları daha yüksek enerji seviyelerine çıkar. Bu duruma uyarılmış atom denir. Uyarılan elektron ise uyarılmış elektron olarak adlandırılır.
Uyarılmış atomlar kararsızdır ve temel hale dönme eğilimindedir. Bu dönüş sırasında, elektron aldığı enerjiyi foton olarak geri verir.
Örneğin, sodyum lambasının sarı ışık yayması, sodyum atomlarının uyarılma ve temel hale dönme sürecinde enerji yaymasından kaynaklanır. Bu olay günlük hayatta gördüğümüz sokak lambalarında kullanılır.

Uyarılmış Atom Örnekleri
Temel haldeki 11Na elementinin elektron dizilimi 1s² 2s² 2p⁶ 3s¹ şeklindedir. Bu atom enerji aldığında farklı uyarılmış hallere geçebilir:
1. Uyarılmış hal: 1s² 2s² 2p⁶ 4s¹ (3s'deki elektron 4s'ye çıkar) 2. Uyarılmış hal: 1s² 2s² 2p⁶ 3p¹ (3s'deki elektron 3p'ye çıkar)
Bu uyarılmış hallerin hepsi temel halden daha yüksek enerjiye sahiptir. Atomlar enerjilerini en aza indirme eğiliminde olduklarından, uyarılmış elektron er ya da geç temel haline geri döner.
Uyarılmış atomlar, neon ışıkları gibi birçok günlük uygulamanın temelini oluşturur.

Orbital Şemalarının Yorumlanması
Bir atomun orbital şeması, elektronların orbitallere nasıl dağıldığını gösterir. Verilen şemada, 1s, 2s, 2p ve 3s orbitallerinin doluluk durumları gösterilmiştir.
Bu K elementi için:
- 1s ve 2s orbitalleri tam dolu
- 2p orbitalleri tam dolu (üç 2p orbitali toplam 6 elektron alır)
- 3s orbitali yarı dolu (1 elektron var)
Bu durumda atom potasyumdur (19K) ve temel haldedir. Uyarılmış halde olsaydı, elektronlar Aufbau ilkesine uymayan bir düzende olurdu. Atom enerji almadan uyarılmış hale geçemez.
Önemli: Temel haldeki atom en düşük enerji seviyesinde bulunur ve elektronlar en az enerjili orbitallere yerleşir.

Değerlik Orbitali ve Değerlik Elektronu
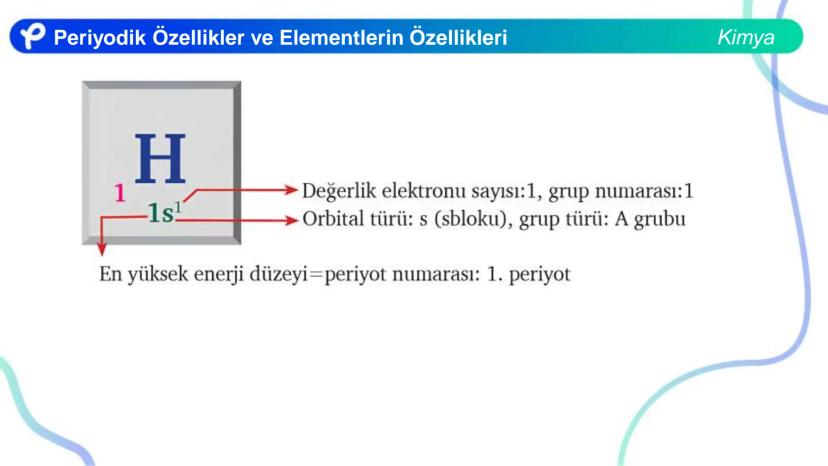
Değerlik orbitalleri, atomun en yüksek enerji düzeyindeki orbitallerdir. Bu orbitallerde bulunan elektronlar değerlik elektronu olarak adlandırılır.
Değerlik elektronları, bir atomun kimyasal davranışını belirleyen elektronlardır. Kimyasal bağlar oluştururken rol oynayan elektronlar bunlardır.
Elektron dizilimi farklı şekilde sonlanan atomların değerlik elektron sayıları:
- ns ile sonlananlar: Değerlik elektronu = ns'deki elektron sayısı
- ns np ile sonlananlar: Değerlik elektronu = ns + np'deki elektron sayısı
- ns d ile sonlananlar: Değerlik elektronu = ns + d'deki elektron sayısı
Değerlik elektronlarını bilmek, elementlerin kimyasal bağ kurma eğilimlerini tahmin etmeyi kolaylaştırır.








































Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Electron Affinity
1Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
Çağdaş Atom Teorisi ve Öne Çıkan İlkeleri
Modern Atom Teorisi ve Periyodik Özellikler konusu, elementlerin elektron dizilimlerini ve bunların periyodik sistemdeki yerlerini belirleme ilkelerini anlamamız için temel oluşturur. Elementlerin fiziksel ve kimyasal özellikleri, atomun yapısı ve elektronların diziliminden kaynaklanır. Bu özellikler periyodik sistemde belirli düzenler gösterir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Modern Atom Teorisi - Periyodik Özellikler
Periyodik tablo, elementlerin atom numaralarına göre sıralandığı ve benzer özellikler gösterenlerin aynı gruplarda toplandığı bilimsel bir düzenlemedir. Modern atom teorisi, elektronların atomda nasıl dizildiğini ve bu dizilimin elementlerin özelliklerini nasıl belirlediğini açıklar.
Periyodik sistemde elementler, elektron dizilimlerine göre sınıflandırılmıştır. Bu dizilimler, elementlerin fiziksel ve kimyasal davranışlarını belirler.
Not: Periyodik tabloyu anlamak, kimyasal reaksiyonları tahmin etmede ve elementlerin özelliklerini kavramada büyük kolaylık sağlar!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
İyonların Elektron Dizilimi
İyonlar, atomların elektron kazanması veya kaybetmesiyle oluşur. Pozitif iyonlar (katyonlar) elektron kaybederek, negatif iyonlar (anyonlar) ise elektron kazanarak oluşur.
Örneğin:
- N atomu (1s² 2s² 2p³) → N³⁻ iyonu (1s² 2s² 2p⁶)
- Ca atomu (1s² 2s² 2p⁶ 3s² 3p⁶ 4s²) → Ca²⁺ iyonu (1s² 2s² 2p⁶ 3s² 3p⁶)
- Fe atomu (1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d⁶) → Fe²⁺ iyonu (1s² 2s² 2p⁶ 3s² 3p⁶ 3d⁶)
Metal atomları genellikle elektron vererek pozitif iyon oluştururken, ametal atomları elektron alarak negatif iyon oluşturur.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
İzoelektronik Tanecikler
İzoelektronik tanecikler, proton sayıları farklı olmasına rağmen aynı elektron sayısına ve elektron dizilimine sahip olan taneciklerdir.
Örnek olarak:
- Na⁺ (11 proton, 10 elektron)
- O²⁻ (8 proton, 10 elektron)
- F⁻ (9 proton, 10 elektron)
Bu taneciklerin hepsi 10 elektrona sahiptir ve [1s² 2s² 2p⁶] elektron dizilimini gösterir.
İzoelektronik taneciklerde, proton sayısı arttıkça iyon yarıçapı küçülür çünkü daha fazla proton aynı sayıda elektronu daha güçlü çeker.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektronların Yerleşim Kuralları
Elektronlar atomda belirli kurallar çerçevesinde orbitallere yerleşir. Bu kurallar:
Aufbau Kuralı: Elektronlar öncelikle düşük enerjili orbitallerden başlayarak yerleşir. Yani önce 1s, sonra 2s, 2p, 3s... şeklinde dolar.
Hund Kuralı: Elektronlar enerjisi aynı olan orbitallere önce birer birer, daha sonra ikinciler zıt spinli olarak yerleşir.
Pauli İlkesi: Bir orbitalde zıt spinli en fazla iki elektron bulunabilir.
İpucu: Bu kuralları şöyle hatırlayabilirsin: Aufbau "inşa etmek" demektir, yani atomu tabandan inşa ederiz. Hund "köpek" demektir, köpekler tek başına olmayı sever. Pauli ise "çift" anlamında düşünülebilir, en fazla bir çift!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
İyonların ve Atomların Karşılaştırılması
₂₉X²⁺ iyonu ve ₂₇Y atomu karşılaştırıldığında:
- X (Cu) atomu [Ar]4s¹3d¹⁰ → X²⁺ iyonu [Ar]3d⁹ olur
- Y (Co) atomu [Ar]4s²3d⁷ şeklindedir
Bu durumda:
- s orbitallerindeki elektron sayıları farklıdır (X²⁺'da 0, Y'de 2)
- İzoelektronik değillerdir (X²⁺'da 27, Y'de 27 elektron)
- Yarı dolu orbital sayıları farklıdır (X²⁺'da 1, Y'de 3)
Atom ve iyonların karşılaştırılması, elementlerin kimyasal davranışlarını anlamada önemli ipuçları verir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Küresel Simetri
Küresel simetri, atomun elektronlarının uzayda her yönde eşit dağıldığı durumu ifade eder. Bu durum, tam dolu veya yarı dolu orbitallere sahip atomlarda görülür.
Verilen seçeneklerden 24Cr elementi küresel simetri gösterir çünkü elektron dizilimi [Ar]4s¹3d⁵ şeklindedir ve 3d orbitallerinin hepsi yarı doludur.
Diğer elementlerin elektron dizilimleri:
- 6C: 1s²2s²2p² (yarı dolu değil)
- 9F: 1s²2s²2p⁵ (tam dolu değil)
- 16S: 1s²2s²2p⁶3s²3p⁴ (ne tam dolu ne yarı dolu)
- 21Sc: 1s²2s²2p⁶3s²3p⁶4s²3d¹ (ne tam dolu ne yarı dolu)

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Uyarılmış Atom
Atomlar enerji aldıklarında, elektronlarının bazıları daha yüksek enerji seviyelerine çıkar. Bu duruma uyarılmış atom denir. Uyarılan elektron ise uyarılmış elektron olarak adlandırılır.
Uyarılmış atomlar kararsızdır ve temel hale dönme eğilimindedir. Bu dönüş sırasında, elektron aldığı enerjiyi foton olarak geri verir.
Örneğin, sodyum lambasının sarı ışık yayması, sodyum atomlarının uyarılma ve temel hale dönme sürecinde enerji yaymasından kaynaklanır. Bu olay günlük hayatta gördüğümüz sokak lambalarında kullanılır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Uyarılmış Atom Örnekleri
Temel haldeki 11Na elementinin elektron dizilimi 1s² 2s² 2p⁶ 3s¹ şeklindedir. Bu atom enerji aldığında farklı uyarılmış hallere geçebilir:
1. Uyarılmış hal: 1s² 2s² 2p⁶ 4s¹ (3s'deki elektron 4s'ye çıkar) 2. Uyarılmış hal: 1s² 2s² 2p⁶ 3p¹ (3s'deki elektron 3p'ye çıkar)
Bu uyarılmış hallerin hepsi temel halden daha yüksek enerjiye sahiptir. Atomlar enerjilerini en aza indirme eğiliminde olduklarından, uyarılmış elektron er ya da geç temel haline geri döner.
Uyarılmış atomlar, neon ışıkları gibi birçok günlük uygulamanın temelini oluşturur.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Orbital Şemalarının Yorumlanması
Bir atomun orbital şeması, elektronların orbitallere nasıl dağıldığını gösterir. Verilen şemada, 1s, 2s, 2p ve 3s orbitallerinin doluluk durumları gösterilmiştir.
Bu K elementi için:
- 1s ve 2s orbitalleri tam dolu
- 2p orbitalleri tam dolu (üç 2p orbitali toplam 6 elektron alır)
- 3s orbitali yarı dolu (1 elektron var)
Bu durumda atom potasyumdur (19K) ve temel haldedir. Uyarılmış halde olsaydı, elektronlar Aufbau ilkesine uymayan bir düzende olurdu. Atom enerji almadan uyarılmış hale geçemez.
Önemli: Temel haldeki atom en düşük enerji seviyesinde bulunur ve elektronlar en az enerjili orbitallere yerleşir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Değerlik Orbitali ve Değerlik Elektronu
Değerlik orbitalleri, atomun en yüksek enerji düzeyindeki orbitallerdir. Bu orbitallerde bulunan elektronlar değerlik elektronu olarak adlandırılır.
Değerlik elektronları, bir atomun kimyasal davranışını belirleyen elektronlardır. Kimyasal bağlar oluştururken rol oynayan elektronlar bunlardır.
Elektron dizilimi farklı şekilde sonlanan atomların değerlik elektron sayıları:
- ns ile sonlananlar: Değerlik elektronu = ns'deki elektron sayısı
- ns np ile sonlananlar: Değerlik elektronu = ns + np'deki elektron sayısı
- ns d ile sonlananlar: Değerlik elektronu = ns + d'deki elektron sayısı
Değerlik elektronlarını bilmek, elementlerin kimyasal bağ kurma eğilimlerini tahmin etmeyi kolaylaştırır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Electron Affinity
1Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅