Kimyasal tepkimelerdeki hesaplamalar, kimya dersinde karşımıza çıkan en önemli konulardan... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
328
•
Güncellendi May 5, 2026
•
Mervan
@mervan_ecevit
Kimyasal tepkimelerdeki hesaplamalar, kimya dersinde karşımıza çıkan en önemli konulardan... Daha fazla göster

















Kimyasal hesaplamalar, bir tepkimenin sonucunu öngörebilmemizi sağlayan önemli bir konudur. Bir deneyi yapmadan önce hangi maddeden ne kadar kullanacağımızı ve ne kadar ürün elde edeceğimizi bilmek istediğimizde bu hesaplamaları kullanırız.
Bu konuyu öğrendiğinde, günlük hayatta da karşılaştığın kimyasal olayları daha iyi anlayabileceksin. Örneğin bir mumu yaktığında gerçekleşen yanma tepkimesinde ne kadar oksijen kullanıldığını hesaplayabilirsin.
⭐ Bilgi Notu: Kimyasal hesaplamalar sadece tepkimelerle sınırlı değildir. Bu hesaplamalar sayesinde maddelerin saflığını kontrol edebilir, molekül formüllerini belirleyebilir ve tepkimelerin verimini hesaplayabilirsin!

Tepkimeye girmeden önce elimizdeki maddelerin ne kadar ürün vereceğini bilmek çok önemlidir. Mesela bir kimya deneyinde az miktarda ürün elde etmek için çok fazla madde kullanmak istemezsin, değil mi?
Kimyasal hesaplamalar sayesinde hem tepkimeye giren maddeleri hem de oluşan ürünleri miktar olarak belirleyebiliriz. Böylece deneylerimizi daha verimli planlar ve kaynakları doğru kullanırız.
Ayrıca, bu hesaplamalar endüstride de çok önemli bir yer tutar. Bir fabrikada üretim yaparken ne kadar ham maddeye ihtiyaç olduğunu ve ne kadar ürün elde edileceğini bilmek, maliyet hesaplamalarını doğru yapmamızı sağlar.
💡 Hatırlatma: Kimyasal hesaplamalar, sadece laboratuvarda değil, günlük yaşamda da karşımıza çıkar. Örneğin, yemek tariflerindeki ölçüler de bir tür kimyasal hesaplamadır!

Kimyasal hesaplamaları yaparken öncelikle tepkime denklemini doğru yazmalı ve denkleştirmelisin. Denkleştirilmemiş bir tepkimede hesaplama yapmak, yanlış sonuçlar elde etmene neden olur.
Tepkime denklemindeki katsayılar çok önemlidir. Bu sayılar, tepkimeye giren ve çıkan maddelerin mol sayılarını gösterir. Örneğin, 2H₂ + O₂ → 2H₂O tepkimesinde 2 mol hidrojen ve 1 mol oksijenden 2 mol su oluşur.
Hesaplamaları yaparken tepkimeyi mol, tanecik, hacim ve kütle açısından yorumlayabilirsin. Bu sayede farklı birimler arasında geçiş yaparak istenen hesaplamaları kolaylıkla yapabilirsin.
🔍 Püf Noktası: Tepkime denklemini denkleştirirken zorlanıyorsan, önce oksijen ve hidrojen dışındaki elementleri denkleştirerek başla. Sonra hidrojen ve en son oksijeni denkleştir. Bu yöntem genellikle işe yarar!
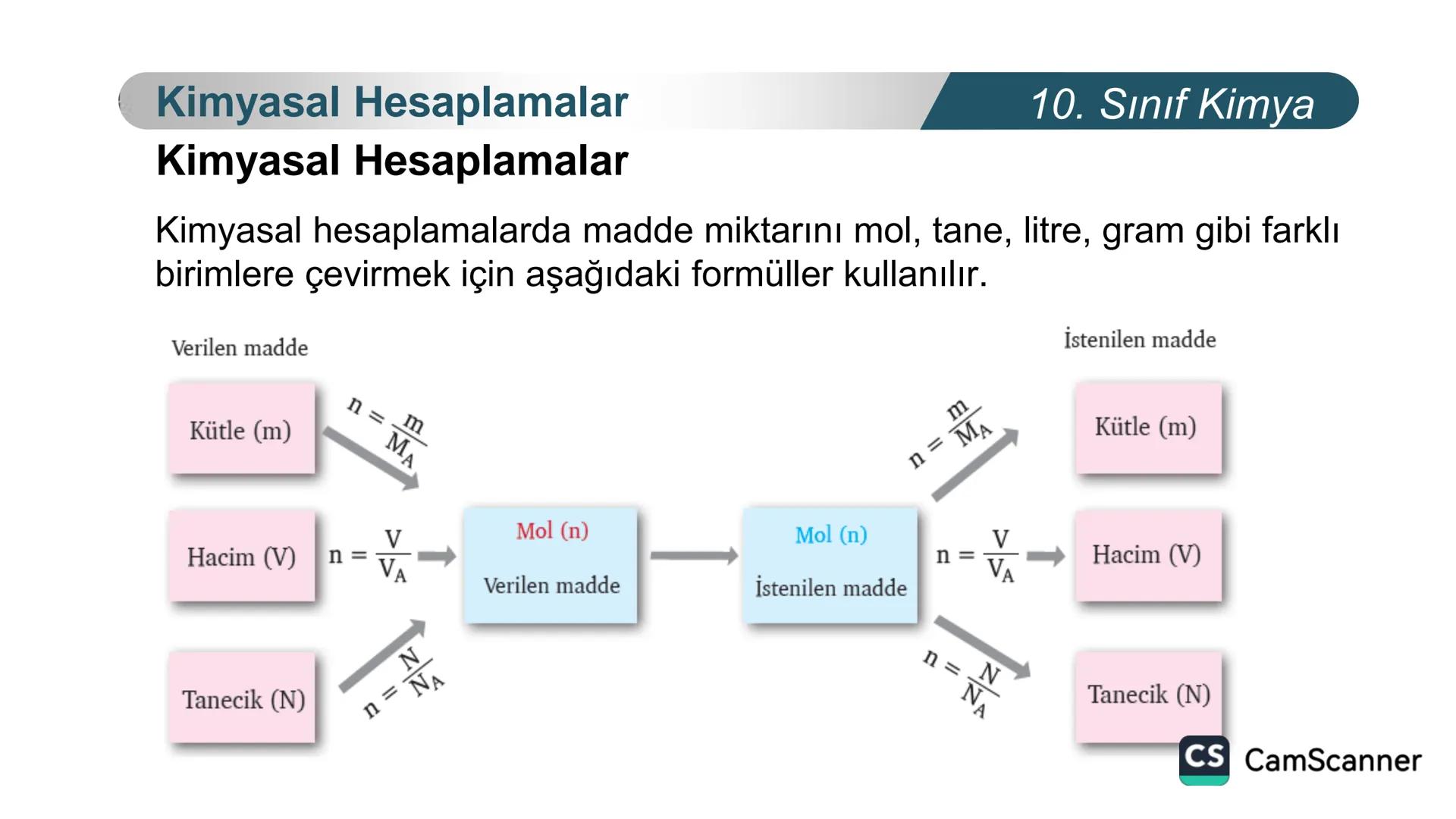
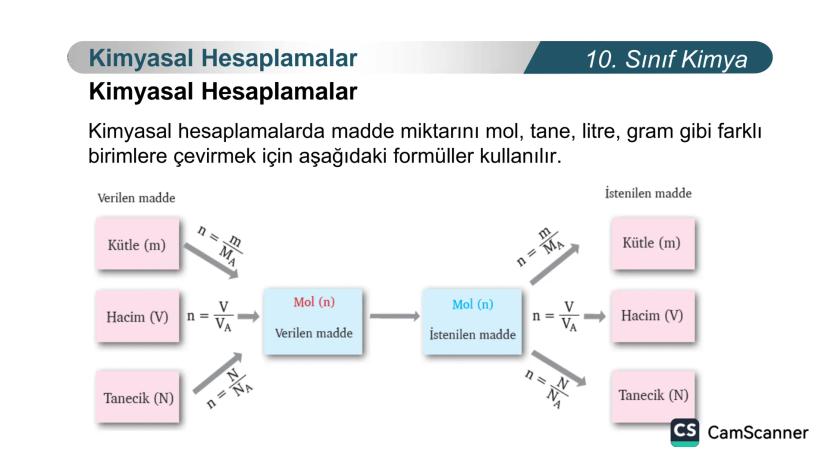
Kimyasal hesaplamalarda farklı birimleri birbirine çevirmen gerekecek. Bunun için bazı temel formülleri bilmen çok önemli.
Bir maddenin kütlesinden mol sayısını bulmak için kütle/mol kütlesi formülünü kullanabilirsin. Örneğin, 18 gram su kaç moldür? Suyun mol kütlesi 18 g/mol olduğuna göre 18/18 = 1 mol su demektir.
Gazlarda hacim ve mol arasında geçiş yapmak için normal koşullarda 1 mol gazın 22,4 litre hacim kapladığını hatırla. Eğer 44,8 litre CO₂ gazın varsa, bu 2 mol CO₂ gazı anlamına gelir.
Tanecik sayısı ile mol arasında geçiş yaparken Avogadro sayısını kullanırız. 1 mol madde 6,02 x 10²³ tane tanecik içerir.
⚠️ Önemli Uyarı: Hesaplamalarda birimlere dikkat et! Eğer mol kütlesi g/mol birimindeyse, kütle birimi gram olmalıdır. Birimler uyuşmadığında doğru sonuca ulaşamazsın.

Kimyasal tepkimelerde maddelerin mol sayıları arasındaki ilişkiye stokiyometri denir. Tepkime denklemindeki katsayılar, bize mol oranlarını gösterir.
Örneğin, C₃H₈ + 5O₂ → 3CO₂ + 4H₂O tepkimesinde 1 mol propan (C₃H₈) yakıldığında 5 mol oksijen harcanır ve 3 mol karbondioksit ile 4 mol su oluşur.
Bu ilişkiyi kullanarak bir maddeden yola çıkıp diğer maddelerin miktarlarını hesaplayabilirsin. Mesela 2 mol propan yakıldığında 10 mol oksijen harcanır ve 6 mol karbondioksit ile 8 mol su oluşur.
🌟 Hatırlatma: Stokiyometriyi günlük hayattan bir örnekle düşünebilirsin: Bir sandviç tarifi 2 dilim ekmek, 1 dilim peynir ve 3 dilim domates gerektiriyorsa, 4 sandviç yapmak için 8 dilim ekmek, 4 dilim peynir ve 12 dilim domates gerekir. Bu da bir tür stokiyometrik hesaplamadır!

Tepkime denkleminde bir maddenin miktarı verildiğinde, diğer maddelerin miktarlarını hesaplayabiliriz. Örneğin, CH₄ + 2O₂ → CO₂ + 2H₂O tepkimesinde 3 mol metan verilmişse:
a) Harcanan O₂ gazının kütlesini bulmak için önce mol sayısını bulmalısın: 3 mol CH₄ × 2 mol O₂/1 mol CH₄ = 6 mol O₂. Oksijen gazının mol kütlesi 32 g/mol olduğundan, 6 mol × 32 g/mol = 192 gram O₂ harcanır.
b) Normal koşullarda 1 mol gaz 22,4 litre hacim kaplar. 3 mol CH₄ yanarsa 3 mol CO₂ oluşur (tepkime denkleminde katsayılar 1:1). Bu durumda 3 mol × 22,4 L/mol = 67,2 litre CO₂ gazı oluşur.
c) Oluşan su miktarı için: 3 mol CH₄ × 2 mol H₂O/1 mol CH₄ = 6 mol H₂O oluşur.
🧠 İpucu: Bu tür sorularda daima tepkime denklemini yazarak başla ve katsayılara dikkat et. Katsayılar arasındaki oranlar, mol sayıları arasındaki oranları verir!

N₂ + 3H₂ → 2NH₃ tepkimesinde 0,6 mol H₂ gazı harcanırsa:
a) N₂ gazı miktarını bulmak için mol oranlarını kullan: 0,6 mol H₂ × = 0,2 mol N₂ harcanır. Tepkimedeki katsayılara göre, 3 mol H₂ için 1 mol N₂ gerektiğinden, 0,6 mol H₂ için 0,2 mol N₂ gerekir.
b) Oluşan NH₃ miktarını hesaplarken yine mol oranlarını kullan: 0,6 mol H₂ × = 0,4 mol NH₃ oluşur.
Oluşan NH₃'ün kütlesini bulmak için mol sayısıyla mol kütlesini çarp. NH₃'ün mol kütlesi = 14 + 3 × 1 = 17 g/mol. Bu durumda 0,4 mol NH₃ × 17 g/mol = 6,8 gram NH₃ oluşur.
🔧 Pratik Yöntem: Kimyasal hesaplamalarda önce mol sayılarıyla çalış, sonra gerekliyse diğer birim çevrimlerini yap. Bu yöntem, karmaşık problemleri basitleştirir.

2Al(k) + 6HCl(suda) → 2AlCl₃(suda) + 3H₂(g) tepkimesinde oluşan H₂ gazının hacmi 6,72 litre ise:
a) Al atomu sayısını bulmak için önce H₂'nin mol sayısını hesaplamalısın. Normal koşullarda 1 mol gaz 22,4 litre olduğundan, 6,72/22,4 = 0,3 mol H₂ oluşmuş demektir. Tepkime denklemine göre, 3 mol H₂ oluştuğunda 2 mol Al harcanır. Buradan 0,3 mol H₂ oluşması için 0,3 × (2/3) = 0,2 mol Al harcanır. Bu da 0,2 mol × 6,02 × 10²³ = 1,204 × 10²³ Al atomu demektir.
b) HCl miktarını bulmak için: 0,3 mol H₂ × = 0,6 mol HCl harcanmıştır.
c) AlCl₃ kütlesini hesaplamak için önce mol sayısını bul: 0,3 mol H₂ × = 0,2 mol AlCl₃ oluşur. AlCl₃'ün mol kütlesi = 27 + 3 × 35,5 = 133,5 g/mol. Bu durumda 0,2 mol × 133,5 g/mol = 26,7 gram AlCl₃ oluşur.
💫 Hatırlatma: Normal koşullar (NŞA), 0°C sıcaklık ve 1 atmosfer basınçtır. Bu koşullarda 1 mol gaz 22,4 litre hacim kaplar. Bu bilgi gaz hesaplamalarında çok işine yarayacak!

Mg(k) + 1/2O₂(g) → MgO(k) tepkimesinde 4 g MgO oluşması için:
a) Magnezyum atomu sayısını bulmak için önce MgO'nun mol sayısını hesaplamalısın. MgO'nun mol kütlesi = 24 + 16 = 40 g/mol. Bu durumda 4 g MgO × = 0,1 mol MgO demektir. Tepkime denklemine göre 1 mol MgO oluştuğunda 1 mol Mg harcanır. Bu durumda 0,1 mol Mg harcanır, bu da 0,1 mol × 6,02 × 10²³ = 6,02 × 10²² tane Mg atomu demektir.
b) O₂ gazı hacmini bulmak için mol sayısını hesapla: 0,1 mol MgO × = 0,05 mol O₂ harcanır. Normal şartlarda 0,05 mol O₂ gazının hacmi = 0,05 mol × 22,4 L/mol = 1,12 litre O₂ gazı harcanır.
🔆 Kolaylaştırıcı Yaklaşım: Hesaplamalarda zorlanıyorsan, adım adım ilerle. Önce verilenleri belirle, sonra isteneni yazıp hangi dönüşümleri yapacağını planla. Bu seni doğru sonuca götürecektir!

4NH₃(g) + 5O₂(g) → 4NO(g) + 6H₂O(g) tepkimesinde 0,6 gram NO oluştuğunda:
a) O₂ gazı hacmini bulmak için önce NO'nun mol sayısını hesaplamalısın. NO'nun mol kütlesi = 14 + 16 = 30 g/mol. Bu durumda 0,6 g NO × = 0,02 mol NO demektir. Tepkime denklemine göre, 4 mol NO oluştuğunda 5 mol O₂ harcanır. Bu durumda 0,02 mol NO için 0,02 × (5/4) = 0,025 mol O₂ harcanır. Normal şartlarda bu miktar O₂ gazının hacmi = 0,025 mol × 22,4 L/mol = 0,56 litre O₂ gazı harcanır.
b) NH₃ kütlesini hesaplamak için: 0,02 mol NO × = 0,02 mol NH₃ harcanır. NH₃'ün mol kütlesi = 14 + 3 × 1 = 17 g/mol. Bu durumda 0,02 mol × 17 g/mol = 0,34 gram NH₃ harcanır.
c) H₂O molekül sayısını bulmak için: 0,02 mol NO × = 0,03 mol H₂O oluşur. Bu da 0,03 mol × 6,02 × 10²³ molekül/mol = 1,806 × 10²² tane H₂O molekülü demektir.
🧩 Problem Çözme Stratejisi: Kompleks tepkimelerde her adımı ayrı ayrı düşün. Önce mol sayısına çevir, sonra tepkime denkleminden mol oranlarını kullanarak diğer maddelerin mol sayılarını bul, en son istenen birime dönüştür.







Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Mervan
@mervan_ecevit
Kimyasal tepkimelerdeki hesaplamalar, kimya dersinde karşımıza çıkan en önemli konulardan biridir. Bu hesaplamalar sayesinde tepkimelerden elde edilecek ürün miktarlarını önceden belirleyebilir, verimliliği ölçebilir ve hangi maddeden ne kadar kullanmamız gerektiğini hesaplayabiliriz.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal hesaplamalar, bir tepkimenin sonucunu öngörebilmemizi sağlayan önemli bir konudur. Bir deneyi yapmadan önce hangi maddeden ne kadar kullanacağımızı ve ne kadar ürün elde edeceğimizi bilmek istediğimizde bu hesaplamaları kullanırız.
Bu konuyu öğrendiğinde, günlük hayatta da karşılaştığın kimyasal olayları daha iyi anlayabileceksin. Örneğin bir mumu yaktığında gerçekleşen yanma tepkimesinde ne kadar oksijen kullanıldığını hesaplayabilirsin.
⭐ Bilgi Notu: Kimyasal hesaplamalar sadece tepkimelerle sınırlı değildir. Bu hesaplamalar sayesinde maddelerin saflığını kontrol edebilir, molekül formüllerini belirleyebilir ve tepkimelerin verimini hesaplayabilirsin!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Tepkimeye girmeden önce elimizdeki maddelerin ne kadar ürün vereceğini bilmek çok önemlidir. Mesela bir kimya deneyinde az miktarda ürün elde etmek için çok fazla madde kullanmak istemezsin, değil mi?
Kimyasal hesaplamalar sayesinde hem tepkimeye giren maddeleri hem de oluşan ürünleri miktar olarak belirleyebiliriz. Böylece deneylerimizi daha verimli planlar ve kaynakları doğru kullanırız.
Ayrıca, bu hesaplamalar endüstride de çok önemli bir yer tutar. Bir fabrikada üretim yaparken ne kadar ham maddeye ihtiyaç olduğunu ve ne kadar ürün elde edileceğini bilmek, maliyet hesaplamalarını doğru yapmamızı sağlar.
💡 Hatırlatma: Kimyasal hesaplamalar, sadece laboratuvarda değil, günlük yaşamda da karşımıza çıkar. Örneğin, yemek tariflerindeki ölçüler de bir tür kimyasal hesaplamadır!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal hesaplamaları yaparken öncelikle tepkime denklemini doğru yazmalı ve denkleştirmelisin. Denkleştirilmemiş bir tepkimede hesaplama yapmak, yanlış sonuçlar elde etmene neden olur.
Tepkime denklemindeki katsayılar çok önemlidir. Bu sayılar, tepkimeye giren ve çıkan maddelerin mol sayılarını gösterir. Örneğin, 2H₂ + O₂ → 2H₂O tepkimesinde 2 mol hidrojen ve 1 mol oksijenden 2 mol su oluşur.
Hesaplamaları yaparken tepkimeyi mol, tanecik, hacim ve kütle açısından yorumlayabilirsin. Bu sayede farklı birimler arasında geçiş yaparak istenen hesaplamaları kolaylıkla yapabilirsin.
🔍 Püf Noktası: Tepkime denklemini denkleştirirken zorlanıyorsan, önce oksijen ve hidrojen dışındaki elementleri denkleştirerek başla. Sonra hidrojen ve en son oksijeni denkleştir. Bu yöntem genellikle işe yarar!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal hesaplamalarda farklı birimleri birbirine çevirmen gerekecek. Bunun için bazı temel formülleri bilmen çok önemli.
Bir maddenin kütlesinden mol sayısını bulmak için kütle/mol kütlesi formülünü kullanabilirsin. Örneğin, 18 gram su kaç moldür? Suyun mol kütlesi 18 g/mol olduğuna göre 18/18 = 1 mol su demektir.
Gazlarda hacim ve mol arasında geçiş yapmak için normal koşullarda 1 mol gazın 22,4 litre hacim kapladığını hatırla. Eğer 44,8 litre CO₂ gazın varsa, bu 2 mol CO₂ gazı anlamına gelir.
Tanecik sayısı ile mol arasında geçiş yaparken Avogadro sayısını kullanırız. 1 mol madde 6,02 x 10²³ tane tanecik içerir.
⚠️ Önemli Uyarı: Hesaplamalarda birimlere dikkat et! Eğer mol kütlesi g/mol birimindeyse, kütle birimi gram olmalıdır. Birimler uyuşmadığında doğru sonuca ulaşamazsın.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal tepkimelerde maddelerin mol sayıları arasındaki ilişkiye stokiyometri denir. Tepkime denklemindeki katsayılar, bize mol oranlarını gösterir.
Örneğin, C₃H₈ + 5O₂ → 3CO₂ + 4H₂O tepkimesinde 1 mol propan (C₃H₈) yakıldığında 5 mol oksijen harcanır ve 3 mol karbondioksit ile 4 mol su oluşur.
Bu ilişkiyi kullanarak bir maddeden yola çıkıp diğer maddelerin miktarlarını hesaplayabilirsin. Mesela 2 mol propan yakıldığında 10 mol oksijen harcanır ve 6 mol karbondioksit ile 8 mol su oluşur.
🌟 Hatırlatma: Stokiyometriyi günlük hayattan bir örnekle düşünebilirsin: Bir sandviç tarifi 2 dilim ekmek, 1 dilim peynir ve 3 dilim domates gerektiriyorsa, 4 sandviç yapmak için 8 dilim ekmek, 4 dilim peynir ve 12 dilim domates gerekir. Bu da bir tür stokiyometrik hesaplamadır!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Tepkime denkleminde bir maddenin miktarı verildiğinde, diğer maddelerin miktarlarını hesaplayabiliriz. Örneğin, CH₄ + 2O₂ → CO₂ + 2H₂O tepkimesinde 3 mol metan verilmişse:
a) Harcanan O₂ gazının kütlesini bulmak için önce mol sayısını bulmalısın: 3 mol CH₄ × 2 mol O₂/1 mol CH₄ = 6 mol O₂. Oksijen gazının mol kütlesi 32 g/mol olduğundan, 6 mol × 32 g/mol = 192 gram O₂ harcanır.
b) Normal koşullarda 1 mol gaz 22,4 litre hacim kaplar. 3 mol CH₄ yanarsa 3 mol CO₂ oluşur (tepkime denkleminde katsayılar 1:1). Bu durumda 3 mol × 22,4 L/mol = 67,2 litre CO₂ gazı oluşur.
c) Oluşan su miktarı için: 3 mol CH₄ × 2 mol H₂O/1 mol CH₄ = 6 mol H₂O oluşur.
🧠 İpucu: Bu tür sorularda daima tepkime denklemini yazarak başla ve katsayılara dikkat et. Katsayılar arasındaki oranlar, mol sayıları arasındaki oranları verir!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
N₂ + 3H₂ → 2NH₃ tepkimesinde 0,6 mol H₂ gazı harcanırsa:
a) N₂ gazı miktarını bulmak için mol oranlarını kullan: 0,6 mol H₂ × = 0,2 mol N₂ harcanır. Tepkimedeki katsayılara göre, 3 mol H₂ için 1 mol N₂ gerektiğinden, 0,6 mol H₂ için 0,2 mol N₂ gerekir.
b) Oluşan NH₃ miktarını hesaplarken yine mol oranlarını kullan: 0,6 mol H₂ × = 0,4 mol NH₃ oluşur.
Oluşan NH₃'ün kütlesini bulmak için mol sayısıyla mol kütlesini çarp. NH₃'ün mol kütlesi = 14 + 3 × 1 = 17 g/mol. Bu durumda 0,4 mol NH₃ × 17 g/mol = 6,8 gram NH₃ oluşur.
🔧 Pratik Yöntem: Kimyasal hesaplamalarda önce mol sayılarıyla çalış, sonra gerekliyse diğer birim çevrimlerini yap. Bu yöntem, karmaşık problemleri basitleştirir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
2Al(k) + 6HCl(suda) → 2AlCl₃(suda) + 3H₂(g) tepkimesinde oluşan H₂ gazının hacmi 6,72 litre ise:
a) Al atomu sayısını bulmak için önce H₂'nin mol sayısını hesaplamalısın. Normal koşullarda 1 mol gaz 22,4 litre olduğundan, 6,72/22,4 = 0,3 mol H₂ oluşmuş demektir. Tepkime denklemine göre, 3 mol H₂ oluştuğunda 2 mol Al harcanır. Buradan 0,3 mol H₂ oluşması için 0,3 × (2/3) = 0,2 mol Al harcanır. Bu da 0,2 mol × 6,02 × 10²³ = 1,204 × 10²³ Al atomu demektir.
b) HCl miktarını bulmak için: 0,3 mol H₂ × = 0,6 mol HCl harcanmıştır.
c) AlCl₃ kütlesini hesaplamak için önce mol sayısını bul: 0,3 mol H₂ × = 0,2 mol AlCl₃ oluşur. AlCl₃'ün mol kütlesi = 27 + 3 × 35,5 = 133,5 g/mol. Bu durumda 0,2 mol × 133,5 g/mol = 26,7 gram AlCl₃ oluşur.
💫 Hatırlatma: Normal koşullar (NŞA), 0°C sıcaklık ve 1 atmosfer basınçtır. Bu koşullarda 1 mol gaz 22,4 litre hacim kaplar. Bu bilgi gaz hesaplamalarında çok işine yarayacak!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Mg(k) + 1/2O₂(g) → MgO(k) tepkimesinde 4 g MgO oluşması için:
a) Magnezyum atomu sayısını bulmak için önce MgO'nun mol sayısını hesaplamalısın. MgO'nun mol kütlesi = 24 + 16 = 40 g/mol. Bu durumda 4 g MgO × = 0,1 mol MgO demektir. Tepkime denklemine göre 1 mol MgO oluştuğunda 1 mol Mg harcanır. Bu durumda 0,1 mol Mg harcanır, bu da 0,1 mol × 6,02 × 10²³ = 6,02 × 10²² tane Mg atomu demektir.
b) O₂ gazı hacmini bulmak için mol sayısını hesapla: 0,1 mol MgO × = 0,05 mol O₂ harcanır. Normal şartlarda 0,05 mol O₂ gazının hacmi = 0,05 mol × 22,4 L/mol = 1,12 litre O₂ gazı harcanır.
🔆 Kolaylaştırıcı Yaklaşım: Hesaplamalarda zorlanıyorsan, adım adım ilerle. Önce verilenleri belirle, sonra isteneni yazıp hangi dönüşümleri yapacağını planla. Bu seni doğru sonuca götürecektir!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
4NH₃(g) + 5O₂(g) → 4NO(g) + 6H₂O(g) tepkimesinde 0,6 gram NO oluştuğunda:
a) O₂ gazı hacmini bulmak için önce NO'nun mol sayısını hesaplamalısın. NO'nun mol kütlesi = 14 + 16 = 30 g/mol. Bu durumda 0,6 g NO × = 0,02 mol NO demektir. Tepkime denklemine göre, 4 mol NO oluştuğunda 5 mol O₂ harcanır. Bu durumda 0,02 mol NO için 0,02 × (5/4) = 0,025 mol O₂ harcanır. Normal şartlarda bu miktar O₂ gazının hacmi = 0,025 mol × 22,4 L/mol = 0,56 litre O₂ gazı harcanır.
b) NH₃ kütlesini hesaplamak için: 0,02 mol NO × = 0,02 mol NH₃ harcanır. NH₃'ün mol kütlesi = 14 + 3 × 1 = 17 g/mol. Bu durumda 0,02 mol × 17 g/mol = 0,34 gram NH₃ harcanır.
c) H₂O molekül sayısını bulmak için: 0,02 mol NO × = 0,03 mol H₂O oluşur. Bu da 0,03 mol × 6,02 × 10²³ molekül/mol = 1,806 × 10²² tane H₂O molekülü demektir.
🧩 Problem Çözme Stratejisi: Kompleks tepkimelerde her adımı ayrı ayrı düşün. Önce mol sayısına çevir, sonra tepkime denkleminden mol oranlarını kullanarak diğer maddelerin mol sayılarını bul, en son istenen birime dönüştür.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
2
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı