Kimyasal tepkimeler ve türleri, maddelerin nasıl etkileşime girip değişim geçirdiğini... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
173
•
Güncellendi May 8, 2026
•
Semra Konak
@semrakonak
Kimyasal tepkimeler ve türleri, maddelerin nasıl etkileşime girip değişim geçirdiğini... Daha fazla göster

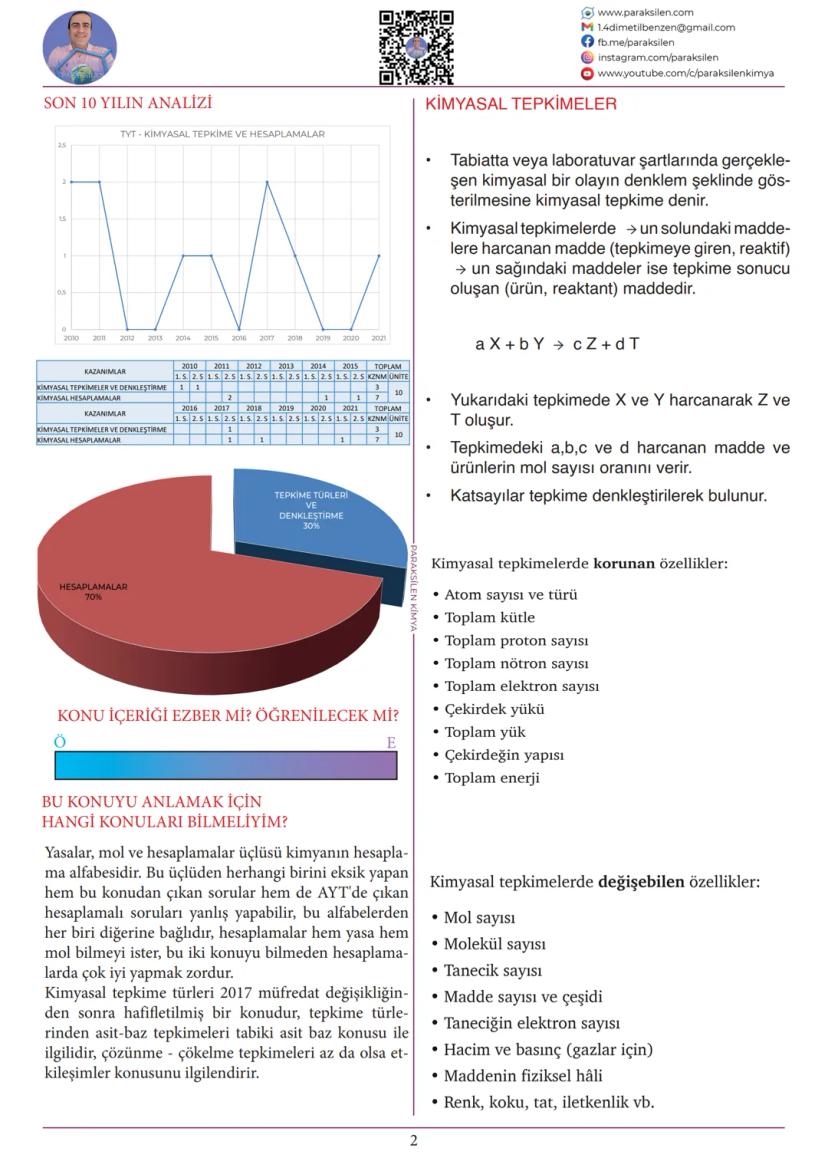








Kimyasal tepkimeler, maddelerin birbirleriyle etkileşerek yeni maddeler oluşturduğu olaylardır. Bu tepkimelerin gerçekleştiği durumları anlamak ve hesaplayabilmek, kimya dersindeki başarının temelidir.
Bu konuda TYT kimya sınavlarında düzenli olarak sorular çıkmaktadır. Son yıllarda özellikle kimyasal tepkime türleri ve denkleştirme ile ilgili sorular karşımıza çıkmaktadır.
İpucu: Kimyasal tepkimeler konusunu anlamak için mol kavramı ve kimya yasalarını iyi bilmen gerekir. Bunlar kimyanın hesaplama alfabesidir!
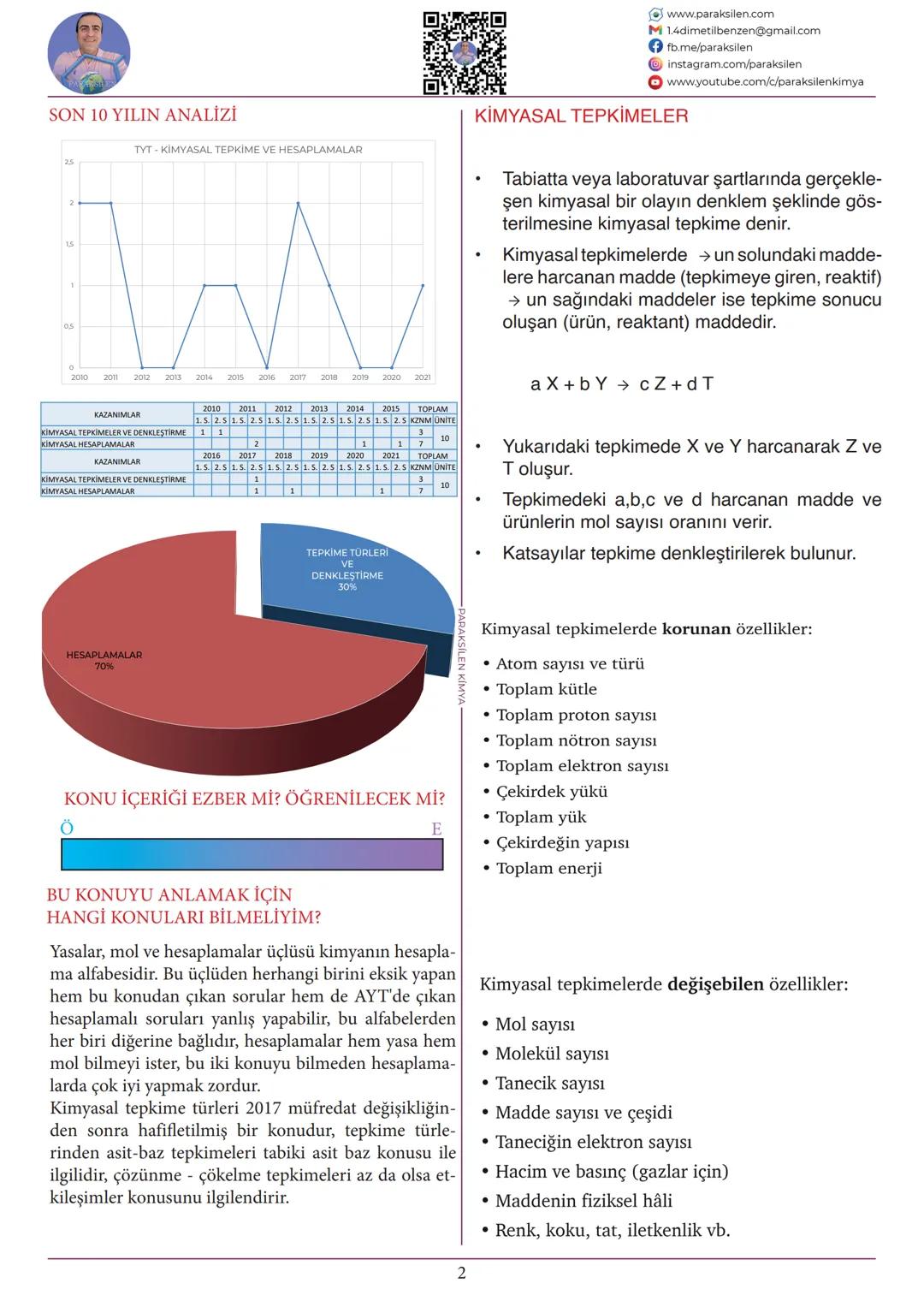
Kimyasal tepkime, tabiatta veya laboratuvarda gerçekleşen olayların denklem şeklinde gösterilmesidir. Tepkimenin sol tarafındaki maddeler reaktif (tepkimeye giren), sağ tarafındakiler ise ürün (tepkime sonucu oluşan) maddelerdir.
Bir tepkimede aX + bY → cZ + dT şeklinde gösterilirken, a, b, c ve d katsayıları tepkimeye giren ve oluşan maddelerin mol sayısı oranını verir. Bu katsayılar denkleştirme yapılarak bulunur.
Kimyasal tepkimelerde korunanlar:
Kimyasal tepkimelerde değişebilen özellikler:
Not: Kimyasal tepkime türleri konusu 2017'den sonra biraz hafifletilmiş olsa da, asit-baz tepkimeleri ve çözünme-çökelme tepkimeleri diğer konularla ilişkilidir.

Denkleştirme, bir tepkimenin girenleri ile ürünlerindeki atom sayılarını eşitleme işlemidir. Bir tepkimede reaktiflerdeki atom sayıları ve türleri ile ürünlerdeki atom sayıları ve türleri birbirine eşit olmalıdır.
Denkleştirme yaparken şu adımları takip edebilirsin:
Örneğin:
Önemli: Denkleştirme yapılırken atomların korunduğu unutulmamalı! Bir tepkime denkleştirildiğinde katsayılar en küçük tam sayı değerlerini almalıdır.
Denkleştirme işlemi, kimyasal hesaplamaların doğru yapılması için çok önemlidir. ÖSYM sınavlarında genellikle denkleştirilmiş tepkimelerdeki katsayılarla ilgili sorular sorulmaktadır.

Reaktiflerinde O₂ olan tüm tepkimeler yanma tepkimesi olarak adlandırılır. Yanma tepkimelerinde:
Elementler yandığında → o elementin oksidi oluşur C + O₂ → CO₂
Bileşikler yandığında → bileşikteki her elementin ayrı ayrı oksit bileşiği oluşur CH₄ + O₂ → CO₂ + H₂O
Hidrokarbonların (C ve H içeren bileşikler) yanmasında CO₂ ve H₂O oluşur Denkleştirme sırasında önce C, sonra H, en son O denkleştirilir
Yanmanın gerçekleşmesi için üç şart gereklidir: Yanıcı madde, yakıcı madde (hava veya O₂) ve tutuşma sıcaklığı.
Dikkat: Eğer ortamda yeterli oksijen yoksa, karbonlu maddeler tam yanmaz ve zehirli CO gazı oluşabilir!
İki veya daha fazla kimyasal maddenin birleşerek yeni bir madde oluşturduğu tepkimelere sentez tepkimesi denir. Sentez tepkimelerinde:
Örnekler:

Bir bileşiğin birden fazla kimyasal türe ayrılmasına analiz tepkimesi denir. Bu tepkimelerde:
Örnekler:
Analiz tepkimeleri, sentez tepkimelerinin tersidir. Sentez tepkimelerinde küçük yapılar birleşerek daha büyük yapılar oluştururken, analiz tepkimelerinde büyük yapılar parçalanarak küçük yapılara dönüşür.
İpucu: Analiz ve sentez tepkimelerini karşılaştırarak öğrenmek daha kolay olabilir. Biri birleşme, diğeri ayrışma gösterir.
Yangın söndürücülerde genellikle yanma koşullarını ortadan kaldıracak gazlar (CO₂, N₂ gibi) kullanılır. Bu gazlar yanma için gerekli oksijeni uzaklaştırır ve tutuşma sıcaklığını düşürür.
Analiz tepkimeleri genellikle ısı, ışık veya elektrik enerjisi gibi dış etkilerle gerçekleşir. Bu tepkimeler kimya laboratuvarlarında maddelerin bileşimini belirlemek için sıkça kullanılır.

Asitler, suda çözündüğünde H⁺ iyonu veren maddelerdir. Ekşi tada sahiptirler. Meyvelerin ekşi tadının kaynağı içerdikleri asitlerdir.
Yaygın asitler:
Asitler suya H⁺ verirken, aslında oluşan H₃O⁺ iyonudur (hidronyum iyonu). Bu nedenle asitler suya H₃O⁺ veren maddeler olarak da tanımlanabilir.
Not: Asit ve bazları günlük hayatta sıkça görürsün. Örneğin limon suyu asidik, sabun ise baziktir.
Bazlar, suda çözündüğünde OH⁻ iyonu veren maddelerdir. Acı tada sahiptirler ve ele kayganlık hissi verirler. Sabunun kaygan olmasının nedeni bazik özelliğidir.
Yaygın bazlar:
Asit ve bazın tepkimeye girerek tuz ve su oluşturmasına nötralleşme tepkimesi denir:

Nötralleşme tepkimelerinde, asitten gelen H⁺ iyonu ile bazdan gelen OH⁻ iyonu birleşerek su (H₂O) oluşturur. Asitten ve bazdan geriye kalan iyonlar ise tuz oluşturur.
H⁺ + OH⁻ → H₂O
Örnek:
Önemli notlar:
Unutma: Nötralleşme tepkimelerinde mutlaka su oluşur. Eğer su oluşmuyorsa, bu sadece bir asit-baz tepkimesidir.
İki sulu çözeltinin karışarak yeni ve suda çözünmeyen bir tuz oluşturması ile gerçekleşen tepkimelere çözünme-çökelme tepkimesi denir.
Çözünme-çökelme tepkimeleri, maddelerin fiziksel halinden anlaşılır: (suda) + (suda) → (k) + (suda)
Örnekler:
Çözünme-çökelme tepkimelerinde çöken maddenin nasıl oluştuğunu gösteren tepkimeye net iyon denklemi, tepkimeye katılmayan iyonlara ise seyirci iyon denir.

Bir tepkimenin hangi tür olduğunu anlamak için şu ipuçlarına dikkat edebilirsin:
Çözünme-çökelme tepkimelerinde 1A metallerinin tuzları ve NO₃⁻ iyonunun tuzları genellikle seyirci iyondur. Bu tepkimelerde net iyon denklemi, gerçekte tepkimeye giren iyonları gösterir.
Pratik bilgi: Tepkimeleri sınıflandırırken reaktif ve ürünlerin fiziksel halleri önemlidir. Çözünme-çökelme tepkimelerinde (suda) + (suda) → (k) + (suda) şeklinde bir düzen görürsün.
Sentez tepkimeleri genellikle ısı açığa çıkarır (ekzotermik), analiz tepkimeleri ise genellikle ısı alır (endotermik).
ÖSYM sınavlarında sıklıkla tepkimelerin türünü belirleme ile ilgili sorular çıkmaktadır. Kimyasal tepkime türlerini iyi anlayarak bu soruları kolayca çözebilirsin.
Örnek: AgNO₃(suda) + NaCl(suda) → AgCl(k) + NaNO₃(suda) Net iyon denklemi: Ag⁺ + Cl⁻ → AgCl(k) Seyirci iyonlar: Na⁺ ve NO₃⁻

Kimyasal tepkimelerin türlerini doğru belirlemek için şu noktaları hatırla:
Yanma tepkimeleri:
Sentez tepkimeleri:
Analiz tepkimeleri:
Asit-baz tepkimeleri:
Çözünme-çökelme tepkimeleri:
Sınav ipucu: Tepkime türlerini belirlerken tepkimedeki maddelerin fiziksel hallerine, tepkimeye giren ve ürün maddelerine dikkat et. Sınavda genellikle tepkimelerin türünü belirleme veya verilen bir tepkimenin hangi türe ait olduğunu sorma şeklinde sorular çıkmaktadır.
Kimyasal tepkimeler ve türleri konusunda kendini geliştirdikçe, mol hesaplamaları ve kimyasal denklemlerle ilgili soruları daha kolay çözebileceksin. Bu konu kimyanın temelidir ve ilerleyen konuları da daha iyi anlamanı sağlayacaktır.
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Semra Konak
@semrakonak
Kimyasal tepkimeler ve türleri, maddelerin nasıl etkileşime girip değişim geçirdiğini anlamamızı sağlar. Bu konu, kimya dersindeki hesaplamalar ve temel kimya yasaları için çok önemlidir. Aşağıda kimyasal tepkime türleri, denkleştirme ve özelliklerini anlaşılır biçimde özetledik.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal tepkimeler, maddelerin birbirleriyle etkileşerek yeni maddeler oluşturduğu olaylardır. Bu tepkimelerin gerçekleştiği durumları anlamak ve hesaplayabilmek, kimya dersindeki başarının temelidir.
Bu konuda TYT kimya sınavlarında düzenli olarak sorular çıkmaktadır. Son yıllarda özellikle kimyasal tepkime türleri ve denkleştirme ile ilgili sorular karşımıza çıkmaktadır.
İpucu: Kimyasal tepkimeler konusunu anlamak için mol kavramı ve kimya yasalarını iyi bilmen gerekir. Bunlar kimyanın hesaplama alfabesidir!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal tepkime, tabiatta veya laboratuvarda gerçekleşen olayların denklem şeklinde gösterilmesidir. Tepkimenin sol tarafındaki maddeler reaktif (tepkimeye giren), sağ tarafındakiler ise ürün (tepkime sonucu oluşan) maddelerdir.
Bir tepkimede aX + bY → cZ + dT şeklinde gösterilirken, a, b, c ve d katsayıları tepkimeye giren ve oluşan maddelerin mol sayısı oranını verir. Bu katsayılar denkleştirme yapılarak bulunur.
Kimyasal tepkimelerde korunanlar:
Kimyasal tepkimelerde değişebilen özellikler:
Not: Kimyasal tepkime türleri konusu 2017'den sonra biraz hafifletilmiş olsa da, asit-baz tepkimeleri ve çözünme-çökelme tepkimeleri diğer konularla ilişkilidir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Denkleştirme, bir tepkimenin girenleri ile ürünlerindeki atom sayılarını eşitleme işlemidir. Bir tepkimede reaktiflerdeki atom sayıları ve türleri ile ürünlerdeki atom sayıları ve türleri birbirine eşit olmalıdır.
Denkleştirme yaparken şu adımları takip edebilirsin:
Örneğin:
Önemli: Denkleştirme yapılırken atomların korunduğu unutulmamalı! Bir tepkime denkleştirildiğinde katsayılar en küçük tam sayı değerlerini almalıdır.
Denkleştirme işlemi, kimyasal hesaplamaların doğru yapılması için çok önemlidir. ÖSYM sınavlarında genellikle denkleştirilmiş tepkimelerdeki katsayılarla ilgili sorular sorulmaktadır.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Reaktiflerinde O₂ olan tüm tepkimeler yanma tepkimesi olarak adlandırılır. Yanma tepkimelerinde:
Elementler yandığında → o elementin oksidi oluşur C + O₂ → CO₂
Bileşikler yandığında → bileşikteki her elementin ayrı ayrı oksit bileşiği oluşur CH₄ + O₂ → CO₂ + H₂O
Hidrokarbonların (C ve H içeren bileşikler) yanmasında CO₂ ve H₂O oluşur Denkleştirme sırasında önce C, sonra H, en son O denkleştirilir
Yanmanın gerçekleşmesi için üç şart gereklidir: Yanıcı madde, yakıcı madde (hava veya O₂) ve tutuşma sıcaklığı.
Dikkat: Eğer ortamda yeterli oksijen yoksa, karbonlu maddeler tam yanmaz ve zehirli CO gazı oluşabilir!
İki veya daha fazla kimyasal maddenin birleşerek yeni bir madde oluşturduğu tepkimelere sentez tepkimesi denir. Sentez tepkimelerinde:
Örnekler:

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bir bileşiğin birden fazla kimyasal türe ayrılmasına analiz tepkimesi denir. Bu tepkimelerde:
Örnekler:
Analiz tepkimeleri, sentez tepkimelerinin tersidir. Sentez tepkimelerinde küçük yapılar birleşerek daha büyük yapılar oluştururken, analiz tepkimelerinde büyük yapılar parçalanarak küçük yapılara dönüşür.
İpucu: Analiz ve sentez tepkimelerini karşılaştırarak öğrenmek daha kolay olabilir. Biri birleşme, diğeri ayrışma gösterir.
Yangın söndürücülerde genellikle yanma koşullarını ortadan kaldıracak gazlar (CO₂, N₂ gibi) kullanılır. Bu gazlar yanma için gerekli oksijeni uzaklaştırır ve tutuşma sıcaklığını düşürür.
Analiz tepkimeleri genellikle ısı, ışık veya elektrik enerjisi gibi dış etkilerle gerçekleşir. Bu tepkimeler kimya laboratuvarlarında maddelerin bileşimini belirlemek için sıkça kullanılır.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Asitler, suda çözündüğünde H⁺ iyonu veren maddelerdir. Ekşi tada sahiptirler. Meyvelerin ekşi tadının kaynağı içerdikleri asitlerdir.
Yaygın asitler:
Asitler suya H⁺ verirken, aslında oluşan H₃O⁺ iyonudur (hidronyum iyonu). Bu nedenle asitler suya H₃O⁺ veren maddeler olarak da tanımlanabilir.
Not: Asit ve bazları günlük hayatta sıkça görürsün. Örneğin limon suyu asidik, sabun ise baziktir.
Bazlar, suda çözündüğünde OH⁻ iyonu veren maddelerdir. Acı tada sahiptirler ve ele kayganlık hissi verirler. Sabunun kaygan olmasının nedeni bazik özelliğidir.
Yaygın bazlar:
Asit ve bazın tepkimeye girerek tuz ve su oluşturmasına nötralleşme tepkimesi denir:

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Nötralleşme tepkimelerinde, asitten gelen H⁺ iyonu ile bazdan gelen OH⁻ iyonu birleşerek su (H₂O) oluşturur. Asitten ve bazdan geriye kalan iyonlar ise tuz oluşturur.
H⁺ + OH⁻ → H₂O
Örnek:
Önemli notlar:
Unutma: Nötralleşme tepkimelerinde mutlaka su oluşur. Eğer su oluşmuyorsa, bu sadece bir asit-baz tepkimesidir.
İki sulu çözeltinin karışarak yeni ve suda çözünmeyen bir tuz oluşturması ile gerçekleşen tepkimelere çözünme-çökelme tepkimesi denir.
Çözünme-çökelme tepkimeleri, maddelerin fiziksel halinden anlaşılır: (suda) + (suda) → (k) + (suda)
Örnekler:
Çözünme-çökelme tepkimelerinde çöken maddenin nasıl oluştuğunu gösteren tepkimeye net iyon denklemi, tepkimeye katılmayan iyonlara ise seyirci iyon denir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bir tepkimenin hangi tür olduğunu anlamak için şu ipuçlarına dikkat edebilirsin:
Çözünme-çökelme tepkimelerinde 1A metallerinin tuzları ve NO₃⁻ iyonunun tuzları genellikle seyirci iyondur. Bu tepkimelerde net iyon denklemi, gerçekte tepkimeye giren iyonları gösterir.
Pratik bilgi: Tepkimeleri sınıflandırırken reaktif ve ürünlerin fiziksel halleri önemlidir. Çözünme-çökelme tepkimelerinde (suda) + (suda) → (k) + (suda) şeklinde bir düzen görürsün.
Sentez tepkimeleri genellikle ısı açığa çıkarır (ekzotermik), analiz tepkimeleri ise genellikle ısı alır (endotermik).
ÖSYM sınavlarında sıklıkla tepkimelerin türünü belirleme ile ilgili sorular çıkmaktadır. Kimyasal tepkime türlerini iyi anlayarak bu soruları kolayca çözebilirsin.
Örnek: AgNO₃(suda) + NaCl(suda) → AgCl(k) + NaNO₃(suda) Net iyon denklemi: Ag⁺ + Cl⁻ → AgCl(k) Seyirci iyonlar: Na⁺ ve NO₃⁻

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal tepkimelerin türlerini doğru belirlemek için şu noktaları hatırla:
Yanma tepkimeleri:
Sentez tepkimeleri:
Analiz tepkimeleri:
Asit-baz tepkimeleri:
Çözünme-çökelme tepkimeleri:
Sınav ipucu: Tepkime türlerini belirlerken tepkimedeki maddelerin fiziksel hallerine, tepkimeye giren ve ürün maddelerine dikkat et. Sınavda genellikle tepkimelerin türünü belirleme veya verilen bir tepkimenin hangi türe ait olduğunu sorma şeklinde sorular çıkmaktadır.
Kimyasal tepkimeler ve türleri konusunda kendini geliştirdikçe, mol hesaplamaları ve kimyasal denklemlerle ilgili soruları daha kolay çözebileceksin. Bu konu kimyanın temelidir ve ilerleyen konuları da daha iyi anlamanı sağlayacaktır.
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
1
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı