Kimyasal Hesaplamalar konusu, kimyanın temel taşlarından biridir. Bu konuda mol... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
493
•
Güncellendi May 2, 2026
•
İrem Karaman
@iremkaram_8os86
Kimyasal Hesaplamalar konusu, kimyanın temel taşlarından biridir. Bu konuda mol... Daha fazla göster



















Kimyasal hesaplamalar, kimyanın matematik yönünü oluşturur. Bu bölümde mol kavramı, atom kütlesi ve molekül ağırlığı gibi temel kavramları öğreneceğiz.
Ayrıca en basit formül bulma, reaksiyon denklemlerini yazma ve stokiyometri hesaplamalarını yapma yeteneği kazanacağız. Bu konular kimya dersinde başarılı olmak için kritik öneme sahiptir.
Hatırlatma: Kimyasal hesaplamalar, laboratuvar deneylerinden endüstriyel üretime kadar kimyanın her alanında kullanılır. Bu hesaplamaları iyi anladığında birçok kimya sorusunu kolaylıkla çözebileceksin!

Mol, bir kimyasal türün miktarını ifade eden temel SI birimidir ve her zaman kimyasal formülle birlikte kullanılır. 1 mol, 12 gram 12C izotopunda bulunan atom sayısı kadar parçacık içerir.
1 mol, Avogadro sayısı kadar atom, molekül veya iyon demektir. Yani:
Bir maddenin mol kütlesi, o maddenin 1 molünün gram cinsinden kütlesidir. Milimol ise molün binde biri (1/1000) olarak tanımlanır.
İpucu: Mol kavramı anlaşılması zor gelebilir, ama günlük hayattan bir örnek düşünebilirsin: Nasıl 1 düzine = 12 tane ise, 1 mol de 6,02×10^23 tane parçacık demektir!

Atomik kütle birimi (akb) veya u, nötral bir 12C atomunun kütlesinin 1/12'si olarak tanımlanır. Atom kütlesi, atomların o kadar küçük olması nedeniyle doğrudan ölçülemediğinden, bağıl olarak ifade edilir.
Bir maddenin mol kütlesi, o maddenin 1 molünün gram cinsinden kütlesidir. Örneğin:
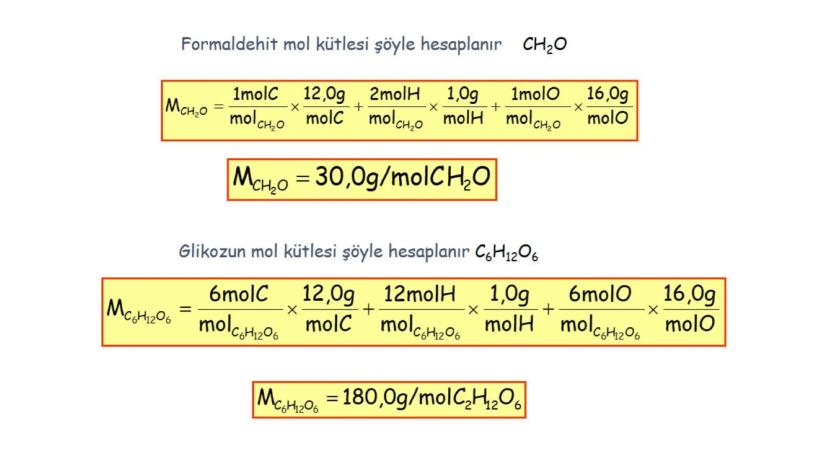
Mol kütlesi, bileşiği oluşturan tüm elementlerin atom kütlelerinin toplamından bulunur. Örneğin formaldehit (CH₂O) için:
Dikkat: Molekül kütlesi atom kütlesi birimi (u) ile, mol kütlesi ise gram ile ifade edilir, ancak sayısal değerleri aynıdır!

Mol hesaplamaları, bir maddenin kütlesiyle mol sayısı arasındaki dönüşümleri yapmamızı sağlar. Temel formül:
Mol sayısı = Maddenin kütlesi (g) / Mol kütlesi
Örneğin, 2,00 gram benzoik asitin kaç mol olduğunu hesaplamak için:
Mol sayısı = 2,00 g / 122,1 g/mol = 0,0164 mol benzoik asit
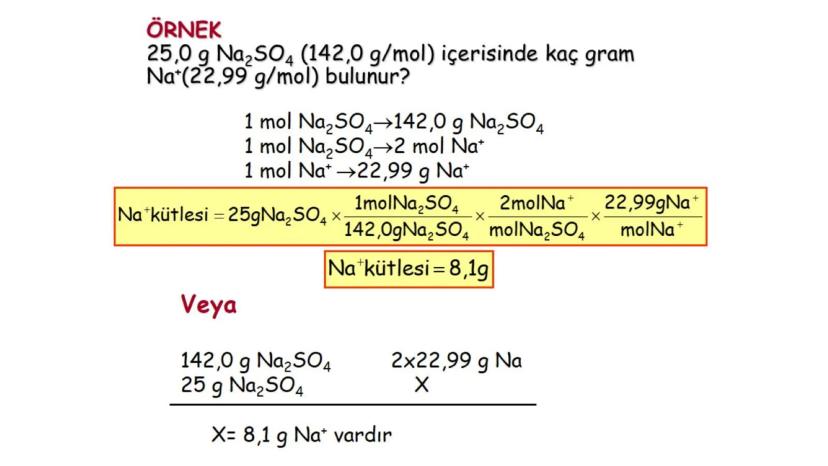
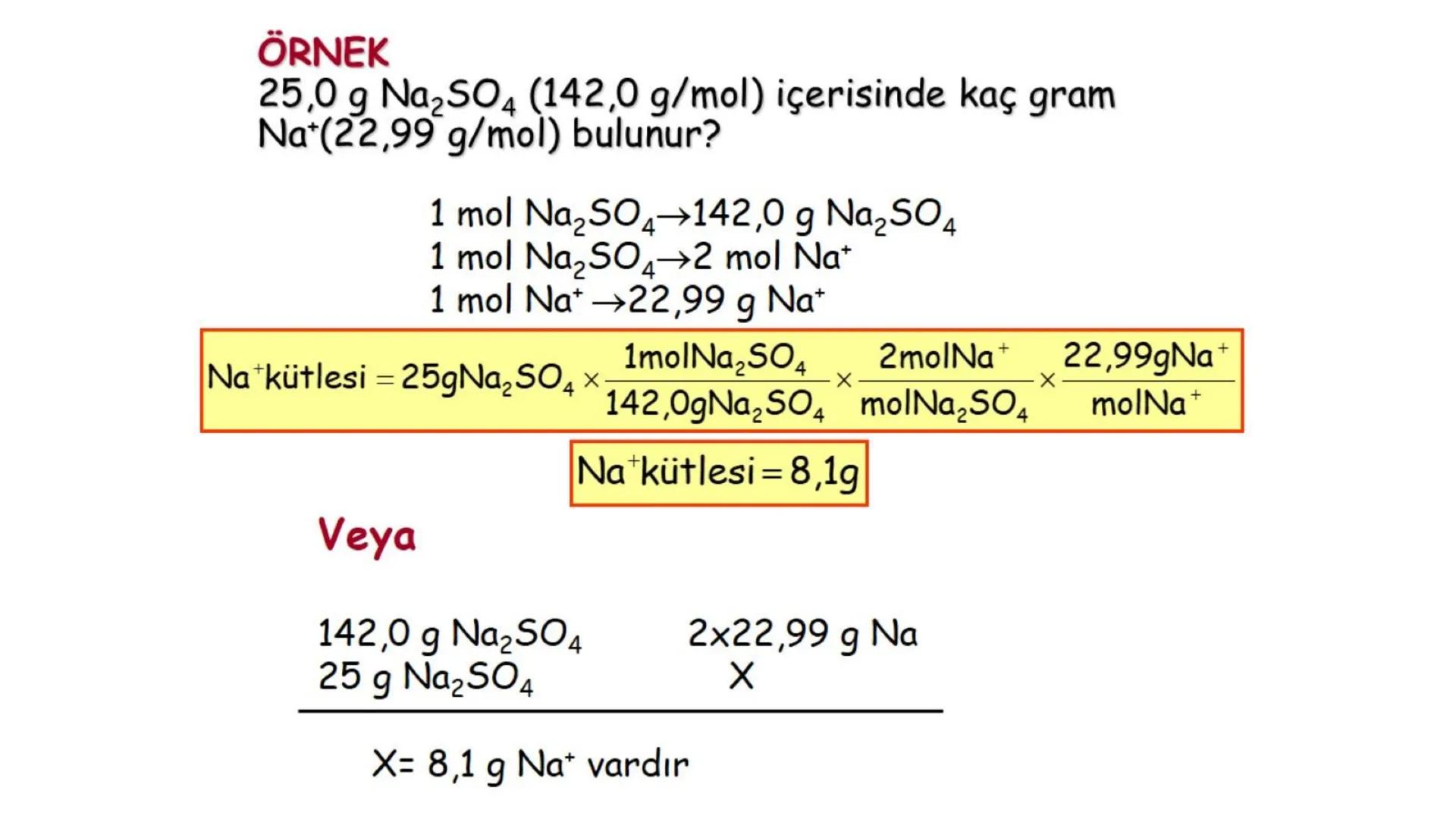
Bir bileşik içindeki bir elementin miktarını hesaplamak için de mol kavramını kullanırız. Örneğin, 25,0 g Na2SO4 içindeki Na miktarını hesaplarken:
Püf nokta: Mol hesaplamalarında birim kontrolü yapmak çok önemlidir! Birimlerin birbirini götürdüğünden emin ol.

Kimyasal tepkime denklemlerini kullanarak, tepkimeye giren ve çıkan maddelerin mol sayılarını hesaplayabiliriz. Bu bize tepkimede ne kadar madde kullanıldığını ve ne kadar ürün oluşacağını hesaplama imkanı verir.
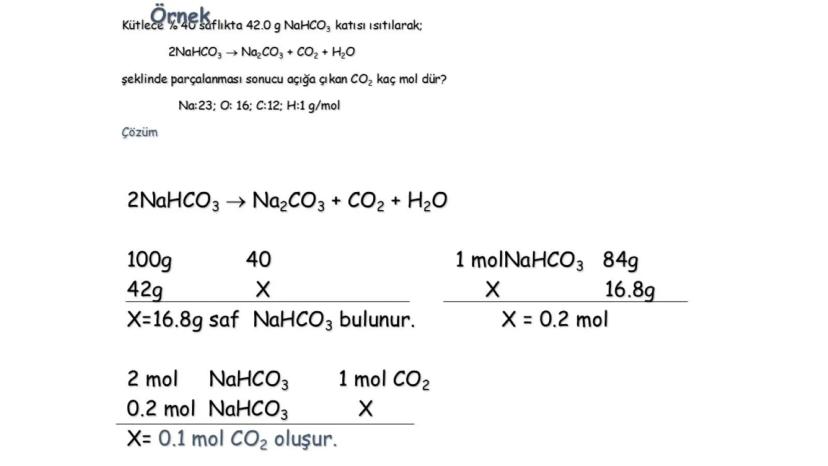
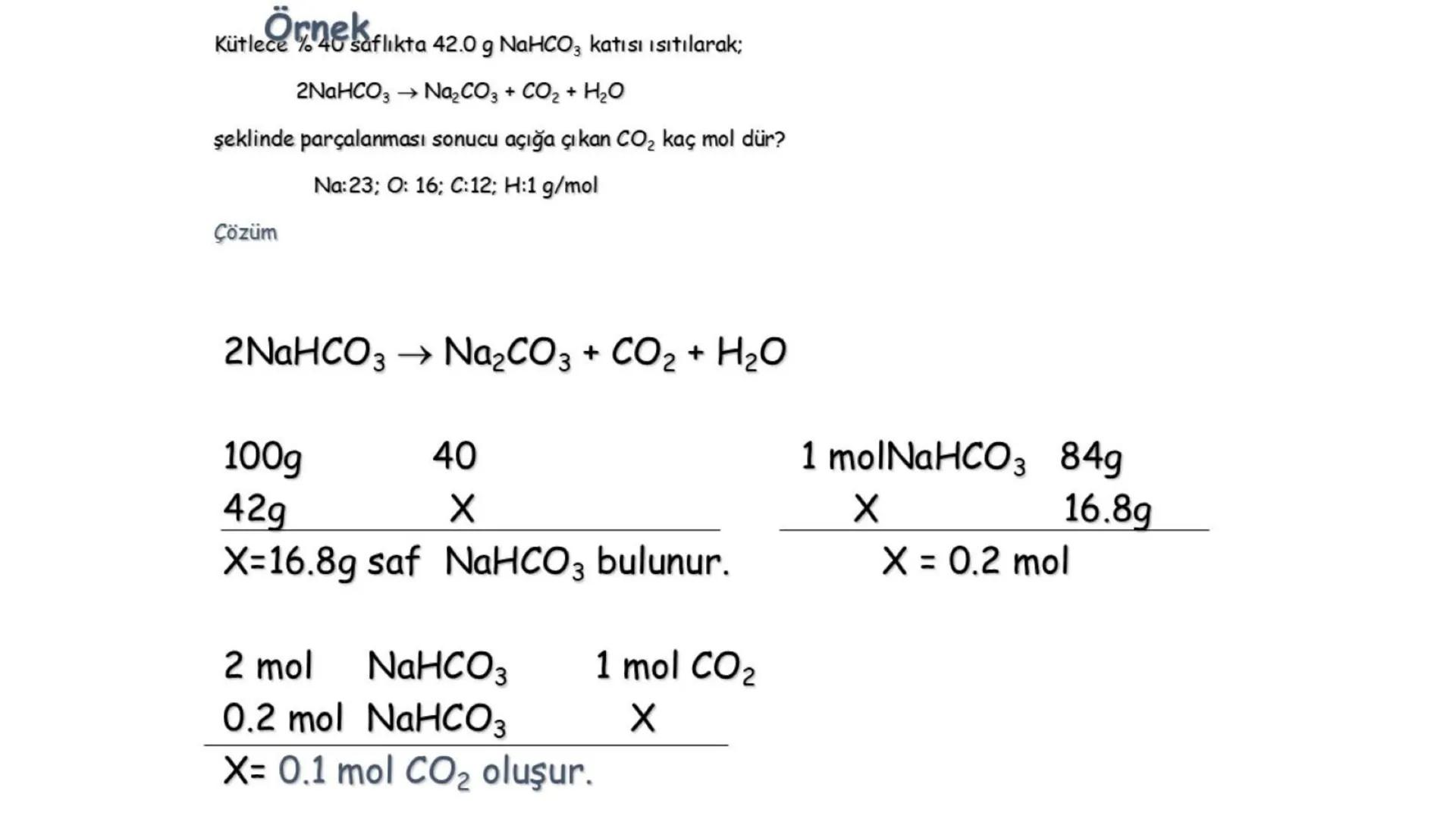
Örnek bir hesaplama: Kütlece %40 saflıkta 42,0 g NaHCO3 katısının ısıtılmasıyla gerçekleşen 2NaHCO3 → Na2CO3 + CO2 + H2O tepkimesinde oluşan CO2 miktarını hesaplayalım:
Önce saf NaHCO3 miktarını bulalım:
Mol hesabı:
Tepkime denkleminden:
Sınav ipucu: Tepkime hesaplamalarında önce saflık gibi faktörleri dikkate alarak gerçek madde miktarını bulmalısın!
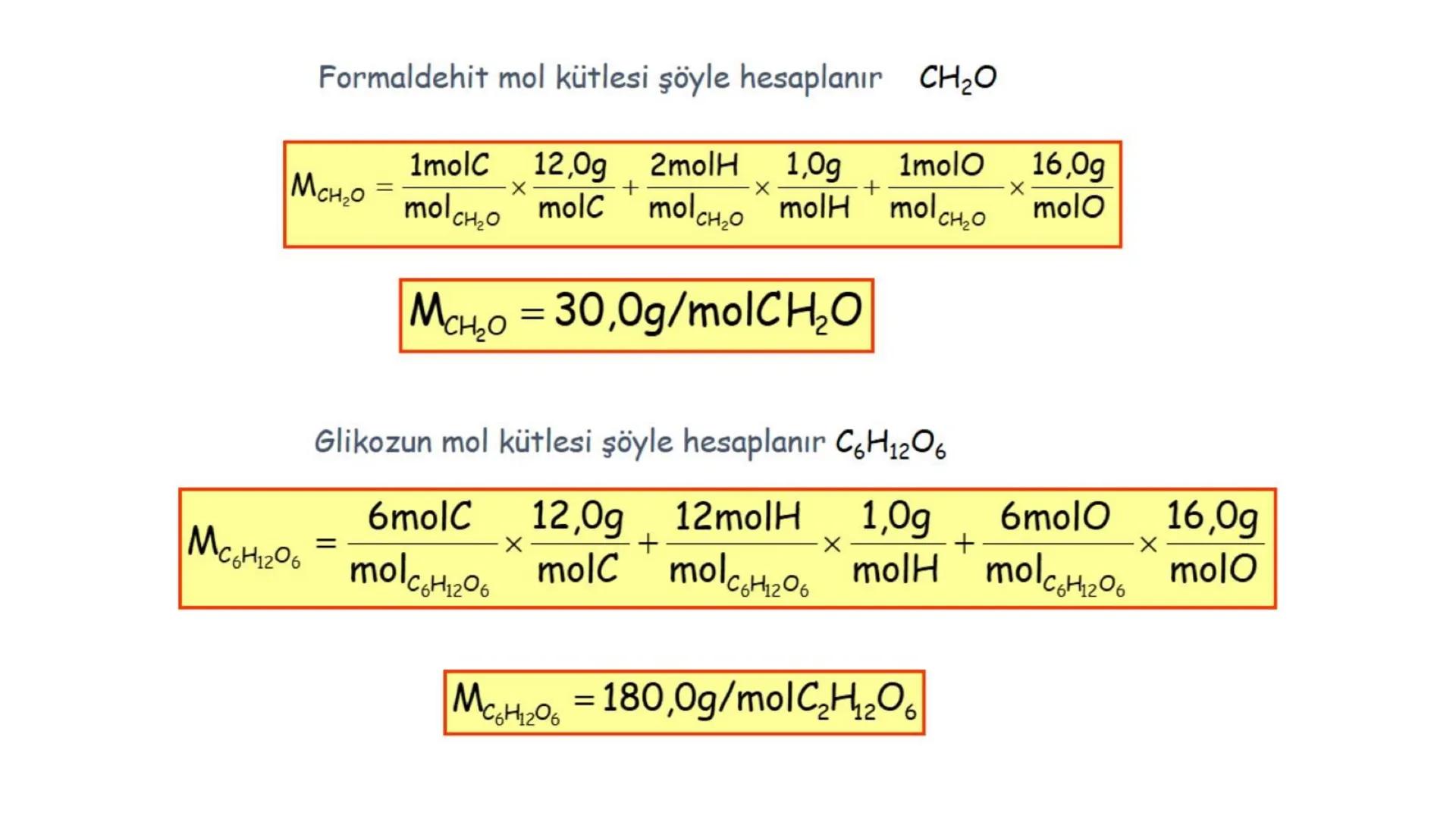
Kimyasal formüller, bileşiklerin yapısı ve bileşimi hakkında bilgi verir. Üç temel formül türü vardır:
Ampirik (En Basit) Formül: Bileşikteki elementlerin en basit tam sayılı oranını gösterir. Örneğin CH₂O (formaldehit için).
Molekül Formülü: Bir moleküldeki atomların gerçek sayısını gösterir. Hesaplanması için bileşiğin mol kütlesinin bilinmesi gerekir. Örneğin, asetik asit (C2H4O2), gliseraldehit (C3H6O3) ve glikoz (C6H12O6) aynı ampirik formüle (CH₂O) sahip olabilir.
Yapısal Formül: Moleküldeki atomların nasıl bağlandığını gösterir. Örneğin, etanol (C2H5OH) ve dimetileter (CH3OCH3) aynı molekül formülüne (C2H6O) sahip olmasına rağmen farklı yapısal formüllere sahiptir.
Hatırlatma: Molekül formülü, ampirik formülün tam sayı katı şeklindedir. Molekül kütlesi ve ampirik formül biliniyorsa molekül formülü bulunabilir.

En basit formülü bulmak için şu adımları izleriz:
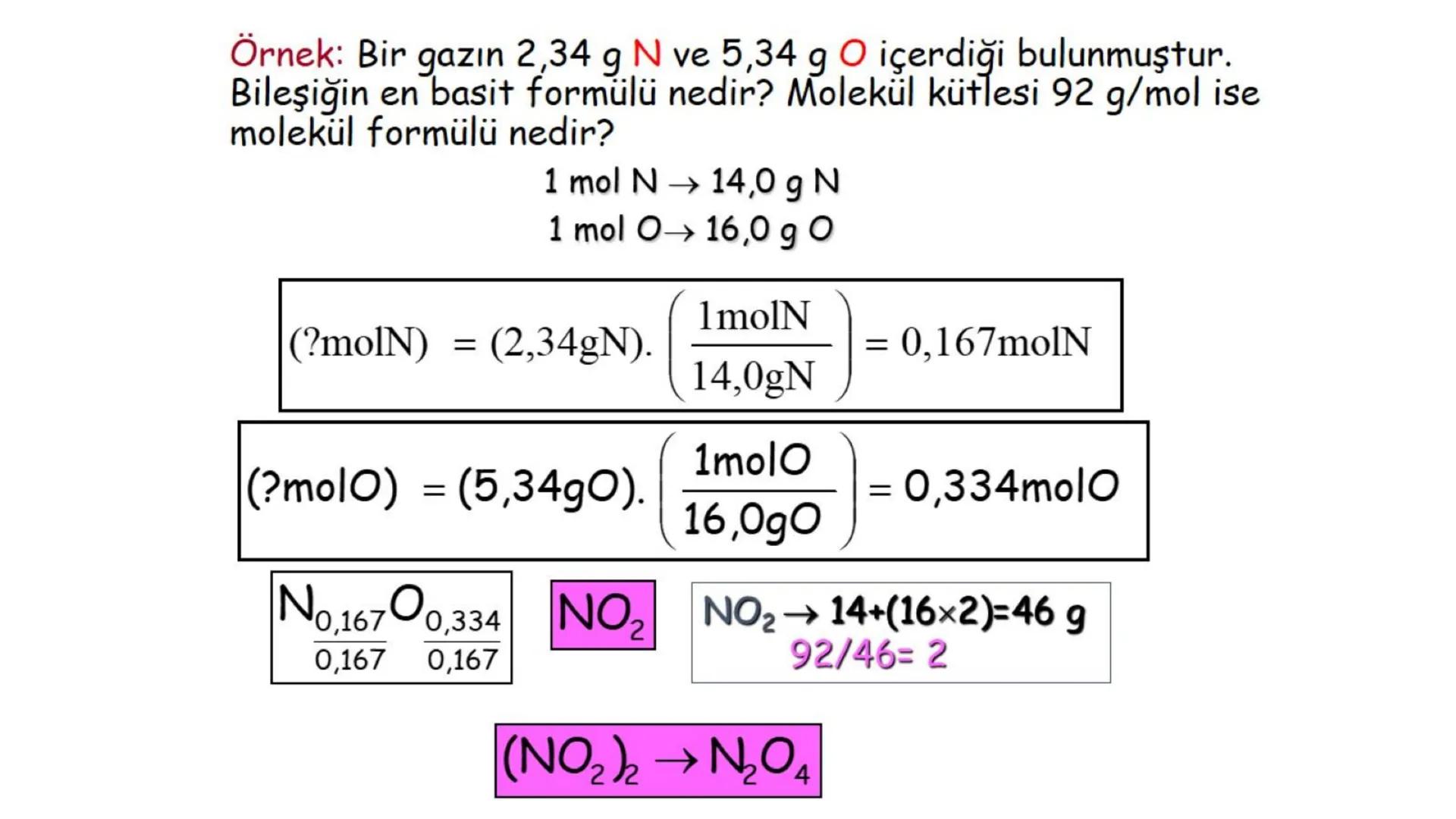
Örnek: %43,7 P ve %56,3 O içeren bir fosfor oksit bileşiğinin en basit formülünü bulalım:
Molekül kütlesi 284 g/mol ise molekül formülü:
İpucu: En basit formül hesaplamalarında daima en küçük oranı 1'e indirgemeli ve sonuçta tam sayıya ulaşmak için uygun bir çarpan bulmalısın!
Redoks reaksiyonları, elektron alışverişinin gerçekleştiği tepkimelerdir. Bu tepkimelerde:
Yükseltgenme sayısı (basamağı), bir atomun sahip olmuş göründüğü yüktür. Bir atomun yükseltgenme sayısını belirlemek için bazı temel kurallar vardır:
Önemli not: Redoks tepkimelerinde, bir madde yükseltgenirken diğeri mutlaka indirgenir. Yükseltgenme ve indirgenme olayları her zaman birlikte gerçekleşir!
Yükseltgenme sayısı hesaplamak için kullanılan bazı önemli kurallar:
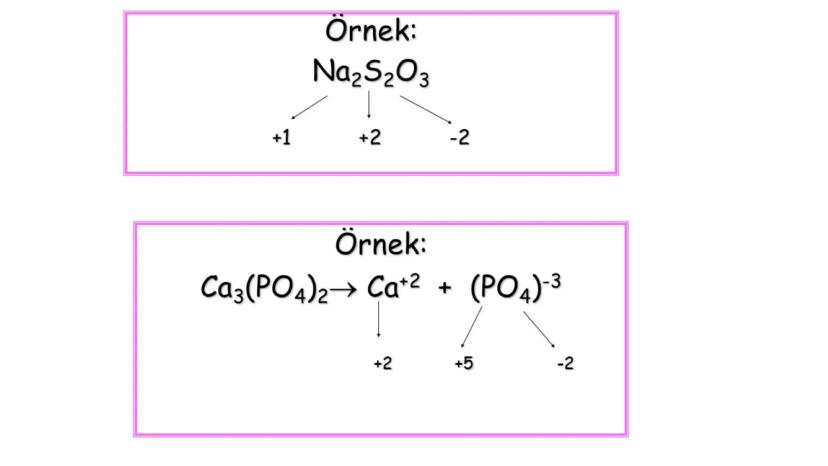
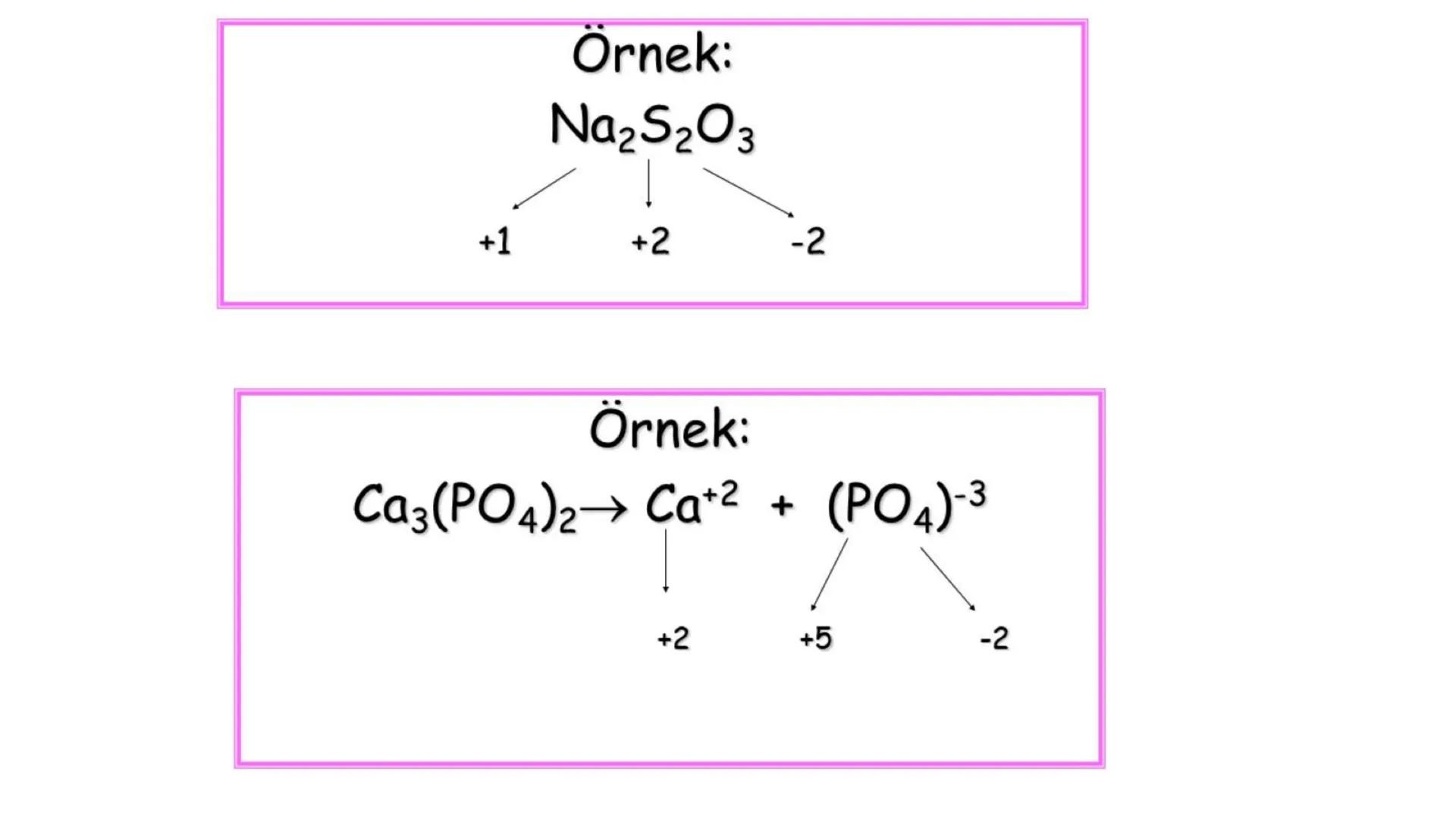
Karmaşık bir bileşikte bilinmeyen yükseltgenme sayısını hesaplamak için, bilinen yükseltgenme sayılarını ve bileşiğin toplam yükünü kullanırız. Örnek:
Na2S2O3 bileşiğinde S'nin yükseltgenme sayısı:
Taktik: Yükseltgenme sayısı hesaplamalarında, bilinen değerleri yazıp toplam yük denkleminden bilinmeyen yükseltgenme sayılarını çözmelisin!











Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
İrem Karaman
@iremkaram_8os86
Kimyasal Hesaplamalar konusu, kimyanın temel taşlarından biridir. Bu konuda mol kavramı, atom kütlesi, moleküler formüller ve reaksiyonlar gibi kimyanın matematiksel yönünü oluşturan kavramları öğreneceğiz. Bu bilgiler kimyanın diğer konularını anlamanın anahtarıdır.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal hesaplamalar, kimyanın matematik yönünü oluşturur. Bu bölümde mol kavramı, atom kütlesi ve molekül ağırlığı gibi temel kavramları öğreneceğiz.
Ayrıca en basit formül bulma, reaksiyon denklemlerini yazma ve stokiyometri hesaplamalarını yapma yeteneği kazanacağız. Bu konular kimya dersinde başarılı olmak için kritik öneme sahiptir.
Hatırlatma: Kimyasal hesaplamalar, laboratuvar deneylerinden endüstriyel üretime kadar kimyanın her alanında kullanılır. Bu hesaplamaları iyi anladığında birçok kimya sorusunu kolaylıkla çözebileceksin!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Mol, bir kimyasal türün miktarını ifade eden temel SI birimidir ve her zaman kimyasal formülle birlikte kullanılır. 1 mol, 12 gram 12C izotopunda bulunan atom sayısı kadar parçacık içerir.
1 mol, Avogadro sayısı kadar atom, molekül veya iyon demektir. Yani:
Bir maddenin mol kütlesi, o maddenin 1 molünün gram cinsinden kütlesidir. Milimol ise molün binde biri (1/1000) olarak tanımlanır.
İpucu: Mol kavramı anlaşılması zor gelebilir, ama günlük hayattan bir örnek düşünebilirsin: Nasıl 1 düzine = 12 tane ise, 1 mol de 6,02×10^23 tane parçacık demektir!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Atomik kütle birimi (akb) veya u, nötral bir 12C atomunun kütlesinin 1/12'si olarak tanımlanır. Atom kütlesi, atomların o kadar küçük olması nedeniyle doğrudan ölçülemediğinden, bağıl olarak ifade edilir.
Bir maddenin mol kütlesi, o maddenin 1 molünün gram cinsinden kütlesidir. Örneğin:
Mol kütlesi, bileşiği oluşturan tüm elementlerin atom kütlelerinin toplamından bulunur. Örneğin formaldehit (CH₂O) için:
Dikkat: Molekül kütlesi atom kütlesi birimi (u) ile, mol kütlesi ise gram ile ifade edilir, ancak sayısal değerleri aynıdır!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Mol hesaplamaları, bir maddenin kütlesiyle mol sayısı arasındaki dönüşümleri yapmamızı sağlar. Temel formül:
Mol sayısı = Maddenin kütlesi (g) / Mol kütlesi
Örneğin, 2,00 gram benzoik asitin kaç mol olduğunu hesaplamak için:
Mol sayısı = 2,00 g / 122,1 g/mol = 0,0164 mol benzoik asit
Bir bileşik içindeki bir elementin miktarını hesaplamak için de mol kavramını kullanırız. Örneğin, 25,0 g Na2SO4 içindeki Na miktarını hesaplarken:
Püf nokta: Mol hesaplamalarında birim kontrolü yapmak çok önemlidir! Birimlerin birbirini götürdüğünden emin ol.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal tepkime denklemlerini kullanarak, tepkimeye giren ve çıkan maddelerin mol sayılarını hesaplayabiliriz. Bu bize tepkimede ne kadar madde kullanıldığını ve ne kadar ürün oluşacağını hesaplama imkanı verir.
Örnek bir hesaplama: Kütlece %40 saflıkta 42,0 g NaHCO3 katısının ısıtılmasıyla gerçekleşen 2NaHCO3 → Na2CO3 + CO2 + H2O tepkimesinde oluşan CO2 miktarını hesaplayalım:
Önce saf NaHCO3 miktarını bulalım:
Mol hesabı:
Tepkime denkleminden:
Sınav ipucu: Tepkime hesaplamalarında önce saflık gibi faktörleri dikkate alarak gerçek madde miktarını bulmalısın!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal formüller, bileşiklerin yapısı ve bileşimi hakkında bilgi verir. Üç temel formül türü vardır:
Ampirik (En Basit) Formül: Bileşikteki elementlerin en basit tam sayılı oranını gösterir. Örneğin CH₂O (formaldehit için).
Molekül Formülü: Bir moleküldeki atomların gerçek sayısını gösterir. Hesaplanması için bileşiğin mol kütlesinin bilinmesi gerekir. Örneğin, asetik asit (C2H4O2), gliseraldehit (C3H6O3) ve glikoz (C6H12O6) aynı ampirik formüle (CH₂O) sahip olabilir.
Yapısal Formül: Moleküldeki atomların nasıl bağlandığını gösterir. Örneğin, etanol (C2H5OH) ve dimetileter (CH3OCH3) aynı molekül formülüne (C2H6O) sahip olmasına rağmen farklı yapısal formüllere sahiptir.
Hatırlatma: Molekül formülü, ampirik formülün tam sayı katı şeklindedir. Molekül kütlesi ve ampirik formül biliniyorsa molekül formülü bulunabilir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
En basit formülü bulmak için şu adımları izleriz:
Örnek: %43,7 P ve %56,3 O içeren bir fosfor oksit bileşiğinin en basit formülünü bulalım:
Molekül kütlesi 284 g/mol ise molekül formülü:
İpucu: En basit formül hesaplamalarında daima en küçük oranı 1'e indirgemeli ve sonuçta tam sayıya ulaşmak için uygun bir çarpan bulmalısın!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Redoks reaksiyonları, elektron alışverişinin gerçekleştiği tepkimelerdir. Bu tepkimelerde:
Yükseltgenme sayısı (basamağı), bir atomun sahip olmuş göründüğü yüktür. Bir atomun yükseltgenme sayısını belirlemek için bazı temel kurallar vardır:
Önemli not: Redoks tepkimelerinde, bir madde yükseltgenirken diğeri mutlaka indirgenir. Yükseltgenme ve indirgenme olayları her zaman birlikte gerçekleşir!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Yükseltgenme sayısı hesaplamak için kullanılan bazı önemli kurallar:
Karmaşık bir bileşikte bilinmeyen yükseltgenme sayısını hesaplamak için, bilinen yükseltgenme sayılarını ve bileşiğin toplam yükünü kullanırız. Örnek:
Na2S2O3 bileşiğinde S'nin yükseltgenme sayısı:
Taktik: Yükseltgenme sayısı hesaplamalarında, bilinen değerleri yazıp toplam yük denkleminden bilinmeyen yükseltgenme sayılarını çözmelisin!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
12
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı