Kimyasal denge, kimya dersinde önemli konulardan biri ve aslında günlük... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
301
•
Güncellendi May 16, 2026
•
eloss
@eloslogy
Kimyasal denge, kimya dersinde önemli konulardan biri ve aslında günlük... Daha fazla göster

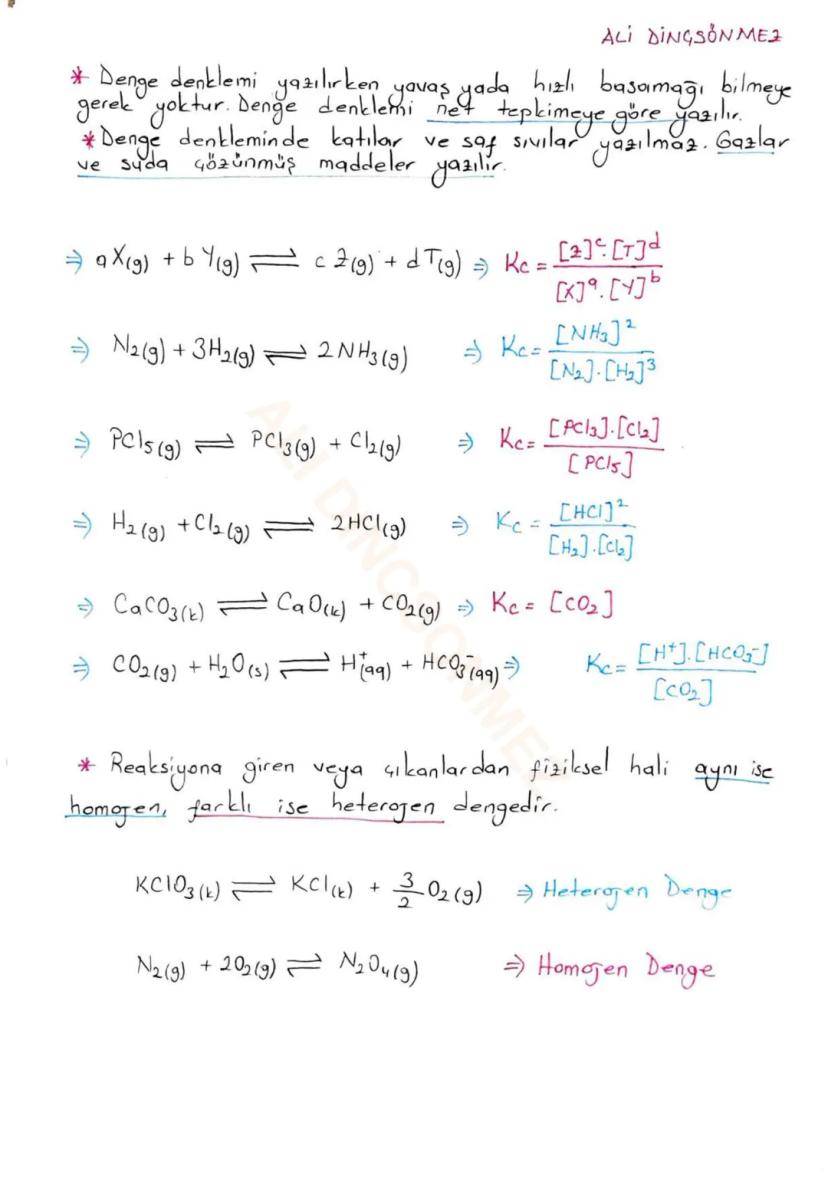

















Günlük hayatta sürekli denge halindeki sistemlerle karşılaşıyorsun - örneğin bardağındaki suyun buharlaşması! Dinamik denge, evrendeki maddelerin maksimum düzensiz olma ve minimum enerjiye sahip olma eğilimlerinin uzlaşmasıyla oluşur.
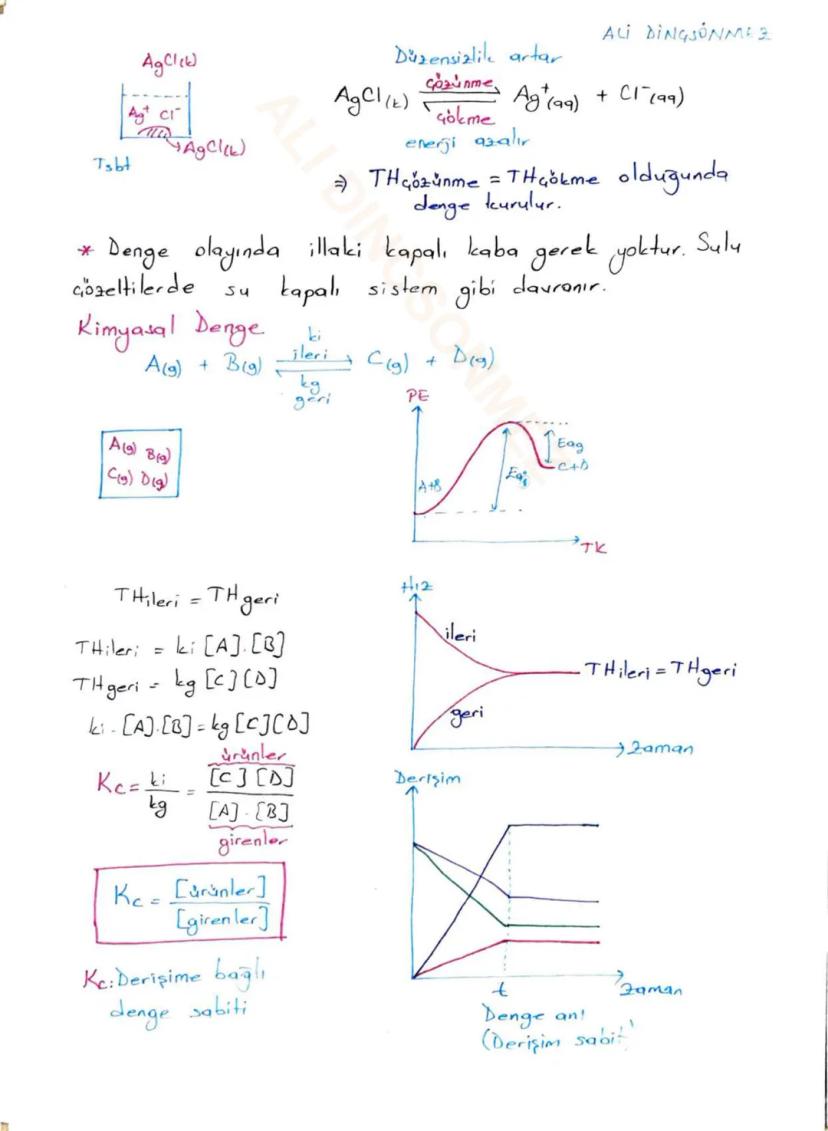
Denge kurulması için iki şart var: sıcaklık sabit olmalı ve sistem kapalı olmalıdir. Denge anında ileri tepkime hızı ile geri tepkime hızı eşit olur .
Bu süreç hiç durmaz - denge dinamiktir! Gözle görülebilir değişiklik olmasa da moleküler düzeyde sürekli hareket vardır. Su örneğinde buharlaşma ve yoğunlaşma hızları eşit olduğunda denge kurulur.
💡 Önemli Not: Dengede maddeler hiçbir zaman tamamen bitmez ve maddelerin derişimi sabittir!
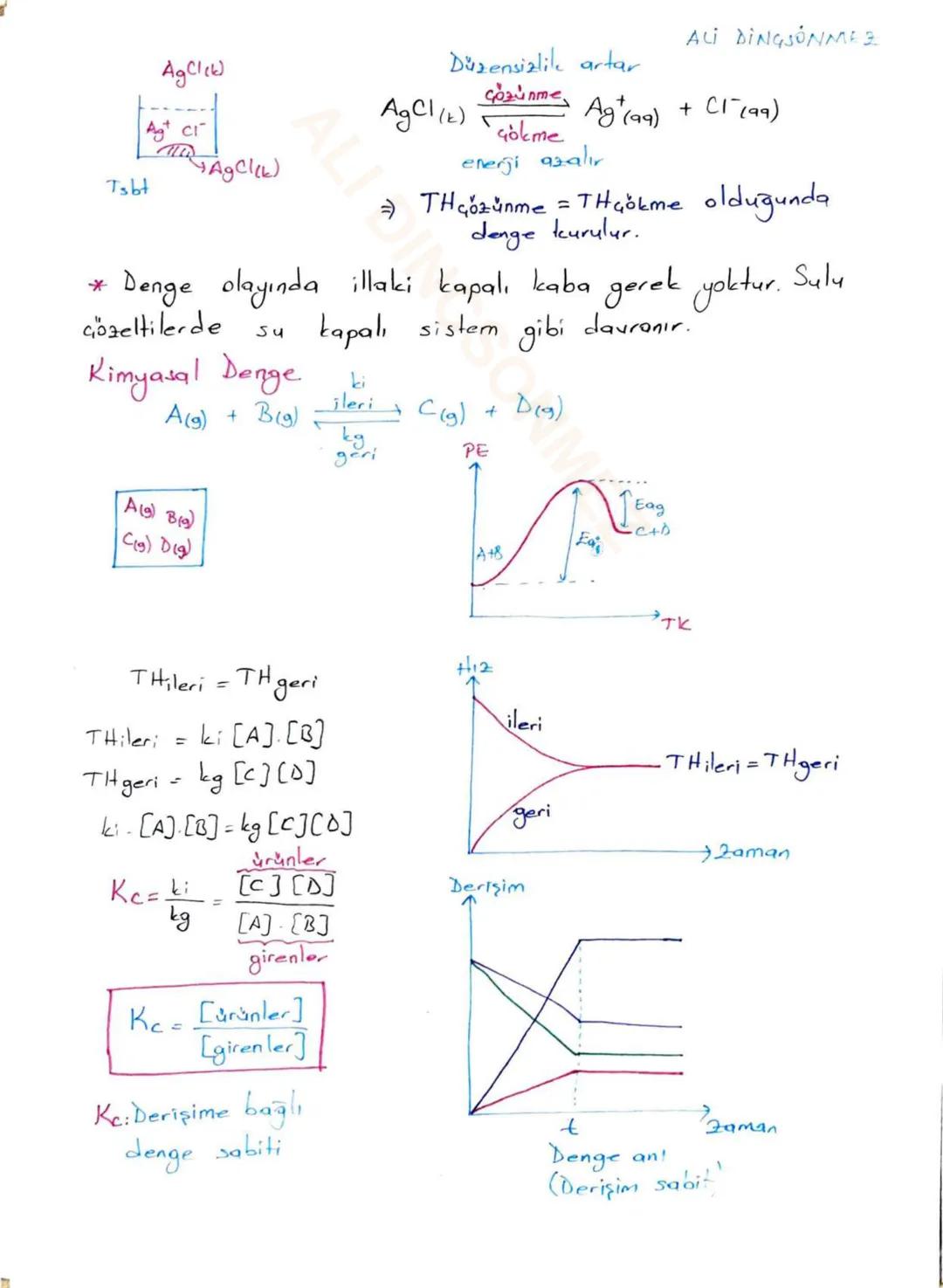
Denge sabitini anlamak aslında çok kolay - sadece ürünlerin derişiminin girenlerin derişimine oranı! Bu oran her zaman aynı kalır ve Kc ile gösterilir.
Genel tepkime için: aA + bB ⇌ cC + dD ise Kc = [C]^c[D]^d / [A]^a[B]^b olur. İleri ve geri tepkime hızları eşit olduğunda bu değer sabit kalır.
Önemli bir nokta: katılar ve saf sıvılar denge ifadesine yazılmaz, sadece gazlar ve suda çözünmüş maddeler yazılır. Bu yüzden CaCO₃(k) ⇌ CaO(k) + CO₂(g) tepkimesinde Kc = [CO₂] olur.
💡 Pratik İpucu: Fiziksel halleri aynı olan maddeler homogen denge, farklı olanlar heterogen denge oluşturur!
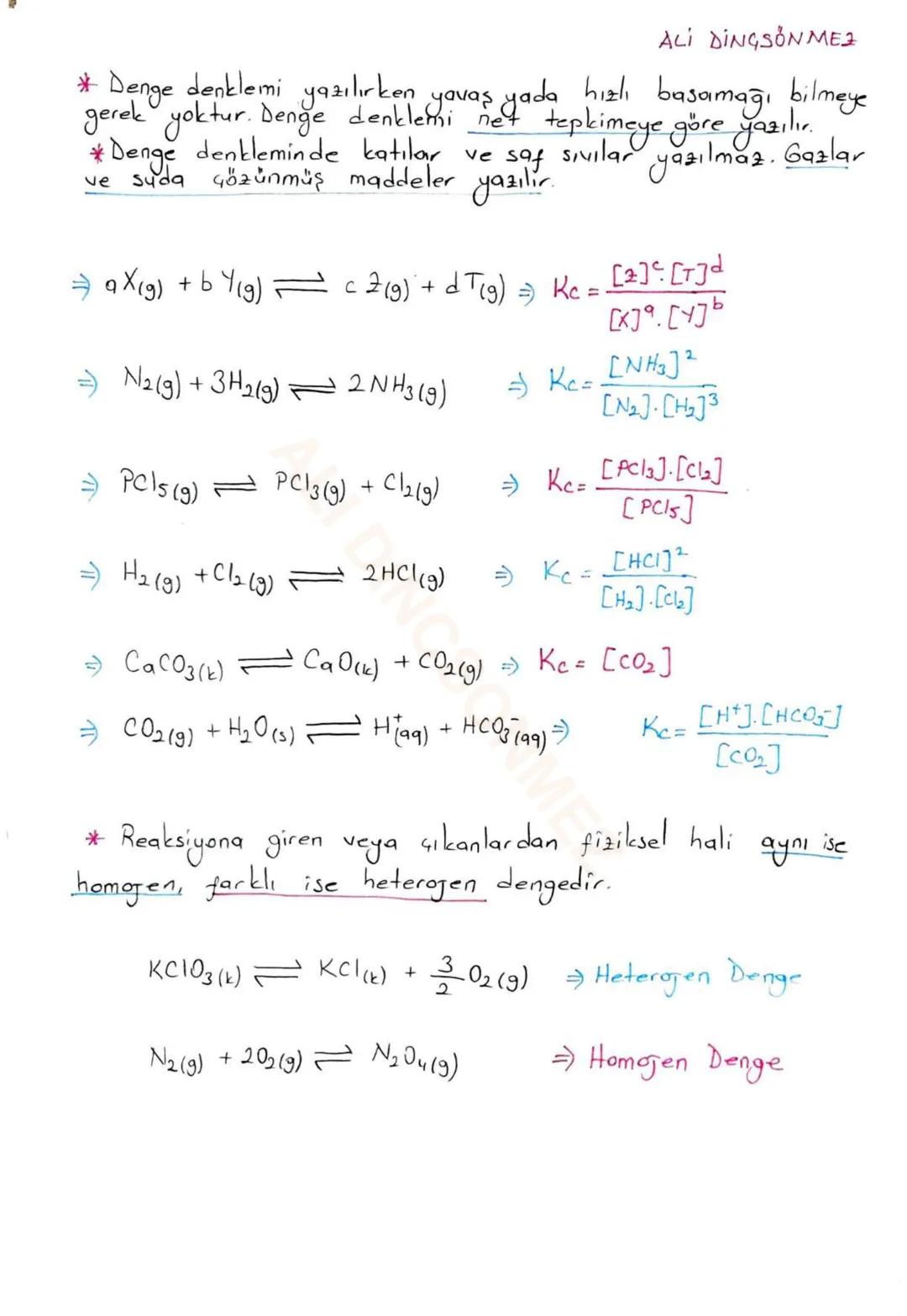
Denge denklemi yazarken net tepkimeyi kullanıyoruz - hangi basamağın yavaş olduğunu bilmeye gerek yok! Bu senin işini çok kolaylaştırır.
Temel kurallar şunlar: Katılar ve saf sıvılar yazılmaz, sadece gazlar ve suda çözünmüş maddeler yazılır. Örneğin N₂(g) + 3H₂(g) ⇌ 2NH₃(g) için Kc = [NH₃]²/[N₂][H₂]³ olur.
PCl₅(g) ⇌ PCl₃(g) + Cl₂(g) gibi basit bir tepkimede Kc = [PCl₃][Cl₂]/[PCl₅] şeklinde yazılır. Üslerin tepkimedeki katsayılara eşit olduğuna dikkat et.
💡 Sınav İpucu: Hangi maddelerin fiziksel halinin aynı olduğunu kontrol ederek homogen mi heterogen mi denge olduğunu kolayca belirleyebilirsin!

Bu örnekler sınavlarda sık karşılaştığın tür sorular! 2SO₂(g) + O₂(g) ⇌ 2SO₃(g) tepkimesinde ΔH<0 olduğu için ekzotermik tepkime - yani enerji açığa çıkıyor.
Minimum enerji eğilimi ekzotermik tepkimelerde ürünler yönündedir çünkü enerji açığa çıkıyor. Ancak denge hiçbir zaman durmuyor - SO₃ oluşumu mikroskobik düzeyde devam ediyor.
Hız bağıntısı yavaş basamağa göre, denge bağıntısı ise net tepkimeye göre yazılır. Bu ayrımı unutma! H₂(g) + 2ICl(g) ⇌ I₂(k) + 2HCl(g) net tepkimesi için Kc = [HCl]²/[H₂][ICl]² olur.
💡 Dikkat: Katı I₂ denge ifadesine yazılmadığı için paydada görünmez!

Denge sabitleri ile matematiksel işlemler yapmak düşündüğünden çok kolay! Temel üç kural var ve bunları bilince her soruyu çözebilirsin.
Birinci kural: Tepkime bir sayıyla çarpılır veya bölünürse, o sayı denge sabitine üs olarak yazılır. 2H₂ + 2Cl₂ ⇌ 4HCl için Kc² olur.
İkinci kural: Tepkime ters çevrilirse denge sabiti 1/Kc olur. Üçüncü kural: Çok basamaklı tepkimelerde net denge sabiti, diğer sabitlerin çarpımına eşittir .
💡 Kolay Hatırlatma: Ters çevirme = ters alma, çarpma = üs alma, toplama = çarpma!

Bu tür sorular ilk başta karmaşık görünse de sistematik yaklaşım ile çok kolay! Verilen tepkimeleri hedef tepkimeyi elde edecek şekilde düzenliyoruz.
C₃H₈ yanma tepkimesi örneğinde üç farklı tepkimeden yararlanıyoruz. Her birini gerektiği kadar çarpıp toplayarak hedef tepkimeyi elde ediyoruz.
Kc = Kc₁² × Kc₂⁴ / Kc₃ formülü, tepkimelere yaptığın işlemlerin denge sabitine yansıması. Birinci tepkimeyi 2 ile çarptın → Kc₁², ikincisini 4 ile çarptın → Kc₂⁴, üçüncüsünü ters çevirdin → 1/Kc₃.
💡 Strateji: Önce hedef tepkimeyi belirle, sonra verilen tepkimeleri nasıl düzenleyeceğini planla!

Gaz fazı tepkimelerinde derişim yerine kısmi basınç kullanabiliriz - bu bazen çok daha pratik! Kp = P_ürünler/P_girenler şeklinde yazılır.
Kp ile Kc arasında Kp = Kc(RT)^Δn ilişkisi var. Burada Δn = ürün gaz katsayısı - giren gaz katsayısı. N₂ + 3H₂ ⇌ 2NH₃ için Δn = 2 - (1+3) = -2 olur.
Özel durum: Eğer Δn = 0 ise Kp = Kc olur. H₂ + Cl₂ ⇌ 2HCl tepkimesinde Δn = 2 - (1+1) = 0 olduğu için bu eşitlik geçerli.
💡 Pratik İpucu: Gazların katsayıları eşitse Kp = Kc, değilse RT hesabı yapman gerekir!

ICE tablosu kullanarak denge hesaplamaları yapmak çok sistematik! 2HI ⇌ H₂ + I₂ tepkimesinde %60 parçalanma verilmişse adım adım ilerle.
5 mol HI'nin %60'ı = 3 mol parçalanır. Başlangıç: 5 mol HI, değişim: -3 mol HI, +1.5 mol H₂, +1.5 mol I₂. Denge: 2 mol HI, 1.5 mol H₂, 1.5 mol I₂.
Kc hesabı: Kc = [H₂][I₂]/[HI]² = (1.5)(1.5)/(2)² = 2.25/4 = 0.56. Kp hesabı için Δn'i bul ve RT ile çarp: Kp = Kc(RT)^Δn formülünü kullan.
💡 Sınav Taktiği: ICE tablosunu her zaman düzenli yaz - hata yapma şansın azalır!

Bu seviye sorular sınavlarda ayırt edici sorular! XY₂ ve XY₃ gazlarının kısmi basınçları verildiğinde sistematik yaklaş.
Kp ifadesini kur: Kp = [PXY₃]/[PXY₂ × PY₂] = 0.25. Verilen değerleri yerine koy: 0.25 = (0.1)²/[(0.2)² × PY₂]. Buradan PY₂ = 1 atm bulunur.
Kc dönüşümü için Δn hesabı yap: Δn = 2-(2+1) = -1. Kp = Kc(RT)^(-1) formülünden Kc = Kp × RT = 0.25 × 22.4 = 5.6. Ters tepkime için denge sabiti 1/Kc alınır.
💡 Master İpucu: Tepkime ters çevrilip katsayılarla çarpılınca, denge sabitine aynı işlemleri uygula!

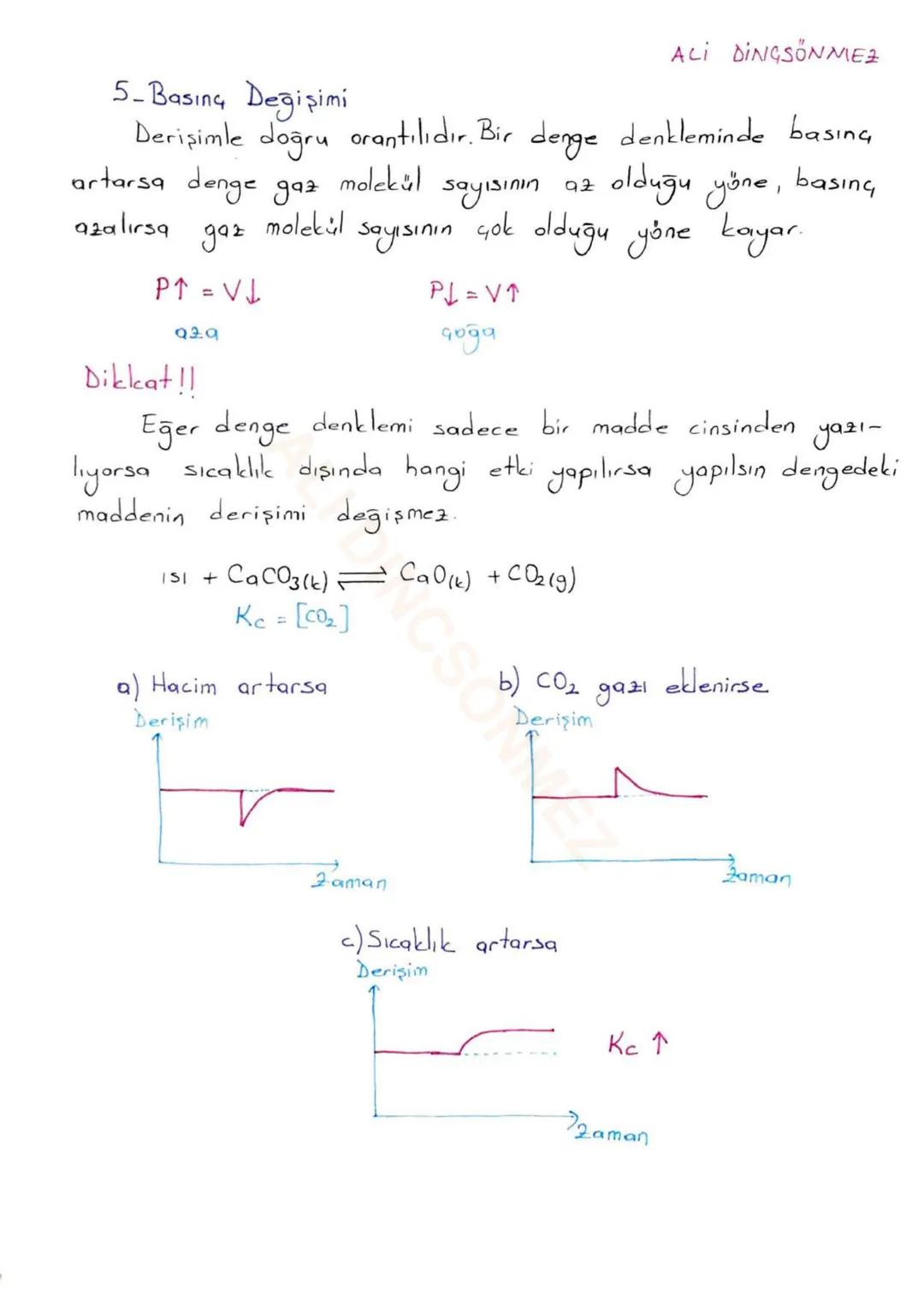
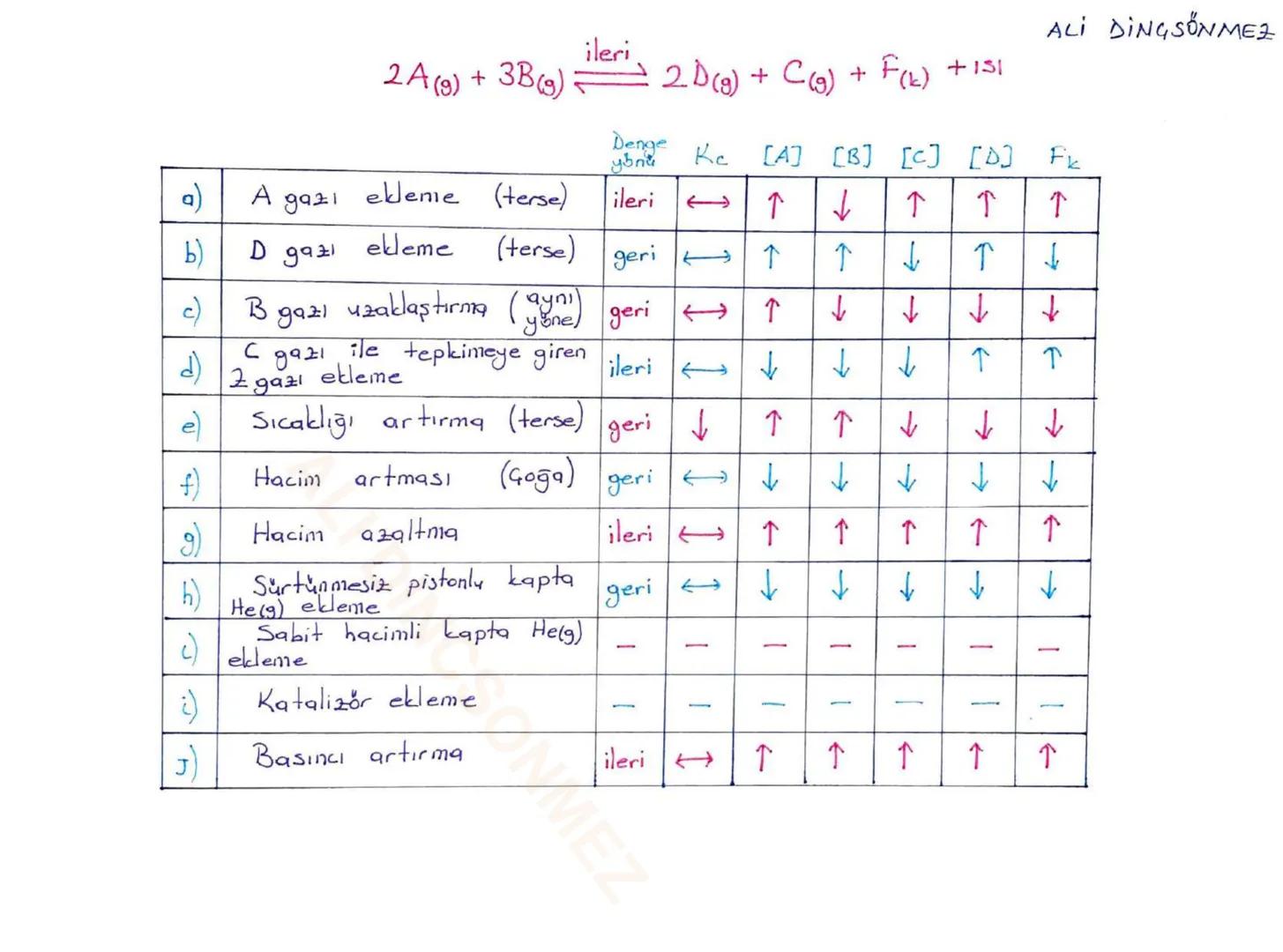
Le Chatelier İlkesi günlük hayatta sürekli karşılaştığın bir durum! Sistem her zaman yapılan etkinin tersini yaparak dengeyi korumaya çalışır.
Madde ekleme: PCl₅ ⇌ PCl₃ + Cl₂ tepkimesinde Cl₂ eklersen, sistem fazla Cl₂'yi tüketmek için sola kayar (girenler yönü). Denge sistemi her zaman rahatsız eden faktörü azaltmaya çalışır.
Madde çıkarma: Aynı tepkimede PCl₅ çıkarırsan, sistem kayıpları telafi etmek için sola kayar (PCl₅ oluşumu artar). Bu mantığı kavrayınca hangi yöne kayacağını tahmin etmek çok kolay.
💡 Kolay Hatırlama: Sistem her zaman "işimin gücümün arasına girme, ben hallederim" der ve tersini yapar!









Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
eloss
@eloslogy
Kimyasal denge, kimya dersinde önemli konulardan biri ve aslında günlük hayatta sürekli karşılaştığımız bir olay. Evrendeki maddelerin iki temel eğilimi - maksimum düzensizlik ve minimum enerji - bir araya geldiğinde dinamik denge oluşur.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Günlük hayatta sürekli denge halindeki sistemlerle karşılaşıyorsun - örneğin bardağındaki suyun buharlaşması! Dinamik denge, evrendeki maddelerin maksimum düzensiz olma ve minimum enerjiye sahip olma eğilimlerinin uzlaşmasıyla oluşur.
Denge kurulması için iki şart var: sıcaklık sabit olmalı ve sistem kapalı olmalıdir. Denge anında ileri tepkime hızı ile geri tepkime hızı eşit olur .
Bu süreç hiç durmaz - denge dinamiktir! Gözle görülebilir değişiklik olmasa da moleküler düzeyde sürekli hareket vardır. Su örneğinde buharlaşma ve yoğunlaşma hızları eşit olduğunda denge kurulur.
💡 Önemli Not: Dengede maddeler hiçbir zaman tamamen bitmez ve maddelerin derişimi sabittir!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Denge sabitini anlamak aslında çok kolay - sadece ürünlerin derişiminin girenlerin derişimine oranı! Bu oran her zaman aynı kalır ve Kc ile gösterilir.
Genel tepkime için: aA + bB ⇌ cC + dD ise Kc = [C]^c[D]^d / [A]^a[B]^b olur. İleri ve geri tepkime hızları eşit olduğunda bu değer sabit kalır.
Önemli bir nokta: katılar ve saf sıvılar denge ifadesine yazılmaz, sadece gazlar ve suda çözünmüş maddeler yazılır. Bu yüzden CaCO₃(k) ⇌ CaO(k) + CO₂(g) tepkimesinde Kc = [CO₂] olur.
💡 Pratik İpucu: Fiziksel halleri aynı olan maddeler homogen denge, farklı olanlar heterogen denge oluşturur!
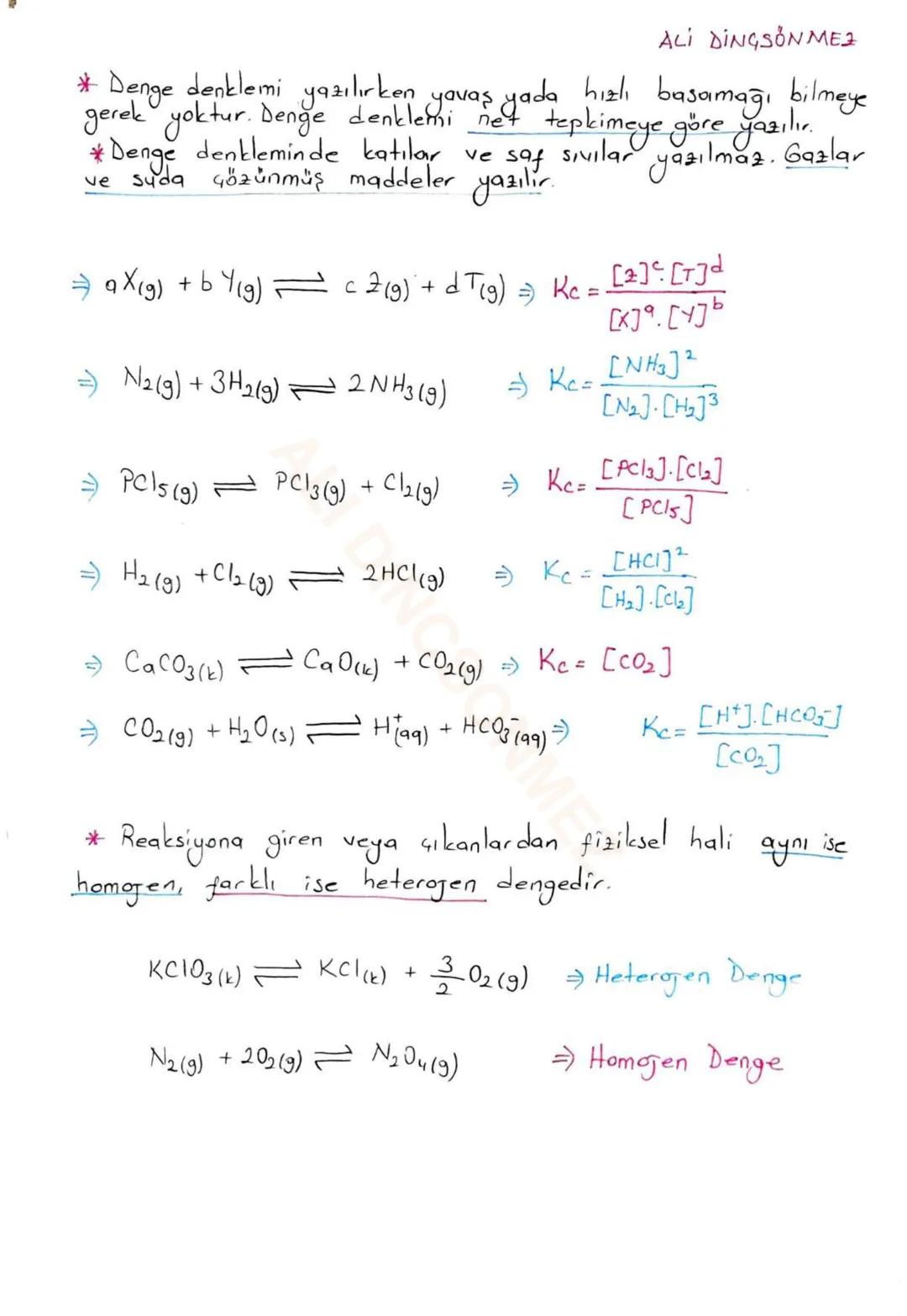
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Denge denklemi yazarken net tepkimeyi kullanıyoruz - hangi basamağın yavaş olduğunu bilmeye gerek yok! Bu senin işini çok kolaylaştırır.
Temel kurallar şunlar: Katılar ve saf sıvılar yazılmaz, sadece gazlar ve suda çözünmüş maddeler yazılır. Örneğin N₂(g) + 3H₂(g) ⇌ 2NH₃(g) için Kc = [NH₃]²/[N₂][H₂]³ olur.
PCl₅(g) ⇌ PCl₃(g) + Cl₂(g) gibi basit bir tepkimede Kc = [PCl₃][Cl₂]/[PCl₅] şeklinde yazılır. Üslerin tepkimedeki katsayılara eşit olduğuna dikkat et.
💡 Sınav İpucu: Hangi maddelerin fiziksel halinin aynı olduğunu kontrol ederek homogen mi heterogen mi denge olduğunu kolayca belirleyebilirsin!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
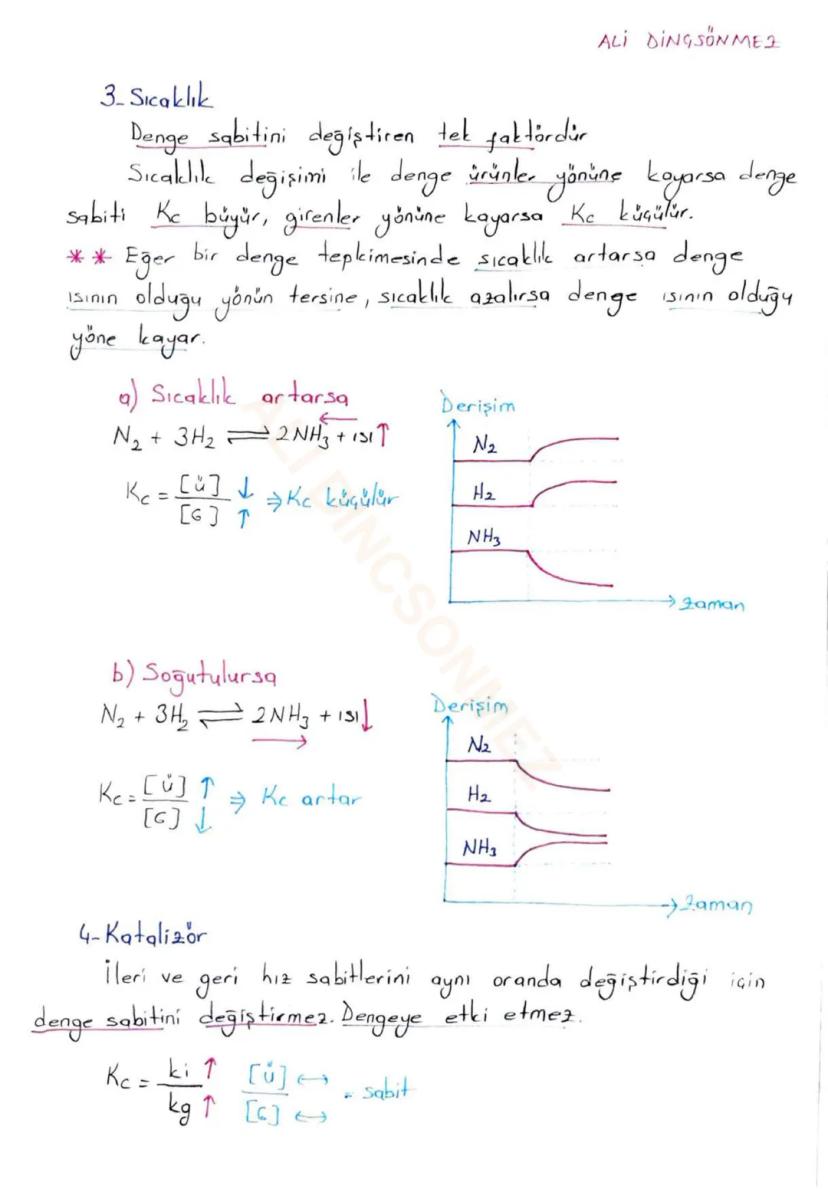
Bu örnekler sınavlarda sık karşılaştığın tür sorular! 2SO₂(g) + O₂(g) ⇌ 2SO₃(g) tepkimesinde ΔH<0 olduğu için ekzotermik tepkime - yani enerji açığa çıkıyor.
Minimum enerji eğilimi ekzotermik tepkimelerde ürünler yönündedir çünkü enerji açığa çıkıyor. Ancak denge hiçbir zaman durmuyor - SO₃ oluşumu mikroskobik düzeyde devam ediyor.
Hız bağıntısı yavaş basamağa göre, denge bağıntısı ise net tepkimeye göre yazılır. Bu ayrımı unutma! H₂(g) + 2ICl(g) ⇌ I₂(k) + 2HCl(g) net tepkimesi için Kc = [HCl]²/[H₂][ICl]² olur.
💡 Dikkat: Katı I₂ denge ifadesine yazılmadığı için paydada görünmez!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Denge sabitleri ile matematiksel işlemler yapmak düşündüğünden çok kolay! Temel üç kural var ve bunları bilince her soruyu çözebilirsin.
Birinci kural: Tepkime bir sayıyla çarpılır veya bölünürse, o sayı denge sabitine üs olarak yazılır. 2H₂ + 2Cl₂ ⇌ 4HCl için Kc² olur.
İkinci kural: Tepkime ters çevrilirse denge sabiti 1/Kc olur. Üçüncü kural: Çok basamaklı tepkimelerde net denge sabiti, diğer sabitlerin çarpımına eşittir .
💡 Kolay Hatırlatma: Ters çevirme = ters alma, çarpma = üs alma, toplama = çarpma!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bu tür sorular ilk başta karmaşık görünse de sistematik yaklaşım ile çok kolay! Verilen tepkimeleri hedef tepkimeyi elde edecek şekilde düzenliyoruz.
C₃H₈ yanma tepkimesi örneğinde üç farklı tepkimeden yararlanıyoruz. Her birini gerektiği kadar çarpıp toplayarak hedef tepkimeyi elde ediyoruz.
Kc = Kc₁² × Kc₂⁴ / Kc₃ formülü, tepkimelere yaptığın işlemlerin denge sabitine yansıması. Birinci tepkimeyi 2 ile çarptın → Kc₁², ikincisini 4 ile çarptın → Kc₂⁴, üçüncüsünü ters çevirdin → 1/Kc₃.
💡 Strateji: Önce hedef tepkimeyi belirle, sonra verilen tepkimeleri nasıl düzenleyeceğini planla!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Gaz fazı tepkimelerinde derişim yerine kısmi basınç kullanabiliriz - bu bazen çok daha pratik! Kp = P_ürünler/P_girenler şeklinde yazılır.
Kp ile Kc arasında Kp = Kc(RT)^Δn ilişkisi var. Burada Δn = ürün gaz katsayısı - giren gaz katsayısı. N₂ + 3H₂ ⇌ 2NH₃ için Δn = 2 - (1+3) = -2 olur.
Özel durum: Eğer Δn = 0 ise Kp = Kc olur. H₂ + Cl₂ ⇌ 2HCl tepkimesinde Δn = 2 - (1+1) = 0 olduğu için bu eşitlik geçerli.
💡 Pratik İpucu: Gazların katsayıları eşitse Kp = Kc, değilse RT hesabı yapman gerekir!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
ICE tablosu kullanarak denge hesaplamaları yapmak çok sistematik! 2HI ⇌ H₂ + I₂ tepkimesinde %60 parçalanma verilmişse adım adım ilerle.
5 mol HI'nin %60'ı = 3 mol parçalanır. Başlangıç: 5 mol HI, değişim: -3 mol HI, +1.5 mol H₂, +1.5 mol I₂. Denge: 2 mol HI, 1.5 mol H₂, 1.5 mol I₂.
Kc hesabı: Kc = [H₂][I₂]/[HI]² = (1.5)(1.5)/(2)² = 2.25/4 = 0.56. Kp hesabı için Δn'i bul ve RT ile çarp: Kp = Kc(RT)^Δn formülünü kullan.
💡 Sınav Taktiği: ICE tablosunu her zaman düzenli yaz - hata yapma şansın azalır!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bu seviye sorular sınavlarda ayırt edici sorular! XY₂ ve XY₃ gazlarının kısmi basınçları verildiğinde sistematik yaklaş.
Kp ifadesini kur: Kp = [PXY₃]/[PXY₂ × PY₂] = 0.25. Verilen değerleri yerine koy: 0.25 = (0.1)²/[(0.2)² × PY₂]. Buradan PY₂ = 1 atm bulunur.
Kc dönüşümü için Δn hesabı yap: Δn = 2-(2+1) = -1. Kp = Kc(RT)^(-1) formülünden Kc = Kp × RT = 0.25 × 22.4 = 5.6. Ters tepkime için denge sabiti 1/Kc alınır.
💡 Master İpucu: Tepkime ters çevrilip katsayılarla çarpılınca, denge sabitine aynı işlemleri uygula!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
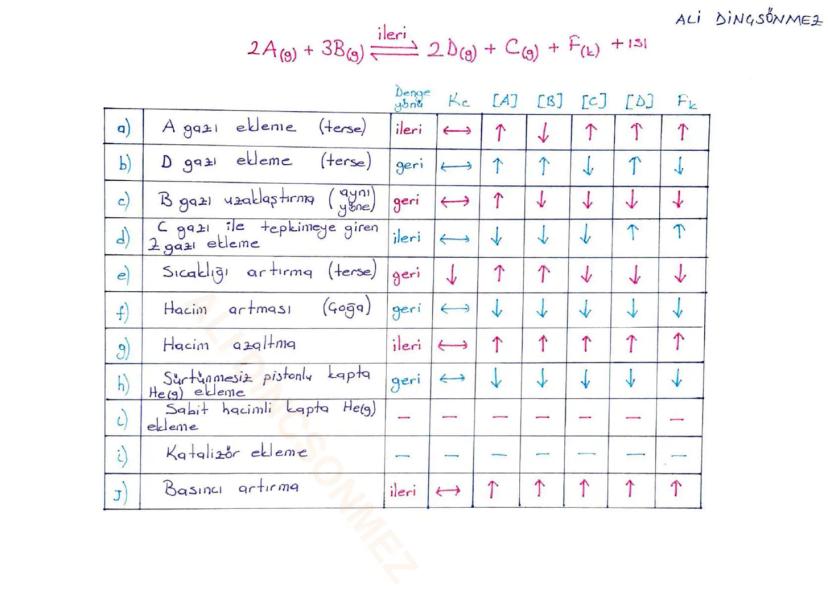
Le Chatelier İlkesi günlük hayatta sürekli karşılaştığın bir durum! Sistem her zaman yapılan etkinin tersini yaparak dengeyi korumaya çalışır.
Madde ekleme: PCl₅ ⇌ PCl₃ + Cl₂ tepkimesinde Cl₂ eklersen, sistem fazla Cl₂'yi tüketmek için sola kayar (girenler yönü). Denge sistemi her zaman rahatsız eden faktörü azaltmaya çalışır.
Madde çıkarma: Aynı tepkimede PCl₅ çıkarırsan, sistem kayıpları telafi etmek için sola kayar (PCl₅ oluşumu artar). Bu mantığı kavrayınca hangi yöne kayacağını tahmin etmek çok kolay.
💡 Kolay Hatırlama: Sistem her zaman "işimin gücümün arasına girme, ben hallederim" der ve tersini yapar!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
11
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı