Kimya dünyasına adım atarken, evrenin en temel yapı taşlarını tanıyacağız.... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
393
•
Güncellendi May 17, 2026
•
Belinay
@blny_trk
Kimya dünyasına adım atarken, evrenin en temel yapı taşlarını tanıyacağız.... Daha fazla göster











Kimya bilimi, maddenin yapısını ve dönüşümlerini inceleyen temel bir bilim dalıdır. Modern kimyanın temelleri, altını başka maddelere dönüştürmeye ve ölümsüzlük iksirini bulmaya çalışan simya çalışmalarına dayanır.
Kimyanın birçok alt disiplini vardır. Organik kimya karbon temelli bileşikleri, anorganik kimya karbon dışı elementleri, biyokimya canlı organizmalardaki kimyasal süreçleri inceler. Analitik kimya, maddelerin yapısını ve bileşimini belirlemek için kullanılır - kan veya besin analizi gibi uygulamalarda karşımıza çıkar.
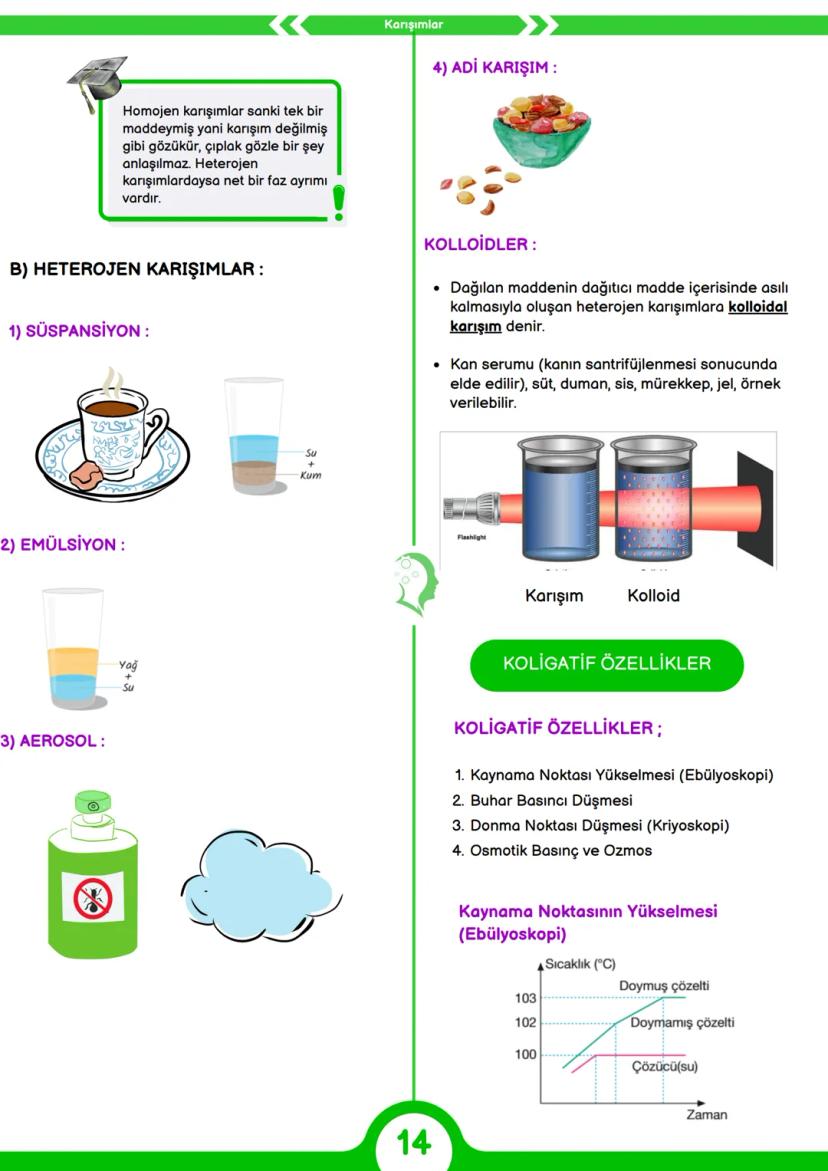
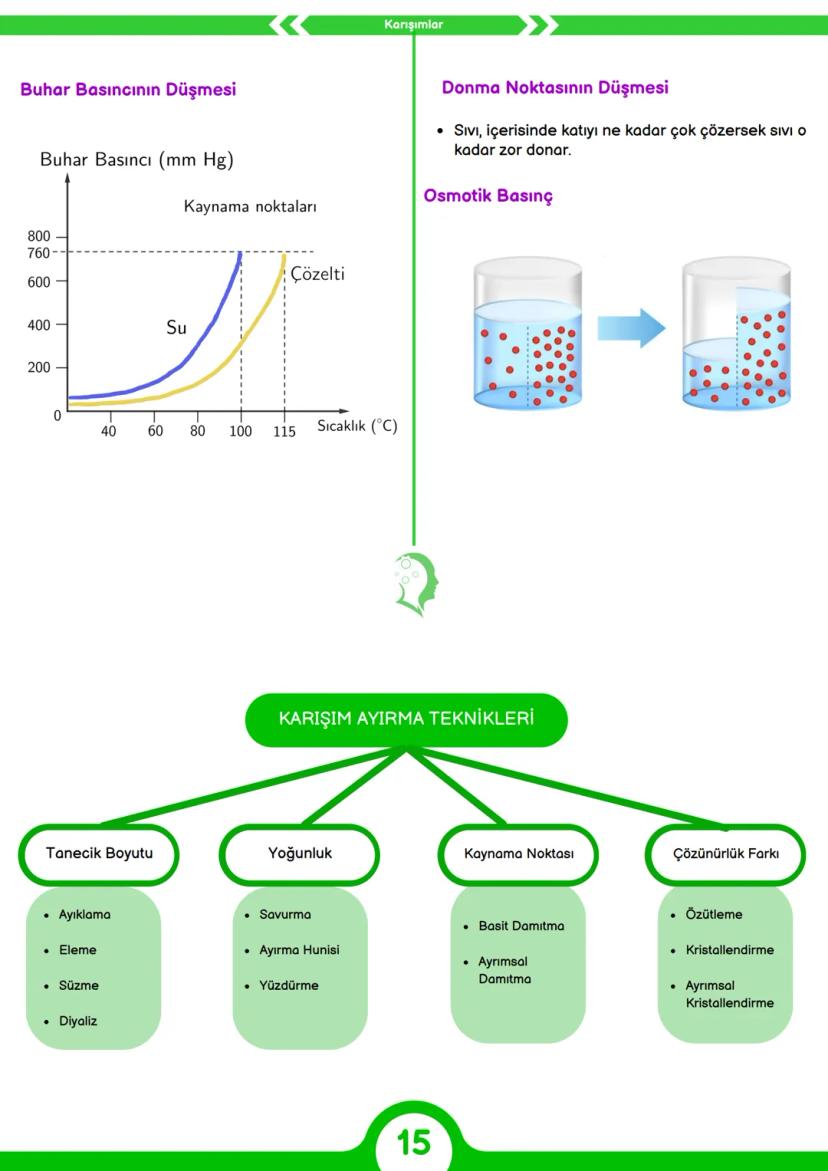
Maddeler yapılarına göre sınıflandırılır. Saf maddeler elementler ve bileşiklerden oluşurken, karışımlar homojen ve heterojen olarak ikiye ayrılır. Günlük hayatta kullandığımız birçok madde aslında birer bileşiktir: H₂O (su), NaCl (yemek tuzu), CaCO₃ (kireç taşı) ve H₂SO₄ (sülfürik asit) bunlara örnek verilebilir.
Merak et! Sirke asidi (CH₃COOH), karınca asidi (HCOOH) ve yemek sodası (NaHCO₃) gibi bileşikleri günlük hayatınızda nerelerde kullandığınızı düşünün. Kimya aslında mutfağınızda!

Bir kimya laboratuvarında farklı işlevlere sahip çeşitli araç-gereçler bulunur. Bu araçların her biri belirli bir amaca hizmet eder ve doğru kullanılmaları güvenli deneyler yapabilmek için çok önemlidir.
Erlenmayer, geniş tabanlı ve dar boyunlu yapısıyla titrasyon işlemlerinde sıklıkla kullanılır. Ayırma hunisi ise birbiriyle karışmayan sıvıları ayırmak için idealdir. Cam balon, çözeltilerin ısıtılması ve kimyasal reaksiyonların gerçekleştirilmesi için kullanılan önemli bir araçtır.
Büret, sıvıları damla damla akıtmak için tasarlanmış hassas bir alettir. Dereceli silindir (mezür) sıvıların hacminin ölçülmesinde, pipet ise çok küçük hacimlerin hassas ölçümlerinde kullanılır.
Laboratuvarda güvenlik çok önemlidir! Kimyasal maddelerin üzerindeki uyarı işaretlerini tanımak gerekir: Oksitleyici (yakıcı), yanıcı, patlayıcı, toksik (zehirli), korozif (aşındırıcı), çevreye zararlı, tahriş edici ve radyoaktif tehlike işaretlerini mutlaka bilmelisiniz.
Güvenlik ipucu: Laboratuvarda herhangi bir işlem yapmadan önce, kullandığınız kimyasal maddelerin üzerindeki uyarı işaretlerini kontrol edin. Güvenliğiniz için koruyucu gözlük ve eldiven kullanmayı ihmal etmeyin!
Atomun yapısını anlamak kimyanın temelidir. Bilim insanları yıllar içinde farklı atom modelleri geliştirerek maddenin bu en küçük yapı taşını açıklamaya çalışmışlardır.
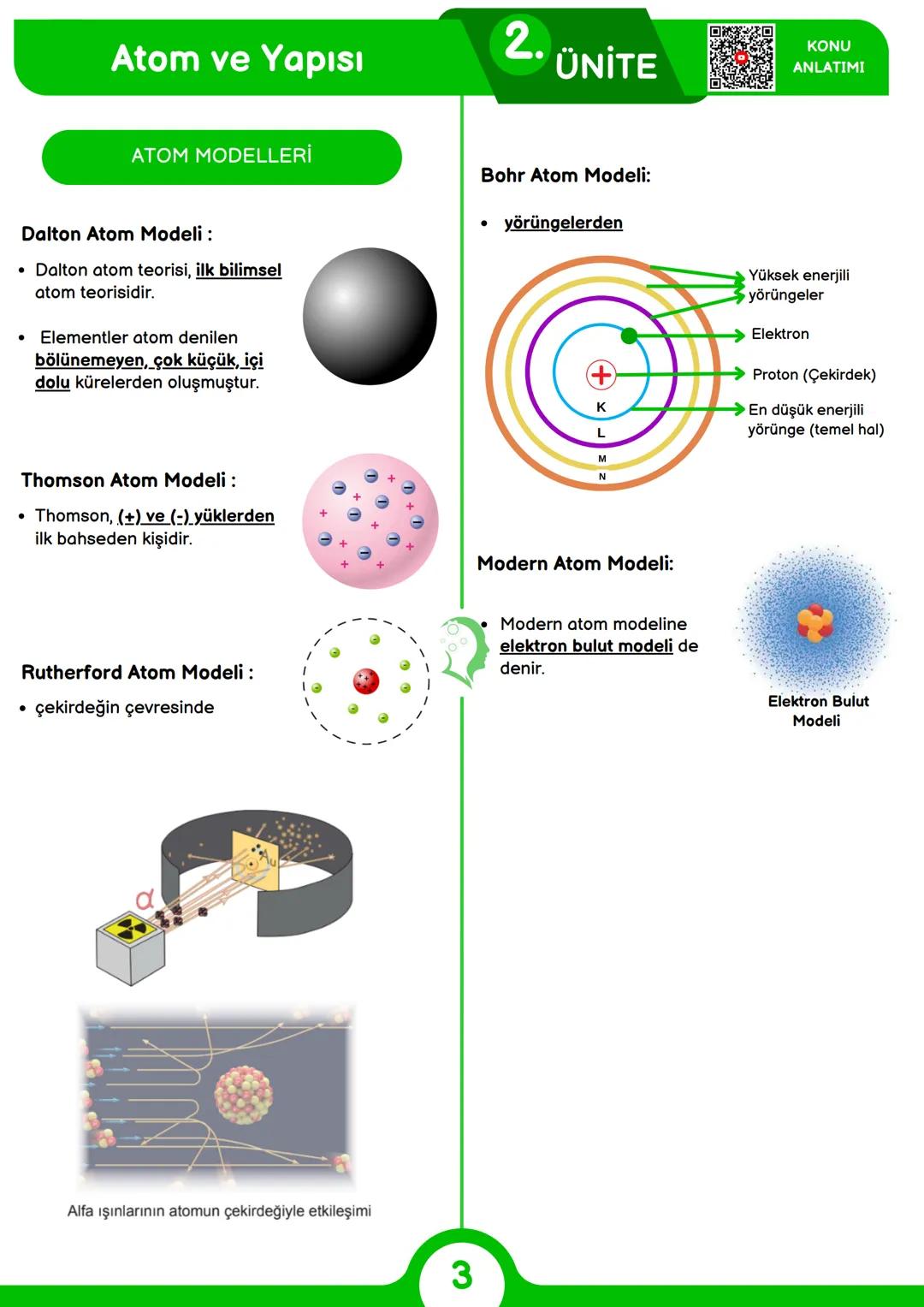
Dalton atom modeli, ilk bilimsel atom teorisidir ve atomları bölünemeyen, içi dolu küreler olarak tanımlar. Thomson atom modeli ise pozitif ve negatif yüklerden ilk bahseden model olarak öne çıkar. Rutherford atom modeli, çekirdeği ve çevresindeki elektronları tanıtmıştır - alfa ışınlarıyla yaptığı ünlü deney sonucunda atomun büyük oranda boşluktan oluştuğunu keşfetmiştir.
Bohr atom modeli, elektronların çekirdeğin etrafında belirli enerji seviyelerindeki yörüngelerde döndüğünü öne sürer. Bu model, elektronların nasıl enerji alıp verdiğini açıklamada önemli bir adımdır. Günümüzde kabul gören modern atom modeli (elektron bulut modeli) ise elektronların belirli bir yörünge yerine, bulut şeklinde bir olasılık dağılımında bulunduğunu gösterir.
İlginç bilgi: Rutherford'un alfa ışınlarıyla yaptığı deney, bilim tarihinin en önemli deneylerinden biridir. Işınların çoğunun altın folyodan geçmesi ancak bazılarının büyük açılarla saçılması, atomun çekirdeğinin keşfine yol açmıştır.
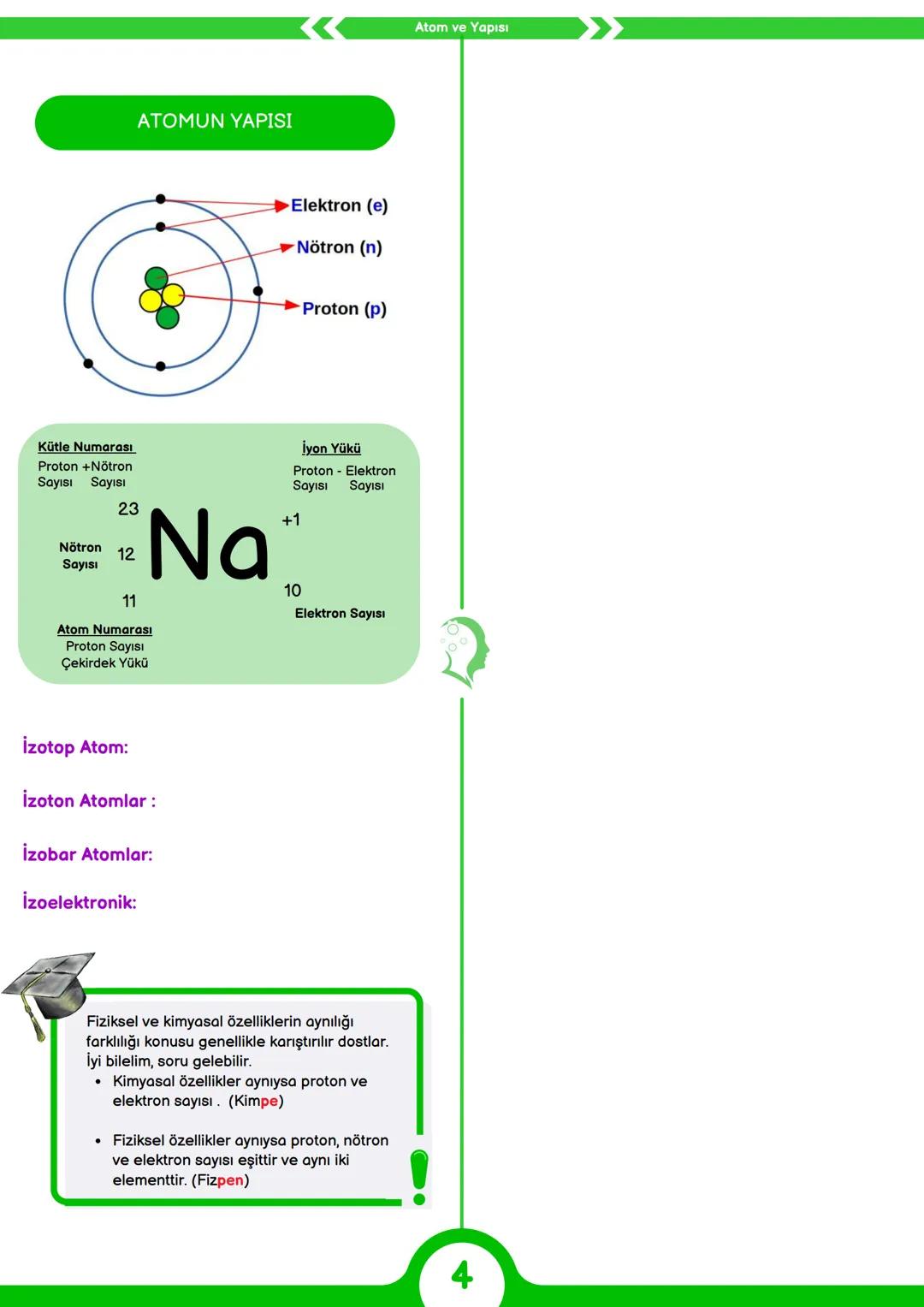
Atomlar üç temel parçacıktan oluşur: elektron (e), proton (p) ve nötron (n). Proton ve nötronlar çekirdekte bulunurken, elektronlar çekirdeğin etrafındaki bulut şeklinde hareket eder.
Atomların kimliklerini belirleyen ve periyodik tablodaki yerlerini gösteren sayı atom numarasıdır ve proton sayısına eşittir. Kütle numarası ise proton ve nötron sayılarının toplamıdır. Örneğin, sodyum (Na) elementinin atom numarası 11, kütle numarası 23'tür, yani 11 protonu ve 12 nötronu vardır.
Atomlar, farklı şekillerde sınıflandırılabilir. İzotop atomlar aynı elementin farklı nötron sayılarına sahip atomlarıdır. İzoton atomlar aynı nötron sayısına sahip farklı elementlerdir. İzobar atomlar kütle numaraları aynı olan atomlardır. İzoelektronik tanecikler ise elektron sayıları aynı olan taneciklerdir.
Atomların özellikleri hakkında önemli bir ayrım vardır: Kimyasal özellikler proton ve elektron sayısına bağlıdır (Kimpe), fiziksel özellikler ise proton, nötron ve elektron sayısının hepsine bağlıdır (Fizpen). Bu ayrım soru çözümlerinde sıkça karşımıza çıkar!
Unutma: Atomun yapısını iyice anlaman, kimyadaki neredeyse tüm konuların temelini oluşturur. Atom numarası, kütle numarası ve izotop kavramlarını kavramak, ilerideki tüm kimya konularını daha rahat anlayabilmen için çok önemli!
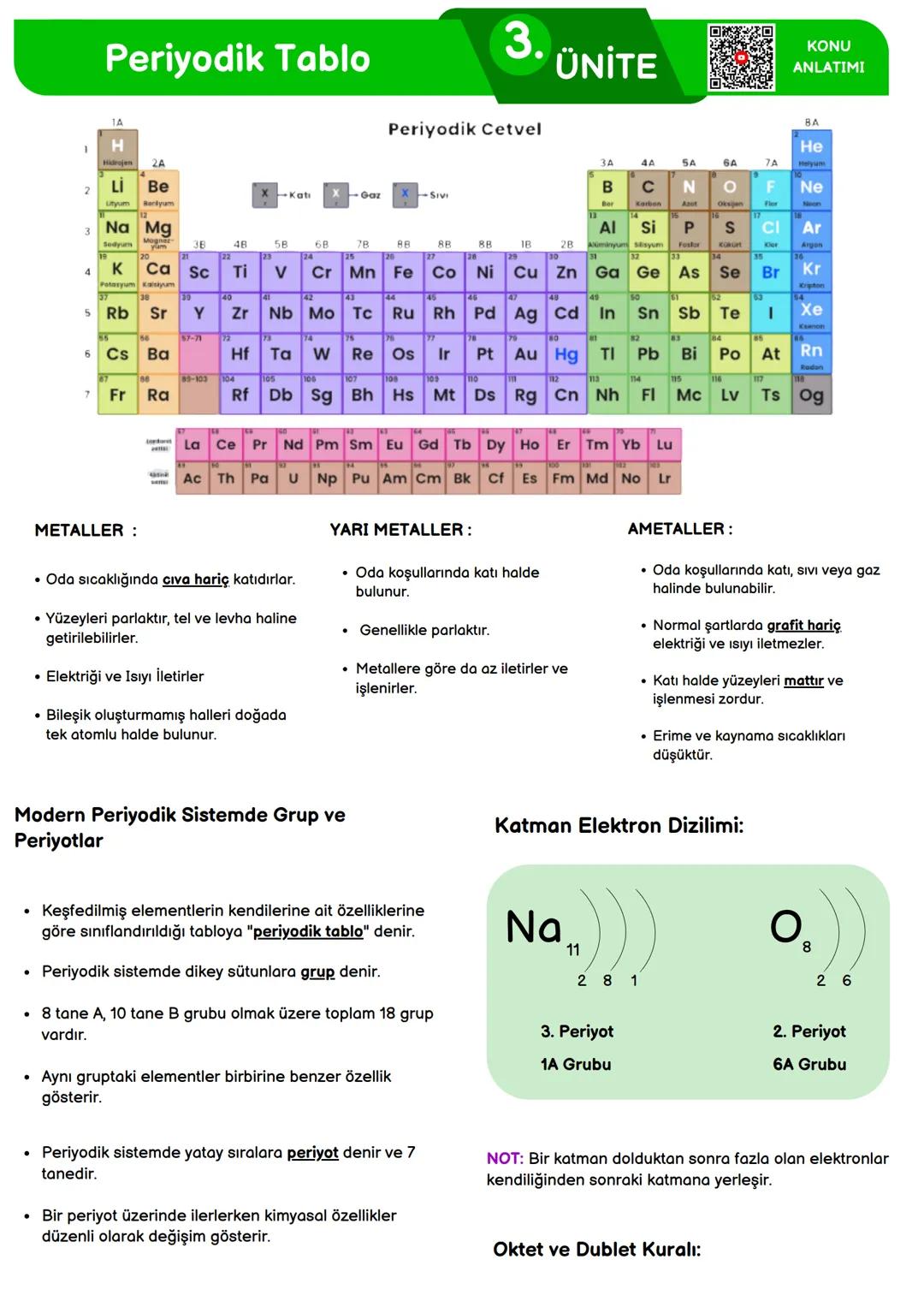
Periyodik tablo, elementlerin özelliklerine göre düzenlendiği temel bir kimya aracıdır. Bu tablo, elementleri benzer özelliklere sahip gruplara ayırarak aralarındaki ilişkileri görmemizi sağlar.
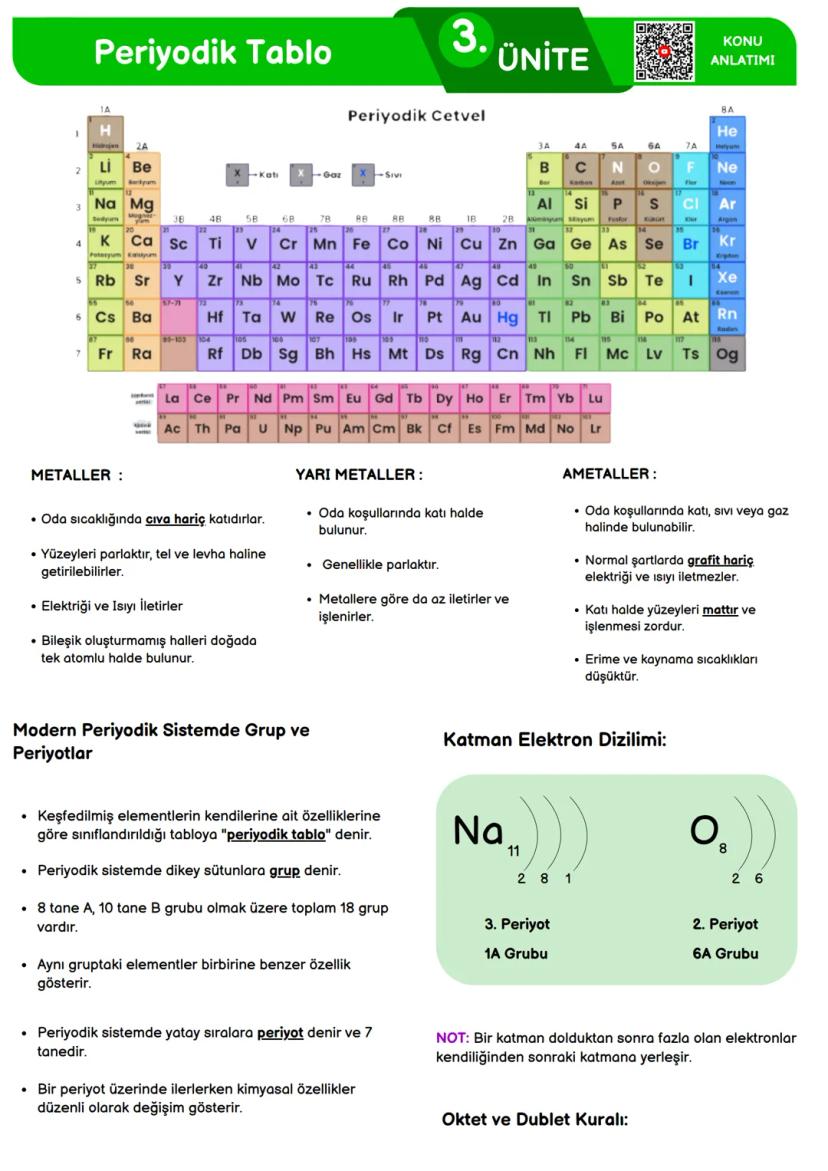
Periyodik sistemde dikey sütunlara grup, yatay sıralara ise periyot denir. Toplam 18 grup (8 A grubu, 10 B grubu) ve 7 periyot vardır. Aynı gruptaki elementler benzer kimyasal özellikler gösterirken, bir periyotta soldan sağa ilerledikçe elementlerin özellikleri düzenli olarak değişir.
Elementler metaller, yarı metaller ve ametaller olarak sınıflandırılır. Metaller genellikle parlak, iletken ve işlenebilir maddelerdir (cıva hariç oda sıcaklığında katıdırlar). Yarı metaller hem metalik hem de ametalik özellikler gösterirler. Ametaller ise mat yüzeyli, kırılgan ve genellikle elektriği iletmeyen maddelerdir.
Bir elementin elektronları katmanlarda bulunur. Örneğin, sodyum (Na) elementinin elektron dizilimi 2-8-1 şeklindedir ve 3. periyot, 1A grubunda yer alır. Oksijen (O) ise 2-6 elektron dizilimiyle 2. periyot, 6A grubundadır.
Önemli ipucu: Periyodik tabloda bir elementin yerini bulabilmek için elektron dizilimini bilmek yeterlidir! Son katmandaki elektron sayısı A grup numarasını, katman sayısı ise periyot numarasını verir.

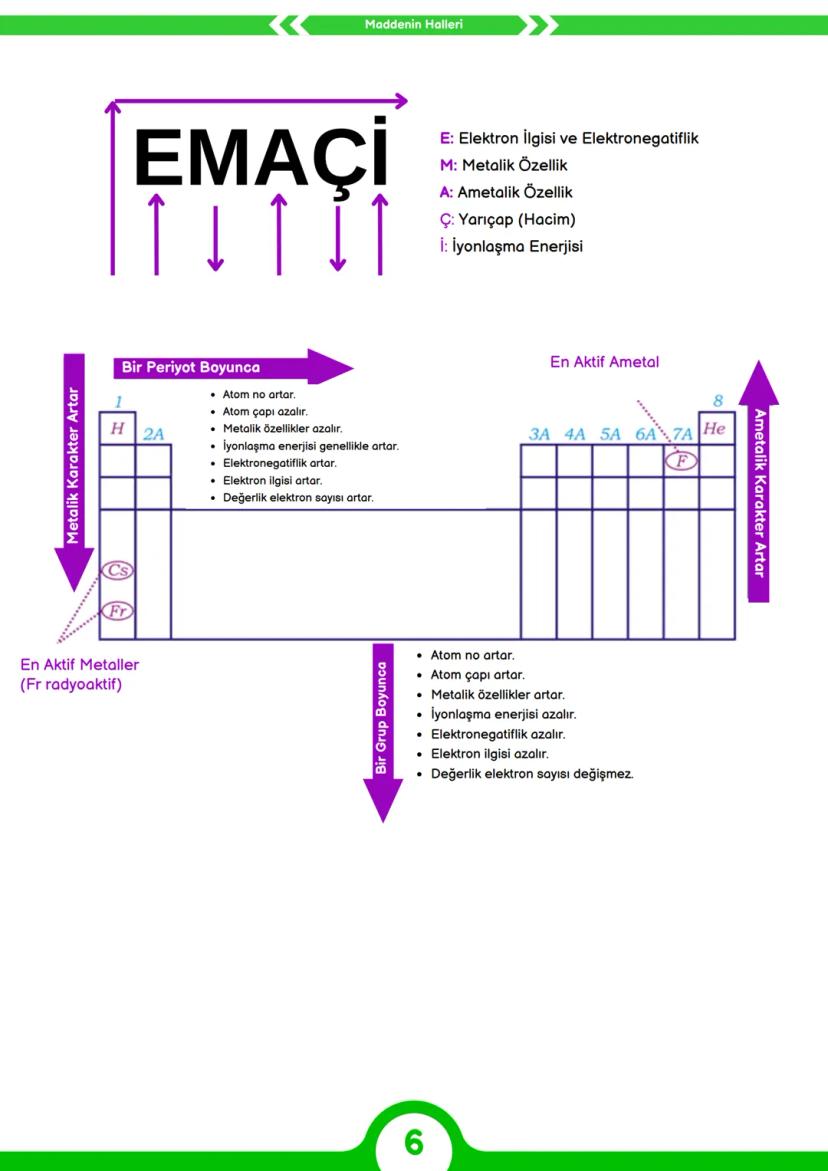
Periyodik tabloda elementlerin özellikleri belirli bir düzen içinde değişir. Bu düzenli değişimleri hatırlamak için "EMAÇİ" kısaltması kullanışlıdır: E (Elektron İlgisi ve Elektronegatiflik), M (Metalik Özellik), A (Ametalik Özellik), Ç , İ (İyonlaşma Enerjisi).
Bir periyot boyunca soldan sağa gidildikçe atom numarası artar, atom çapı küçülür ve metalik özellikler azalır. İyonlaşma enerjisi, elektronegatiflik, elektron ilgisi ve değerlik elektron sayısı genellikle artar. Periyodun en sağında bulunan elementler (halojenler) en aktif ametallerdir.
Bir grup boyunca yukarıdan aşağıya inildikçe atom numarası ve atom çapı artar, metalik özellikler güçlenir. İyonlaşma enerjisi, elektronegatiflik ve elektron ilgisi azalır. Değerlik elektron sayısı ise değişmez. 1A grubunun en altında bulunan elementler (alkali metaller) en aktif metallerdir.
Periyodik tabloda en aktif metal Fransiyum (Fr) iken, en aktif ametal Flor (F)'dur. Bu aktiflik sıralaması, elementlerin elektron verme veya alma eğilimlerini gösterir.
Ezber kolaylığı: Periyodik özellikler için "Sağa gittikçe ametalik artar, aşağıya indikçe metallik artar" cümlesini aklında tut. Bu, neredeyse tüm periyodik özelliklerin nasıl değişeceğini tahmin etmene yardımcı olacaktır!
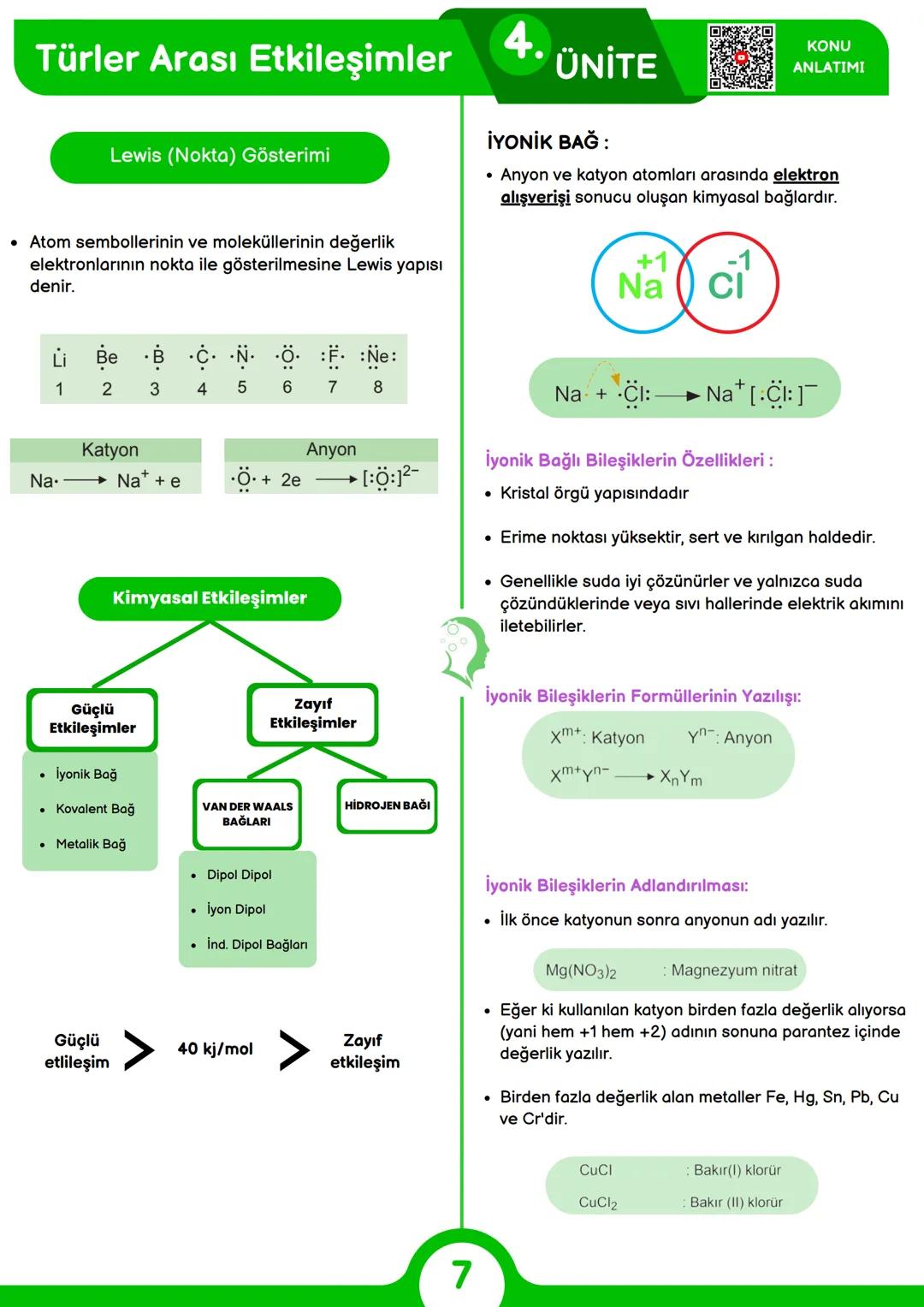
Elementler birbirleriyle etkileşime girerek bağlar oluşturur. Bu bağlar, güçlü etkileşimler (iyonik, kovalent, metalik) ve zayıf etkileşimler (van der Waals, hidrojen bağı) olarak ikiye ayrılır.
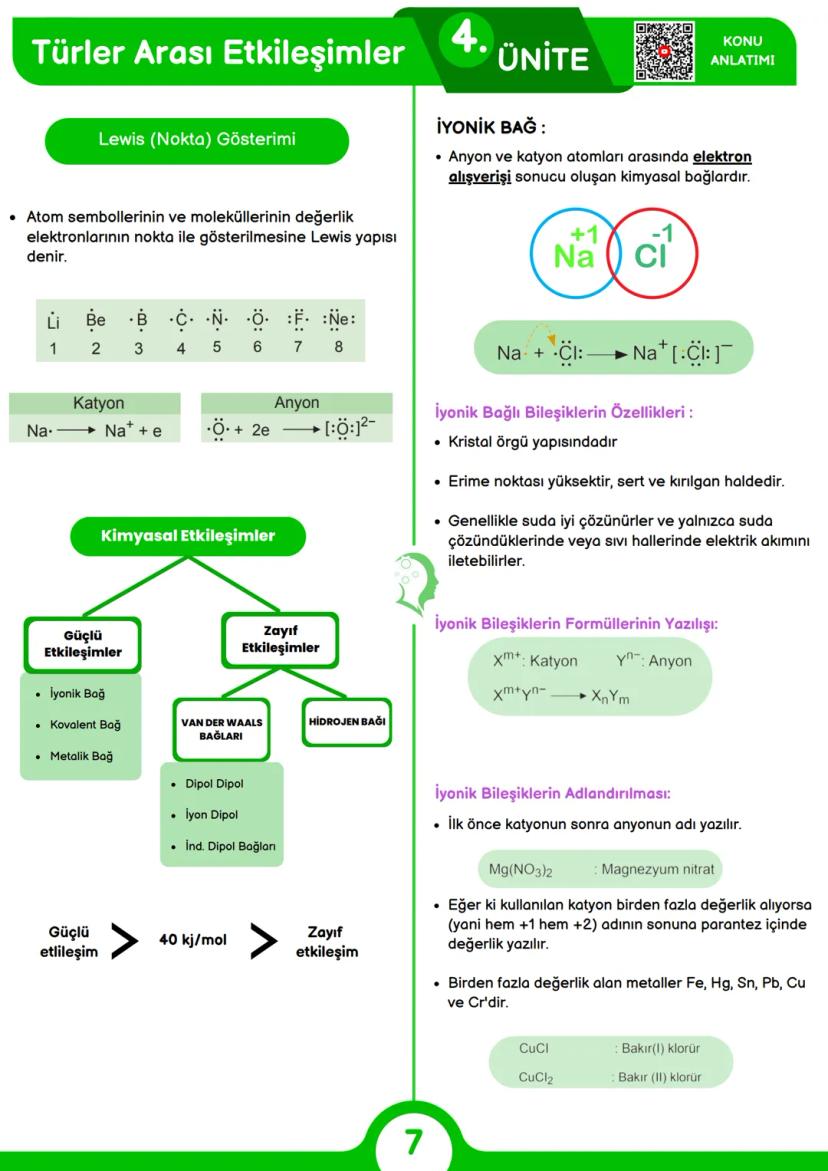
İyonik bağ, bir metal ile ametal arasında elektron alışverişi sonucu oluşur. Metal elektron vererek pozitif yüklü katyon, ametal elektron alarak negatif yüklü anyon haline gelir. Örneğin, Na+ ve Cl- iyonları arasında iyonik bağ vardır. İyonik bileşikler genellikle kristal yapıdadır, sert ve kırılgandır, yüksek erime noktalarına sahiptir ve çözeltileri elektrik iletir.
İyonik bileşiklerin formülü yazılırken katyonun ve anyonun yükleri çapraz yazılır: Xm+ + Yn- → XnYm. Örneğin, Mg2+ ve NO3- iyonlarından Mg(NO3)2 bileşiği oluşur.
İyonik bileşikler adlandırılırken önce katyonun, sonra anyonun adı yazılır. Örneğin NaCl "sodyum klorür" olarak adlandırılır. Birden fazla değerlik alabilen metaller (Fe, Hg, Sn, Pb, Cu, Cr) parantez içinde Roma rakamıyla belirtilir: CuCl "bakır(I) klorür", CuCl2 "bakır(II) klorür" gibi.
Hatırlatma: Elementlerin değerlik elektronlarını noktalarla gösterdiğimiz Lewis yapısı, bağ oluşumunu anlamada çok önemlidir. Metal-ametal etkileşimlerinde iyonik bağ, ametal-ametal etkileşimlerinde kovalent bağ oluşur!
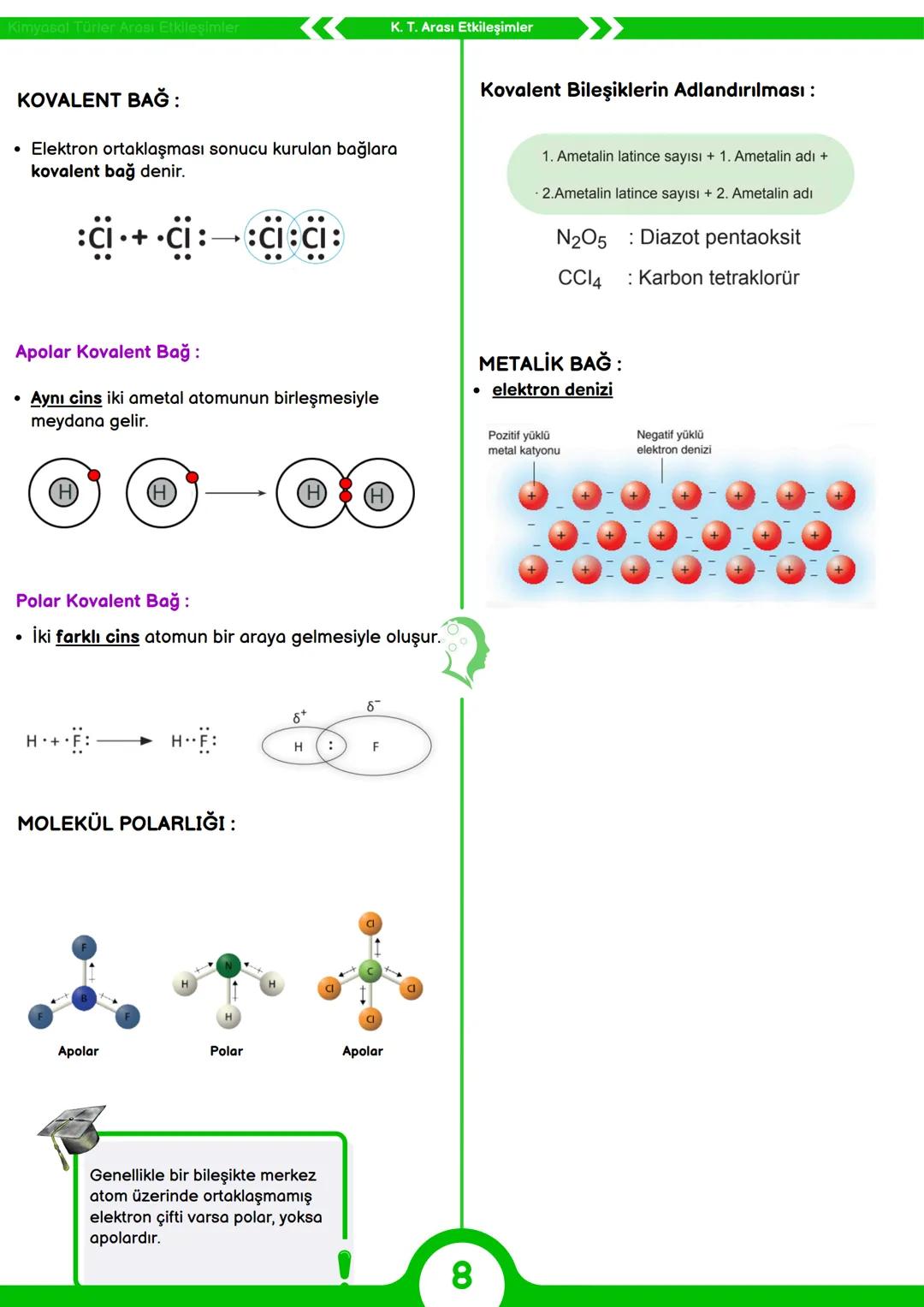
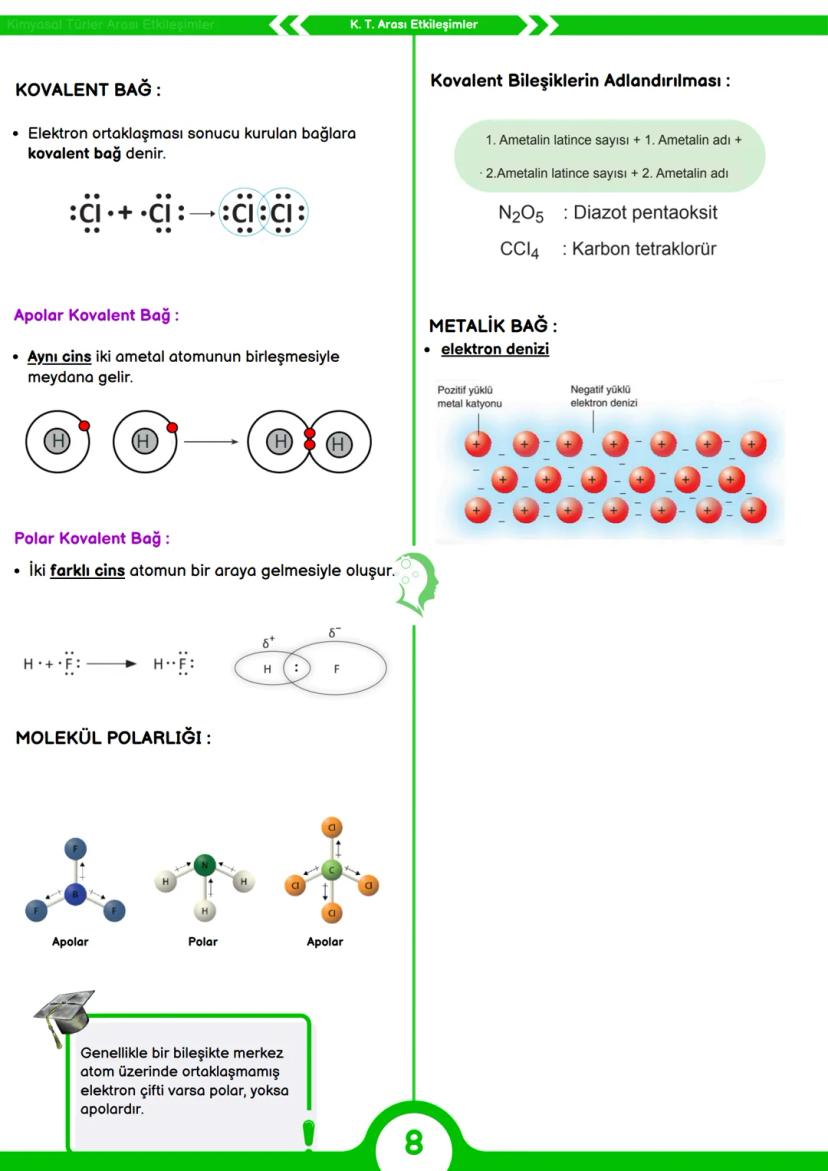
Kovalent bağ, atomlar arasında elektron ortaklaşması sonucu oluşan güçlü bir etkileşimdir. İki ametal arasında gerçekleşir ve elektronlar atomlar arasında paylaşılır.
Kovalent bağlar iki türlüdür: Apolar kovalent bağ aynı cins iki ametal atomu arasında oluşur (örneğin H2, Cl2). Polar kovalent bağ ise farklı cins ametaller arasında oluşur (örneğin HF). Polar bağda elektronlar elektronegatifliği yüksek olan atoma doğru daha yakın bulunur.
Kovalent bileşikler adlandırılırken latince sayılar kullanılır: ilk ametalin latince sayısı + ilk ametalin adı + ikinci ametalin latince sayısı + ikinci ametalin adı. Örneğin, N2O5 "diazot pentaoksit", CCl4 "karbon tetraklorür" olarak adlandırılır.
Metalik bağ ise metal atomları arasında oluşan bir bağ türüdür. Metaller değerlik elektronlarını ortaklaşa kullanır, bu elektronlar serbest hareket ederek "elektron denizi" oluşturur. Bu yapı metallerin elektrik ve ısıyı iyi iletmesini, dövülebilir ve işlenebilir olmasını sağlar.
Moleküllerde bağların dağılımı molekül polarlığını belirler. Genellikle bir molekülde merkez atom üzerinde ortaklaşmamış elektron çifti varsa molekül polar, yoksa apolar olma eğilimindedir.
Dikkat: Moleküllerin polar veya apolar oluşu, çözünürlüklerini ve fiziksel özelliklerini büyük ölçüde etkiler. "Benzer benzeri çözer" prensibi kimyada çok işimize yarar - polar maddeler polar çözücülerde, apolar maddeler apolar çözücülerde çözünür!
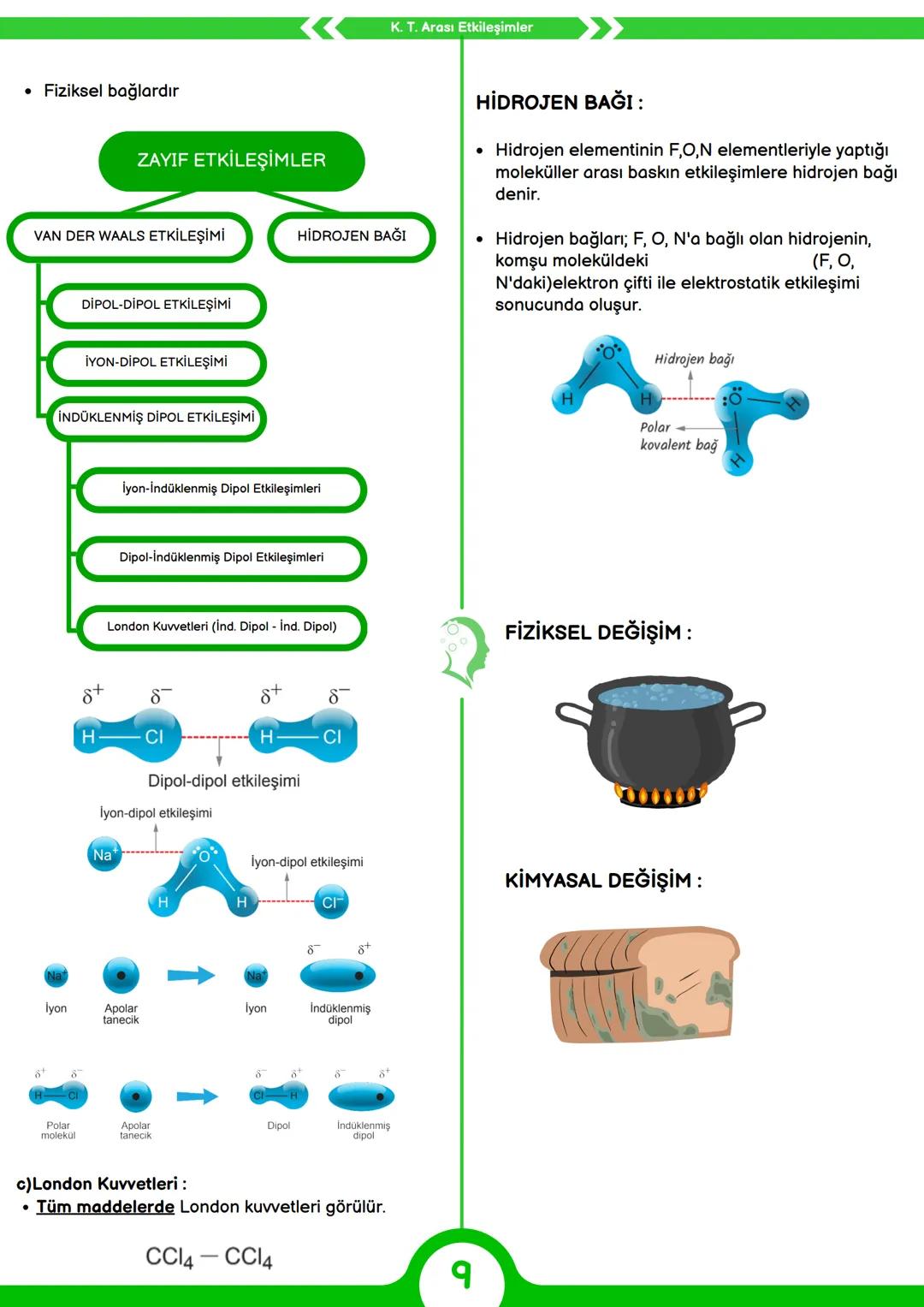
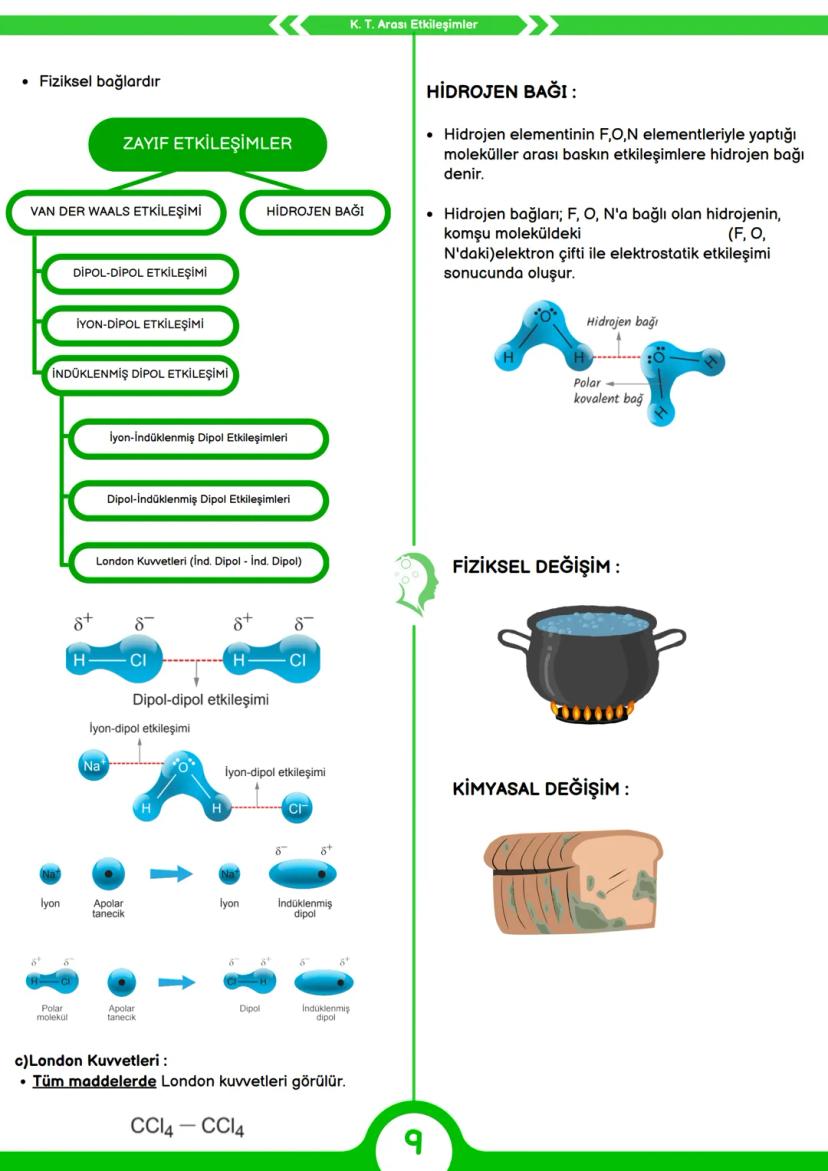
Kimyasal türler arasında güçlü bağların yanında çeşitli zayıf etkileşimler de bulunur. Bu fiziksel bağlar maddelerin fiziksel özelliklerini ve davranışlarını belirlemede büyük rol oynar.
Hidrojen bağı, hidrojen atomunun flor, oksijen veya azot elementlerine (FON) bağlandığı moleküller arasında oluşan özel bir etkileşimdir. Örneğin su molekülleri arasında hidrojen bağları vardır. Bu bağlar diğer zayıf etkileşimlerden daha güçlüdür ve suyun yüksek kaynama noktası gibi birçok özelliğin nedenidir.
Van der Waals etkileşimleri çeşitli zayıf etkileşimleri kapsar. Dipol-dipol etkileşimleri polar moleküller arasında gerçekleşir (örneğin HCl molekülleri arasında). İyon-dipol etkileşimleri ise iyonlar ile polar moleküller arasında görülür .
İndüklenmiş dipol etkileşimleri üç şekilde olabilir: İyon-indüklenmiş dipol, dipol-indüklenmiş dipol ve London kuvvetleri . London kuvvetleri tüm maddelerde görülür, hatta apolar moleküller arasındaki tek etkileşim türüdür (örneğin CCl4 molekülleri arasında).
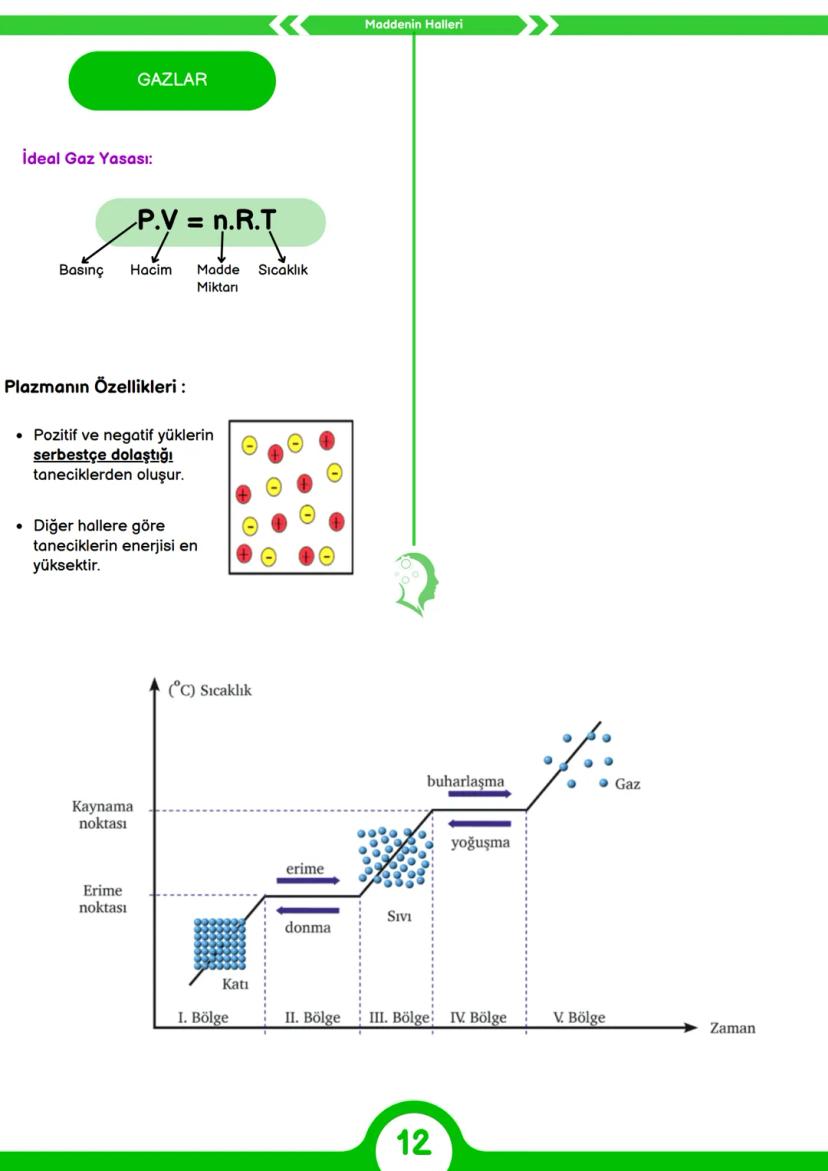
Pratik bilgi: Maddelerin fiziksel halleri (katı, sıvı, gaz) ve fiziksel özellikleri (erime noktası, kaynama noktası, çözünürlük) büyük oranda bu zayıf etkileşimlere bağlıdır. Suyun özel özellikleri, parfümlerin yayılması ve DNA'nın çift sarmal yapısı hep bu etkileşimler sayesinde gerçekleşir!

Kimyanın temel kanunları, kimyasal reaksiyonların nasıl gerçekleştiğini açıklayan önemli kurallardır ve kimya biliminin temelini oluşturur.
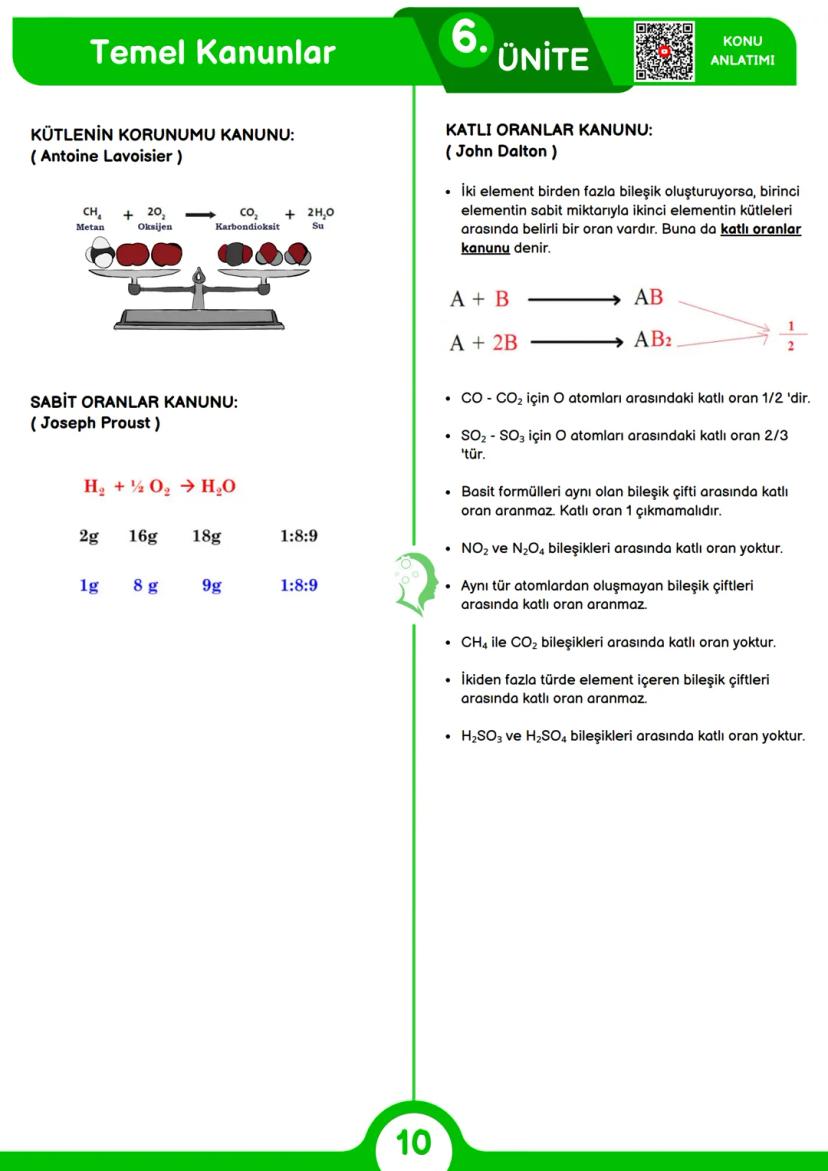
Kütlenin Korunumu Kanunu (Antoine Lavoisier) kimyasal reaksiyonlarda toplam kütlenin değişmediğini belirtir. Örneğin, metan yanması reaksiyonunda giren maddelerin toplam kütlesi, çıkan maddelerin toplam kütlesine eşittir.
Sabit Oranlar Kanunu (Joseph Proust) bir bileşiği oluşturan elementlerin kütlelerinin her zaman sabit bir oranda olduğunu söyler. Örneğin, suyun (H₂O) oluşumunda hidrojen ve oksijenin kütlece oranı her zaman 1:8'dir ve bu oran değişmez.
Katlı Oranlar Kanunu (John Dalton) aynı iki elementin oluşturduğu farklı bileşiklerde, elementlerden birinin sabit miktarıyla diğerinin kütleleri arasında tam sayılı bir oran vardır. Örneğin, karbon monoksit (CO) ve karbon dioksit (CO₂) için oksijen atomları arasındaki katlı oran 1:2'dir.
Katlı oranlar kanununda bazı önemli kısıtlamalar vardır: Basit formülleri aynı olan bileşikler arasında (NO₂ ve N₂O₄ gibi), farklı element türleri içeren bileşikler arasında (CH₄ ve CO₂ gibi) veya ikiden fazla element içeren bileşikler arasında (H₂SO₃ ve H₂SO₄ gibi) katlı oran aranmaz.
Önemli hatırlatma: Bu temel kanunlar, modern kimyanın temelini oluşturan atom teorisinin gelişmesine yol açmıştır. Özellikle kimyasal reaksiyon denklemlerini denkleştirirken kütlenin korunumu kanunu sürekli kullanılır!







Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Belinay
@blny_trk
Kimya dünyasına adım atarken, evrenin en temel yapı taşlarını tanıyacağız. Bu notlar kimyanın temel kavramlarını, atomun yapısını, periyodik tabloyu ve maddelerin birbirleriyle nasıl etkileşime girdiğini anlamamızı sağlayacak.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimya bilimi, maddenin yapısını ve dönüşümlerini inceleyen temel bir bilim dalıdır. Modern kimyanın temelleri, altını başka maddelere dönüştürmeye ve ölümsüzlük iksirini bulmaya çalışan simya çalışmalarına dayanır.
Kimyanın birçok alt disiplini vardır. Organik kimya karbon temelli bileşikleri, anorganik kimya karbon dışı elementleri, biyokimya canlı organizmalardaki kimyasal süreçleri inceler. Analitik kimya, maddelerin yapısını ve bileşimini belirlemek için kullanılır - kan veya besin analizi gibi uygulamalarda karşımıza çıkar.
Maddeler yapılarına göre sınıflandırılır. Saf maddeler elementler ve bileşiklerden oluşurken, karışımlar homojen ve heterojen olarak ikiye ayrılır. Günlük hayatta kullandığımız birçok madde aslında birer bileşiktir: H₂O (su), NaCl (yemek tuzu), CaCO₃ (kireç taşı) ve H₂SO₄ (sülfürik asit) bunlara örnek verilebilir.
Merak et! Sirke asidi (CH₃COOH), karınca asidi (HCOOH) ve yemek sodası (NaHCO₃) gibi bileşikleri günlük hayatınızda nerelerde kullandığınızı düşünün. Kimya aslında mutfağınızda!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bir kimya laboratuvarında farklı işlevlere sahip çeşitli araç-gereçler bulunur. Bu araçların her biri belirli bir amaca hizmet eder ve doğru kullanılmaları güvenli deneyler yapabilmek için çok önemlidir.
Erlenmayer, geniş tabanlı ve dar boyunlu yapısıyla titrasyon işlemlerinde sıklıkla kullanılır. Ayırma hunisi ise birbiriyle karışmayan sıvıları ayırmak için idealdir. Cam balon, çözeltilerin ısıtılması ve kimyasal reaksiyonların gerçekleştirilmesi için kullanılan önemli bir araçtır.
Büret, sıvıları damla damla akıtmak için tasarlanmış hassas bir alettir. Dereceli silindir (mezür) sıvıların hacminin ölçülmesinde, pipet ise çok küçük hacimlerin hassas ölçümlerinde kullanılır.
Laboratuvarda güvenlik çok önemlidir! Kimyasal maddelerin üzerindeki uyarı işaretlerini tanımak gerekir: Oksitleyici (yakıcı), yanıcı, patlayıcı, toksik (zehirli), korozif (aşındırıcı), çevreye zararlı, tahriş edici ve radyoaktif tehlike işaretlerini mutlaka bilmelisiniz.
Güvenlik ipucu: Laboratuvarda herhangi bir işlem yapmadan önce, kullandığınız kimyasal maddelerin üzerindeki uyarı işaretlerini kontrol edin. Güvenliğiniz için koruyucu gözlük ve eldiven kullanmayı ihmal etmeyin!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Atomun yapısını anlamak kimyanın temelidir. Bilim insanları yıllar içinde farklı atom modelleri geliştirerek maddenin bu en küçük yapı taşını açıklamaya çalışmışlardır.
Dalton atom modeli, ilk bilimsel atom teorisidir ve atomları bölünemeyen, içi dolu küreler olarak tanımlar. Thomson atom modeli ise pozitif ve negatif yüklerden ilk bahseden model olarak öne çıkar. Rutherford atom modeli, çekirdeği ve çevresindeki elektronları tanıtmıştır - alfa ışınlarıyla yaptığı ünlü deney sonucunda atomun büyük oranda boşluktan oluştuğunu keşfetmiştir.
Bohr atom modeli, elektronların çekirdeğin etrafında belirli enerji seviyelerindeki yörüngelerde döndüğünü öne sürer. Bu model, elektronların nasıl enerji alıp verdiğini açıklamada önemli bir adımdır. Günümüzde kabul gören modern atom modeli (elektron bulut modeli) ise elektronların belirli bir yörünge yerine, bulut şeklinde bir olasılık dağılımında bulunduğunu gösterir.
İlginç bilgi: Rutherford'un alfa ışınlarıyla yaptığı deney, bilim tarihinin en önemli deneylerinden biridir. Işınların çoğunun altın folyodan geçmesi ancak bazılarının büyük açılarla saçılması, atomun çekirdeğinin keşfine yol açmıştır.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Atomlar üç temel parçacıktan oluşur: elektron (e), proton (p) ve nötron (n). Proton ve nötronlar çekirdekte bulunurken, elektronlar çekirdeğin etrafındaki bulut şeklinde hareket eder.
Atomların kimliklerini belirleyen ve periyodik tablodaki yerlerini gösteren sayı atom numarasıdır ve proton sayısına eşittir. Kütle numarası ise proton ve nötron sayılarının toplamıdır. Örneğin, sodyum (Na) elementinin atom numarası 11, kütle numarası 23'tür, yani 11 protonu ve 12 nötronu vardır.
Atomlar, farklı şekillerde sınıflandırılabilir. İzotop atomlar aynı elementin farklı nötron sayılarına sahip atomlarıdır. İzoton atomlar aynı nötron sayısına sahip farklı elementlerdir. İzobar atomlar kütle numaraları aynı olan atomlardır. İzoelektronik tanecikler ise elektron sayıları aynı olan taneciklerdir.
Atomların özellikleri hakkında önemli bir ayrım vardır: Kimyasal özellikler proton ve elektron sayısına bağlıdır (Kimpe), fiziksel özellikler ise proton, nötron ve elektron sayısının hepsine bağlıdır (Fizpen). Bu ayrım soru çözümlerinde sıkça karşımıza çıkar!
Unutma: Atomun yapısını iyice anlaman, kimyadaki neredeyse tüm konuların temelini oluşturur. Atom numarası, kütle numarası ve izotop kavramlarını kavramak, ilerideki tüm kimya konularını daha rahat anlayabilmen için çok önemli!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Periyodik tablo, elementlerin özelliklerine göre düzenlendiği temel bir kimya aracıdır. Bu tablo, elementleri benzer özelliklere sahip gruplara ayırarak aralarındaki ilişkileri görmemizi sağlar.
Periyodik sistemde dikey sütunlara grup, yatay sıralara ise periyot denir. Toplam 18 grup (8 A grubu, 10 B grubu) ve 7 periyot vardır. Aynı gruptaki elementler benzer kimyasal özellikler gösterirken, bir periyotta soldan sağa ilerledikçe elementlerin özellikleri düzenli olarak değişir.
Elementler metaller, yarı metaller ve ametaller olarak sınıflandırılır. Metaller genellikle parlak, iletken ve işlenebilir maddelerdir (cıva hariç oda sıcaklığında katıdırlar). Yarı metaller hem metalik hem de ametalik özellikler gösterirler. Ametaller ise mat yüzeyli, kırılgan ve genellikle elektriği iletmeyen maddelerdir.
Bir elementin elektronları katmanlarda bulunur. Örneğin, sodyum (Na) elementinin elektron dizilimi 2-8-1 şeklindedir ve 3. periyot, 1A grubunda yer alır. Oksijen (O) ise 2-6 elektron dizilimiyle 2. periyot, 6A grubundadır.
Önemli ipucu: Periyodik tabloda bir elementin yerini bulabilmek için elektron dizilimini bilmek yeterlidir! Son katmandaki elektron sayısı A grup numarasını, katman sayısı ise periyot numarasını verir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Periyodik tabloda elementlerin özellikleri belirli bir düzen içinde değişir. Bu düzenli değişimleri hatırlamak için "EMAÇİ" kısaltması kullanışlıdır: E (Elektron İlgisi ve Elektronegatiflik), M (Metalik Özellik), A (Ametalik Özellik), Ç , İ (İyonlaşma Enerjisi).
Bir periyot boyunca soldan sağa gidildikçe atom numarası artar, atom çapı küçülür ve metalik özellikler azalır. İyonlaşma enerjisi, elektronegatiflik, elektron ilgisi ve değerlik elektron sayısı genellikle artar. Periyodun en sağında bulunan elementler (halojenler) en aktif ametallerdir.
Bir grup boyunca yukarıdan aşağıya inildikçe atom numarası ve atom çapı artar, metalik özellikler güçlenir. İyonlaşma enerjisi, elektronegatiflik ve elektron ilgisi azalır. Değerlik elektron sayısı ise değişmez. 1A grubunun en altında bulunan elementler (alkali metaller) en aktif metallerdir.
Periyodik tabloda en aktif metal Fransiyum (Fr) iken, en aktif ametal Flor (F)'dur. Bu aktiflik sıralaması, elementlerin elektron verme veya alma eğilimlerini gösterir.
Ezber kolaylığı: Periyodik özellikler için "Sağa gittikçe ametalik artar, aşağıya indikçe metallik artar" cümlesini aklında tut. Bu, neredeyse tüm periyodik özelliklerin nasıl değişeceğini tahmin etmene yardımcı olacaktır!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Elementler birbirleriyle etkileşime girerek bağlar oluşturur. Bu bağlar, güçlü etkileşimler (iyonik, kovalent, metalik) ve zayıf etkileşimler (van der Waals, hidrojen bağı) olarak ikiye ayrılır.
İyonik bağ, bir metal ile ametal arasında elektron alışverişi sonucu oluşur. Metal elektron vererek pozitif yüklü katyon, ametal elektron alarak negatif yüklü anyon haline gelir. Örneğin, Na+ ve Cl- iyonları arasında iyonik bağ vardır. İyonik bileşikler genellikle kristal yapıdadır, sert ve kırılgandır, yüksek erime noktalarına sahiptir ve çözeltileri elektrik iletir.
İyonik bileşiklerin formülü yazılırken katyonun ve anyonun yükleri çapraz yazılır: Xm+ + Yn- → XnYm. Örneğin, Mg2+ ve NO3- iyonlarından Mg(NO3)2 bileşiği oluşur.
İyonik bileşikler adlandırılırken önce katyonun, sonra anyonun adı yazılır. Örneğin NaCl "sodyum klorür" olarak adlandırılır. Birden fazla değerlik alabilen metaller (Fe, Hg, Sn, Pb, Cu, Cr) parantez içinde Roma rakamıyla belirtilir: CuCl "bakır(I) klorür", CuCl2 "bakır(II) klorür" gibi.
Hatırlatma: Elementlerin değerlik elektronlarını noktalarla gösterdiğimiz Lewis yapısı, bağ oluşumunu anlamada çok önemlidir. Metal-ametal etkileşimlerinde iyonik bağ, ametal-ametal etkileşimlerinde kovalent bağ oluşur!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kovalent bağ, atomlar arasında elektron ortaklaşması sonucu oluşan güçlü bir etkileşimdir. İki ametal arasında gerçekleşir ve elektronlar atomlar arasında paylaşılır.
Kovalent bağlar iki türlüdür: Apolar kovalent bağ aynı cins iki ametal atomu arasında oluşur (örneğin H2, Cl2). Polar kovalent bağ ise farklı cins ametaller arasında oluşur (örneğin HF). Polar bağda elektronlar elektronegatifliği yüksek olan atoma doğru daha yakın bulunur.
Kovalent bileşikler adlandırılırken latince sayılar kullanılır: ilk ametalin latince sayısı + ilk ametalin adı + ikinci ametalin latince sayısı + ikinci ametalin adı. Örneğin, N2O5 "diazot pentaoksit", CCl4 "karbon tetraklorür" olarak adlandırılır.
Metalik bağ ise metal atomları arasında oluşan bir bağ türüdür. Metaller değerlik elektronlarını ortaklaşa kullanır, bu elektronlar serbest hareket ederek "elektron denizi" oluşturur. Bu yapı metallerin elektrik ve ısıyı iyi iletmesini, dövülebilir ve işlenebilir olmasını sağlar.
Moleküllerde bağların dağılımı molekül polarlığını belirler. Genellikle bir molekülde merkez atom üzerinde ortaklaşmamış elektron çifti varsa molekül polar, yoksa apolar olma eğilimindedir.
Dikkat: Moleküllerin polar veya apolar oluşu, çözünürlüklerini ve fiziksel özelliklerini büyük ölçüde etkiler. "Benzer benzeri çözer" prensibi kimyada çok işimize yarar - polar maddeler polar çözücülerde, apolar maddeler apolar çözücülerde çözünür!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal türler arasında güçlü bağların yanında çeşitli zayıf etkileşimler de bulunur. Bu fiziksel bağlar maddelerin fiziksel özelliklerini ve davranışlarını belirlemede büyük rol oynar.
Hidrojen bağı, hidrojen atomunun flor, oksijen veya azot elementlerine (FON) bağlandığı moleküller arasında oluşan özel bir etkileşimdir. Örneğin su molekülleri arasında hidrojen bağları vardır. Bu bağlar diğer zayıf etkileşimlerden daha güçlüdür ve suyun yüksek kaynama noktası gibi birçok özelliğin nedenidir.
Van der Waals etkileşimleri çeşitli zayıf etkileşimleri kapsar. Dipol-dipol etkileşimleri polar moleküller arasında gerçekleşir (örneğin HCl molekülleri arasında). İyon-dipol etkileşimleri ise iyonlar ile polar moleküller arasında görülür .
İndüklenmiş dipol etkileşimleri üç şekilde olabilir: İyon-indüklenmiş dipol, dipol-indüklenmiş dipol ve London kuvvetleri . London kuvvetleri tüm maddelerde görülür, hatta apolar moleküller arasındaki tek etkileşim türüdür (örneğin CCl4 molekülleri arasında).
Pratik bilgi: Maddelerin fiziksel halleri (katı, sıvı, gaz) ve fiziksel özellikleri (erime noktası, kaynama noktası, çözünürlük) büyük oranda bu zayıf etkileşimlere bağlıdır. Suyun özel özellikleri, parfümlerin yayılması ve DNA'nın çift sarmal yapısı hep bu etkileşimler sayesinde gerçekleşir!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyanın temel kanunları, kimyasal reaksiyonların nasıl gerçekleştiğini açıklayan önemli kurallardır ve kimya biliminin temelini oluşturur.
Kütlenin Korunumu Kanunu (Antoine Lavoisier) kimyasal reaksiyonlarda toplam kütlenin değişmediğini belirtir. Örneğin, metan yanması reaksiyonunda giren maddelerin toplam kütlesi, çıkan maddelerin toplam kütlesine eşittir.
Sabit Oranlar Kanunu (Joseph Proust) bir bileşiği oluşturan elementlerin kütlelerinin her zaman sabit bir oranda olduğunu söyler. Örneğin, suyun (H₂O) oluşumunda hidrojen ve oksijenin kütlece oranı her zaman 1:8'dir ve bu oran değişmez.
Katlı Oranlar Kanunu (John Dalton) aynı iki elementin oluşturduğu farklı bileşiklerde, elementlerden birinin sabit miktarıyla diğerinin kütleleri arasında tam sayılı bir oran vardır. Örneğin, karbon monoksit (CO) ve karbon dioksit (CO₂) için oksijen atomları arasındaki katlı oran 1:2'dir.
Katlı oranlar kanununda bazı önemli kısıtlamalar vardır: Basit formülleri aynı olan bileşikler arasında (NO₂ ve N₂O₄ gibi), farklı element türleri içeren bileşikler arasında (CH₄ ve CO₂ gibi) veya ikiden fazla element içeren bileşikler arasında (H₂SO₃ ve H₂SO₄ gibi) katlı oran aranmaz.
Önemli hatırlatma: Bu temel kanunlar, modern kimyanın temelini oluşturan atom teorisinin gelişmesine yol açmıştır. Özellikle kimyasal reaksiyon denklemlerini denkleştirirken kütlenin korunumu kanunu sürekli kullanılır!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
8
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı