Modern atom teorisi ve periyodik özellikler konusu, atom yapısını, elektronların... Daha fazla göster
Kimya Orbital Teorisi



















Modern Atom Teorisi
Bohr atom modelinden sonra modern atom teorisine geçiş, birçok bilim insanının katkılarıyla olmuştur. Maxwell ışığın elektromanyetik dalgalardan oluştuğunu, Planck ise atomların enerjiyi küçük paketler (kuant) halinde yayınlayıp soğurduğunu keşfetti. Einstein'ın fotoelektrik etkisi de atom modeline önemli katkı sağladı.
Bohr atom modelinde elektronlar çekirdek çevresinde belirli enerjili dairesel yörüngelerde dolanır. Çekirdeğe yakın yörüngelerin enerjisi düşük, uzak yörüngelerin enerjisi yüksektir. Elektronlar enerji alarak üst yörüngelere geçer (uyarılmış hal) veya enerji vererek alt yörüngelere döner. Ancak bu model , , gibi tek elektronlu tanecikler için geçerliyken çok elektronlu yapılar için yetersiz kalmıştır. Ayrıca elektronların neden çekirdeğe düşmediğini açıklayamamıştır.
De Broglie'nin elektronların dalga özelliği gösterdiğini keşfetmesi ve Heisenberg'in elektronun konumu ve hızının aynı anda belirlenemeyeceğini (belirsizlik ilkesi) ortaya koymasıyla modern atom teorisine geçildi. Schrödinger'in dalga fonksiyonu denklemi ile elektronların bulunma olasılığının yüksek olduğu bölgeler olan orbitaller kavramı ortaya çıktı.
Önemli Bilgi: Modern atom teorisinde elektronların kesin yerini bilemeyiz, yalnızca bulunma olasılıklarını hesaplayabiliriz. Bu durum, atomun davranışını anlamak için kuantum mekaniğinin gerekliliğini gösterir.

Yörünge ve Orbital Kavramları
Yörünge ve orbital arasında önemli farklar vardır. Yörünge, elektronun izlediği dairesel yoldur ve iki boyutludur. Orbital ise elektronun bulunma olasılığının yüksek olduğu, üç boyutlu bölgedir. Her orbitalde en fazla 2 elektron bulunabilir.
Atomdaki elektronların durumlarını tanımlamak için kuantum sayıları kullanılır:
Baş Kuantum Sayısı (n): Elektronun enerji düzeyini ve çekirdeğe olan ortalama uzaklığı gösterir. "n" ile gösterilir ve pozitif tam sayı değerleri alır . Katmanlar K, L, M, N şeklinde de gösterilir.
Açısal Momentum Kuantum Sayısı (l): Orbitalin şeklini ve bir enerji düzeyinde kaç tane alt enerji düzeyi olduğunu belirtir. Yan ya da ikincil kuantum sayısı da denir. Değerleri l=0'dan l=n-1'e kadardır. l değerleri orbital türünü belirtir:
l=0 → s orbitali
l=1 → p orbitali
l=2 → d orbitali
l=3 → f orbitali
Her enerji düzeyinde (n) bulunabilecek orbital türleri ve toplam orbital sayısı (n²) belirlidir. Örneğin n=3 için l=0,1,2 yani s, p ve d orbitalleri bulunur ve toplam 9 orbital vardır.
Dikkat: Elektronların orbital düzenini belirlerken kuantum sayıları çok önemlidir. Bu sayılar, elektronların yerleşimini ve atomların kimyasal özelliklerini doğrudan etkiler.

Manyetik Kuantum Sayısı ve Orbital Türleri
Manyetik Kuantum Sayısı (ml): Alt enerji düzeyinde kaç tane orbital olduğunu gösterir. Değerleri -l,...,0,...,+l şeklindedir. Bir orbital türünün kaç tane olduğu ml=2l+1 formülü ile hesaplanır:
- s orbitali : ml=0 → 1 tane
- p orbitali : ml=-1,0,+1 → 3 tane
- d orbitali : ml=-2,-1,0,+1,+2 → 5 tane
- f orbitali : ml=-3,-2,-1,0,+1,+2,+3 → 7 tane
Spin Kuantum Sayısı (ms): Elektronun kendi ekseni etrafındaki dönme hareketini gösterir. Değerleri +1/2 (saat yönünde) veya -1/2 (saat yönünün tersinde) olabilir.
s Orbitali: Küresel şekle sahiptir. Her enerji seviyesinde sadece 1 tane bulunur (1s, 2s, 3s gibi).
p Orbitali: Uzayda üç farklı yönelimde (px, py, pz) bulunur. Her enerji seviyesinde 3 tane p orbitali vardır.
d Orbitali: Beş farklı yönelimde bulunur. Her enerji seviyesinde 5 tane d orbitali vardır.
Bilimsel Not: Orbitaller aslında matematiksel fonksiyonlardır ve sadece yüksek olasılıklı elektron bulunma bölgelerini gösterirler. Gerçekte elektronlar bu bölgelerde dalgasal davranış gösterirler.

f Orbitali ve Orbitallerin Enerjileri
f Orbitali: l=3 değerine sahiptir ve ml=-3,-2,-1,0,+1,+2,+3 olmak üzere 7 farklı yönelimde bulunur. Her enerji seviyesinde 7 tane f orbitali vardır.
Orbitallerin Enerjileri: Orbitallerin enerji seviyeleri n+l değerlerine göre belirlenir:
- n+l değeri arttıkça orbital enerjisi artar.
- n+l değerleri eşit olan orbitallerden n değeri büyük olanın enerjisi daha büyüktür.
Bu kurala göre orbitallerin enerji sıralaması şöyledir: 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f < 5d < 6p < 7s...
Elektron dizilimlerini yazarken bu sıra takip edilir. Her orbital en fazla 2 elektron alabilir. Buna göre, her enerji seviyesindeki (n) maksimum elektron sayısı 2n² formülü ile hesaplanır:
- n=1: maksimum 2 elektron
- n=2: maksimum 8 elektron
- n=3: maksimum 18 elektron
- n=4: maksimum 32 elektron
Elektron dizilimini şematik olarak göstermek için orbitallerde bulunan elektronlar ↑↓ şeklinde gösterilir.
Hatırlatma: 24Cr ve 29Cu elementlerinin elektron dizilimleri standart dizilimden farklılık gösterir. Cr'da 4s²3d⁴ yerine 4s¹3d⁵, Cu'da 4s²3d⁹ yerine 4s¹3d¹⁰ görülür. Bunun nedeni yarı dolu veya tam dolu d orbitallerinin daha kararlı olmasıdır.

Elektronların Orbitallere Yerleşimi
Elektronlar atomda belirli kurallara göre yerleşir:
Pauli İlkesi: Bir atomda bulunan iki elektronun dört kuantum sayısı aynı olamaz. Her orbital en fazla 2 elektron alabilir ve bu elektronların spinleri zıt yönlüdür.
Aufbau Kuralı: Elektronlar orbitallere düşük enerjili orbitalden başlayarak yerleşir. Örneğin, ¹¹Na atomunda elektronlar 1s²2s²2p⁶3s¹ şeklinde dağılır.
Hund Kuralı: Elektronlar eş enerjili orbitallere yerleşirken önce boş orbitallere aynı spinli olacak şekilde birer birer yerleşir. Daha sonra elektronlar zıt spinli olacak şekilde her orbitale yerleşir. Örneğin, ⁸O atomunda 2p orbitallerine elektronlar önce tek tek, sonra çift olarak yerleşir.
Küresel Simetri: Bir elektron diziliminin son orbital grubunun tam dolu (s², p⁶, d¹⁰, f¹⁴) ya da yarı dolu (s¹, p³, d⁵, f⁷) olması durumudur. Bu durumlar özel kararlılık gösterir.
İyonların Elektron Dizilimi: Bir atom elektron verirken önce en dış katmandan ve en yüksek enerjili orbitalden başlar. Örneğin, ¹¹Na → ¹¹Na⁺ olurken 3s¹ orbitalindeki elektronu verir.
Kimya Notu: İyonlaşma sırasında öncelikle en dış katmandaki elektronlar verilir, çünkü bunlar çekirdeğe en uzak ve en az bağlı olan elektronlardır. Bu bilgi, elementlerin kimyasal reaktifliğini anlamak için çok önemlidir!

Değerlik Orbitali ve Grup-Periyot İlişkisi
Değerlik Orbitalleri: Atomun en yüksek enerjili orbitalleridir. Bu orbitallerdeki elektronlara değerlik elektronları denir.
Grup-Periyot İlişkisi: Değerlik elektron sayısı elementlerin grup numarasını, en yüksek enerji düzeyi (en büyük baş kuantum sayısı) ise periyot numarasını belirtir.
Bir element atomunun temel elektron diziliminin son terimine bakılarak A veya B grubu belirlenir:
- s veya p ile bitiyorsa → A grubu
- d veya f ile bitiyorsa → B grubu
A grubu elementlerinin değerlik elektron sayısı doğrudan grup numarasını verir:
- ns¹ → 1A grubu
- ns² → 2A grubu
- ns²np¹ → 3A grubu
- ns²np² → 4A grubu
- ns²np³ → 5A grubu
- ns²np⁴ → 6A grubu
- ns²np⁵ → 7A grubu
- ns²np⁶ → 8A grubu
B grubu elementlerinde değerlik elektron sayısı hesaplanırken s ve d orbitallerindeki elektronlar toplanır:
- ns²d¹ → 3B grubu
- ns²d² → 4B grubu
- ns²d¹⁰ → 2B grubu
Önemli İpucu: Elektron diziliminin son terimi d orbitali olan elementlerde, değerlik elektron sayısı 10'dan büyükse grup numarası bulunurken değerlik elektron sayısından 10 çıkarılır.

Periyodik Özellikler - Atomik Yarıçap
Atomik Yarıçap: Atom çekirdeği ile en dış katmandaki elektron arasındaki uzaklıktır. Dört farklı türü vardır:
- Kovalent Yarıçap: İki atom arasında kovalent bağ olduğunda ölçülen yarıçaptır.
- Van der Waals Yarıçapı: Zayıf etkileşimli atomlar arasındaki mesafenin yarısıdır.
- Metalik Yarıçap: Metal atomlarının çekirdekleri arasındaki uzaklığın yarısıdır.
- İyonik Yarıçap: İyonik bileşiklerdeki bir iyonun yarıçapıdır.
İyonik Yarıçap Değişimi:
- Bir atom elektron verdiğinde yarıçapı küçülür.
- Bir atom elektron aldığında yarıçapı büyür.
Periyodik Tabloda Yarıçap Değişimi:
- Aynı grupta periyot sayısı arttıkça atom yarıçapı artar.
- Aynı periyotta soldan sağa doğru proton sayısı arttıkça atom yarıçapı azalır.
Aynı Elektron Dizilimli İyonlar: Elektron sayısı ve dizilimi aynı olan iki iyondan proton sayısı küçük olanın yarıçapı daha büyüktür.
Örneğin, ²⁰Ca²⁺ ve ¹⁷Cl⁻ iyonlarının elektron dizilimleri aynıdır (1s²2s²2p⁶3s²3p⁶), ancak Cl⁻'nin yarıçapı Ca²⁺'den büyüktür çünkü proton sayısı daha azdır.
Periyodik Sistem Bağlantısı: Atom yarıçapı, tüm periyodik özellikleri etkileyen temel faktördür. Elementlerin fiziksel ve kimyasal özellikleri, bu yarıçap değişimlerinden büyük ölçüde etkilenir.

Metalik-Ametalik Aktiflik ve İyonlaşma Enerjisi
Metalik Aktiflik: Elektron verme eğilimidir. Atom yarıçapı arttıkça metalik aktiflik artar.
- Aynı grupta yukarıdan aşağıya doğru artar.
- Aynı periyotta soldan sağa doğru azalır.
Ametalik Aktiflik: Elektron alma eğilimidir. Atom yarıçapı azaldıkça ametalik aktiflik artar.
- Aynı grupta yukarıdan aşağıya doğru azalır.
- Aynı periyotta soldan sağa doğru artar.
İyonlaşma Enerjisi: Temel haldeki nötr bir gaz atomundan elektron koparmak için gereken enerjidir. Atom yarıçapı ile genellikle ters orantılıdır.
Birinci iyonlaşma enerjisi (E₁): X(g) + E₁ → X(g)⁺ + e⁻ İkinci iyonlaşma enerjisi (E₂): X(g)⁺ + E₂ → X(g)²⁺ + e⁻
İyonlaşma Enerjisi Değişimleri:
- Bir atomdan elektron koparıldıkça iyonlaşma enerjisi artar (1.İE < 2.İE < 3.İE...)
- Aynı grupta yukarıdan aşağı doğru yarıçap artarken iyonlaşma enerjisi azalır.
- Aynı periyotta soldan sağa doğru iyonlaşma enerjisi genellikle artar.
İstisnalar: 2A grubunun iyonlaşma enerjisi 3A grubundan ve 5A grubunun iyonlaşma enerjisi 6A grubundan büyüktür. Bunun nedeni 2A ve 5A gruplarının küresel simetri özelliği göstermesidir.
Kimya Sınavı Notu: İyonlaşma enerjisindeki ani artışlar, elementlerin grup numaralarını belirleme konusunda ipucu verir. Bir iyonlaşma enerjisinden diğerine geçişte en az 3,5-4 kat ani artış görüldüğünde, değerlik elektronlarının bittiğini ve bir alt kabuğa geçildiğini gösterir.

Elektron İlgisi ve Elektronegatiflik
Elektron İlgisi: Gaz halindeki nötr bir atomun bir elektron alması sırasında gerçekleşen enerji değişimidir. Açığa çıkan enerji değeri büyüdükçe atomun elektron ilgisi artar.
X(g) + e⁻ → X(g)⁻ + E₁
Elektron İlgisinin Periyodik Değişimi:
- Aynı periyotta grup numarası arttıkça elektron ilgisi genellikle artar (soy gazlar hariç).
- Aynı grupta periyot sayısı arttıkça elektron ilgisi azalır.
- İstisna olarak Cl'nin elektron ilgisi F'den büyüktür.
Elektronegatiflik: Bir atomun kimyasal bağdaki elektronları kendine doğru çekebilme yeteneğinin bir ölçüsüdür.
Elektronegatifliğin Periyodik Değişimi:
- Aynı periyotta grup numarası arttıkça elektronegatiflik genellikle artar (soy gazlar hariç).
- Aynı grupta periyot sayısı arttıkça elektronegatiflik azalır.
- En elektronegatif element F'dir.
Oksit ve Hidroksitlerin Asit-Baz Özelliği:
- Aynı grupta periyot sayısı arttıkça hidroksit bileşiklerinin bazlık karakteri artar (KOH > NaOH).
- 7A grubu elementlerinin hidrojenli bileşikleri asidik özellik gösterir. Bu grupta yukarıdan aşağı inildikçe asidik özellik artar (HI > HBr > HCl > HF).
- Genellikle metallerin oksitleri bazik, ametallerin oksitleri ise asidik özellik gösterir.
Pratik Bilgi: Periyodik tabloda F en elektronegatif element olmasına rağmen, Cl'nin elektron ilgisi F'den daha büyüktür. Bu durumun nedeni F atomunun çok küçük olması ve elektronlar arasındaki itme kuvvetinin fazla olmasıdır.

Periyodik Tabloda Grupların Özellikleri
1A Grubu (Alkali Metaller):
- H, Li, Na, K, Rb, Cs, Fr elementlerini içerir (H hariç alkali metaller).
- Bileşiklerinde +1 yüklü iyon halinde bulunurlar.
- Bulundukları periyodun en aktif metalleridir.
- Oksitleri bazik özellik gösterir.
- Asitler ve suyla tepkime verirler: Na + H₂O → NaOH + ½H₂
2A Grubu (Toprak Alkali Metaller):
- Be, Mg, Ca, Sr, Ba, Ra elementlerini içerir.
- Bileşiklerinde +2 yüklü iyon halinde bulunurlar.
- Alkali metallerden sonra kimyasal olarak en aktif metallerdir.
- Oksitleri bazik özellik gösterir (Be hariç, Be'nin oksitleri amfoter).
7A Grubu (Halojenler):
- F, Cl, Br, I, At elementlerini içerir.
- Oda şartlarında F₂ ve Cl₂ gaz, Br₂ sıvı, I₂ katı haldedir.
- F sadece -1 değerlik alırken, diğerleri -1 ile +7 arası tüm değerlikleri alabilir.
8A Grubu (Soy Gazlar):
- He, Ne, Ar, Kr, Xe, Rn elementlerini içerir.
- Renksiz ve monoatomik yapıdadırlar.
- Kararlı elektronik yapıya sahip oldukları için bileşik yapmazlar.
- He'nin değerlik elektron sayısı 2, diğerlerininki 8'dir.
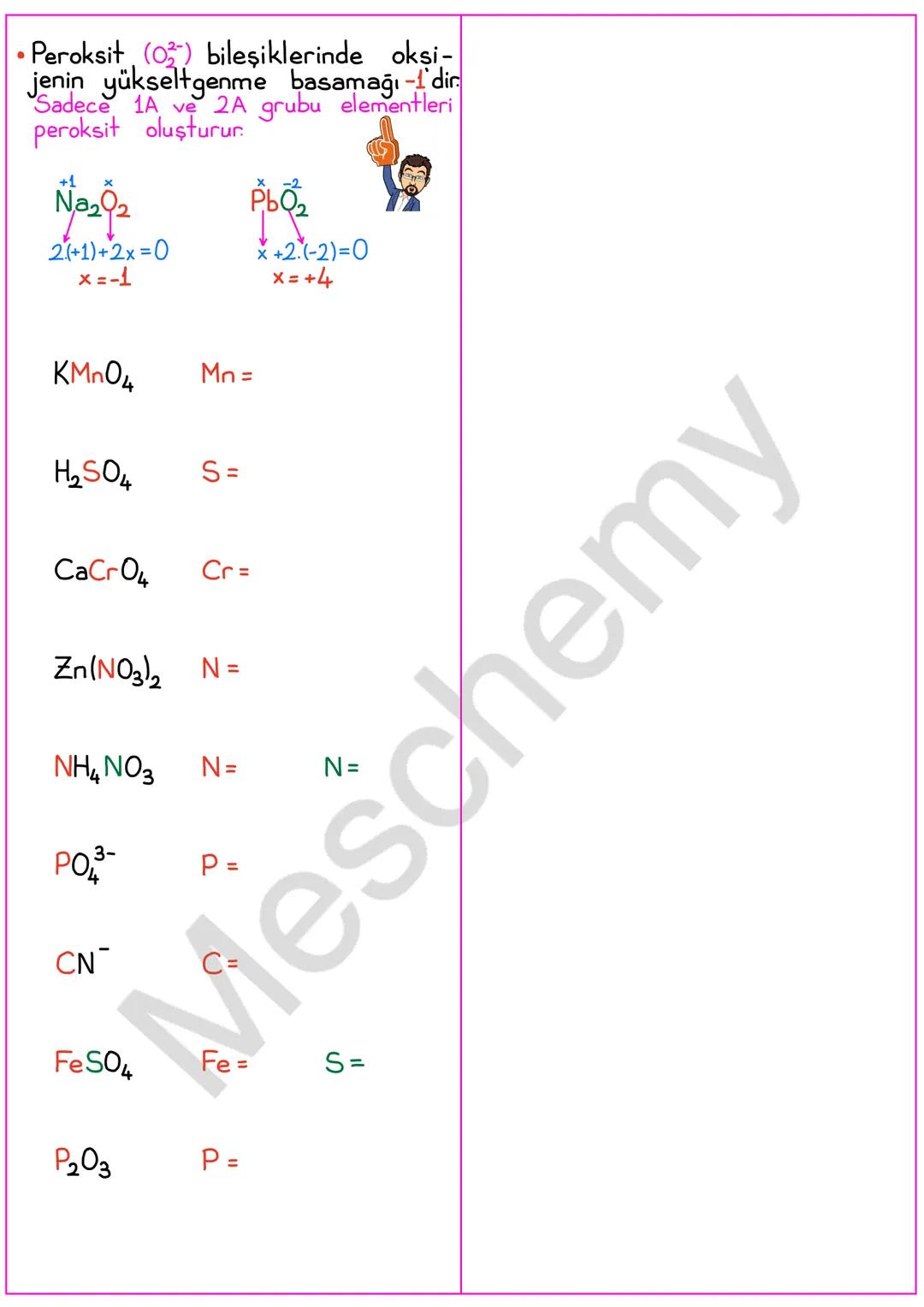
İlginç Bilgi: Peroksit (O₂²⁻) bileşiklerinde oksijenin yükseltgenme basamağı -1'dir ve sadece 1A ve 2A grubu elementleri peroksit oluşturabilir. Örneğin Na₂O₂'de oksijen -1 yükseltgenme basamağına sahiptir.







Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Orbital
99. Sınıf atom modelleri yeni müfredat
Ders notu
AYT KİMYA MODERN ATOM TEORİSİ
MODERN ATOM TEORİSİ
11 Kimya
11. sınıf kimya orbitaller Ayt kimya 1. ünite
9 . Sınıf kimya orbitaller
Umarım faydalı olur
Kimya 9. Sınıf ORBİTALLER
Orbital şekilleri, orbitallerin sıralanışı, küresel simetri, anyon ve katyon, orbital kuralları, temel hal ve uyarılmış hal, valans elektron ve orbital konularını içerir.
modern atom teorisi
11. sınıf kimya modern atom teorisi
ayt kimya 1.ünite
modern atom teorisi
9. Sınıf KİMYA
1.1 YAZILI ÖRNEĞİ
Atom Orbitalleri 9.sınıf (TYT)
Orbital nedir ve orbital türleri nelerdir?
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
Kimya Orbital Teorisi
Modern atom teorisi ve periyodik özellikler konusu, atom yapısını, elektronların atomdaki davranışlarını ve elementlerin periyodik özelliklere göre sınıflandırılmasını anlatır. Bu konular, kimyanın temelini oluşturur ve maddelerin özelliklerini anlamamızı sağlar.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Modern Atom Teorisi
Bohr atom modelinden sonra modern atom teorisine geçiş, birçok bilim insanının katkılarıyla olmuştur. Maxwell ışığın elektromanyetik dalgalardan oluştuğunu, Planck ise atomların enerjiyi küçük paketler (kuant) halinde yayınlayıp soğurduğunu keşfetti. Einstein'ın fotoelektrik etkisi de atom modeline önemli katkı sağladı.
Bohr atom modelinde elektronlar çekirdek çevresinde belirli enerjili dairesel yörüngelerde dolanır. Çekirdeğe yakın yörüngelerin enerjisi düşük, uzak yörüngelerin enerjisi yüksektir. Elektronlar enerji alarak üst yörüngelere geçer (uyarılmış hal) veya enerji vererek alt yörüngelere döner. Ancak bu model , , gibi tek elektronlu tanecikler için geçerliyken çok elektronlu yapılar için yetersiz kalmıştır. Ayrıca elektronların neden çekirdeğe düşmediğini açıklayamamıştır.
De Broglie'nin elektronların dalga özelliği gösterdiğini keşfetmesi ve Heisenberg'in elektronun konumu ve hızının aynı anda belirlenemeyeceğini (belirsizlik ilkesi) ortaya koymasıyla modern atom teorisine geçildi. Schrödinger'in dalga fonksiyonu denklemi ile elektronların bulunma olasılığının yüksek olduğu bölgeler olan orbitaller kavramı ortaya çıktı.
Önemli Bilgi: Modern atom teorisinde elektronların kesin yerini bilemeyiz, yalnızca bulunma olasılıklarını hesaplayabiliriz. Bu durum, atomun davranışını anlamak için kuantum mekaniğinin gerekliliğini gösterir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Yörünge ve Orbital Kavramları
Yörünge ve orbital arasında önemli farklar vardır. Yörünge, elektronun izlediği dairesel yoldur ve iki boyutludur. Orbital ise elektronun bulunma olasılığının yüksek olduğu, üç boyutlu bölgedir. Her orbitalde en fazla 2 elektron bulunabilir.
Atomdaki elektronların durumlarını tanımlamak için kuantum sayıları kullanılır:
Baş Kuantum Sayısı (n): Elektronun enerji düzeyini ve çekirdeğe olan ortalama uzaklığı gösterir. "n" ile gösterilir ve pozitif tam sayı değerleri alır . Katmanlar K, L, M, N şeklinde de gösterilir.
Açısal Momentum Kuantum Sayısı (l): Orbitalin şeklini ve bir enerji düzeyinde kaç tane alt enerji düzeyi olduğunu belirtir. Yan ya da ikincil kuantum sayısı da denir. Değerleri l=0'dan l=n-1'e kadardır. l değerleri orbital türünü belirtir:
l=0 → s orbitali
l=1 → p orbitali
l=2 → d orbitali
l=3 → f orbitali
Her enerji düzeyinde (n) bulunabilecek orbital türleri ve toplam orbital sayısı (n²) belirlidir. Örneğin n=3 için l=0,1,2 yani s, p ve d orbitalleri bulunur ve toplam 9 orbital vardır.
Dikkat: Elektronların orbital düzenini belirlerken kuantum sayıları çok önemlidir. Bu sayılar, elektronların yerleşimini ve atomların kimyasal özelliklerini doğrudan etkiler.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Manyetik Kuantum Sayısı ve Orbital Türleri
Manyetik Kuantum Sayısı (ml): Alt enerji düzeyinde kaç tane orbital olduğunu gösterir. Değerleri -l,...,0,...,+l şeklindedir. Bir orbital türünün kaç tane olduğu ml=2l+1 formülü ile hesaplanır:
- s orbitali : ml=0 → 1 tane
- p orbitali : ml=-1,0,+1 → 3 tane
- d orbitali : ml=-2,-1,0,+1,+2 → 5 tane
- f orbitali : ml=-3,-2,-1,0,+1,+2,+3 → 7 tane
Spin Kuantum Sayısı (ms): Elektronun kendi ekseni etrafındaki dönme hareketini gösterir. Değerleri +1/2 (saat yönünde) veya -1/2 (saat yönünün tersinde) olabilir.
s Orbitali: Küresel şekle sahiptir. Her enerji seviyesinde sadece 1 tane bulunur (1s, 2s, 3s gibi).
p Orbitali: Uzayda üç farklı yönelimde (px, py, pz) bulunur. Her enerji seviyesinde 3 tane p orbitali vardır.
d Orbitali: Beş farklı yönelimde bulunur. Her enerji seviyesinde 5 tane d orbitali vardır.
Bilimsel Not: Orbitaller aslında matematiksel fonksiyonlardır ve sadece yüksek olasılıklı elektron bulunma bölgelerini gösterirler. Gerçekte elektronlar bu bölgelerde dalgasal davranış gösterirler.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
f Orbitali ve Orbitallerin Enerjileri
f Orbitali: l=3 değerine sahiptir ve ml=-3,-2,-1,0,+1,+2,+3 olmak üzere 7 farklı yönelimde bulunur. Her enerji seviyesinde 7 tane f orbitali vardır.
Orbitallerin Enerjileri: Orbitallerin enerji seviyeleri n+l değerlerine göre belirlenir:
- n+l değeri arttıkça orbital enerjisi artar.
- n+l değerleri eşit olan orbitallerden n değeri büyük olanın enerjisi daha büyüktür.
Bu kurala göre orbitallerin enerji sıralaması şöyledir: 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f < 5d < 6p < 7s...
Elektron dizilimlerini yazarken bu sıra takip edilir. Her orbital en fazla 2 elektron alabilir. Buna göre, her enerji seviyesindeki (n) maksimum elektron sayısı 2n² formülü ile hesaplanır:
- n=1: maksimum 2 elektron
- n=2: maksimum 8 elektron
- n=3: maksimum 18 elektron
- n=4: maksimum 32 elektron
Elektron dizilimini şematik olarak göstermek için orbitallerde bulunan elektronlar ↑↓ şeklinde gösterilir.
Hatırlatma: 24Cr ve 29Cu elementlerinin elektron dizilimleri standart dizilimden farklılık gösterir. Cr'da 4s²3d⁴ yerine 4s¹3d⁵, Cu'da 4s²3d⁹ yerine 4s¹3d¹⁰ görülür. Bunun nedeni yarı dolu veya tam dolu d orbitallerinin daha kararlı olmasıdır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektronların Orbitallere Yerleşimi
Elektronlar atomda belirli kurallara göre yerleşir:
Pauli İlkesi: Bir atomda bulunan iki elektronun dört kuantum sayısı aynı olamaz. Her orbital en fazla 2 elektron alabilir ve bu elektronların spinleri zıt yönlüdür.
Aufbau Kuralı: Elektronlar orbitallere düşük enerjili orbitalden başlayarak yerleşir. Örneğin, ¹¹Na atomunda elektronlar 1s²2s²2p⁶3s¹ şeklinde dağılır.
Hund Kuralı: Elektronlar eş enerjili orbitallere yerleşirken önce boş orbitallere aynı spinli olacak şekilde birer birer yerleşir. Daha sonra elektronlar zıt spinli olacak şekilde her orbitale yerleşir. Örneğin, ⁸O atomunda 2p orbitallerine elektronlar önce tek tek, sonra çift olarak yerleşir.
Küresel Simetri: Bir elektron diziliminin son orbital grubunun tam dolu (s², p⁶, d¹⁰, f¹⁴) ya da yarı dolu (s¹, p³, d⁵, f⁷) olması durumudur. Bu durumlar özel kararlılık gösterir.
İyonların Elektron Dizilimi: Bir atom elektron verirken önce en dış katmandan ve en yüksek enerjili orbitalden başlar. Örneğin, ¹¹Na → ¹¹Na⁺ olurken 3s¹ orbitalindeki elektronu verir.
Kimya Notu: İyonlaşma sırasında öncelikle en dış katmandaki elektronlar verilir, çünkü bunlar çekirdeğe en uzak ve en az bağlı olan elektronlardır. Bu bilgi, elementlerin kimyasal reaktifliğini anlamak için çok önemlidir!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Değerlik Orbitali ve Grup-Periyot İlişkisi
Değerlik Orbitalleri: Atomun en yüksek enerjili orbitalleridir. Bu orbitallerdeki elektronlara değerlik elektronları denir.
Grup-Periyot İlişkisi: Değerlik elektron sayısı elementlerin grup numarasını, en yüksek enerji düzeyi (en büyük baş kuantum sayısı) ise periyot numarasını belirtir.
Bir element atomunun temel elektron diziliminin son terimine bakılarak A veya B grubu belirlenir:
- s veya p ile bitiyorsa → A grubu
- d veya f ile bitiyorsa → B grubu
A grubu elementlerinin değerlik elektron sayısı doğrudan grup numarasını verir:
- ns¹ → 1A grubu
- ns² → 2A grubu
- ns²np¹ → 3A grubu
- ns²np² → 4A grubu
- ns²np³ → 5A grubu
- ns²np⁴ → 6A grubu
- ns²np⁵ → 7A grubu
- ns²np⁶ → 8A grubu
B grubu elementlerinde değerlik elektron sayısı hesaplanırken s ve d orbitallerindeki elektronlar toplanır:
- ns²d¹ → 3B grubu
- ns²d² → 4B grubu
- ns²d¹⁰ → 2B grubu
Önemli İpucu: Elektron diziliminin son terimi d orbitali olan elementlerde, değerlik elektron sayısı 10'dan büyükse grup numarası bulunurken değerlik elektron sayısından 10 çıkarılır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Periyodik Özellikler - Atomik Yarıçap
Atomik Yarıçap: Atom çekirdeği ile en dış katmandaki elektron arasındaki uzaklıktır. Dört farklı türü vardır:
- Kovalent Yarıçap: İki atom arasında kovalent bağ olduğunda ölçülen yarıçaptır.
- Van der Waals Yarıçapı: Zayıf etkileşimli atomlar arasındaki mesafenin yarısıdır.
- Metalik Yarıçap: Metal atomlarının çekirdekleri arasındaki uzaklığın yarısıdır.
- İyonik Yarıçap: İyonik bileşiklerdeki bir iyonun yarıçapıdır.
İyonik Yarıçap Değişimi:
- Bir atom elektron verdiğinde yarıçapı küçülür.
- Bir atom elektron aldığında yarıçapı büyür.
Periyodik Tabloda Yarıçap Değişimi:
- Aynı grupta periyot sayısı arttıkça atom yarıçapı artar.
- Aynı periyotta soldan sağa doğru proton sayısı arttıkça atom yarıçapı azalır.
Aynı Elektron Dizilimli İyonlar: Elektron sayısı ve dizilimi aynı olan iki iyondan proton sayısı küçük olanın yarıçapı daha büyüktür.
Örneğin, ²⁰Ca²⁺ ve ¹⁷Cl⁻ iyonlarının elektron dizilimleri aynıdır (1s²2s²2p⁶3s²3p⁶), ancak Cl⁻'nin yarıçapı Ca²⁺'den büyüktür çünkü proton sayısı daha azdır.
Periyodik Sistem Bağlantısı: Atom yarıçapı, tüm periyodik özellikleri etkileyen temel faktördür. Elementlerin fiziksel ve kimyasal özellikleri, bu yarıçap değişimlerinden büyük ölçüde etkilenir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Metalik-Ametalik Aktiflik ve İyonlaşma Enerjisi
Metalik Aktiflik: Elektron verme eğilimidir. Atom yarıçapı arttıkça metalik aktiflik artar.
- Aynı grupta yukarıdan aşağıya doğru artar.
- Aynı periyotta soldan sağa doğru azalır.
Ametalik Aktiflik: Elektron alma eğilimidir. Atom yarıçapı azaldıkça ametalik aktiflik artar.
- Aynı grupta yukarıdan aşağıya doğru azalır.
- Aynı periyotta soldan sağa doğru artar.
İyonlaşma Enerjisi: Temel haldeki nötr bir gaz atomundan elektron koparmak için gereken enerjidir. Atom yarıçapı ile genellikle ters orantılıdır.
Birinci iyonlaşma enerjisi (E₁): X(g) + E₁ → X(g)⁺ + e⁻ İkinci iyonlaşma enerjisi (E₂): X(g)⁺ + E₂ → X(g)²⁺ + e⁻
İyonlaşma Enerjisi Değişimleri:
- Bir atomdan elektron koparıldıkça iyonlaşma enerjisi artar (1.İE < 2.İE < 3.İE...)
- Aynı grupta yukarıdan aşağı doğru yarıçap artarken iyonlaşma enerjisi azalır.
- Aynı periyotta soldan sağa doğru iyonlaşma enerjisi genellikle artar.
İstisnalar: 2A grubunun iyonlaşma enerjisi 3A grubundan ve 5A grubunun iyonlaşma enerjisi 6A grubundan büyüktür. Bunun nedeni 2A ve 5A gruplarının küresel simetri özelliği göstermesidir.
Kimya Sınavı Notu: İyonlaşma enerjisindeki ani artışlar, elementlerin grup numaralarını belirleme konusunda ipucu verir. Bir iyonlaşma enerjisinden diğerine geçişte en az 3,5-4 kat ani artış görüldüğünde, değerlik elektronlarının bittiğini ve bir alt kabuğa geçildiğini gösterir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektron İlgisi ve Elektronegatiflik
Elektron İlgisi: Gaz halindeki nötr bir atomun bir elektron alması sırasında gerçekleşen enerji değişimidir. Açığa çıkan enerji değeri büyüdükçe atomun elektron ilgisi artar.
X(g) + e⁻ → X(g)⁻ + E₁
Elektron İlgisinin Periyodik Değişimi:
- Aynı periyotta grup numarası arttıkça elektron ilgisi genellikle artar (soy gazlar hariç).
- Aynı grupta periyot sayısı arttıkça elektron ilgisi azalır.
- İstisna olarak Cl'nin elektron ilgisi F'den büyüktür.
Elektronegatiflik: Bir atomun kimyasal bağdaki elektronları kendine doğru çekebilme yeteneğinin bir ölçüsüdür.
Elektronegatifliğin Periyodik Değişimi:
- Aynı periyotta grup numarası arttıkça elektronegatiflik genellikle artar (soy gazlar hariç).
- Aynı grupta periyot sayısı arttıkça elektronegatiflik azalır.
- En elektronegatif element F'dir.
Oksit ve Hidroksitlerin Asit-Baz Özelliği:
- Aynı grupta periyot sayısı arttıkça hidroksit bileşiklerinin bazlık karakteri artar (KOH > NaOH).
- 7A grubu elementlerinin hidrojenli bileşikleri asidik özellik gösterir. Bu grupta yukarıdan aşağı inildikçe asidik özellik artar (HI > HBr > HCl > HF).
- Genellikle metallerin oksitleri bazik, ametallerin oksitleri ise asidik özellik gösterir.
Pratik Bilgi: Periyodik tabloda F en elektronegatif element olmasına rağmen, Cl'nin elektron ilgisi F'den daha büyüktür. Bu durumun nedeni F atomunun çok küçük olması ve elektronlar arasındaki itme kuvvetinin fazla olmasıdır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Periyodik Tabloda Grupların Özellikleri
1A Grubu (Alkali Metaller):
- H, Li, Na, K, Rb, Cs, Fr elementlerini içerir (H hariç alkali metaller).
- Bileşiklerinde +1 yüklü iyon halinde bulunurlar.
- Bulundukları periyodun en aktif metalleridir.
- Oksitleri bazik özellik gösterir.
- Asitler ve suyla tepkime verirler: Na + H₂O → NaOH + ½H₂
2A Grubu (Toprak Alkali Metaller):
- Be, Mg, Ca, Sr, Ba, Ra elementlerini içerir.
- Bileşiklerinde +2 yüklü iyon halinde bulunurlar.
- Alkali metallerden sonra kimyasal olarak en aktif metallerdir.
- Oksitleri bazik özellik gösterir (Be hariç, Be'nin oksitleri amfoter).
7A Grubu (Halojenler):
- F, Cl, Br, I, At elementlerini içerir.
- Oda şartlarında F₂ ve Cl₂ gaz, Br₂ sıvı, I₂ katı haldedir.
- F sadece -1 değerlik alırken, diğerleri -1 ile +7 arası tüm değerlikleri alabilir.
8A Grubu (Soy Gazlar):
- He, Ne, Ar, Kr, Xe, Rn elementlerini içerir.
- Renksiz ve monoatomik yapıdadırlar.
- Kararlı elektronik yapıya sahip oldukları için bileşik yapmazlar.
- He'nin değerlik elektron sayısı 2, diğerlerininki 8'dir.
İlginç Bilgi: Peroksit (O₂²⁻) bileşiklerinde oksijenin yükseltgenme basamağı -1'dir ve sadece 1A ve 2A grubu elementleri peroksit oluşturabilir. Örneğin Na₂O₂'de oksijen -1 yükseltgenme basamağına sahiptir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Orbital
99. Sınıf atom modelleri yeni müfredat
Ders notu
AYT KİMYA MODERN ATOM TEORİSİ
MODERN ATOM TEORİSİ
11 Kimya
11. sınıf kimya orbitaller Ayt kimya 1. ünite
9 . Sınıf kimya orbitaller
Umarım faydalı olur
Kimya 9. Sınıf ORBİTALLER
Orbital şekilleri, orbitallerin sıralanışı, küresel simetri, anyon ve katyon, orbital kuralları, temel hal ve uyarılmış hal, valans elektron ve orbital konularını içerir.
modern atom teorisi
11. sınıf kimya modern atom teorisi
ayt kimya 1.ünite
modern atom teorisi
9. Sınıf KİMYA
1.1 YAZILI ÖRNEĞİ
Atom Orbitalleri 9.sınıf (TYT)
Orbital nedir ve orbital türleri nelerdir?
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅