Kovalent bağlar, atomların elektronları ortaklaşa kullanarak oluşturduğu kimyasal bağlardır. Ametaller... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
1,239
•
Güncellendi May 10, 2026
•
Zeliha Gül Dernek
@zelihagldernek
Kovalent bağlar, atomların elektronları ortaklaşa kullanarak oluşturduğu kimyasal bağlardır. Ametaller... Daha fazla göster









Ametal atomları birbirleriyle bağ yaparken nasıl davranır? İşte bu sorunun cevabı kovalent bağda gizli!
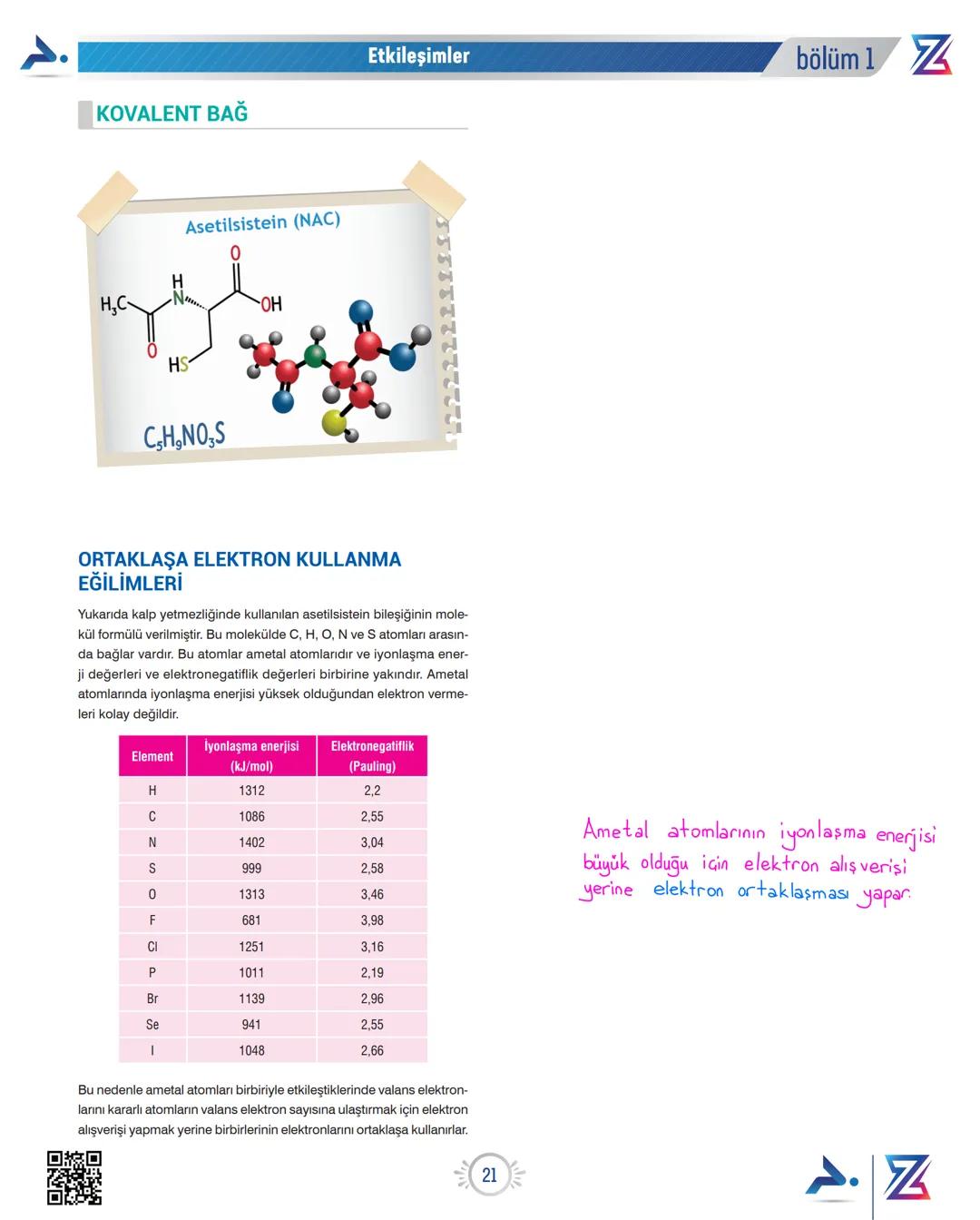
Ametaller (C, H, O, N, S gibi elementler) elektron vermeyi pek sevmezler çünkü yüksek iyonlaşma enerjisi değerlerine sahiptirler. Bu nedenle, birbirleriyle etkileşime girdiklerinde elektron alışverişi yerine elektronlarını ortaklaşa kullanmayı tercih ederler.
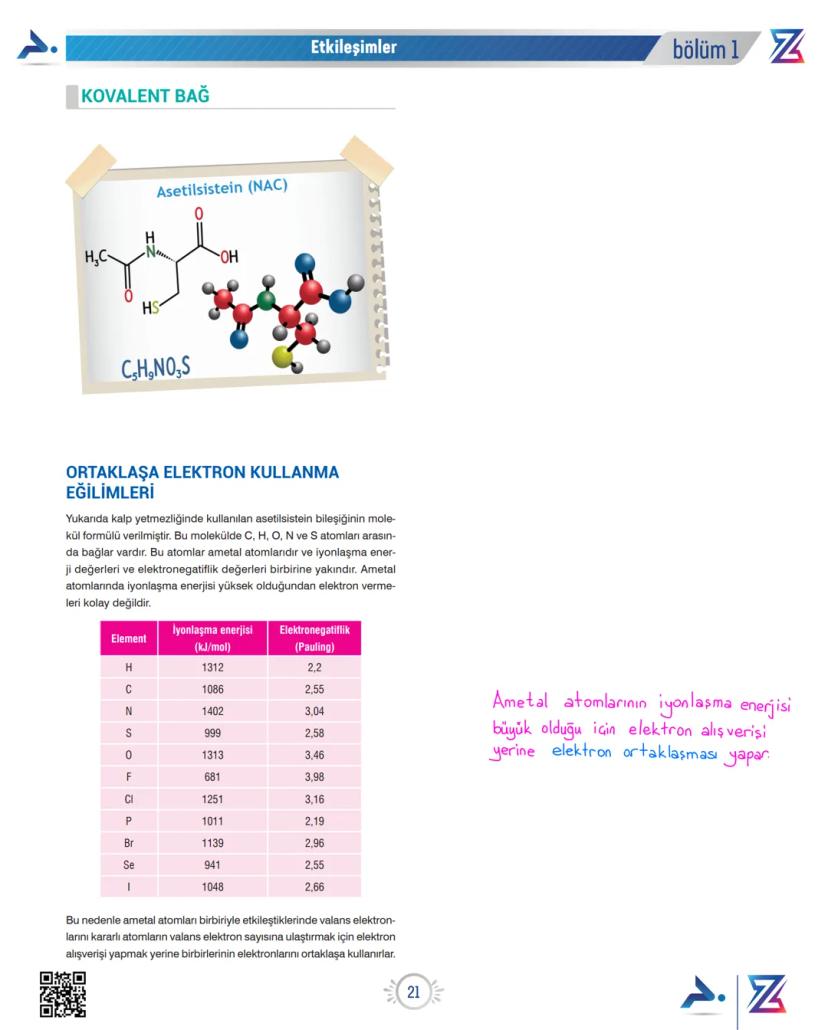
Örneğin kalp yetmezliğinde kullanılan asetilsistein (NAC) molekülünde C, H, O, N ve S atomları arasında kovalent bağlar vardır. Bu elementlerin birbirine yakın elektronegatiflik değerleri, elektronları paylaşarak bağ oluşturmalarını sağlar.
Bunu biliyormuydunuz? Ametal atomları iyonlaşma enerjileri büyük olduğu için elektron alışverişi yapmak yerine elektronları ortaklaşa kullanırlar.
Kovalent bağlarda atomlar, kararlı bir elektron dizilimine ulaşmak için elektronlarını paylaşırlar. Bu paylaşım, hem element moleküllerinde (örneğin H₂) hem de bileşik moleküllerinde (örneğin H₂O) gerçekleşir.

Kovalent bağ, ametaller arasında elektronların ortaklaşa kullanılmasıyla oluşur. Metal atomları ise elektron vererek iyonik bağ yaparlar, hatırlatmakta fayda var!
Aynı tür ametal atomları arasında (H₂, O₂, N₂) veya farklı ametal atomları arasında (H₂O) kovalent bağlar oluşabilir. Elektronların ortaklaşa kullanılmasıyla oluşan bu kimyasal bağ türüne kovalent bağ diyoruz.
Nasıl oluşur bu bağlar? İşte H₂ molekülünün oluşumu örneğinden anlayalım:
H₂ molekülünde ortaklaşa kullanılan elektronlar sürekli hareket halindedir. Elektrostatik çekimler, bu iki hidrojen atomunun bir arada kalmasını sağlar.
Not: Bir kovalent bağ, bir elektron çiftinden oluşur ve atomlar arasındaki mesafeye "bağ uzunluğu" denir.

H₂ molekülündeki kovalent bağda çekirdekler arasındaki itme kuvvetleri ile çekirdek-elektron arasındaki çekme kuvvetleri denge halindedir. Peki bu denge nasıl oluşur?
Bağ oluşumu sırasında üç temel durum görülür:
Kovalent bağ ile bağlanan atomların oluşturduğu taneciklere molekül denir. Örneğin H₂, O₂ gibi element molekülleri veya H₂O, CO₂ gibi bileşik molekülleri.
Önemli! Kovalent bağlı bir molekül, o element veya bileşiğin kimyasal özelliklerine sahip en küçük yapı birimidir.
Kovalent bağda, ortaklaşa kullanılan elektron çiftine bağlayıcı elektron çifti denir. Atomlar arasındaki uzaklık ise bağ uzunluğu olarak adlandırılır.

Kovalent bağlar, bağı oluşturan atomların türüne göre ikiye ayrılır: Apolar ve polar kovalent bağ.
Apolar kovalent bağ, aynı tür ametal atomları arasında oluşan, elektron çiftinin atomlar arasında eşit paylaşıldığı bağlardır. Moleküldeki atomların elektronegatiflik değerleri aynı olduğundan, elektronlara sahip çıkma istekleri de eşittir.
Apolar kovalent bağlarda elektron yük yoğunluğu atomlar üzerine eşit dağıldığı için bir kutuplaşma yoktur ve bu nedenle %100 kovalent bağ olarak kabul edilirler.
H₂, F₂, O₂, N₂ moleküllerindeki atomlar arasında apolar kovalent bağlar vardır. Şimdi bunları inceleyelim:
H₂ Molekülü H atomu tek elektronunu ortaklaşa kullanarak, He atomu gibi 2 elektronlu kararlı yapıya (dublete) ulaşır. H₂ molekülünde:
Hatırlatma: Kovalent bağlarda ortaklaşa kullanılan elektronlara bağlayıcı elektron, ortaklanmış elektron veya eşleşmiş elektron de denir.

F₂ Molekülü
O₂ Molekülü
Kimyada İpucu: Apolar kovalent bağda, elektronlar iki atom arasında eşit paylaşılır. Bu nedenle molekülde elektronların yük dağılımları da dengelidir.
O₂ molekülünde elektronların bulut şeklinde gösteriminde, yük dağılımının her iki oksijen atomunun etrafında simetrik olduğunu görebilirsiniz.
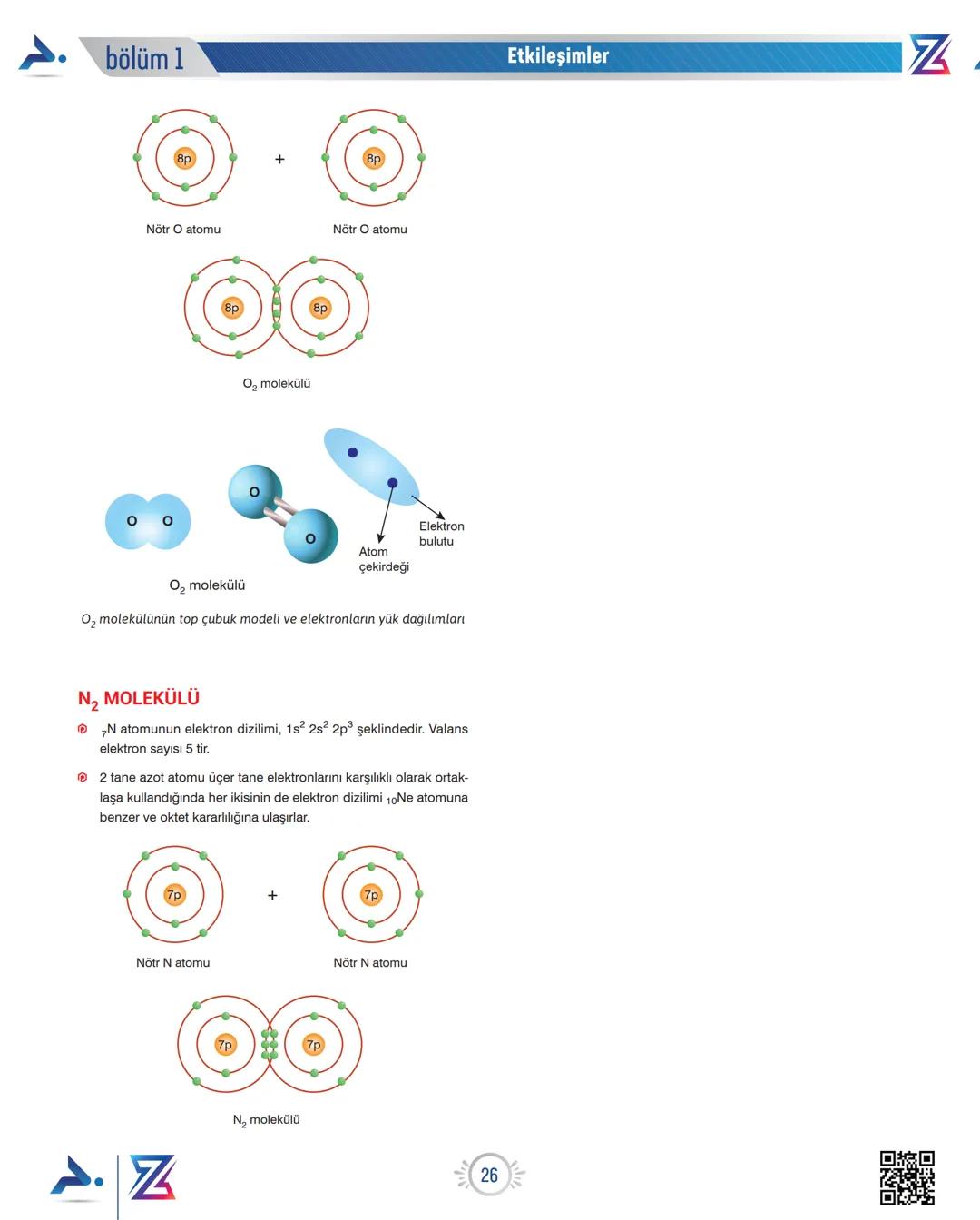
N₂ Molekülü
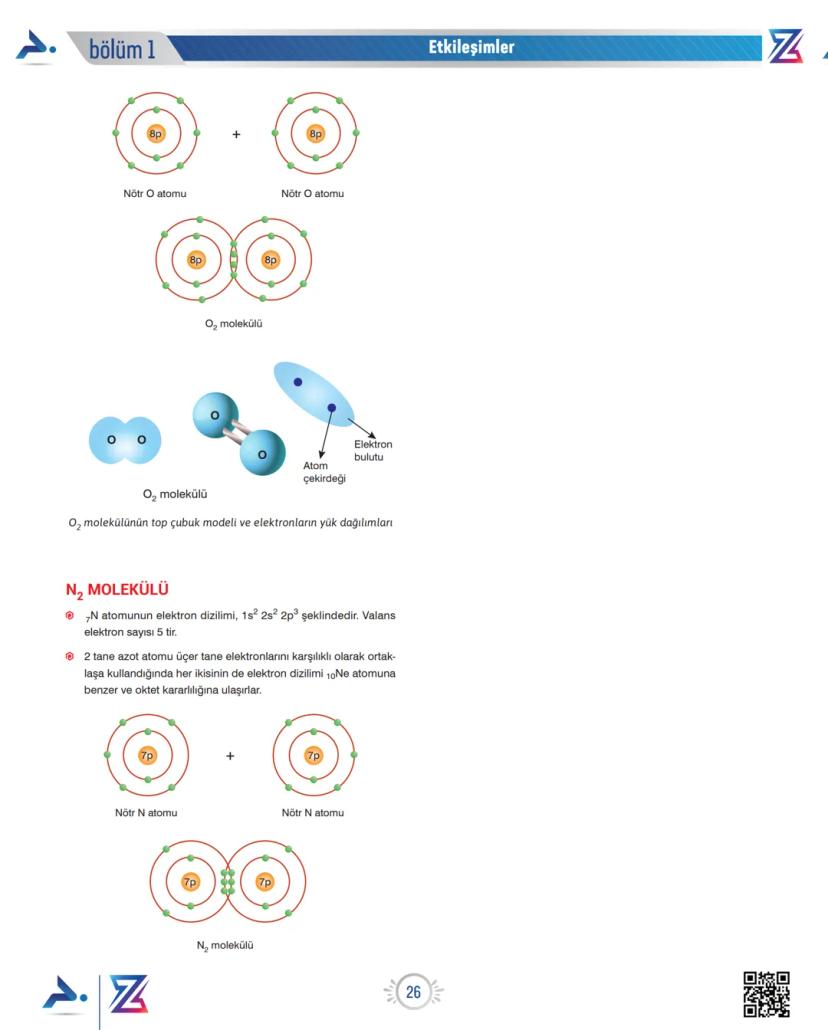
N atomunun elektron dizilimi 1s² 2s² 2p³ şeklindedir ve valans elektron sayısı 5'tir. İki azot atomu üçer elektronlarını ortaklaşa kullandıklarında, her biri oktet kararlılığına ulaşır.
N₂ molekülünde:
Üçlü bağ, molekülün çok kararlı olmasını sağlar ve bu nedenle N₂ gazı oda sıcaklığında oldukça inert (tepkimeye girmez) bir maddedir.
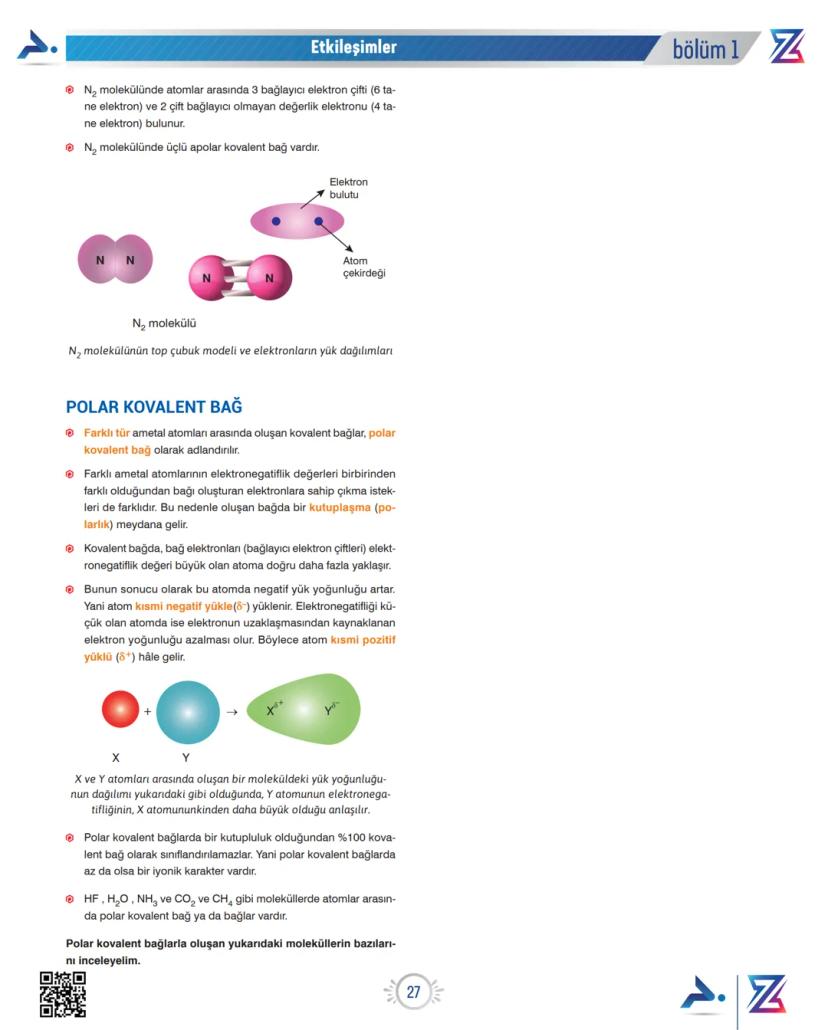
Top-çubuk modelinde N₂ molekülünün gösterimi, iki azot atomu arasında üç çizgi ile gösterilir. Bu üç çizgi, üç elektron çiftinin paylaşıldığını temsil eder.
Elektron bulutu gösteriminde, elektronların her iki azot atomu arasında eşit yoğunlukta dağıldığını görebiliriz - bu apolar bağın özelliğidir.
Önemli Not: Üçlü bağlar, moleküllerin en kuvvetli kovalent bağlarıdır ve koparılmaları zordur. Bu nedenle N₂ molekülü çok kararlıdır.
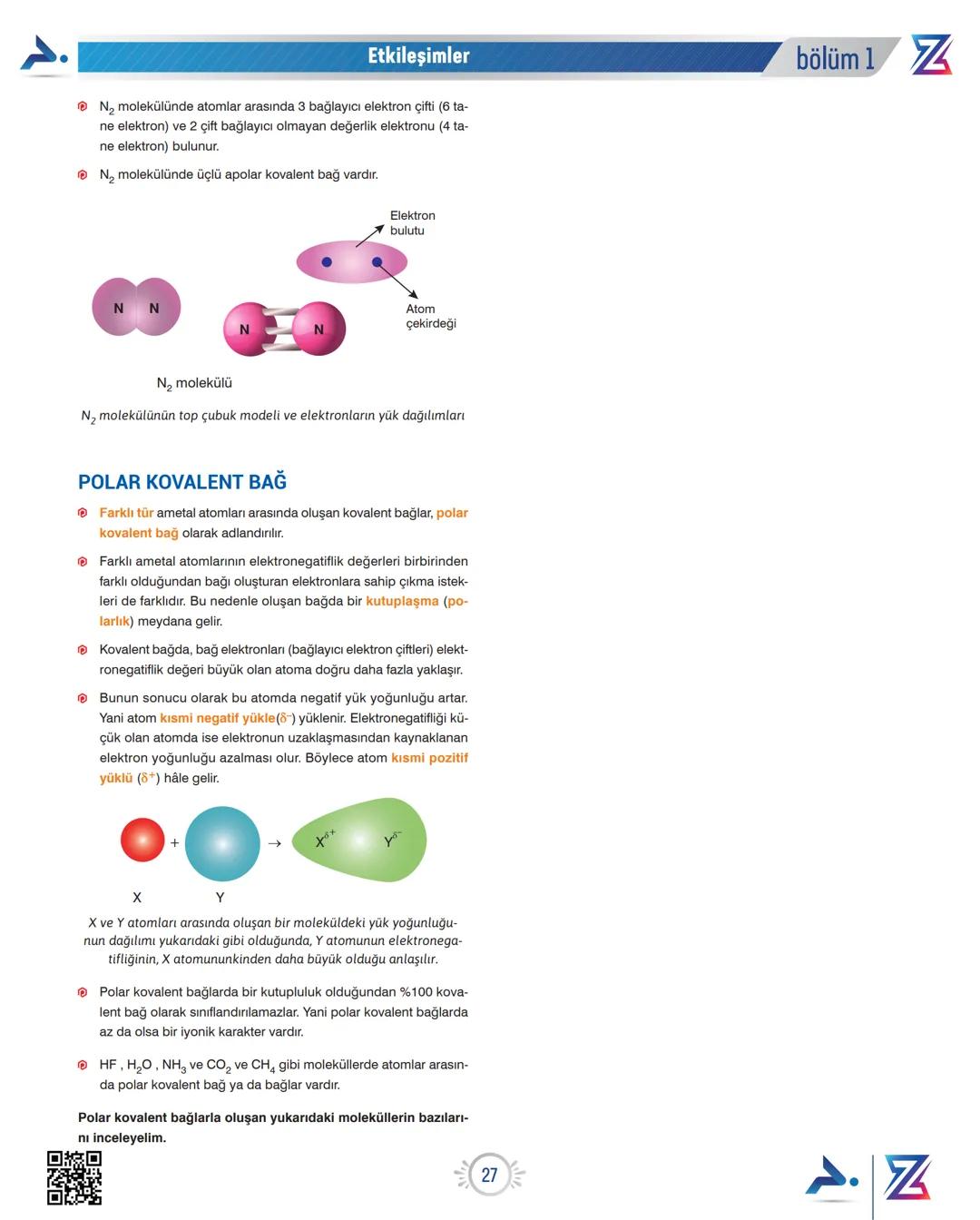
Polar Kovalent Bağ Nedir?
Farklı tür ametal atomları arasında oluşan kovalent bağlara polar kovalent bağ denir. Bu bağlarda, atomların elektronegatiflik değerleri farklı olduğundan, elektronlara sahip çıkma istekleri de farklıdır.
Polar kovalent bağda önemli özellikler:
HF, H₂O, NH₃, CO₂, CH₄ gibi moleküllerde atomlar arasında polar kovalent bağlar bulunur.
Molekülde Kutuplaşma: Eğer bir molekülde X ve Y atomları arasında Y tarafında daha fazla elektron yoğunluğu varsa, Y'nin elektronegatifliği X'ten daha büyüktür.
Polar kovalent bağların iyonik karakteri, atomlar arasındaki elektronegatiflik farkıyla doğru orantılıdır. Fark büyüdükçe, bağın iyonik karakteri artar.

HF Molekülü
H₂O Molekülü
Gerçek Hayat Uygulaması: H₂O'daki polar bağlar, suyun iyi bir çözücü olmasını ve hayatın devamı için gerekli birçok özelliğini sağlar.
Bu polar yapı, su moleküllerinin birbirlerine hidrojen bağlarıyla bağlanmasına olanak tanır, bu da suyun yüksek kaynama noktası ve yüzey gerilimi gibi özelliklerinin sebebidir.

CO₂ Molekülü
NH₃ Molekülü
Bunu Düşündünüz mü? Ortaklaşa kullanılan elektronlar elektronegatif atoma daha yakın olduğu için, elektronegatiflik farkı arttıkça bağın polar karakteri de artar.
Polar kovalent bağlar, moleküllere özel fiziksel ve kimyasal özellikler kazandırır. Örneğin, NH₃'ün polar yapısı, onu iyi bir çözücü ve zayıf bir baz yapar.

Kovalent bağlı maddelerin ortak özellikleri şunlardır:
Moleküler Yapı: Formüllerine karşılık gelen sayıda atom içeren bağımsız birimlerden (moleküllerden) oluşurlar.
Zayıf Moleküller Arası Etkileşimler: Moleküller arasında genellikle zayıf etkileşimler bulunur (iyonik bileşiklerden farklı olarak).
Çeşitli Fiziksel Haller: Oda koşullarında katı , sıvı veya gaz olabilirler.
Elektriksel İletkenlik: Katı ve sıvı halde elektriği iletmezler. Ancak suda iyonlaşabilen HCl ve NH₃ gibi bileşiklerin çözeltileri elektriği iletebilir.
Kimyada Pratik Bilgi: Kovalent bileşiklerin erime ve kaynama noktaları genellikle iyonik bileşiklerden daha düşüktür çünkü moleküller arası zayıf etkileşimleri kırmak, güçlü iyonik çekimleri kırmaktan daha kolaydır.
Bu özellikler, kovalent bağlı moleküllerin davranışlarını anlamak için önemlidir. Örneğin, çoğu biyolojik molekül (proteinler, DNA) kovalent bağlar içerir ve bu bağların özellikleri canlı sistemlerin işleyişinde kritik rol oynar.


Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Zeliha Gül Dernek
@zelihagldernek
Kovalent bağlar, atomların elektronları ortaklaşa kullanarak oluşturduğu kimyasal bağlardır. Ametaller arasında gerçekleşen bu bağlanma, günlük hayatımızda karşılaştığımız pek çok maddenin temelini oluşturur. Bu ders notlarında kovalent bağların oluşumu, türleri ve özellikleri hakkında detaylı bilgi edineceksiniz.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Ametal atomları birbirleriyle bağ yaparken nasıl davranır? İşte bu sorunun cevabı kovalent bağda gizli!
Ametaller (C, H, O, N, S gibi elementler) elektron vermeyi pek sevmezler çünkü yüksek iyonlaşma enerjisi değerlerine sahiptirler. Bu nedenle, birbirleriyle etkileşime girdiklerinde elektron alışverişi yerine elektronlarını ortaklaşa kullanmayı tercih ederler.
Örneğin kalp yetmezliğinde kullanılan asetilsistein (NAC) molekülünde C, H, O, N ve S atomları arasında kovalent bağlar vardır. Bu elementlerin birbirine yakın elektronegatiflik değerleri, elektronları paylaşarak bağ oluşturmalarını sağlar.
Bunu biliyormuydunuz? Ametal atomları iyonlaşma enerjileri büyük olduğu için elektron alışverişi yapmak yerine elektronları ortaklaşa kullanırlar.
Kovalent bağlarda atomlar, kararlı bir elektron dizilimine ulaşmak için elektronlarını paylaşırlar. Bu paylaşım, hem element moleküllerinde (örneğin H₂) hem de bileşik moleküllerinde (örneğin H₂O) gerçekleşir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kovalent bağ, ametaller arasında elektronların ortaklaşa kullanılmasıyla oluşur. Metal atomları ise elektron vererek iyonik bağ yaparlar, hatırlatmakta fayda var!
Aynı tür ametal atomları arasında (H₂, O₂, N₂) veya farklı ametal atomları arasında (H₂O) kovalent bağlar oluşabilir. Elektronların ortaklaşa kullanılmasıyla oluşan bu kimyasal bağ türüne kovalent bağ diyoruz.
Nasıl oluşur bu bağlar? İşte H₂ molekülünün oluşumu örneğinden anlayalım:
H₂ molekülünde ortaklaşa kullanılan elektronlar sürekli hareket halindedir. Elektrostatik çekimler, bu iki hidrojen atomunun bir arada kalmasını sağlar.
Not: Bir kovalent bağ, bir elektron çiftinden oluşur ve atomlar arasındaki mesafeye "bağ uzunluğu" denir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
H₂ molekülündeki kovalent bağda çekirdekler arasındaki itme kuvvetleri ile çekirdek-elektron arasındaki çekme kuvvetleri denge halindedir. Peki bu denge nasıl oluşur?
Bağ oluşumu sırasında üç temel durum görülür:
Kovalent bağ ile bağlanan atomların oluşturduğu taneciklere molekül denir. Örneğin H₂, O₂ gibi element molekülleri veya H₂O, CO₂ gibi bileşik molekülleri.
Önemli! Kovalent bağlı bir molekül, o element veya bileşiğin kimyasal özelliklerine sahip en küçük yapı birimidir.
Kovalent bağda, ortaklaşa kullanılan elektron çiftine bağlayıcı elektron çifti denir. Atomlar arasındaki uzaklık ise bağ uzunluğu olarak adlandırılır.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kovalent bağlar, bağı oluşturan atomların türüne göre ikiye ayrılır: Apolar ve polar kovalent bağ.
Apolar kovalent bağ, aynı tür ametal atomları arasında oluşan, elektron çiftinin atomlar arasında eşit paylaşıldığı bağlardır. Moleküldeki atomların elektronegatiflik değerleri aynı olduğundan, elektronlara sahip çıkma istekleri de eşittir.
Apolar kovalent bağlarda elektron yük yoğunluğu atomlar üzerine eşit dağıldığı için bir kutuplaşma yoktur ve bu nedenle %100 kovalent bağ olarak kabul edilirler.
H₂, F₂, O₂, N₂ moleküllerindeki atomlar arasında apolar kovalent bağlar vardır. Şimdi bunları inceleyelim:
H₂ Molekülü H atomu tek elektronunu ortaklaşa kullanarak, He atomu gibi 2 elektronlu kararlı yapıya (dublete) ulaşır. H₂ molekülünde:
Hatırlatma: Kovalent bağlarda ortaklaşa kullanılan elektronlara bağlayıcı elektron, ortaklanmış elektron veya eşleşmiş elektron de denir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
F₂ Molekülü
O₂ Molekülü
Kimyada İpucu: Apolar kovalent bağda, elektronlar iki atom arasında eşit paylaşılır. Bu nedenle molekülde elektronların yük dağılımları da dengelidir.
O₂ molekülünde elektronların bulut şeklinde gösteriminde, yük dağılımının her iki oksijen atomunun etrafında simetrik olduğunu görebilirsiniz.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
N₂ Molekülü
N atomunun elektron dizilimi 1s² 2s² 2p³ şeklindedir ve valans elektron sayısı 5'tir. İki azot atomu üçer elektronlarını ortaklaşa kullandıklarında, her biri oktet kararlılığına ulaşır.
N₂ molekülünde:
Üçlü bağ, molekülün çok kararlı olmasını sağlar ve bu nedenle N₂ gazı oda sıcaklığında oldukça inert (tepkimeye girmez) bir maddedir.
Top-çubuk modelinde N₂ molekülünün gösterimi, iki azot atomu arasında üç çizgi ile gösterilir. Bu üç çizgi, üç elektron çiftinin paylaşıldığını temsil eder.
Elektron bulutu gösteriminde, elektronların her iki azot atomu arasında eşit yoğunlukta dağıldığını görebiliriz - bu apolar bağın özelliğidir.
Önemli Not: Üçlü bağlar, moleküllerin en kuvvetli kovalent bağlarıdır ve koparılmaları zordur. Bu nedenle N₂ molekülü çok kararlıdır.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Polar Kovalent Bağ Nedir?
Farklı tür ametal atomları arasında oluşan kovalent bağlara polar kovalent bağ denir. Bu bağlarda, atomların elektronegatiflik değerleri farklı olduğundan, elektronlara sahip çıkma istekleri de farklıdır.
Polar kovalent bağda önemli özellikler:
HF, H₂O, NH₃, CO₂, CH₄ gibi moleküllerde atomlar arasında polar kovalent bağlar bulunur.
Molekülde Kutuplaşma: Eğer bir molekülde X ve Y atomları arasında Y tarafında daha fazla elektron yoğunluğu varsa, Y'nin elektronegatifliği X'ten daha büyüktür.
Polar kovalent bağların iyonik karakteri, atomlar arasındaki elektronegatiflik farkıyla doğru orantılıdır. Fark büyüdükçe, bağın iyonik karakteri artar.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
HF Molekülü
H₂O Molekülü
Gerçek Hayat Uygulaması: H₂O'daki polar bağlar, suyun iyi bir çözücü olmasını ve hayatın devamı için gerekli birçok özelliğini sağlar.
Bu polar yapı, su moleküllerinin birbirlerine hidrojen bağlarıyla bağlanmasına olanak tanır, bu da suyun yüksek kaynama noktası ve yüzey gerilimi gibi özelliklerinin sebebidir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
CO₂ Molekülü
NH₃ Molekülü
Bunu Düşündünüz mü? Ortaklaşa kullanılan elektronlar elektronegatif atoma daha yakın olduğu için, elektronegatiflik farkı arttıkça bağın polar karakteri de artar.
Polar kovalent bağlar, moleküllere özel fiziksel ve kimyasal özellikler kazandırır. Örneğin, NH₃'ün polar yapısı, onu iyi bir çözücü ve zayıf bir baz yapar.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kovalent bağlı maddelerin ortak özellikleri şunlardır:
Moleküler Yapı: Formüllerine karşılık gelen sayıda atom içeren bağımsız birimlerden (moleküllerden) oluşurlar.
Zayıf Moleküller Arası Etkileşimler: Moleküller arasında genellikle zayıf etkileşimler bulunur (iyonik bileşiklerden farklı olarak).
Çeşitli Fiziksel Haller: Oda koşullarında katı , sıvı veya gaz olabilirler.
Elektriksel İletkenlik: Katı ve sıvı halde elektriği iletmezler. Ancak suda iyonlaşabilen HCl ve NH₃ gibi bileşiklerin çözeltileri elektriği iletebilir.
Kimyada Pratik Bilgi: Kovalent bileşiklerin erime ve kaynama noktaları genellikle iyonik bileşiklerden daha düşüktür çünkü moleküller arası zayıf etkileşimleri kırmak, güçlü iyonik çekimleri kırmaktan daha kolaydır.
Bu özellikler, kovalent bağlı moleküllerin davranışlarını anlamak için önemlidir. Örneğin, çoğu biyolojik molekül (proteinler, DNA) kovalent bağlar içerir ve bu bağların özellikleri canlı sistemlerin işleyişinde kritik rol oynar.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
10
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı