Modern Atom Teorisi, elektronların atom içindeki davranışlarını ve yerleşimlerini açıklayan... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
358
•
Güncellendi May 22, 2026
•
Senaa
@senaa_07
Modern Atom Teorisi, elektronların atom içindeki davranışlarını ve yerleşimlerini açıklayan... Daha fazla göster


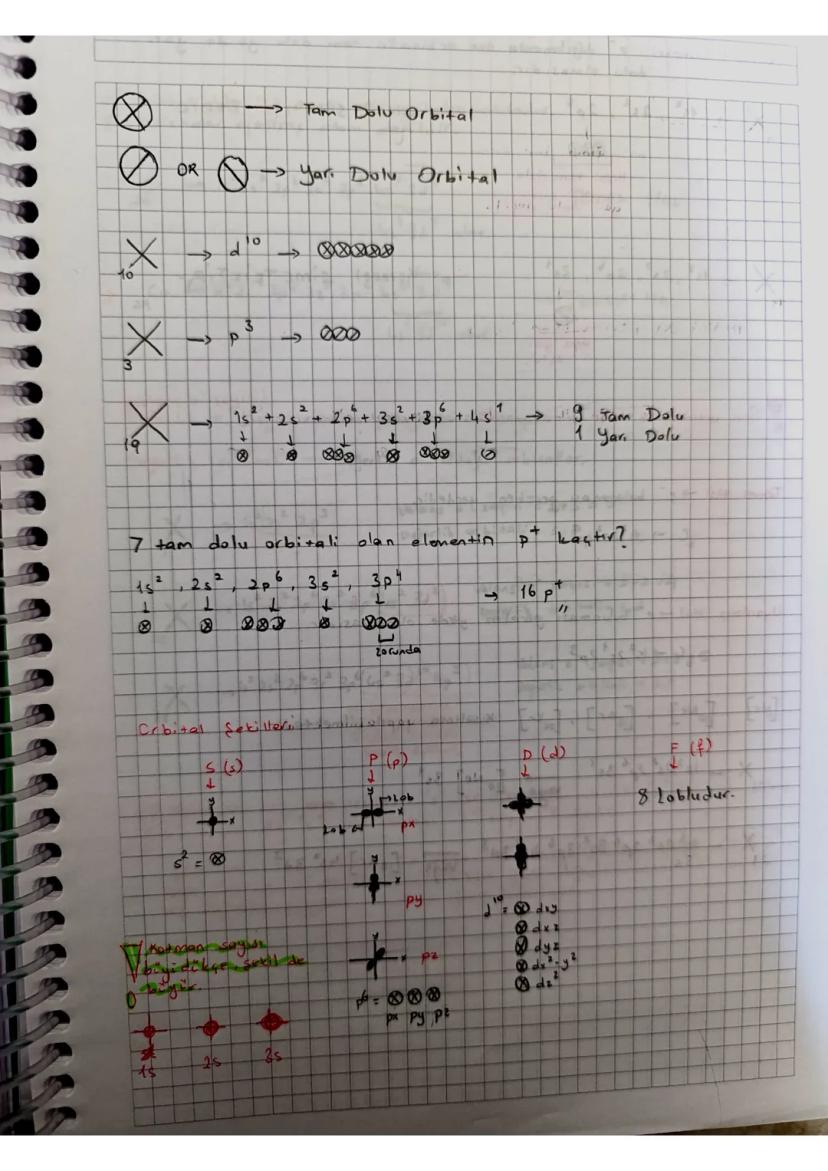



Modern atom teorisinde elektronların konumları tam olarak belirlenemez, sadece yoğun bulundukları bölgeler tespit edilebilir. Bu bölgelere elektron bulutu ya da orbital denir. Ervin Schrödinger tarafından geliştirilen bu model, elektronların davranışlarını dalga fonksiyonlarıyla açıklar.
Orbitaller dört çeşittir: s, p, d ve f. Her periyotta farklı orbitaller bulunur. 1. periyotta sadece s orbitali, 2. periyotta s ve p orbitali, 3. periyotta s, p ve d orbitali bulunabilir. 4. periyot ve sonrasında tüm orbital çeşitleri (s, p, d ve f) olabilir.
Her orbital türünün elektron kapasitesi farklıdır: s orbitali 2 elektron, p orbitali 6 elektron (3 orbital x 2 elektron), d orbitali 10 elektron (5 orbital x 2 elektron) ve f orbitali 14 elektron (7 orbital x 2 elektron) alabilir.
Hatırlatma: Orbitaller şema üzerinde kutu (□) şeklinde gösterilir ve içlerine elektronlar yerleştirilirken yukarı (↑) veya aşağı (↓) oklar kullanılır.

Pauli Kuralı: Bir orbitale en fazla zıt spinli iki elektron yerleştirilebilir (↑↓). Okların yönü zıt olduğu sürece yukarı veya aşağı bakmasının önemi yoktur. Bu kuralla her orbital türünün toplam kapasite hesabı yapılır: s→2e-, p→6e-, d→10e-, f→14e-.
Hund Kuralı: Aynı enerji düzeyindeki orbitallere elektronlar önce tek tek yerleştirilir. Örneğin, p² için doğru gösterim (↑)(↑)(□) şeklindedir, (↑↓)(□)(□) şeklinde değildir. Elektronlar paralel spinle (aynı yönde) yerleştirilir.
Aufbau Kuralı: Elektronlar orbitallere en düşük enerjiden en yüksek enerjiye doğru yerleştirilir. Enerji düzeyi sıralaması şöyledir: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f...
Önemli Not: "Yüksek katmandaki elektronun enerjisi daha yüksektir" ifadesi YANLIŞTIR! Enerji sıralaması katman sayısı ve orbital türüne göre değişir.
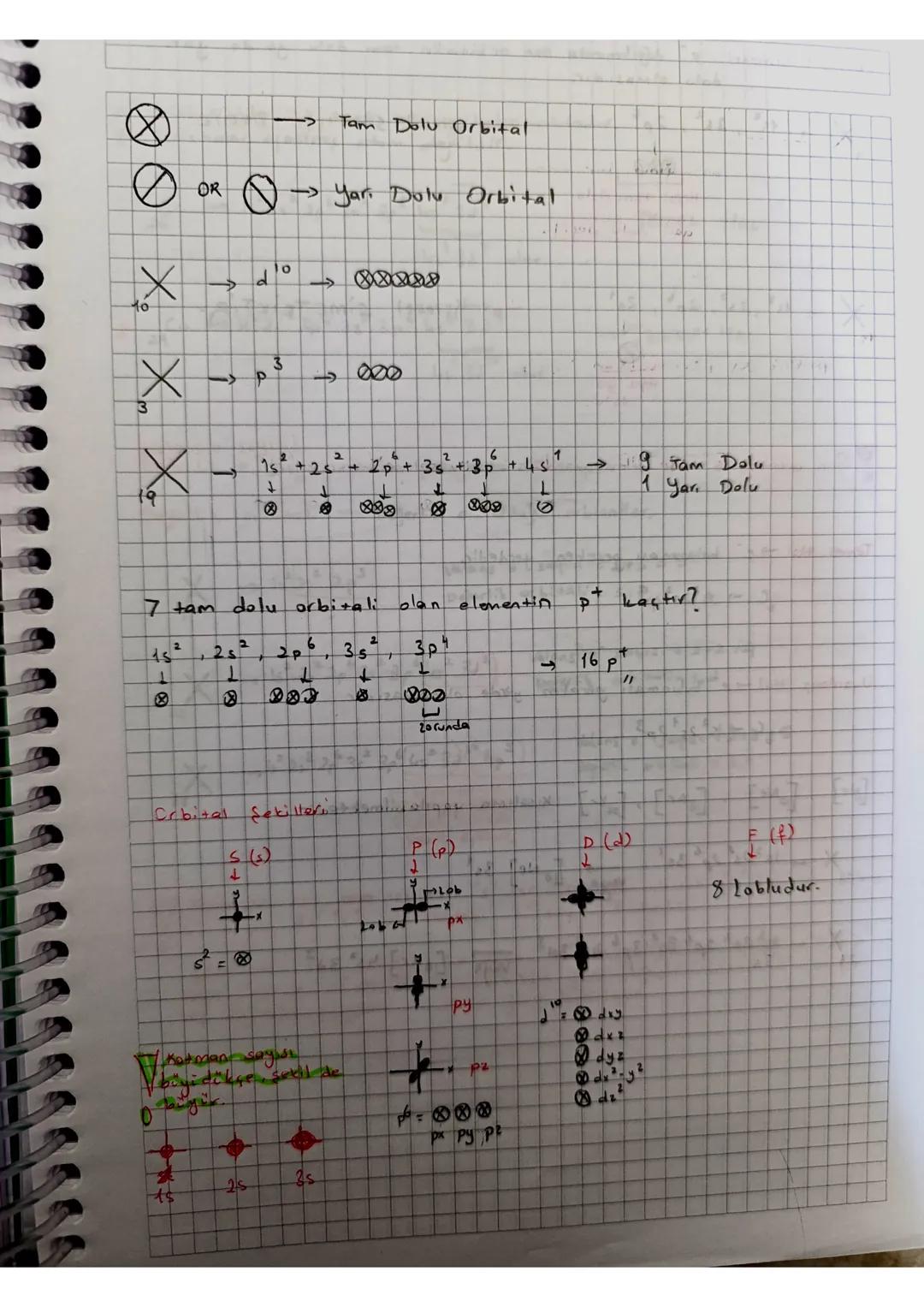
Orbitaller doluluk durumuna göre tam dolu orbital (↑↓) veya yarı dolu orbital (↑) olarak adlandırılır. Örneğin 1s² + 2s² + 2p⁶ + 3s² + 3p⁶ + 4s¹ gösteriminde 9 tam dolu ve 1 yarı dolu orbital bulunur.
Orbitallerin şekilleri de birbirinden farklıdır. s orbitali küreseldir ve tek lobludur. p orbitalleri (px, py, pz) çift lobludur ve x, y, z eksenlerinde uzanır. d orbitalleri daha karmaşık yapıdadır ve 4 lobludur.
Katman sayısı büyüdükçe orbitallerin boyutu da artar. Yani 3s orbitali, 2s orbitalinden daha büyüktür. Bu, elektronların çekirdekten daha uzakta bulunabildiğini gösterir.
İpucu: Orbital hesaplamalarında zorlanıyorsanız, önce orbital türüne göre maksimum elektron sayısını hatırlayın: s→2, p→6, d→10, f→14. Sonra dolu orbitalleri sayın.

Küresel simetri, elektron dağılımında son orbitalin tam dolu veya yarı dolu olması durumudur. Örneğin 1s², 2s², 2p⁶, 3s¹ diziliminde son orbital (3s¹) yarı dolu olduğu için küresel simetriktir. Eğer son orbital "s" ise, element her zaman küresel simetriktir.
Elektronlar temel halde bulunması gereken yerdedir. Uyarılmış halde ise elektron bulunması gereken yerde değildir. Örneğin karbon elementinin temel hali 1s² 2s² 2p² iken, uyarılmış hali 1s² 2s¹ 2p³ olabilir.
Elektron dizilimini yazarken soygaz kısaltmaları kullanılabilir. Örneğin [He] 2s² 2p² veya [Ne] 3s² gibi. Bu, yazmayı kolaylaştırır ve özellikle büyük atomlarda pratiktir.
Dikkat: Elektron dağılımında kısaltma kullanırken hangi soygazı kullandığınızı ve sonrasında hangi orbitallerin geldiğini doğru belirleyin!

Elektron dağılımında iki önemli istisna bulunur: Krom (Cr) ve Bakır (Cu). Bu elementlerde 4s ve 3d arasında elektron kayması olur. Krom için 4s¹ 3d⁵, bakır için 4s¹ 3d¹⁰ dizilimi görülür. Bu istisnalar uyarılmış hal değil, temel haldir!
Değerlik elektronları, son yörüngedeki elektronlardır ve elementin kimyasal özelliklerini belirler. Değerlik orbital türü, son katmandaki orbital türüne bağlıdır. Örneğin 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d³ diziliminde, son katmanda s ve d orbitalleri vardır, değerlik elektron sayısı 2+3=5'tir.
Değerlik orbitali belirlenirken dikkat edilmesi gereken nokta, son katmanda hangi orbital türlerinin bulunduğudur. Eğer son orbital "s" ise, değerlik orbitali "s" ve değerlik elektron sayısı da bu orbitaldeki elektron sayısıdır. Son orbital "p" veya "d" ise, değerlik orbitalleri "s ve p" veya "s ve d" şeklindedir.
Püf Nokta: Değerlik elektronlarını belirlerken önce periyodik tablodaki yerini düşünün, sonra elektron dizilimini inceleyerek son katmandaki orbital türlerini ve elektron sayılarını toplayın.
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Senaa
@senaa_07
Modern Atom Teorisi, elektronların atom içindeki davranışlarını ve yerleşimlerini açıklayan önemli bir konudur. Bu teori, elektronların belirli kurallara göre orbitallere nasıl yerleştiğini ve atomların özelliklerini nasıl etkilediğini anlatır.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Modern atom teorisinde elektronların konumları tam olarak belirlenemez, sadece yoğun bulundukları bölgeler tespit edilebilir. Bu bölgelere elektron bulutu ya da orbital denir. Ervin Schrödinger tarafından geliştirilen bu model, elektronların davranışlarını dalga fonksiyonlarıyla açıklar.
Orbitaller dört çeşittir: s, p, d ve f. Her periyotta farklı orbitaller bulunur. 1. periyotta sadece s orbitali, 2. periyotta s ve p orbitali, 3. periyotta s, p ve d orbitali bulunabilir. 4. periyot ve sonrasında tüm orbital çeşitleri (s, p, d ve f) olabilir.
Her orbital türünün elektron kapasitesi farklıdır: s orbitali 2 elektron, p orbitali 6 elektron (3 orbital x 2 elektron), d orbitali 10 elektron (5 orbital x 2 elektron) ve f orbitali 14 elektron (7 orbital x 2 elektron) alabilir.
Hatırlatma: Orbitaller şema üzerinde kutu (□) şeklinde gösterilir ve içlerine elektronlar yerleştirilirken yukarı (↑) veya aşağı (↓) oklar kullanılır.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Pauli Kuralı: Bir orbitale en fazla zıt spinli iki elektron yerleştirilebilir (↑↓). Okların yönü zıt olduğu sürece yukarı veya aşağı bakmasının önemi yoktur. Bu kuralla her orbital türünün toplam kapasite hesabı yapılır: s→2e-, p→6e-, d→10e-, f→14e-.
Hund Kuralı: Aynı enerji düzeyindeki orbitallere elektronlar önce tek tek yerleştirilir. Örneğin, p² için doğru gösterim (↑)(↑)(□) şeklindedir, (↑↓)(□)(□) şeklinde değildir. Elektronlar paralel spinle (aynı yönde) yerleştirilir.
Aufbau Kuralı: Elektronlar orbitallere en düşük enerjiden en yüksek enerjiye doğru yerleştirilir. Enerji düzeyi sıralaması şöyledir: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f...
Önemli Not: "Yüksek katmandaki elektronun enerjisi daha yüksektir" ifadesi YANLIŞTIR! Enerji sıralaması katman sayısı ve orbital türüne göre değişir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Orbitaller doluluk durumuna göre tam dolu orbital (↑↓) veya yarı dolu orbital (↑) olarak adlandırılır. Örneğin 1s² + 2s² + 2p⁶ + 3s² + 3p⁶ + 4s¹ gösteriminde 9 tam dolu ve 1 yarı dolu orbital bulunur.
Orbitallerin şekilleri de birbirinden farklıdır. s orbitali küreseldir ve tek lobludur. p orbitalleri (px, py, pz) çift lobludur ve x, y, z eksenlerinde uzanır. d orbitalleri daha karmaşık yapıdadır ve 4 lobludur.
Katman sayısı büyüdükçe orbitallerin boyutu da artar. Yani 3s orbitali, 2s orbitalinden daha büyüktür. Bu, elektronların çekirdekten daha uzakta bulunabildiğini gösterir.
İpucu: Orbital hesaplamalarında zorlanıyorsanız, önce orbital türüne göre maksimum elektron sayısını hatırlayın: s→2, p→6, d→10, f→14. Sonra dolu orbitalleri sayın.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Küresel simetri, elektron dağılımında son orbitalin tam dolu veya yarı dolu olması durumudur. Örneğin 1s², 2s², 2p⁶, 3s¹ diziliminde son orbital (3s¹) yarı dolu olduğu için küresel simetriktir. Eğer son orbital "s" ise, element her zaman küresel simetriktir.
Elektronlar temel halde bulunması gereken yerdedir. Uyarılmış halde ise elektron bulunması gereken yerde değildir. Örneğin karbon elementinin temel hali 1s² 2s² 2p² iken, uyarılmış hali 1s² 2s¹ 2p³ olabilir.
Elektron dizilimini yazarken soygaz kısaltmaları kullanılabilir. Örneğin [He] 2s² 2p² veya [Ne] 3s² gibi. Bu, yazmayı kolaylaştırır ve özellikle büyük atomlarda pratiktir.
Dikkat: Elektron dağılımında kısaltma kullanırken hangi soygazı kullandığınızı ve sonrasında hangi orbitallerin geldiğini doğru belirleyin!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Elektron dağılımında iki önemli istisna bulunur: Krom (Cr) ve Bakır (Cu). Bu elementlerde 4s ve 3d arasında elektron kayması olur. Krom için 4s¹ 3d⁵, bakır için 4s¹ 3d¹⁰ dizilimi görülür. Bu istisnalar uyarılmış hal değil, temel haldir!
Değerlik elektronları, son yörüngedeki elektronlardır ve elementin kimyasal özelliklerini belirler. Değerlik orbital türü, son katmandaki orbital türüne bağlıdır. Örneğin 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d³ diziliminde, son katmanda s ve d orbitalleri vardır, değerlik elektron sayısı 2+3=5'tir.
Değerlik orbitali belirlenirken dikkat edilmesi gereken nokta, son katmanda hangi orbital türlerinin bulunduğudur. Eğer son orbital "s" ise, değerlik orbitali "s" ve değerlik elektron sayısı da bu orbitaldeki elektron sayısıdır. Son orbital "p" veya "d" ise, değerlik orbitalleri "s ve p" veya "s ve d" şeklindedir.
Püf Nokta: Değerlik elektronlarını belirlerken önce periyodik tablodaki yerini düşünün, sonra elektron dizilimini inceleyerek son katmandaki orbital türlerini ve elektron sayılarını toplayın.
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
2
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı