Elektrokimya, elektronların hareketinin kimyasal tepkimelerde nasıl rol oynadığını inceleyen konudur.... Daha fazla göster
Elektrokimya: Kolay ve Detaylı Anlatım






























Elektrokimya ve Değerlik Kuralları
Elektrokimya dünyasına girmeden önce değerlik hesaplama kurallarını bilmen gerekiyor. Bu kurallar sayesinde kimyasal formüllerdeki elementlerin yüklerini kolayca bulabilirsin.
Alkali metaller (Li, Na, K, Rb, Cs, Fr) her zaman +1, toprak alkali metaller (Be, Mg, Ca, Sr, Ba, Ra) ise her zaman +2 değerlik alır. Bu metaller bileşiklerinde hiç değişmez!
Hidrojen metallerde -1 (NaH gibi), ametallerde +1 (HCl gibi) değerlik alır. Oksijen genellikle -2'dir ama peroksitlerde (H₂O₂) -1, süperoksitlerde -1/2 değerlik alabilir.
💡 Önemli Not: Serbest haldeki tüm elementlerin değerliği sıfırdır (O₂, N₂, Fe gibi).

Değerlik ve Kimyasal Kökler
Halojenler (F, Cl, Br, I) metallerde daima -1 değerlik alır. Ametallerde ise duruma göre farklı değerlikler gösterebilir.
Kimyasal kökler özellikle önemli! -1'lik kökler: OH⁻ (hidroksit), NO₃⁻ (nitrat), CN⁻ (siyanür). -2'lik kökler: SO₄²⁻ (sülfat), CO₃²⁻ (karbonat), CrO₄²⁻ (kromat). -3'lük kök: PO₄³⁻ (fosfat).
Değerlik hesaplarken a.c + b.d = m formülünü kullan. Burada a ve b atom sayıları, c ve d değerlikler, m ise toplam yüktür.
⚡ Pratik İpucu: NH₄⁺ (amonyum) tek +1'lik katyondur, onu hep hatırla!

Redoks Tepkimeleri
Redoks tepkimeleri elektron alış-verişi ile gerçekleşir. Bir tepkimede elementlerden birinin değerliği değişiyorsa o tepkime redokstur.
Yanma tepkimeleri redokstur çünkü değerlikler değişir. Ama asit-baz tepkimeleri redoks değildir.
Metal-asit tepkimelerinde H₂ gazı çıkıyorsa mutlaka redokstur. Çünkü H⁺'dan H₂'ye geçiş oluyor.
🔬 Test İpucu: Tepkimede serbest element varsa kesinlikle redokstur!

İndirgenme ve Yükseltgenme
İndirgenme: Elektron alarak değerliğin azalması. N + 3e⁻ → N³⁻ gibi. Elektron alan indirgenir!
Yükseltgenme: Elektron vererek değerliğin artması. Fe → 2e⁻ + Fe²⁺ gibi. Elektron veren yükseltgenir!
Bu kavramları karıştırma! Elektron alan indirgenir ama yükseltgendir. Elektron veren yükseltgenir ama indirgendir. Bu tanımlar önemli çünkü sınavda sıkça soruluyor.
🎯 Akılda Kalıcı: "İndirgen elektron verir, yükseltgen elektron alır" diye hatırla!

Redoks Denklemlerini Denkleştirme
Redoks denklemlerini denkleştirmek için sistematik bir yöntem kullan. Önce değerlikleri bul, sonra değişen elementleri tespit et.
Alınan ve verilen elektron sayılarını eşitle. C + HNO₃ → CO₂ + NO₂ örneğinde: C → C⁴⁺ + 4e⁻ ve N⁵⁺ + e⁻ → N⁴⁺ tepkimeleri oluyor.
Son adımda H ve O atomlarını denkleştir. Bu method her zaman işe yarar ve sınavda zaman kazandırır.
📝 Sınav Taktiği: Önce elektron sayılarını eşitle, sonra diğer atomlara bak!

Aktiflik Kavramı
Aktiflik elementlerin bileşik yapma isteğidir. Metaller elektron vererek, ametaller elektron alarak aktiflik gösterir.
Metallerde aktiflik = elektron verme eğilimi. Aktif metal pasif metali açığa çıkarır. Mg + CuCl₂ → MgCl₂ + Cu tepkimesinde Mg, Cu'dan daha aktiftir.
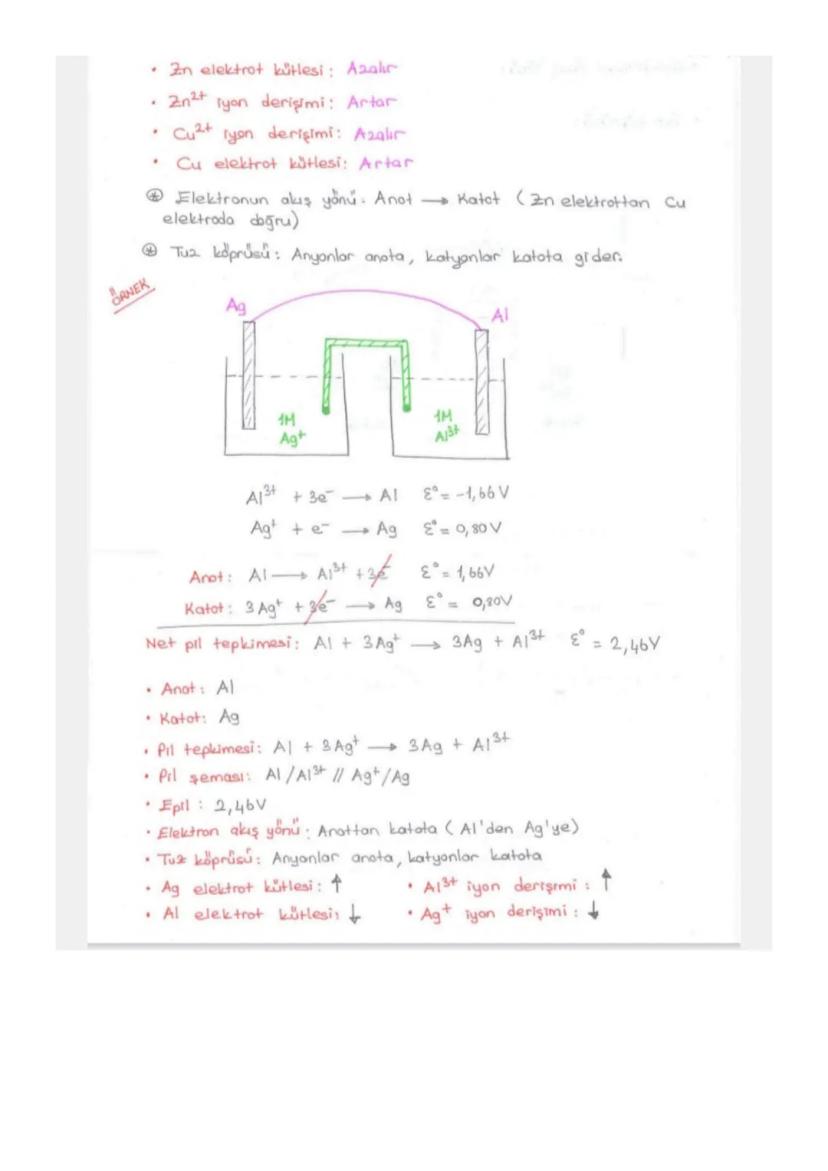
Tepkimelerden aktiflik sırasını bulabilirsin. X + Y²⁺ → X²⁺ + Y tepkimesi kendiliğinden oluyorsa X > Y'dir.
⚡ Önemli: Aktif metal = kolay aşınan metal = kolay yükseltgenen metal!
Aktiflik Karşılaştırmaları
Aktiflik sorularında hangi tepkimelerin kendiliğinden olacağını belirlemelisin. Aktif element pasifi açığa çıkarır kuralını kullan.
Metal çubuk sorularında aktif olan çubuk aşınır. Çözeltide kendi iyonu varsa çubuk aşınmaz.
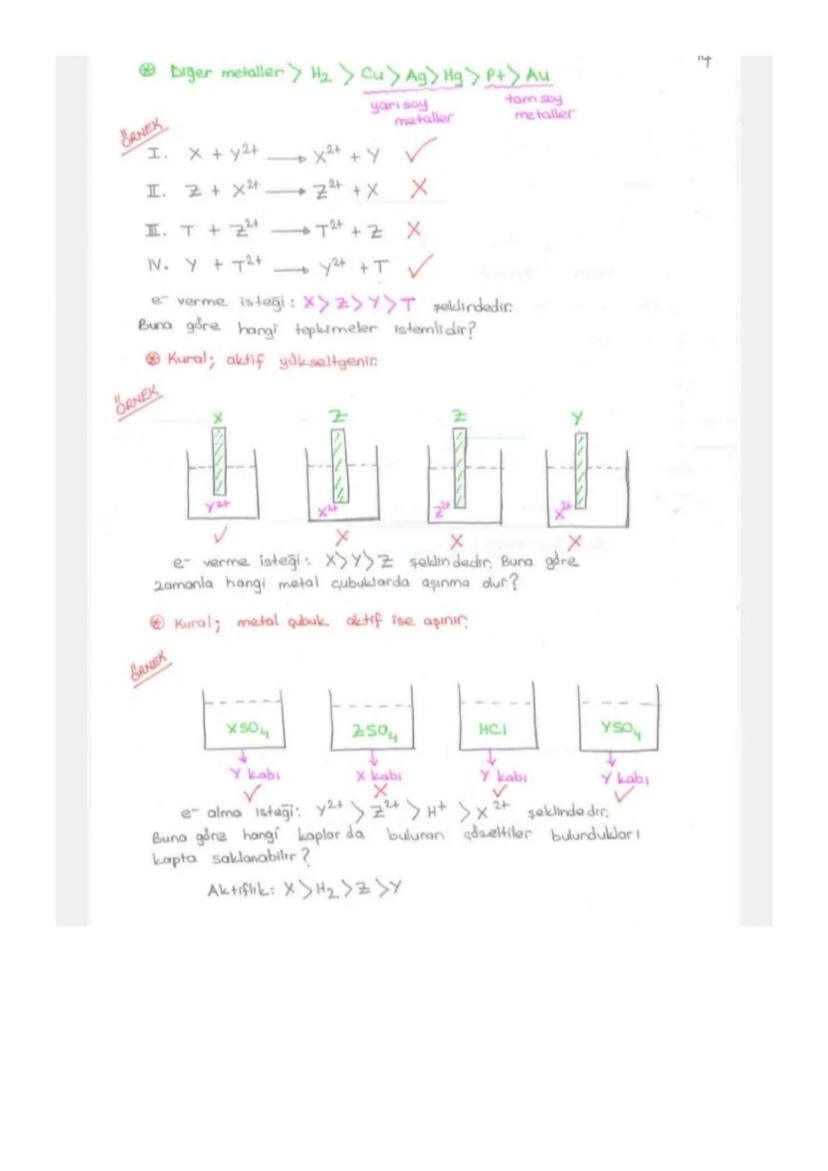
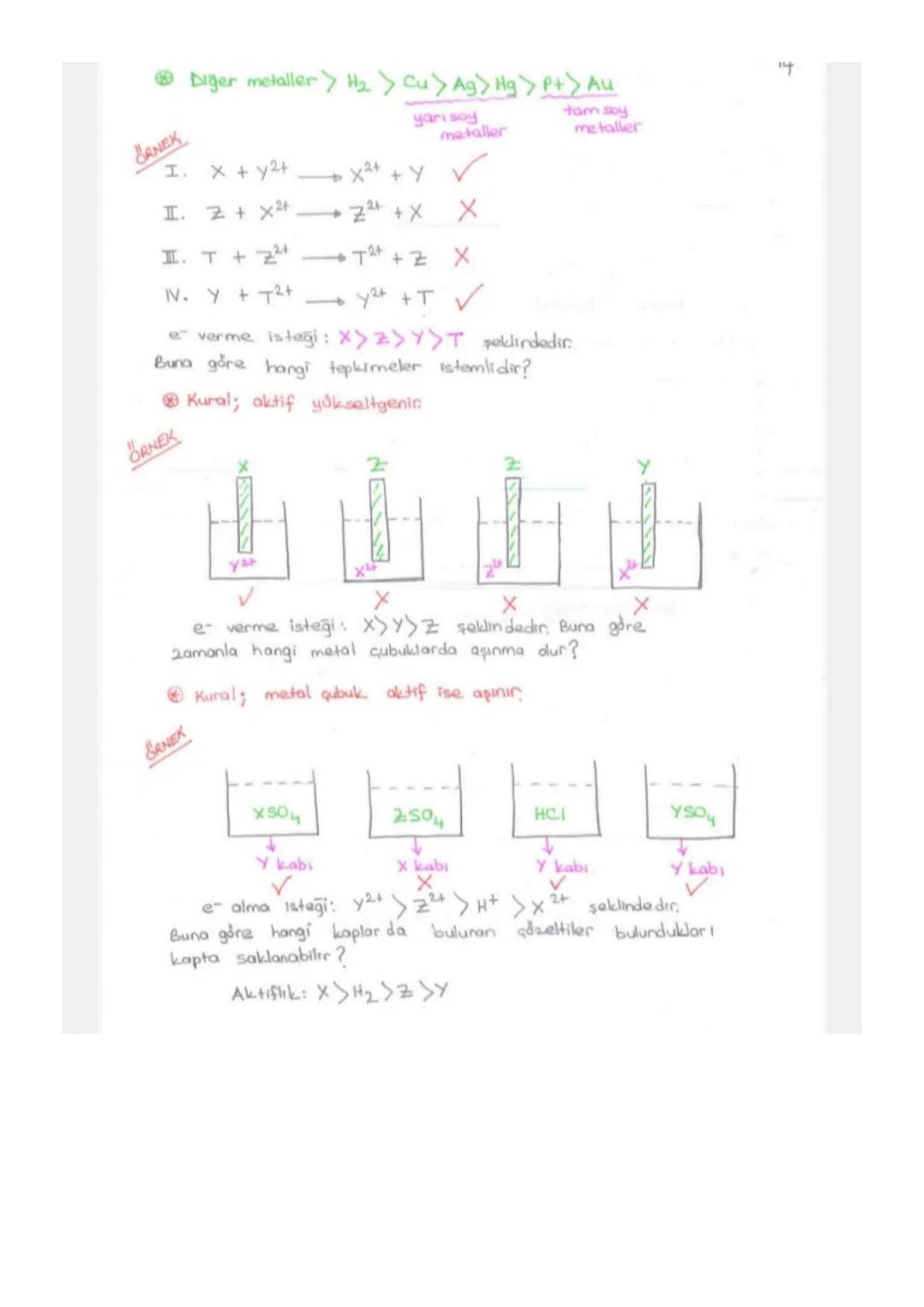
Genel aktiflik sırası: Alkali metaller > Toprak alkali metaller > Diğer metaller > H₂ > Yarı soy metaller (Cu, Ag, Hg) > Tam soy metaller (Au, Pt).
🔍 Çözüm Stratejisi: Verilen tepkimelerden aktiflik sırasını çıkar, sonra diğer soruları bu sıraya göre çöz!

Metal Türleri ve Özellikleri
Metalleri tepkime verme özelliklerine göre sınıflandırabilirsin. Su ile H₂ çıkaran metaller çok aktiftir (1A ve 2A grupları).
Suyla tepkime vermeyen ama asitle H₂ çıkaran metaller H⁺'dan aktiftir. Yarı soy metaller (Cu, Hg, Ag) oksijensiz asitlerle tepkime vermez.
Tam soy metaller (Au, Pt) hiçbir saf asitle tepkime vermez. Amfoter metaller (Zn, Al, Sn, Be) kuvvetli bazlarla da tepkime verir.
🧪 Lab Bilgisi: Amfoter metaller hem asit hem baz gibi davranabilir, bu yüzden NaOH ile tepkime verirler!

Aktiflik Uygulamaları
Aktiflik bilgini pratik sorularda kullanmayı öğren. Metal çubuk hangi çözeltide duruyorsa, o metalden daha aktifse aşınır.
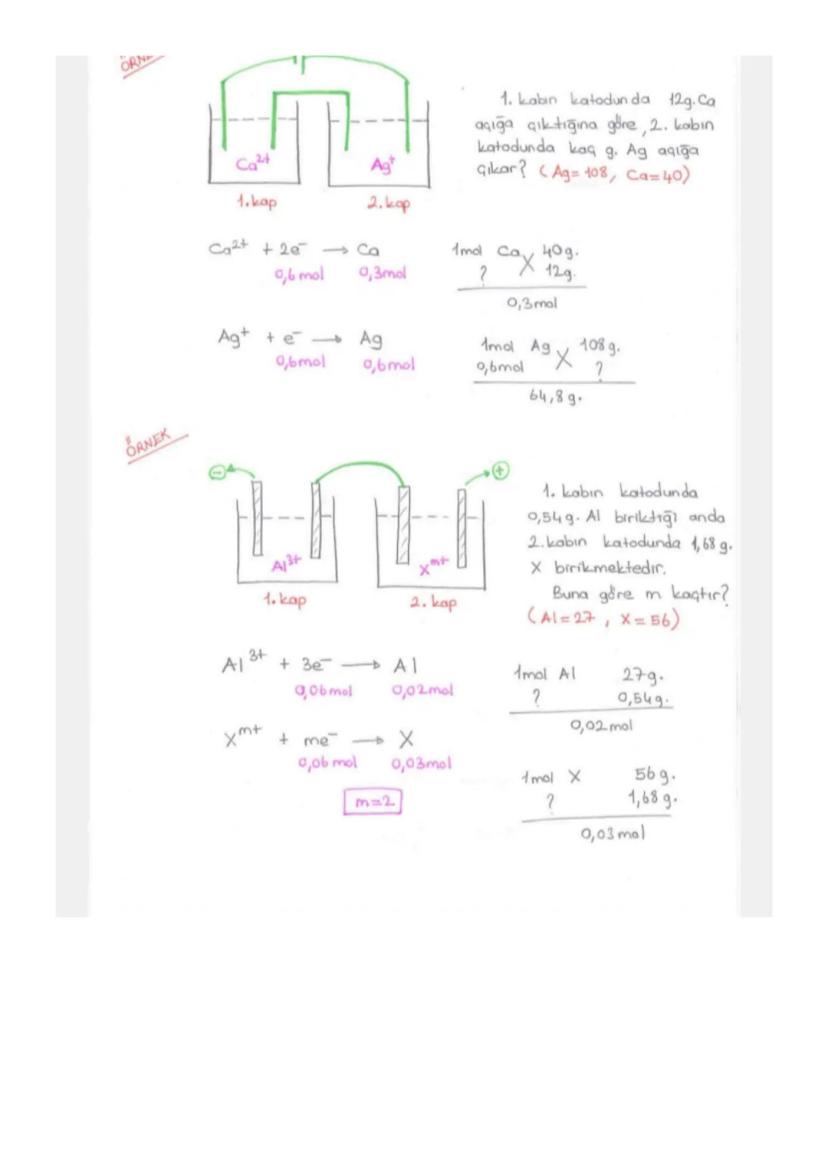
Kütle hesapları yaparken mol oranlarını kullan. Al çubuğundan 5,4g azalma varsa 0,2 mol Al yükseltgenmiş demektir.
2Al + 3Cu²⁺ → 2Al³⁺ + 3Cu tepkimesinde 0,2 mol Al'a karşılık 0,3 mol Cu açığa çıkar. Bu da 19,2g Cu yapar.
📊 Hesaplama İpucu: Redoks tepkimelerinde elektron sayıları eşit olmalı, mol oranlarını buna göre ayarla!

Ametalik Aktiflik ve Elektrot Potansiyeli
Ametalik aktiflik elektron alma isteğidir. F₂ > Cl₂ > Br₂ > I₂ sıralaması vardır. Aktif ametal pasifi açığa çıkarır.
Elektrot potansiyeli yükseltgenme veya indirgenme sırasındaki potansiyel değişimidir. Hidrojenin potansiyeli sıfır kabul edilir .
H'den aktif elementlerin yükseltgenme potansiyeli pozitif, pasif olanların negatiftir. Tepkime ters çevrilirse işaret değişir ama sayıyla çarpılırsa potansiyel değişmez.
⚖️ Temel Kural: Potansiyel hesaplarında hidrojen referans noktasıdır, diğer tüm değerler ona göre belirlenir!




















Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
Elektrokimya: Kolay ve Detaylı Anlatım
Elektrokimya, elektronların hareketinin kimyasal tepkimelerde nasıl rol oynadığını inceleyen konudur. Bu bölümde değerlik hesaplama, redoks tepkimeleri, elementlerin aktifliği ve elektrokimyasal potansiyeller gibi temel kavramları öğreneceksin.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektrokimya ve Değerlik Kuralları
Elektrokimya dünyasına girmeden önce değerlik hesaplama kurallarını bilmen gerekiyor. Bu kurallar sayesinde kimyasal formüllerdeki elementlerin yüklerini kolayca bulabilirsin.
Alkali metaller (Li, Na, K, Rb, Cs, Fr) her zaman +1, toprak alkali metaller (Be, Mg, Ca, Sr, Ba, Ra) ise her zaman +2 değerlik alır. Bu metaller bileşiklerinde hiç değişmez!
Hidrojen metallerde -1 (NaH gibi), ametallerde +1 (HCl gibi) değerlik alır. Oksijen genellikle -2'dir ama peroksitlerde (H₂O₂) -1, süperoksitlerde -1/2 değerlik alabilir.
💡 Önemli Not: Serbest haldeki tüm elementlerin değerliği sıfırdır (O₂, N₂, Fe gibi).

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Değerlik ve Kimyasal Kökler
Halojenler (F, Cl, Br, I) metallerde daima -1 değerlik alır. Ametallerde ise duruma göre farklı değerlikler gösterebilir.
Kimyasal kökler özellikle önemli! -1'lik kökler: OH⁻ (hidroksit), NO₃⁻ (nitrat), CN⁻ (siyanür). -2'lik kökler: SO₄²⁻ (sülfat), CO₃²⁻ (karbonat), CrO₄²⁻ (kromat). -3'lük kök: PO₄³⁻ (fosfat).
Değerlik hesaplarken a.c + b.d = m formülünü kullan. Burada a ve b atom sayıları, c ve d değerlikler, m ise toplam yüktür.
⚡ Pratik İpucu: NH₄⁺ (amonyum) tek +1'lik katyondur, onu hep hatırla!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Redoks Tepkimeleri
Redoks tepkimeleri elektron alış-verişi ile gerçekleşir. Bir tepkimede elementlerden birinin değerliği değişiyorsa o tepkime redokstur.
Yanma tepkimeleri redokstur çünkü değerlikler değişir. Ama asit-baz tepkimeleri redoks değildir.
Metal-asit tepkimelerinde H₂ gazı çıkıyorsa mutlaka redokstur. Çünkü H⁺'dan H₂'ye geçiş oluyor.
🔬 Test İpucu: Tepkimede serbest element varsa kesinlikle redokstur!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
İndirgenme ve Yükseltgenme
İndirgenme: Elektron alarak değerliğin azalması. N + 3e⁻ → N³⁻ gibi. Elektron alan indirgenir!
Yükseltgenme: Elektron vererek değerliğin artması. Fe → 2e⁻ + Fe²⁺ gibi. Elektron veren yükseltgenir!
Bu kavramları karıştırma! Elektron alan indirgenir ama yükseltgendir. Elektron veren yükseltgenir ama indirgendir. Bu tanımlar önemli çünkü sınavda sıkça soruluyor.
🎯 Akılda Kalıcı: "İndirgen elektron verir, yükseltgen elektron alır" diye hatırla!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Redoks Denklemlerini Denkleştirme
Redoks denklemlerini denkleştirmek için sistematik bir yöntem kullan. Önce değerlikleri bul, sonra değişen elementleri tespit et.
Alınan ve verilen elektron sayılarını eşitle. C + HNO₃ → CO₂ + NO₂ örneğinde: C → C⁴⁺ + 4e⁻ ve N⁵⁺ + e⁻ → N⁴⁺ tepkimeleri oluyor.
Son adımda H ve O atomlarını denkleştir. Bu method her zaman işe yarar ve sınavda zaman kazandırır.
📝 Sınav Taktiği: Önce elektron sayılarını eşitle, sonra diğer atomlara bak!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Aktiflik Kavramı
Aktiflik elementlerin bileşik yapma isteğidir. Metaller elektron vererek, ametaller elektron alarak aktiflik gösterir.
Metallerde aktiflik = elektron verme eğilimi. Aktif metal pasif metali açığa çıkarır. Mg + CuCl₂ → MgCl₂ + Cu tepkimesinde Mg, Cu'dan daha aktiftir.
Tepkimelerden aktiflik sırasını bulabilirsin. X + Y²⁺ → X²⁺ + Y tepkimesi kendiliğinden oluyorsa X > Y'dir.
⚡ Önemli: Aktif metal = kolay aşınan metal = kolay yükseltgenen metal!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Aktiflik Karşılaştırmaları
Aktiflik sorularında hangi tepkimelerin kendiliğinden olacağını belirlemelisin. Aktif element pasifi açığa çıkarır kuralını kullan.
Metal çubuk sorularında aktif olan çubuk aşınır. Çözeltide kendi iyonu varsa çubuk aşınmaz.
Genel aktiflik sırası: Alkali metaller > Toprak alkali metaller > Diğer metaller > H₂ > Yarı soy metaller (Cu, Ag, Hg) > Tam soy metaller (Au, Pt).
🔍 Çözüm Stratejisi: Verilen tepkimelerden aktiflik sırasını çıkar, sonra diğer soruları bu sıraya göre çöz!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Metal Türleri ve Özellikleri
Metalleri tepkime verme özelliklerine göre sınıflandırabilirsin. Su ile H₂ çıkaran metaller çok aktiftir (1A ve 2A grupları).
Suyla tepkime vermeyen ama asitle H₂ çıkaran metaller H⁺'dan aktiftir. Yarı soy metaller (Cu, Hg, Ag) oksijensiz asitlerle tepkime vermez.
Tam soy metaller (Au, Pt) hiçbir saf asitle tepkime vermez. Amfoter metaller (Zn, Al, Sn, Be) kuvvetli bazlarla da tepkime verir.
🧪 Lab Bilgisi: Amfoter metaller hem asit hem baz gibi davranabilir, bu yüzden NaOH ile tepkime verirler!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
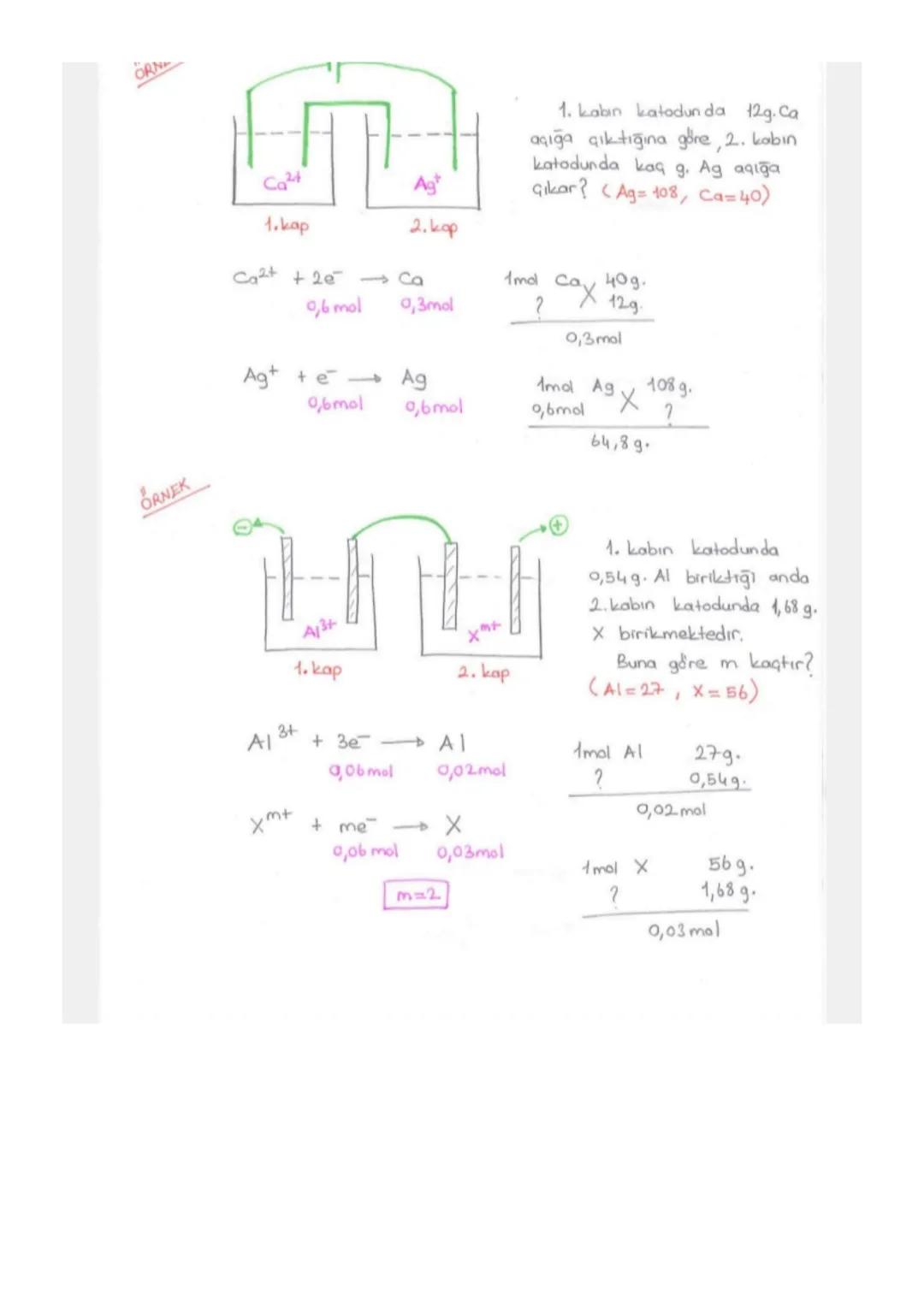
Aktiflik Uygulamaları
Aktiflik bilgini pratik sorularda kullanmayı öğren. Metal çubuk hangi çözeltide duruyorsa, o metalden daha aktifse aşınır.
Kütle hesapları yaparken mol oranlarını kullan. Al çubuğundan 5,4g azalma varsa 0,2 mol Al yükseltgenmiş demektir.
2Al + 3Cu²⁺ → 2Al³⁺ + 3Cu tepkimesinde 0,2 mol Al'a karşılık 0,3 mol Cu açığa çıkar. Bu da 19,2g Cu yapar.
📊 Hesaplama İpucu: Redoks tepkimelerinde elektron sayıları eşit olmalı, mol oranlarını buna göre ayarla!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
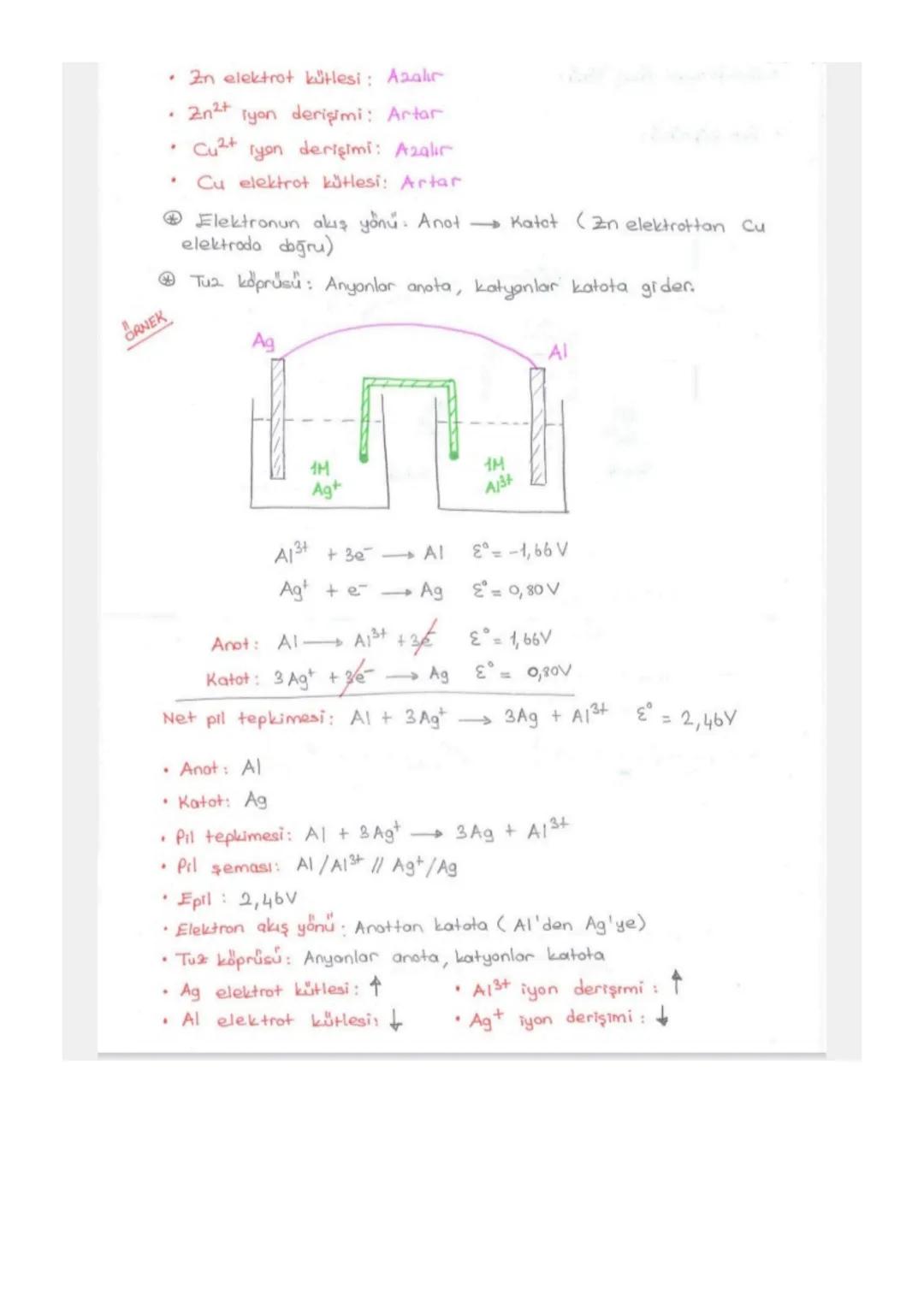
Ametalik Aktiflik ve Elektrot Potansiyeli
Ametalik aktiflik elektron alma isteğidir. F₂ > Cl₂ > Br₂ > I₂ sıralaması vardır. Aktif ametal pasifi açığa çıkarır.
Elektrot potansiyeli yükseltgenme veya indirgenme sırasındaki potansiyel değişimidir. Hidrojenin potansiyeli sıfır kabul edilir .
H'den aktif elementlerin yükseltgenme potansiyeli pozitif, pasif olanların negatiftir. Tepkime ters çevrilirse işaret değişir ama sayıyla çarpılırsa potansiyel değişmez.
⚖️ Temel Kural: Potansiyel hesaplarında hidrojen referans noktasıdır, diğer tüm değerler ona göre belirlenir!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅