Atom fiziği kimyanın temelidir ve 11. sınıf müfredatının en önemli... Daha fazla göster
Kimya 11. Sınıf Ders Notları ve Çalışma Kaynakları













Atomun Kuantum Modeli Temelleri
Bohr Atom Modeli sadece hidrojen ve tek elektronlu iyonları (He⁺, Li²⁺ gibi) açıklayabilir. Çok elektronlu atomlarda elektron-elektron etkileşimleri nedeniyle yetersiz kalır.
Orbital ve yörünge kavramları arasındaki fark önemli! Orbital, elektronun bulunma olasılığının yüksek olduğu üç boyutlu bölgedir. Her orbitalde maksimum 2 elektron bulunur ve farklı enerji düzeylerinde değişik orbital türleri (s, p, d, f) vardır.
Kuantum sayıları atomdaki elektronları tanımlar: Baş kuantum sayısı (n) enerji düzeyini, yan kuantum sayısı (ℓ) orbital şeklini, manyetik kuantum sayısı (m) orbitalin uzaydaki yönelimini belirtir. 2p orbitali için n=2, ℓ=1'dir ve mₗ değeri -1, 0, +1 olabilir.
💡 İpucu: Kuantum sayıları arasındaki ilişkileri ezberlemek yerine mantığını anla. n değeri arttıkça mümkün ℓ değerleri de artar .

Orbital Şekilleri ve Enerji Seviyeleri
s orbitali küresel, p orbitalleri ikili lob şeklindedir. p orbitalleri (px, py, pz) birbirlerine dik eksenlerde yönelir. d orbitalleri daha karmaşık şekillere sahiptir.
Enerji sıralaması kritik bir konudur! Aynı ana enerji düzeyindeki orbitaller bile farklı enerjilere sahip olabilir. 4s orbitali 3d'den önce dolar çünkü enerjisi daha düşüktür: 4s < 3d < 4p.
2. enerji düzeyinde sadece s ve p orbitalleri bulunur (2s, 2p). Toplam 2 tür orbital, maksimum 4 orbital (1 tane 2s, 3 tane 2p) vardır. Bu da toplam 8 elektron alabilir.
💡 Dikkat: Kuantum sayı kombinasyonlarında n ≥ ℓ+1 kuralı geçerlidir. Örneğin ℓ=2 için n en az 3 olmalıdır.

Elektron Dizilimleri ve Periyodik Sistem
Elektron dizilimi yazarken Aufbau prensibini kullan: elektronlar en düşük enerjili orbitallerden başlayarak dolar. ¹²Mg için doğru dizilim: 1s² 2s² 2p⁶ 3s²'dir.
Orbital şeması çizerken Hund kuralına dikkat et! Aynı enerjili orbitallerde elektronlar önce tek tek, sonra çift olarak yerleşir. Çift elektronlar zıt spinlere sahiptir.
Periyodik sistem blokları elektron dizilimine göre belirlenir: s bloku , p bloku , d bloku (geçiş metalleri), f bloku (iç geçiş metalleri). Elementin son elektronu hangi orbital türüne girerse o blokta yer alır.
💡 Önemli: Kısa elektron dizilimi için en yakın soy gazı köşeli parantez içinde yaz: [Ar] 4s¹ 3d¹⁰ gibi.

İyonlar ve İstisnai Durumlar
İyon oluşumunda önce en dış kabuktan elektronlar kopar! ²⁵Mn²⁺ için önce 4s elektronları, sonra 3d elektronları çıkar: [Ar] 3d⁵.
Krom ve bakır gibi elementlerde istisna durumlar vardır. ²⁴Cr'un elektron dizilimi [Ar] 4s¹ 3d⁵'tir (4s² 3d⁴ değil). Bu yarı dolu d orbitalinin stabilitesinden kaynaklanır.
Periyodik sistemde 7 periyot, 18 grup vardır. A grubu elementleri (baş grup) s ve p bloklarında, B grubu elementleri d bloğunda yer alır. Metal sayısı periyot boyunca değişir.
💡 Pratik Bilgi: Tam dolu ve yarı dolu orbital sayısını bulurken sistematik git. Önce tam dolu olanları say, sonra yarı doluları ekle.

Periyodik Özellikler: Atom Yarıçapı ve İyonlaşma Enerjisi
Atom yarıçapı periyotta soldan sağa azalır, grupta yukarıdan aşağıya artar. Çekirdek yükü artarken elektron sayısı eşit artmadığı için çekim gücü artar. K > Ca > Cl > Ne şeklinde sıralanır.
İyon yarıçapları farklı davranır! Katyon (pozitif iyon) ana atomdan küçük, anyon (negatif iyon) büyüktür. İzoelektronik iyonlarda çekirdek yükü fazla olanın yarıçapı küçüktür.
İyonlaşma enerjisi tablolarında büyük sıçramalar önemli ipuçları verir. 1. ve 2. iyonlaşma enerjisi arasında büyük fark varsa element 1A grubunda, 2. ve 3. arasında büyük fark varsa 2A grubunda olabilir.
💡 CaO Örneği: İyon yarıçapları toplamı = mesafe. Ca²⁺ (1 Å) + O²⁻ (x) = 2,40 Å ise O²⁻ = 1,40 Å'dur.

Elektronegatiflik ve Periyodik Trendler
İyonlaşma enerjisi periyotta soldan sağa genellikle artar. Ancak 2A-3A ve 5A-6A grupları arasında küçük düşüşler görülür. Bu orbital yapılarının stabilitesinden kaynaklanır.
Van der Waals yarıçapı sadece soy gazlar ve ametal moleküller için geçerlidir. Metaller için kovalent veya metalik yarıçap kullanılır.
Bazlık kuvveti metal oksitlerinde metalin aktifliği ile doğru orantılıdır. Rb₂O > K₂O > Na₂O şeklinde sıralanır. Daha aktif metal, daha güçlü baz yapar.
💡 7A Grubu: Elektronegatifliği en büyük olan en güçlü asit yapar (HF > HCl > HBr). Atom numarası büyük olan fiziksel özellikler bakımından farklılık gösterir.

Element Blokları ve Özellikler
s bloku elementleri genellikle metaldir ve oksitleri bazik karakterlidir. Değerlik elektron sayıları 1 veya 2'dir. Çoğu su ile tepkimeye girerek H₂ gazı çıkarır.
7A grubu (halojenler) en aktif ametallerdir. Elektron dizilimleri ns² np⁵ ile sonlanır. Elektronegatiflik değerleri yüksek olduğu için elektron ilgileri de büyüktür.
d bloku elementleri (geçiş metalleri) farklı pozitif değerlikler alabilir ve renkli bileşikler yapar. Minimum 3. periyottan başlar. f bloku elementleri iç geçiş metalleridir ve genellikle +3 değerlik gösterir.
💡 Önemli Ayrım: p blokunda hem metal hem ametal bulunur (Al metal, Cl ametaldir). Sadece d bloku elementlerinin tamamı metaldir.
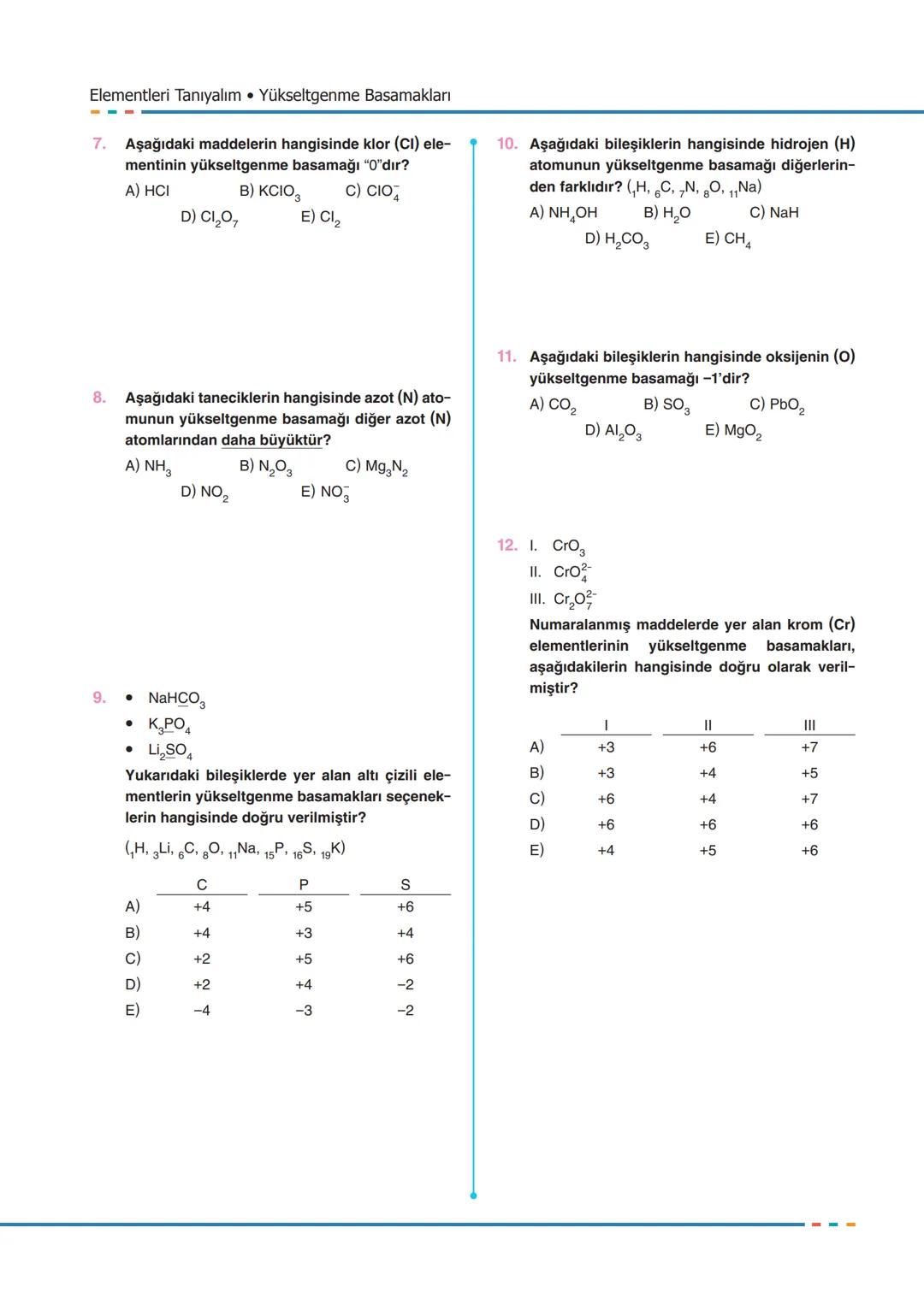
Yükseltgenme Basamakları
Yükseltgenme basamağı kuralları: Serbest haldeki elementlerin yükseltgenme basamağı sıfırdır . Oksijen genellikle -2, hidrojen genellikle +1 değerlik alır.
Hidrojen istisnaları: Metal hidritlerdə (NaH) hidrojen -1 değerlik alır. Oksijen de peroksitlerde (MgO₂) -1 değerlik gösterir.
Bileşik iyonlarda toplam yük, yükseltgenme basamaklarının cebirsel toplamına eşittir. NO₃⁻ iyonunda N = +5, O = -2'dir ve (-2×3) + (+5) = -1 olur.
💡 Pratik Yöntem: Bildiğin elementlerin değerliklerini kullanarak bilinmeyeni hesapla. NaHCO₃'te Na(+1), H(+1), O(-2) biliyorsak C'yi bulabiliriz.

Modern Atom Teorisi Tarama
4d orbitali için n=4, ℓ=2 ve mₗ = -2, -1, 0, +1, +2 değerlerini alır. d orbitallerinin 5 farklı yönelimi vardır.
4. enerji düzeyi 4s, 4p, 4d ve 4f orbitallerini içerir (4 tür). Toplam elektron kapasitesi 32'dir (2+6+10+14).
Fe³⁺ iyonu için elektron dizilimi: Önce 4s, sonra 3d'den elektronlar çıkar. ²⁶Fe'den 3 elektron çıkınca 1s² 2s² 2p⁶ 3s² 3p⁶ 3d⁵ olur.
💡 Hund Kuralı: Aynı enerjili orbitallerde elektronlar önce tek tek yerleşir, hepsi yarı dolduktan sonra çiftleşme başlar.

Periyodik Özellikler ve Yükseltgenme Durumları
Tanecik yarıçapları karşılaştırması: Anyon > nötral atom > katyon. S²⁻ > S > S²⁺ şeklinde sıralanır. Elektron sayısı arttıkça yarıçap artar.
2A grubu elementleri (toprak alkali metaller) oldukça aktiftir ve +2 yükseltgenme basamağı gösterir. Halojenlerle iyonik bileşikler oluşturur.
İyonlaşma enerjisi trendi: Mg > Al > Na. Magnezyumun tam dolu s orbitali nedeniyle iyonlaşma enerjisi alüminyumdan yüksektir.
💡 Yükseltgenme Basamağı: Al(NO₃)₃'te Al = +3, N = +5, O = -2'dir. Çok atomlu iyonlarda (NO₃⁻) ayrı ayrı hesapla.


Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Element
99. sınıf kimya tüm konular
9. sınıf yazılılarında işe yarar
Element ve sembolleri
Elementler
Kimyanın sembolik dili
Uzunca anlatim
Kimya yaygın bilinen elementler
İlk yirmi element Elementler Bileşiklerin adları Kimya
İndirgenme yükseltgenme tepkimeleri
Ayt kimya
Atom ve Periyoduk Sistem
atom ve periyodik sistem konusu konu anlatımı
Element ve bileşik farkı
Kimya element bileşik ve karışımlar Kimya ders notu Tyt kimya
tyt kimya
tyt kimya notları
Kimya bilimine giriş
9 .sınıf kimya dersinde 1 .ünite olan kimya dersine giriş konusunda önemli konu notları içerir
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
Kimya 11. Sınıf Ders Notları ve Çalışma Kaynakları
Atom fiziği kimyanın temelidir ve 11. sınıf müfredatının en önemli konularından biridir. Bu test sorularında atomun kuantum modeli, periyodik sistem, elektron dizilimleri ve periyodik özellikler gibi kritik konular ele alınıyor.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Atomun Kuantum Modeli Temelleri
Bohr Atom Modeli sadece hidrojen ve tek elektronlu iyonları (He⁺, Li²⁺ gibi) açıklayabilir. Çok elektronlu atomlarda elektron-elektron etkileşimleri nedeniyle yetersiz kalır.
Orbital ve yörünge kavramları arasındaki fark önemli! Orbital, elektronun bulunma olasılığının yüksek olduğu üç boyutlu bölgedir. Her orbitalde maksimum 2 elektron bulunur ve farklı enerji düzeylerinde değişik orbital türleri (s, p, d, f) vardır.
Kuantum sayıları atomdaki elektronları tanımlar: Baş kuantum sayısı (n) enerji düzeyini, yan kuantum sayısı (ℓ) orbital şeklini, manyetik kuantum sayısı (m) orbitalin uzaydaki yönelimini belirtir. 2p orbitali için n=2, ℓ=1'dir ve mₗ değeri -1, 0, +1 olabilir.
💡 İpucu: Kuantum sayıları arasındaki ilişkileri ezberlemek yerine mantığını anla. n değeri arttıkça mümkün ℓ değerleri de artar .

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Orbital Şekilleri ve Enerji Seviyeleri
s orbitali küresel, p orbitalleri ikili lob şeklindedir. p orbitalleri (px, py, pz) birbirlerine dik eksenlerde yönelir. d orbitalleri daha karmaşık şekillere sahiptir.
Enerji sıralaması kritik bir konudur! Aynı ana enerji düzeyindeki orbitaller bile farklı enerjilere sahip olabilir. 4s orbitali 3d'den önce dolar çünkü enerjisi daha düşüktür: 4s < 3d < 4p.
2. enerji düzeyinde sadece s ve p orbitalleri bulunur (2s, 2p). Toplam 2 tür orbital, maksimum 4 orbital (1 tane 2s, 3 tane 2p) vardır. Bu da toplam 8 elektron alabilir.
💡 Dikkat: Kuantum sayı kombinasyonlarında n ≥ ℓ+1 kuralı geçerlidir. Örneğin ℓ=2 için n en az 3 olmalıdır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektron Dizilimleri ve Periyodik Sistem
Elektron dizilimi yazarken Aufbau prensibini kullan: elektronlar en düşük enerjili orbitallerden başlayarak dolar. ¹²Mg için doğru dizilim: 1s² 2s² 2p⁶ 3s²'dir.
Orbital şeması çizerken Hund kuralına dikkat et! Aynı enerjili orbitallerde elektronlar önce tek tek, sonra çift olarak yerleşir. Çift elektronlar zıt spinlere sahiptir.
Periyodik sistem blokları elektron dizilimine göre belirlenir: s bloku , p bloku , d bloku (geçiş metalleri), f bloku (iç geçiş metalleri). Elementin son elektronu hangi orbital türüne girerse o blokta yer alır.
💡 Önemli: Kısa elektron dizilimi için en yakın soy gazı köşeli parantez içinde yaz: [Ar] 4s¹ 3d¹⁰ gibi.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
İyonlar ve İstisnai Durumlar
İyon oluşumunda önce en dış kabuktan elektronlar kopar! ²⁵Mn²⁺ için önce 4s elektronları, sonra 3d elektronları çıkar: [Ar] 3d⁵.
Krom ve bakır gibi elementlerde istisna durumlar vardır. ²⁴Cr'un elektron dizilimi [Ar] 4s¹ 3d⁵'tir (4s² 3d⁴ değil). Bu yarı dolu d orbitalinin stabilitesinden kaynaklanır.
Periyodik sistemde 7 periyot, 18 grup vardır. A grubu elementleri (baş grup) s ve p bloklarında, B grubu elementleri d bloğunda yer alır. Metal sayısı periyot boyunca değişir.
💡 Pratik Bilgi: Tam dolu ve yarı dolu orbital sayısını bulurken sistematik git. Önce tam dolu olanları say, sonra yarı doluları ekle.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Periyodik Özellikler: Atom Yarıçapı ve İyonlaşma Enerjisi
Atom yarıçapı periyotta soldan sağa azalır, grupta yukarıdan aşağıya artar. Çekirdek yükü artarken elektron sayısı eşit artmadığı için çekim gücü artar. K > Ca > Cl > Ne şeklinde sıralanır.
İyon yarıçapları farklı davranır! Katyon (pozitif iyon) ana atomdan küçük, anyon (negatif iyon) büyüktür. İzoelektronik iyonlarda çekirdek yükü fazla olanın yarıçapı küçüktür.
İyonlaşma enerjisi tablolarında büyük sıçramalar önemli ipuçları verir. 1. ve 2. iyonlaşma enerjisi arasında büyük fark varsa element 1A grubunda, 2. ve 3. arasında büyük fark varsa 2A grubunda olabilir.
💡 CaO Örneği: İyon yarıçapları toplamı = mesafe. Ca²⁺ (1 Å) + O²⁻ (x) = 2,40 Å ise O²⁻ = 1,40 Å'dur.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektronegatiflik ve Periyodik Trendler
İyonlaşma enerjisi periyotta soldan sağa genellikle artar. Ancak 2A-3A ve 5A-6A grupları arasında küçük düşüşler görülür. Bu orbital yapılarının stabilitesinden kaynaklanır.
Van der Waals yarıçapı sadece soy gazlar ve ametal moleküller için geçerlidir. Metaller için kovalent veya metalik yarıçap kullanılır.
Bazlık kuvveti metal oksitlerinde metalin aktifliği ile doğru orantılıdır. Rb₂O > K₂O > Na₂O şeklinde sıralanır. Daha aktif metal, daha güçlü baz yapar.
💡 7A Grubu: Elektronegatifliği en büyük olan en güçlü asit yapar (HF > HCl > HBr). Atom numarası büyük olan fiziksel özellikler bakımından farklılık gösterir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Element Blokları ve Özellikler
s bloku elementleri genellikle metaldir ve oksitleri bazik karakterlidir. Değerlik elektron sayıları 1 veya 2'dir. Çoğu su ile tepkimeye girerek H₂ gazı çıkarır.
7A grubu (halojenler) en aktif ametallerdir. Elektron dizilimleri ns² np⁵ ile sonlanır. Elektronegatiflik değerleri yüksek olduğu için elektron ilgileri de büyüktür.
d bloku elementleri (geçiş metalleri) farklı pozitif değerlikler alabilir ve renkli bileşikler yapar. Minimum 3. periyottan başlar. f bloku elementleri iç geçiş metalleridir ve genellikle +3 değerlik gösterir.
💡 Önemli Ayrım: p blokunda hem metal hem ametal bulunur (Al metal, Cl ametaldir). Sadece d bloku elementlerinin tamamı metaldir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Yükseltgenme Basamakları
Yükseltgenme basamağı kuralları: Serbest haldeki elementlerin yükseltgenme basamağı sıfırdır . Oksijen genellikle -2, hidrojen genellikle +1 değerlik alır.
Hidrojen istisnaları: Metal hidritlerdə (NaH) hidrojen -1 değerlik alır. Oksijen de peroksitlerde (MgO₂) -1 değerlik gösterir.
Bileşik iyonlarda toplam yük, yükseltgenme basamaklarının cebirsel toplamına eşittir. NO₃⁻ iyonunda N = +5, O = -2'dir ve (-2×3) + (+5) = -1 olur.
💡 Pratik Yöntem: Bildiğin elementlerin değerliklerini kullanarak bilinmeyeni hesapla. NaHCO₃'te Na(+1), H(+1), O(-2) biliyorsak C'yi bulabiliriz.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Modern Atom Teorisi Tarama
4d orbitali için n=4, ℓ=2 ve mₗ = -2, -1, 0, +1, +2 değerlerini alır. d orbitallerinin 5 farklı yönelimi vardır.
4. enerji düzeyi 4s, 4p, 4d ve 4f orbitallerini içerir (4 tür). Toplam elektron kapasitesi 32'dir (2+6+10+14).
Fe³⁺ iyonu için elektron dizilimi: Önce 4s, sonra 3d'den elektronlar çıkar. ²⁶Fe'den 3 elektron çıkınca 1s² 2s² 2p⁶ 3s² 3p⁶ 3d⁵ olur.
💡 Hund Kuralı: Aynı enerjili orbitallerde elektronlar önce tek tek yerleşir, hepsi yarı dolduktan sonra çiftleşme başlar.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Periyodik Özellikler ve Yükseltgenme Durumları
Tanecik yarıçapları karşılaştırması: Anyon > nötral atom > katyon. S²⁻ > S > S²⁺ şeklinde sıralanır. Elektron sayısı arttıkça yarıçap artar.
2A grubu elementleri (toprak alkali metaller) oldukça aktiftir ve +2 yükseltgenme basamağı gösterir. Halojenlerle iyonik bileşikler oluşturur.
İyonlaşma enerjisi trendi: Mg > Al > Na. Magnezyumun tam dolu s orbitali nedeniyle iyonlaşma enerjisi alüminyumdan yüksektir.
💡 Yükseltgenme Basamağı: Al(NO₃)₃'te Al = +3, N = +5, O = -2'dir. Çok atomlu iyonlarda (NO₃⁻) ayrı ayrı hesapla.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Element
99. sınıf kimya tüm konular
9. sınıf yazılılarında işe yarar
Element ve sembolleri
Elementler
Kimyanın sembolik dili
Uzunca anlatim
Kimya yaygın bilinen elementler
İlk yirmi element Elementler Bileşiklerin adları Kimya
İndirgenme yükseltgenme tepkimeleri
Ayt kimya
Atom ve Periyoduk Sistem
atom ve periyodik sistem konusu konu anlatımı
Element ve bileşik farkı
Kimya element bileşik ve karışımlar Kimya ders notu Tyt kimya
tyt kimya
tyt kimya notları
Kimya bilimine giriş
9 .sınıf kimya dersinde 1 .ünite olan kimya dersine giriş konusunda önemli konu notları içerir
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅