Atomun yapısını anlamak kimyanın temelini oluşturur! Bu konu, elektronların nasıl... Daha fazla göster
11. Sınıf Kimya: Modern Atom Teorisi, Periyodik Tablo ve Gazların Özellikleri









Yörünge, Orbital ve Kuantum Sayıları
Atomdaki elektronları anlamak için önce yörünge ve orbital arasındaki farkı bilmen gerekiyor. Yörünge elektronun varsayılan dairesel yolu, orbital ise elektronun bulunma olasılığının yüksek olduğu üç boyutlu bölgeler.
Kuantum sayıları elektronların adresini verir. Baş kuantum sayısı (n) çekirdeğe uzaklığı, açısal momentum kuantum sayısı (l) orbital şeklini belirler. Manyetik kuantum sayısı (ml) aynı tür orbitalleri ayırırken, spin kuantum sayısı (ms) elektronun dönme yönünü gösterir.
Elektron dizilimi için üç önemli kural var: Aufbau kuralı (düşük enerjiden başla), Hund kuralı (önce tek elektronlar yerleş), Pauli kuralı (aynı orbitalde zıt spinler).
💡 İpucu: Elektron dizilimi yaparken "1s² 2s² 2p⁶ 3s²..." şeklindeki sırayı ezberle!

Elektron Dizilimi ve İstisnalar
Elektron diziliminde n+l değeri önemlidir - bu değer arttıkça orbital enerjisi artar. Eşit n+l değerlerinde ise n'i büyük olan daha yüksek enerjili olur.
Soy gazlar (He, Ne, Ar, Kr, Xe) sayesinde kısa yazım yapabilirsin. Örneğin Fe₂₆: [Ar₁₈]4s²3d⁶ şeklinde yazılır.
Uyarılmış halda elektronlar normal kuralları bozmaya zorlanır. Bu atomlar kararsız ve yüksek enerjili olur. Krom (Cr₂₄) ve bakır (Cu₂₉) gibi elementlerde yarı kararlı ve tam kararlı dizilimler için istisnalar vardır.
İyon oluştururken elektronlar en dış katmandan verilir. Bu nedenle Fe³⁺ iyonunda önce 4s elektronları gider.

Atom Yarıçapı ve Türleri
Atomun büyüklüğünü anlamak için farklı yarıçap türleri var. Atomik yarıçap çekirdekten en dış elektrona olan uzaklık, kovalent yarıçap bağlı atomlar arası mesafenin yarısı.
Van der Waals yarıçapı bağsız atomlar için kullanılır. İyon yarıçapında önemli kural şu: elektron verilince yarıçap küçülür, alınca büyür.
Periyodik cetvelde atom yarıçapı aşağı doğru artar (yeni katman eklenir), sağa doğru azalır (proton sayısı artıp elektronları daha güçlü çeker).
Bu bilgiler atomların nasıl bağ yaptığını anlamanda çok kritik!
💡 Hatırla: X → X⁺ → X²⁺ şeklinde elektron verilirken yarıçap sürekli küçülür.

Periyodik Özellikler
Metalik özellik kolay elektron verebilme yeteneğidir. Atom yarıçapı büyük olan elementler daha metaliktir. Sol alt köşeye doğru gidildikçe metalik özellik artar.
Ametalik özellik bunun tam tersidir - kolay elektron alma yeteneği. Sağ üst köşeye doğru artar.
İyonlaşma enerjisi elektronu koparmak için gereken enerjidir. Atom yarıçapı küçüldükçe artar. Ardışık iyonlaşma enerjileri daima artar çünkü pozitif yük arttıkça elektronları tutma gücü artar.
Elektron ilgisi elektron alırken açığa çıkan enerjidir. Genelde sağa ve yukarı doğru artar ama Cl > F gibi istisnalar vardır.
💡 Önemli: Soy gazların elektron ilgisi yoktur - zaten kararlılar!

Elektronegatiflik ve Blok Elementleri
Elektronegatiflik atomun bağdaki elektronları kendine çekme gücüdür. En yüksek değer fluorda bulunur. Periyotta sağa, grupta yukarı doğru artar.
s blok elementleri (1A, 2A, He) en büyük yarıçaplı elementlerdir. Mineral yağda saklanırlar. 1A grubu +1, 2A grubu +2 değerlik alır.
p blok elementleri çok çeşitlidir - metal, ametal, yarımetal içerir. 7A grubu diatomik, 8A grubu tek atomlu gaz halinde bulunur.
d blok elementleri geçiş metalleridir. Sert yapıda, yüksek erime noktası, birden fazla pozitif değerlik alabilirler.
💡 Dikkat: Bağda elektronegatifliği yüksek olan taraf kısmen negatif olur!
Gazlar ve Temel Özellikler
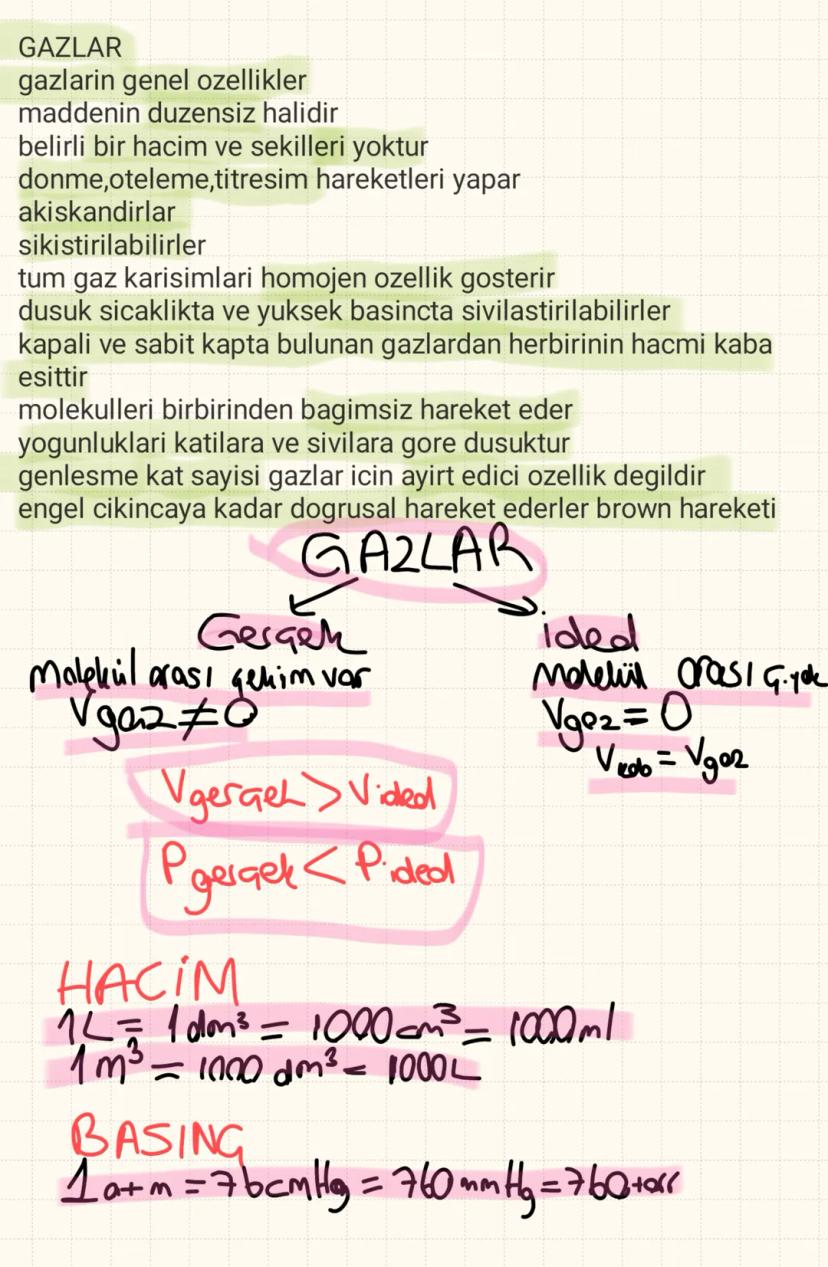
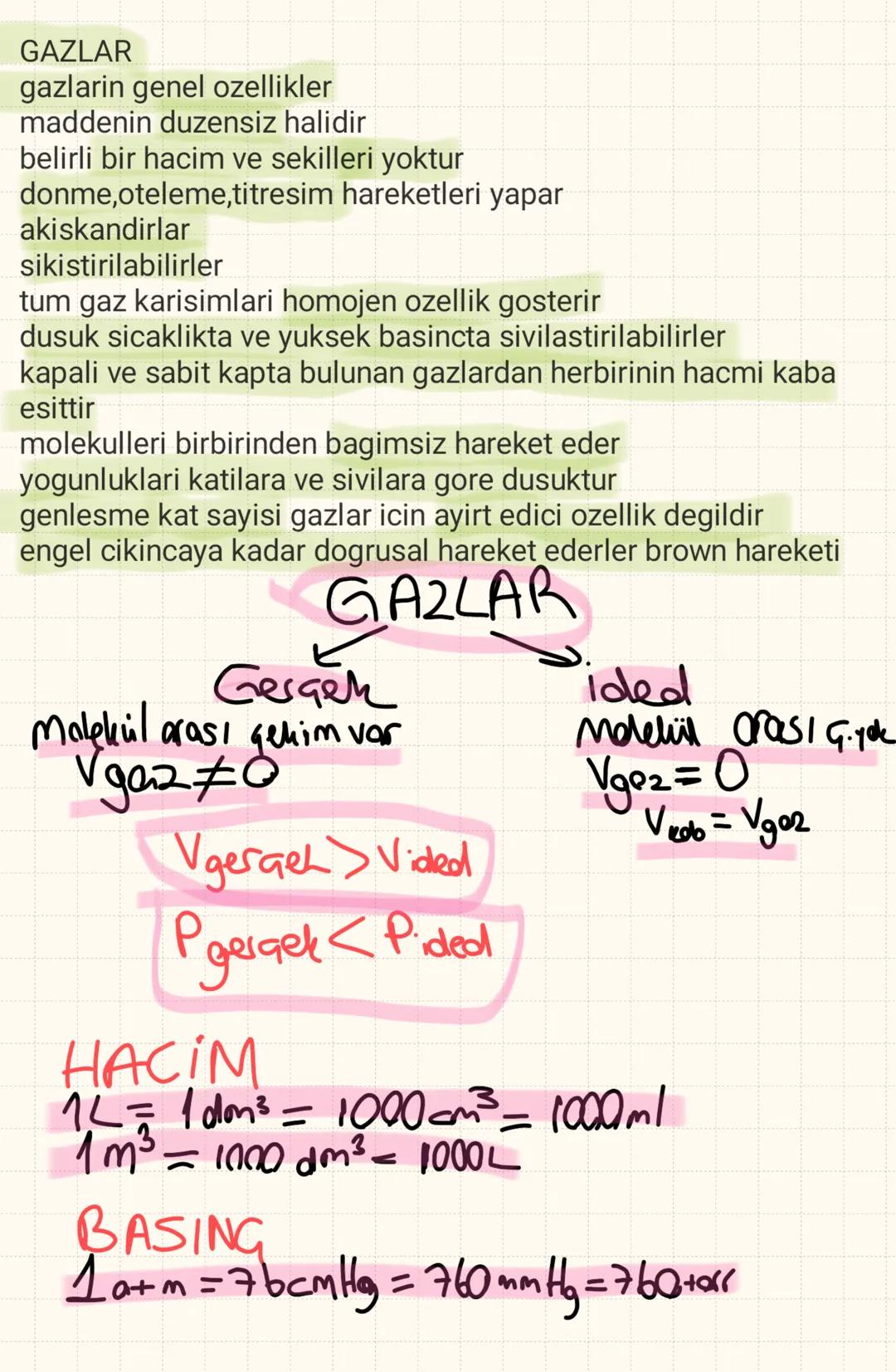
Gazlar maddenin en düzensiz halidir. Belirli hacim ve şekilleri yoktur, sıkıştırılabilir ve akışkandırlar. Molekülleri birbirinden bağımsız hareket eder.
İdeal gazlarda moleküller arası çekim yok, molekül hacmi sıfır. Gerçek gazlarda ise moleküller arası çekim var, bu yüzden basınç idealden düşük, hacim idealden büyük.
Önemli birim dönüşümleri:
- Hacim: 1L = 1000mL = 1000cm³
- Basınç: 1atm = 760mmHg = 760torr
- Sıcaklık: K = °C + 273
Mol sayısı hesaplamaları: n = m/MA = N/NA = V/22.4 (STP'de)
💡 Neden civa kullanılır: Sıvı, renkli, yoğun, az uçucu ve gazlarla tepkime vermez!

Tek Değerlikli Elementler
Tek değerlik alan elementler kimyasal hesaplamalarda çok işine yarar. Bu elementlerin değerlikleri değişmez, bu da hesaplamaları kolaylaştırır.
+1 değerlikli: H⁺, Na⁺, K⁺, Ag⁺ gibi elementler. +2 değerlikli: Be²⁺, Mg²⁺, Ca²⁺, Zn²⁺ gibi. +3 değerlikli: Al³⁺ en önemlisi.
Negatif değerlikler: F⁻, Cl⁻, Br⁻, I⁻ (-1), O²⁻, S²⁻ (-2), N³⁻, P³⁻ (-3) şeklinde.
Karbon hem +4 hem -4 değerlik alabilir. Bu durum organik kimyada çok önemli rol oynar.
Basınç formülü: P_atm = h·d·g (h: yükseklik, d: yoğunluk, g: yerçekimi ivmesi)
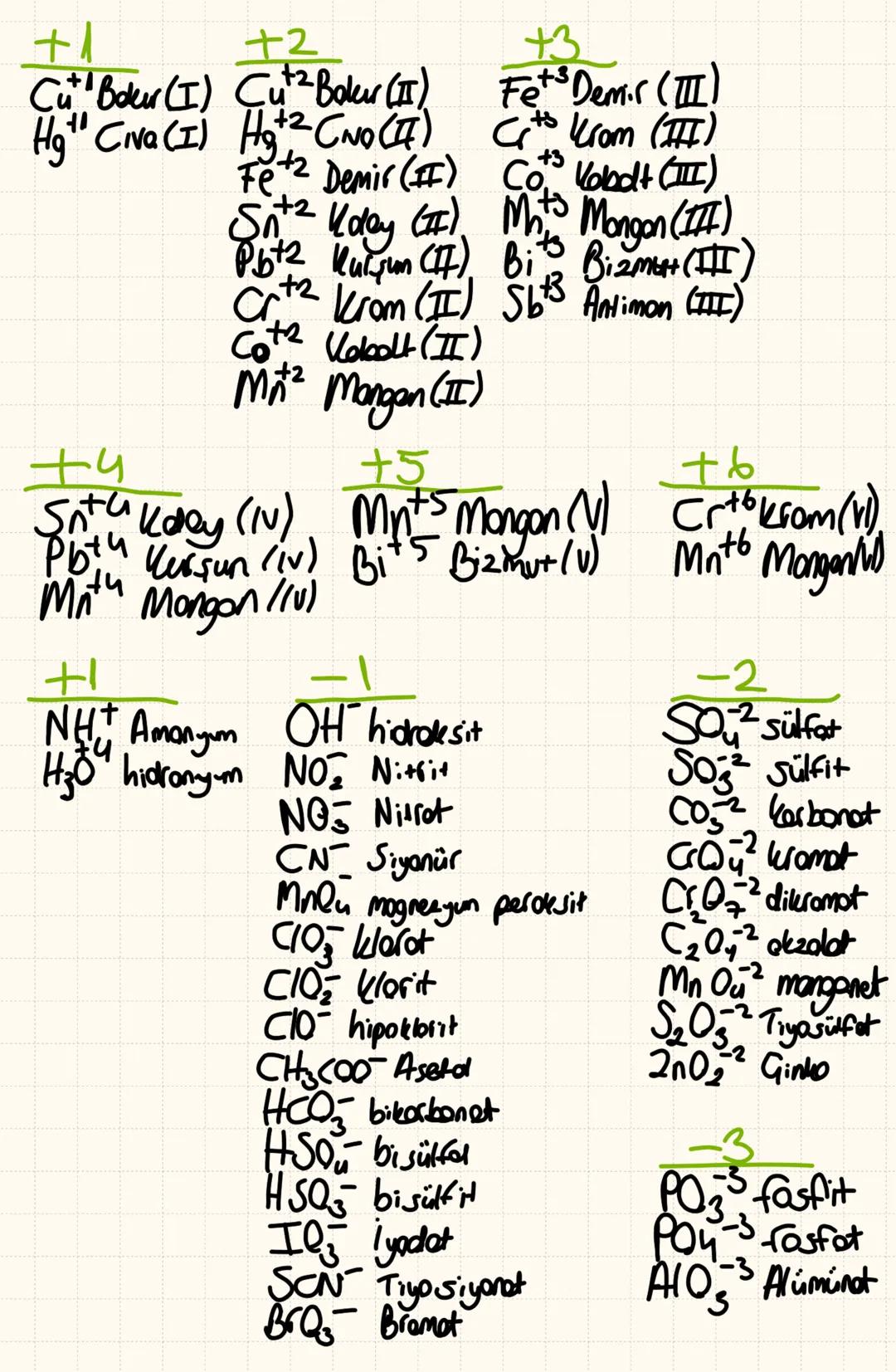
Çok Değerlikli Elementler ve İyonlar
Geçiş metalleri birden fazla değerlik alabilir. Demir Fe²⁺ ve Fe³⁺, bakır Cu⁺ ve Cu²⁺, krom Cr²⁺, Cr³⁺, Cr⁶⁺ değerlikleri alabilir.
Çok atomlu iyonlar çok önemli:
- Pozitif: NH₄⁺ (amonyum), H₃O⁺ (hidronyum)
- -1 yüklü: OH⁻ (hidroksit), NO₃⁻ (nitrat), CH₃COO⁻ (asetat)
- -2 yüklü: SO₄²⁻ (sülfat), CO₃²⁻ (karbonat)
- -3 yüklü: PO₄³⁻ (fosfat)
Bu iyonları ezberlemen gerekiyor çünkü kimyasal formüllerde sürekli kullanılacaklar. Klor oksitlerinde ClO⁻ (hipoklorit), ClO₂⁻ (klorit), ClO₃⁻ (klorat) şeklinde isimler değişir.
💡 Püf nokta: Çok atomlu iyonları gruplar halinde ezberle - sülfat grubu, nitrat grubu gibi!

Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Periodic Trends
9Kimya Periyodik Sistem
Kimya Periyodik Sistem
KİMYA 9.SINIF
1.tema konu anlatımı
periyodik özelliklerin değişimi
atom yarıçapı,iyonlaşma enerjisi,elektroni ilgisi ve elektronegatiflik ile ilgili detaylı konu anlatım notları
Periyodik tabloya ait bilinmesi gerekenler
Tyt kimya periyodik tabloya ait bilinmesi gerekenler
Periyodik özellikler
9.sınıf kimya
Periyodik Özellikler
Periyodik özelliklerin değişimi.
Periyodik özellikler
11.sınıf kimya periyodik özellikler konu anlatımı
Periyodik özellikler
Ders notu
Periyodik sistem
Tyt kimya atom ve periyodik sistem, periyodik sistem kısmı
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
11. Sınıf Kimya: Modern Atom Teorisi, Periyodik Tablo ve Gazların Özellikleri
Atomun yapısını anlamak kimyanın temelini oluşturur! Bu konu, elektronların nasıl dizildiğinden atomların özelliklerine kadar birçok önemli kavramı içerir. Ayrıca gazların davranışlarını ve değerlik kavramlarını da öğreneceksin.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Yörünge, Orbital ve Kuantum Sayıları
Atomdaki elektronları anlamak için önce yörünge ve orbital arasındaki farkı bilmen gerekiyor. Yörünge elektronun varsayılan dairesel yolu, orbital ise elektronun bulunma olasılığının yüksek olduğu üç boyutlu bölgeler.
Kuantum sayıları elektronların adresini verir. Baş kuantum sayısı (n) çekirdeğe uzaklığı, açısal momentum kuantum sayısı (l) orbital şeklini belirler. Manyetik kuantum sayısı (ml) aynı tür orbitalleri ayırırken, spin kuantum sayısı (ms) elektronun dönme yönünü gösterir.
Elektron dizilimi için üç önemli kural var: Aufbau kuralı (düşük enerjiden başla), Hund kuralı (önce tek elektronlar yerleş), Pauli kuralı (aynı orbitalde zıt spinler).
💡 İpucu: Elektron dizilimi yaparken "1s² 2s² 2p⁶ 3s²..." şeklindeki sırayı ezberle!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektron Dizilimi ve İstisnalar
Elektron diziliminde n+l değeri önemlidir - bu değer arttıkça orbital enerjisi artar. Eşit n+l değerlerinde ise n'i büyük olan daha yüksek enerjili olur.
Soy gazlar (He, Ne, Ar, Kr, Xe) sayesinde kısa yazım yapabilirsin. Örneğin Fe₂₆: [Ar₁₈]4s²3d⁶ şeklinde yazılır.
Uyarılmış halda elektronlar normal kuralları bozmaya zorlanır. Bu atomlar kararsız ve yüksek enerjili olur. Krom (Cr₂₄) ve bakır (Cu₂₉) gibi elementlerde yarı kararlı ve tam kararlı dizilimler için istisnalar vardır.
İyon oluştururken elektronlar en dış katmandan verilir. Bu nedenle Fe³⁺ iyonunda önce 4s elektronları gider.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Atom Yarıçapı ve Türleri
Atomun büyüklüğünü anlamak için farklı yarıçap türleri var. Atomik yarıçap çekirdekten en dış elektrona olan uzaklık, kovalent yarıçap bağlı atomlar arası mesafenin yarısı.
Van der Waals yarıçapı bağsız atomlar için kullanılır. İyon yarıçapında önemli kural şu: elektron verilince yarıçap küçülür, alınca büyür.
Periyodik cetvelde atom yarıçapı aşağı doğru artar (yeni katman eklenir), sağa doğru azalır (proton sayısı artıp elektronları daha güçlü çeker).
Bu bilgiler atomların nasıl bağ yaptığını anlamanda çok kritik!
💡 Hatırla: X → X⁺ → X²⁺ şeklinde elektron verilirken yarıçap sürekli küçülür.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Periyodik Özellikler
Metalik özellik kolay elektron verebilme yeteneğidir. Atom yarıçapı büyük olan elementler daha metaliktir. Sol alt köşeye doğru gidildikçe metalik özellik artar.
Ametalik özellik bunun tam tersidir - kolay elektron alma yeteneği. Sağ üst köşeye doğru artar.
İyonlaşma enerjisi elektronu koparmak için gereken enerjidir. Atom yarıçapı küçüldükçe artar. Ardışık iyonlaşma enerjileri daima artar çünkü pozitif yük arttıkça elektronları tutma gücü artar.
Elektron ilgisi elektron alırken açığa çıkan enerjidir. Genelde sağa ve yukarı doğru artar ama Cl > F gibi istisnalar vardır.
💡 Önemli: Soy gazların elektron ilgisi yoktur - zaten kararlılar!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektronegatiflik ve Blok Elementleri
Elektronegatiflik atomun bağdaki elektronları kendine çekme gücüdür. En yüksek değer fluorda bulunur. Periyotta sağa, grupta yukarı doğru artar.
s blok elementleri (1A, 2A, He) en büyük yarıçaplı elementlerdir. Mineral yağda saklanırlar. 1A grubu +1, 2A grubu +2 değerlik alır.
p blok elementleri çok çeşitlidir - metal, ametal, yarımetal içerir. 7A grubu diatomik, 8A grubu tek atomlu gaz halinde bulunur.
d blok elementleri geçiş metalleridir. Sert yapıda, yüksek erime noktası, birden fazla pozitif değerlik alabilirler.
💡 Dikkat: Bağda elektronegatifliği yüksek olan taraf kısmen negatif olur!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Gazlar ve Temel Özellikler
Gazlar maddenin en düzensiz halidir. Belirli hacim ve şekilleri yoktur, sıkıştırılabilir ve akışkandırlar. Molekülleri birbirinden bağımsız hareket eder.
İdeal gazlarda moleküller arası çekim yok, molekül hacmi sıfır. Gerçek gazlarda ise moleküller arası çekim var, bu yüzden basınç idealden düşük, hacim idealden büyük.
Önemli birim dönüşümleri:
- Hacim: 1L = 1000mL = 1000cm³
- Basınç: 1atm = 760mmHg = 760torr
- Sıcaklık: K = °C + 273
Mol sayısı hesaplamaları: n = m/MA = N/NA = V/22.4 (STP'de)
💡 Neden civa kullanılır: Sıvı, renkli, yoğun, az uçucu ve gazlarla tepkime vermez!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Tek Değerlikli Elementler
Tek değerlik alan elementler kimyasal hesaplamalarda çok işine yarar. Bu elementlerin değerlikleri değişmez, bu da hesaplamaları kolaylaştırır.
+1 değerlikli: H⁺, Na⁺, K⁺, Ag⁺ gibi elementler. +2 değerlikli: Be²⁺, Mg²⁺, Ca²⁺, Zn²⁺ gibi. +3 değerlikli: Al³⁺ en önemlisi.
Negatif değerlikler: F⁻, Cl⁻, Br⁻, I⁻ (-1), O²⁻, S²⁻ (-2), N³⁻, P³⁻ (-3) şeklinde.
Karbon hem +4 hem -4 değerlik alabilir. Bu durum organik kimyada çok önemli rol oynar.
Basınç formülü: P_atm = h·d·g (h: yükseklik, d: yoğunluk, g: yerçekimi ivmesi)

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Çok Değerlikli Elementler ve İyonlar
Geçiş metalleri birden fazla değerlik alabilir. Demir Fe²⁺ ve Fe³⁺, bakır Cu⁺ ve Cu²⁺, krom Cr²⁺, Cr³⁺, Cr⁶⁺ değerlikleri alabilir.
Çok atomlu iyonlar çok önemli:
- Pozitif: NH₄⁺ (amonyum), H₃O⁺ (hidronyum)
- -1 yüklü: OH⁻ (hidroksit), NO₃⁻ (nitrat), CH₃COO⁻ (asetat)
- -2 yüklü: SO₄²⁻ (sülfat), CO₃²⁻ (karbonat)
- -3 yüklü: PO₄³⁻ (fosfat)
Bu iyonları ezberlemen gerekiyor çünkü kimyasal formüllerde sürekli kullanılacaklar. Klor oksitlerinde ClO⁻ (hipoklorit), ClO₂⁻ (klorit), ClO₃⁻ (klorat) şeklinde isimler değişir.
💡 Püf nokta: Çok atomlu iyonları gruplar halinde ezberle - sülfat grubu, nitrat grubu gibi!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Periodic Trends
9Kimya Periyodik Sistem
Kimya Periyodik Sistem
KİMYA 9.SINIF
1.tema konu anlatımı
periyodik özelliklerin değişimi
atom yarıçapı,iyonlaşma enerjisi,elektroni ilgisi ve elektronegatiflik ile ilgili detaylı konu anlatım notları
Periyodik tabloya ait bilinmesi gerekenler
Tyt kimya periyodik tabloya ait bilinmesi gerekenler
Periyodik özellikler
9.sınıf kimya
Periyodik Özellikler
Periyodik özelliklerin değişimi.
Periyodik özellikler
11.sınıf kimya periyodik özellikler konu anlatımı
Periyodik özellikler
Ders notu
Periyodik sistem
Tyt kimya atom ve periyodik sistem, periyodik sistem kısmı
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅