Kimyasal bağlar, maddelerin yapı taşları olan atomların bir arada kalmasını... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
134
•
Güncellendi May 6, 2026
•
Talha Ahmet Çopur
@ahmett
Kimyasal bağlar, maddelerin yapı taşları olan atomların bir arada kalmasını... Daha fazla göster










İyonik bağ, metal ve ametal atomları arasında elektron alışverişi sonucu oluşur. Metal atomları elektron verirken, ametal atomları elektron alır. Bu sayede her ikisi de kararlı yapıya kavuşur.
Lewis yapısı, bir elementin sembolü ve son katman elektronlarını gösteren noktalardan oluşur. Lewis yapısını bulmak için şu adımları izleriz: Önce elementin katman elektron dizilimini yazarız, element sembolünü yazarız, son katmandaki elektron sayısını buluruz ve sembolün çevresine değerlik elektron sayısı kadar nokta koyarız.
Örneğin, Flor elementi (F) için elektron dizilimi 2,7'dir. Son katmandaki elektron sayısı 7 olduğu için, F sembolünün etrafına 7 nokta yerleştirilir. Sodyum (Na) ise 2,8,1 elektron dizilimine sahiptir ve son katmanında 1 elektron vardır. Na bir katyon olduğu için elektron vereceğinden, [Na]⁺ şeklinde gösterilir.
💡 İpucu: Lewis yapıları çizerken, noktaları önce sembolün dört tarafına teker teker yerleştir. Eğer dörtten fazla nokta varsa, noktaları ikişerli olacak şekilde yerleştirmeyi unutma!

İyonik bileşikler oda koşullarında katıdırlar ve çok yüksek erime noktalarına sahiptirler. Atom yükü arttıkça erime noktaları da artar. Bu bileşikler katı haldeyken elektriği iletmezler, ancak sıvı halde veya çözeltide elektriği iletirler. Kristal örgü biçimindedirler ve molekül yapısına sahip değildirler.
İyonik bileşiklerin formülleri yazılırken önce metal iyonu (katyon), sonra ametal iyonu (anyon) yazılır. Metaldeki fazla elektron sayısı, ametal atomununun sağ alt köşesine; ametalin vereceği elektron sayısı da metalin sağ alt köşesine yazılır. İyonların yükleri eşit veya birbirinin katı ise sadeleştirme yapılır.
Örneğin, Ca²⁺ ve O²⁻ iyonları için formül şöyle yazılır: Ca²⁺ O²⁻ → Ca₂O₂ = CaO. Çaprazlama yaparken yüklerin kutupları yazılmaz.
⚠️ Dikkat: Katyon ve çok atomlu iyondan (kök) oluşan bileşiklerde, kökün altına sayı yazılacaksa kökü parantez içine almayı unutmayın! Örneğin: Mg²⁺ PO₄³⁻ → Mg₃(PO₄)₂
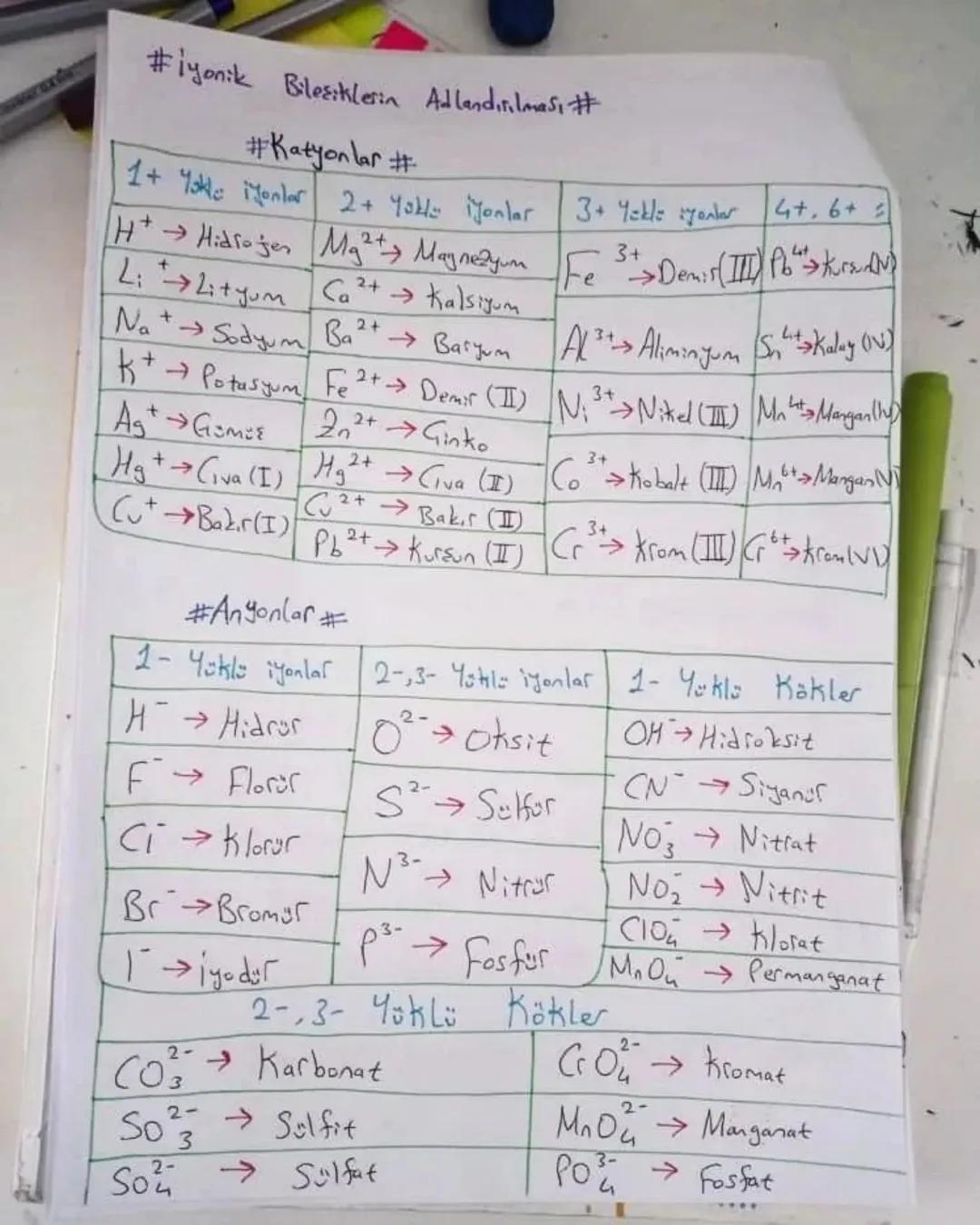
İyonik bileşikleri doğru adlandırmak için öncelikle katyonları ve anyonları tanımalıyız. Katyonlar pozitif yüklü iyonlardır ve metaller genellikle katyon oluşturur.
1+ yüklü katyonlar arasında Hidrojen (H⁺), Lityum (Li⁺), Sodyum (Na⁺) ve Potasyum (K⁺) bulunur. 2+ yüklü katyonlar arasında Magnezyum (Mg²⁺), Kalsiyum (Ca²⁺) ve Baryum (Ba²⁺) sayılabilir. Bazı metaller farklı yüklerde iyonlar oluşturabilir, örneğin Demir (Fe²⁺, Fe³⁺) veya Bakır (Cu⁺, Cu²⁺).
Anyonlar ise negatif yüklü iyonlardır. 1- yüklü anyonlar arasında Hidrür (H⁻), Florür (F⁻), Klorür (Cl⁻) ve Bromür (Br⁻) bulunur. 2- yüklü anyonlar arasında Oksit (O²⁻) ve Sülfür (S²⁻) vardır. Ayrıca, birden fazla atomdan oluşan çok atomlu iyonlar (kökler) de vardır, örneğin Hidroksit (OH⁻), Nitrat (NO₃⁻) ve Karbonat (CO₃²⁻).
💡 İpucu: Çok atomlu iyonları (kökleri) ezberlemeye çalış, çünkü bunlar bileşik adlandırmasında sıkça kullanılır. Örneğin, Sülfat (SO₄²⁻), Fosfat (PO₄³⁻) ve Nitrit (NO₂⁻).

Kovalent bağ, ametal atomları arasında elektron ortaklaşması sonucu oluşan bağdır. İyonik bağdan farklı olarak, kovalent bağda atomlar arasındaki elektronegativite farkı daha azdır. Bu nedenle bir atom elektronunu tamamen vermez, diğeri de tamamen almaz. Elektron ortaklaşa kullanılır.
Kovalent bağ iki türe ayrılır: Polar kovalent bağ ve Apolar kovalent bağ. Kovalent bağ oluştururken elementlerin değerlik elektronlarının bir kısmı bağ yapımına katılmaz. Bu elektronlara ortaklaşmamış elektron çifti denir.
H₂, O₂, CO₂, H₂O ve NH₃ gibi moleküller kovalent bağa örnek olarak verilebilir. Kök ve kök bileşiklerinin adlandırılmasında önce katyon olan kökün adı, sonra anyon olan kökün adı yazılır. Örneğin, NH₄OH (Amonyum hidroksit) veya (NH₄)₂SO₄ (Amonyum sülfat).
🔍 Önemli: Kovalent bağda, elektronları ortak kullanan atomlar "molekül" oluştururlar. İyonik bileşiklerden farklı olarak, kovalent moleküller genellikle daha düşük erime ve kaynama noktalarına sahiptir.

Bir molekülün polar veya apolar olması, moleküldeki elektron dağılımına bağlıdır. Eğer moleküldeki ortak atomda bağ yapmayan elektron çifti varsa (yani Lewis yapısında nokta varsa), yük dağılımı eşit olmadığından molekül polar olur. Eğer yoksa, molekül apolardır.
H₂O molekülünü inceleyelim. Oksijen atomunda bağ yapmayan elektron çiftleri vardır ve yük dağılımı eşit değildir, bu nedenle H₂O molekülü polardır. NH₃ molekülünde de azot atomunda bağ yapmayan elektron çiftleri vardır, dolayısıyla bu da polar bir moleküldür.
CH₄ ve N₂ moleküllerinde ise tüm elektronlar bağ yapmıştır. Yük dağılımı dengeli olduğundan bu moleküller apolardır. Cl₂ molekülünde bağ yapan elektron çifti 1 tanedir, klor atomları arasında tek bağ oluşur. Cl₂ molekülü apolar kovalent bağ içerir ve molekül apolardır.
💡 Hatırlayalım: Moleküldeki yük dağılımının nasıl olduğunu anlamak için Lewis yapısını çizmek çok yardımcı olur. Eğer merkez atomda bağ yapmayan elektron çifti varsa, molekül genellikle polardır.

Polar kovalent bağ, elektronegativitesi farklı iki ametal atomu arasında oluşur. Elektronlar iki atomda eşit dağılmaz, bu nedenle atomlarda kısmi (+) ve (-) yükler oluşur, yani kutuplar oluşur. CO₂, H₂O, NH₃, CH₄, HCl gibi bileşikler polar kovalent bağa örnektir.
Apolar kovalent bağ ise aynı iki ametal atomu arasında oluşur. Elektronlar iki atomda eşit dağılır ve kutuplar oluşmaz. H₂, N₂, O₂, F₂ gibi moleküller apolar kovalent bağa örnektir.
Kovalent bileşiklerin Lewis yapısı yazılırken, iki elektronun ortaklaşmasıyla oluşan bağ elektronları genellikle çizgi "-" ile gösterilir. Bir bileşiğin Lewis yapısı, molekülün polarlığı hakkında bilgi verir. Eğer yük molekülün tamamına eşit dağılmışsa molekül apolar, yük dağılımı her yönde aynı değilse molekül polardır.
🧪 Pratik Bilgi: Bir molekülün polar olup olmadığını anlamanın en kolay yolu, Lewis yapısını incelemek ve merkez atomda bağ yapmayan elektron çifti olup olmadığına bakmaktır. Bağ yapmayan elektron çiftleri, molekülde asimetrik yük dağılımına neden olur.

H₂O molekülünü inceleyelim: Oksijen atomu iki elektronunu iki hidrojen atomu ile ortaklaşa kullanırken, her bir hidrojen atomu birer elektronunu oksijen atomu ile ortaklaşa kullanır. Böylece aralarında tekli bağ oluşur. Oksijen atomunda iki adet ortaklaşmamış elektron çifti bulunur ve molekül polardır.
Kovalent bileşiklerin sistematik adlandırılması şu şekildedir:
Eğer 1. ametalin sayısı bir ise, Latince adı (mono) söylenmez.
Örneğin:
🔍 Bilgi: Latince sayı önekleri şunlardır: mono (1), di (2), tri (3), tetra (4), penta (5), heksa (6), hepta (7), okta (8), nona (9), deka (10). Bu önekler kovalent bileşiklerin adlandırılmasında çok önemlidir.

Metalik bağ, metal atomları arasında oluşur. Metal atomları bir arada bulunduğunda, son katmandaki elektronlar hem kendi katmanlarında hem de komşu atomların katmanlarında rahatlıkla dolaşabilirler. Elektronlar sadece kendi atomlarının çekirdeği tarafından değil, komşu atomların çekirdekleri tarafından da çekilir ve metal atomları birbirine tutunur.
Metal atomları bir araya geldiğinde, son katmandaki elektronlarını vermiş gibi davranan metal katyonları ve ortamda serbest dolaşan son katman elektronları adeta bir elektron denizi oluşturur. Bu elektron denizi ile pozitif metal iyonları arasındaki elektrostatik çekim, metalik bağ olarak adlandırılır.
Metalik bağlar metallere şu özellikleri kazandırır:
⚡ İlginç Bilgi: Metallerin iyi iletken olmasının sebebi, içerdikleri serbest elektronların rahatlıkla hareket edebilmesidir. Bu "elektron denizi" modeli, metallerin parlaklığını ve esnekliğini de açıklar.

İyonik bileşikler adlandırılırken önce katyon adı, sonra anyon adı okunur. Bu kuralları iki ana kategoride inceleyebiliriz:
1. Metal + Ametal Bileşiklerinin Adlandırılması: Metalin adı + ametal iyonunun adı yazılır. Eğer metal atomu birden fazla değerlik alabiliyorsa, adın sonuna değerlik parantez içinde Roma rakamıyla belirtilir.
Örnekler:
2. Metal + Kök Bileşiğinin Adlandırılması: Metalin adı + kök adı yazılır. Kök'ün birim sayısı "1" değilse parantez içine alınır.
Örnekler:
🔑 Unutma: Değişken değerlikli metallerin (Fe, Cu, Pb gibi) oluşturduğu bileşikleri adlandırırken, metalin değerliğini Roma rakamlarıyla belirtmelisin. Örneğin: Fe(OH)₃ → Demir (III) hidroksit.
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Talha Ahmet Çopur
@ahmett
Kimyasal bağlar, maddelerin yapı taşları olan atomların bir arada kalmasını sağlayan kuvvetlerdir. Bu konuda iyonik, kovalent ve metalik bağların özelliklerini, Lewis yapılarını ve bileşiklerin adlandırılmasını öğreneceğiz. Bu bilgiler kimyanın temelini oluşturur ve maddelerin davranışlarını anlamamıza yardımcı olur.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
İyonik bağ, metal ve ametal atomları arasında elektron alışverişi sonucu oluşur. Metal atomları elektron verirken, ametal atomları elektron alır. Bu sayede her ikisi de kararlı yapıya kavuşur.
Lewis yapısı, bir elementin sembolü ve son katman elektronlarını gösteren noktalardan oluşur. Lewis yapısını bulmak için şu adımları izleriz: Önce elementin katman elektron dizilimini yazarız, element sembolünü yazarız, son katmandaki elektron sayısını buluruz ve sembolün çevresine değerlik elektron sayısı kadar nokta koyarız.
Örneğin, Flor elementi (F) için elektron dizilimi 2,7'dir. Son katmandaki elektron sayısı 7 olduğu için, F sembolünün etrafına 7 nokta yerleştirilir. Sodyum (Na) ise 2,8,1 elektron dizilimine sahiptir ve son katmanında 1 elektron vardır. Na bir katyon olduğu için elektron vereceğinden, [Na]⁺ şeklinde gösterilir.
💡 İpucu: Lewis yapıları çizerken, noktaları önce sembolün dört tarafına teker teker yerleştir. Eğer dörtten fazla nokta varsa, noktaları ikişerli olacak şekilde yerleştirmeyi unutma!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
İyonik bileşikler oda koşullarında katıdırlar ve çok yüksek erime noktalarına sahiptirler. Atom yükü arttıkça erime noktaları da artar. Bu bileşikler katı haldeyken elektriği iletmezler, ancak sıvı halde veya çözeltide elektriği iletirler. Kristal örgü biçimindedirler ve molekül yapısına sahip değildirler.
İyonik bileşiklerin formülleri yazılırken önce metal iyonu (katyon), sonra ametal iyonu (anyon) yazılır. Metaldeki fazla elektron sayısı, ametal atomununun sağ alt köşesine; ametalin vereceği elektron sayısı da metalin sağ alt köşesine yazılır. İyonların yükleri eşit veya birbirinin katı ise sadeleştirme yapılır.
Örneğin, Ca²⁺ ve O²⁻ iyonları için formül şöyle yazılır: Ca²⁺ O²⁻ → Ca₂O₂ = CaO. Çaprazlama yaparken yüklerin kutupları yazılmaz.
⚠️ Dikkat: Katyon ve çok atomlu iyondan (kök) oluşan bileşiklerde, kökün altına sayı yazılacaksa kökü parantez içine almayı unutmayın! Örneğin: Mg²⁺ PO₄³⁻ → Mg₃(PO₄)₂

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
İyonik bileşikleri doğru adlandırmak için öncelikle katyonları ve anyonları tanımalıyız. Katyonlar pozitif yüklü iyonlardır ve metaller genellikle katyon oluşturur.
1+ yüklü katyonlar arasında Hidrojen (H⁺), Lityum (Li⁺), Sodyum (Na⁺) ve Potasyum (K⁺) bulunur. 2+ yüklü katyonlar arasında Magnezyum (Mg²⁺), Kalsiyum (Ca²⁺) ve Baryum (Ba²⁺) sayılabilir. Bazı metaller farklı yüklerde iyonlar oluşturabilir, örneğin Demir (Fe²⁺, Fe³⁺) veya Bakır (Cu⁺, Cu²⁺).
Anyonlar ise negatif yüklü iyonlardır. 1- yüklü anyonlar arasında Hidrür (H⁻), Florür (F⁻), Klorür (Cl⁻) ve Bromür (Br⁻) bulunur. 2- yüklü anyonlar arasında Oksit (O²⁻) ve Sülfür (S²⁻) vardır. Ayrıca, birden fazla atomdan oluşan çok atomlu iyonlar (kökler) de vardır, örneğin Hidroksit (OH⁻), Nitrat (NO₃⁻) ve Karbonat (CO₃²⁻).
💡 İpucu: Çok atomlu iyonları (kökleri) ezberlemeye çalış, çünkü bunlar bileşik adlandırmasında sıkça kullanılır. Örneğin, Sülfat (SO₄²⁻), Fosfat (PO₄³⁻) ve Nitrit (NO₂⁻).

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kovalent bağ, ametal atomları arasında elektron ortaklaşması sonucu oluşan bağdır. İyonik bağdan farklı olarak, kovalent bağda atomlar arasındaki elektronegativite farkı daha azdır. Bu nedenle bir atom elektronunu tamamen vermez, diğeri de tamamen almaz. Elektron ortaklaşa kullanılır.
Kovalent bağ iki türe ayrılır: Polar kovalent bağ ve Apolar kovalent bağ. Kovalent bağ oluştururken elementlerin değerlik elektronlarının bir kısmı bağ yapımına katılmaz. Bu elektronlara ortaklaşmamış elektron çifti denir.
H₂, O₂, CO₂, H₂O ve NH₃ gibi moleküller kovalent bağa örnek olarak verilebilir. Kök ve kök bileşiklerinin adlandırılmasında önce katyon olan kökün adı, sonra anyon olan kökün adı yazılır. Örneğin, NH₄OH (Amonyum hidroksit) veya (NH₄)₂SO₄ (Amonyum sülfat).
🔍 Önemli: Kovalent bağda, elektronları ortak kullanan atomlar "molekül" oluştururlar. İyonik bileşiklerden farklı olarak, kovalent moleküller genellikle daha düşük erime ve kaynama noktalarına sahiptir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bir molekülün polar veya apolar olması, moleküldeki elektron dağılımına bağlıdır. Eğer moleküldeki ortak atomda bağ yapmayan elektron çifti varsa (yani Lewis yapısında nokta varsa), yük dağılımı eşit olmadığından molekül polar olur. Eğer yoksa, molekül apolardır.
H₂O molekülünü inceleyelim. Oksijen atomunda bağ yapmayan elektron çiftleri vardır ve yük dağılımı eşit değildir, bu nedenle H₂O molekülü polardır. NH₃ molekülünde de azot atomunda bağ yapmayan elektron çiftleri vardır, dolayısıyla bu da polar bir moleküldür.
CH₄ ve N₂ moleküllerinde ise tüm elektronlar bağ yapmıştır. Yük dağılımı dengeli olduğundan bu moleküller apolardır. Cl₂ molekülünde bağ yapan elektron çifti 1 tanedir, klor atomları arasında tek bağ oluşur. Cl₂ molekülü apolar kovalent bağ içerir ve molekül apolardır.
💡 Hatırlayalım: Moleküldeki yük dağılımının nasıl olduğunu anlamak için Lewis yapısını çizmek çok yardımcı olur. Eğer merkez atomda bağ yapmayan elektron çifti varsa, molekül genellikle polardır.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Polar kovalent bağ, elektronegativitesi farklı iki ametal atomu arasında oluşur. Elektronlar iki atomda eşit dağılmaz, bu nedenle atomlarda kısmi (+) ve (-) yükler oluşur, yani kutuplar oluşur. CO₂, H₂O, NH₃, CH₄, HCl gibi bileşikler polar kovalent bağa örnektir.
Apolar kovalent bağ ise aynı iki ametal atomu arasında oluşur. Elektronlar iki atomda eşit dağılır ve kutuplar oluşmaz. H₂, N₂, O₂, F₂ gibi moleküller apolar kovalent bağa örnektir.
Kovalent bileşiklerin Lewis yapısı yazılırken, iki elektronun ortaklaşmasıyla oluşan bağ elektronları genellikle çizgi "-" ile gösterilir. Bir bileşiğin Lewis yapısı, molekülün polarlığı hakkında bilgi verir. Eğer yük molekülün tamamına eşit dağılmışsa molekül apolar, yük dağılımı her yönde aynı değilse molekül polardır.
🧪 Pratik Bilgi: Bir molekülün polar olup olmadığını anlamanın en kolay yolu, Lewis yapısını incelemek ve merkez atomda bağ yapmayan elektron çifti olup olmadığına bakmaktır. Bağ yapmayan elektron çiftleri, molekülde asimetrik yük dağılımına neden olur.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
H₂O molekülünü inceleyelim: Oksijen atomu iki elektronunu iki hidrojen atomu ile ortaklaşa kullanırken, her bir hidrojen atomu birer elektronunu oksijen atomu ile ortaklaşa kullanır. Böylece aralarında tekli bağ oluşur. Oksijen atomunda iki adet ortaklaşmamış elektron çifti bulunur ve molekül polardır.
Kovalent bileşiklerin sistematik adlandırılması şu şekildedir:
Eğer 1. ametalin sayısı bir ise, Latince adı (mono) söylenmez.
Örneğin:
🔍 Bilgi: Latince sayı önekleri şunlardır: mono (1), di (2), tri (3), tetra (4), penta (5), heksa (6), hepta (7), okta (8), nona (9), deka (10). Bu önekler kovalent bileşiklerin adlandırılmasında çok önemlidir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Metalik bağ, metal atomları arasında oluşur. Metal atomları bir arada bulunduğunda, son katmandaki elektronlar hem kendi katmanlarında hem de komşu atomların katmanlarında rahatlıkla dolaşabilirler. Elektronlar sadece kendi atomlarının çekirdeği tarafından değil, komşu atomların çekirdekleri tarafından da çekilir ve metal atomları birbirine tutunur.
Metal atomları bir araya geldiğinde, son katmandaki elektronlarını vermiş gibi davranan metal katyonları ve ortamda serbest dolaşan son katman elektronları adeta bir elektron denizi oluşturur. Bu elektron denizi ile pozitif metal iyonları arasındaki elektrostatik çekim, metalik bağ olarak adlandırılır.
Metalik bağlar metallere şu özellikleri kazandırır:
⚡ İlginç Bilgi: Metallerin iyi iletken olmasının sebebi, içerdikleri serbest elektronların rahatlıkla hareket edebilmesidir. Bu "elektron denizi" modeli, metallerin parlaklığını ve esnekliğini de açıklar.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
İyonik bileşikler adlandırılırken önce katyon adı, sonra anyon adı okunur. Bu kuralları iki ana kategoride inceleyebiliriz:
1. Metal + Ametal Bileşiklerinin Adlandırılması: Metalin adı + ametal iyonunun adı yazılır. Eğer metal atomu birden fazla değerlik alabiliyorsa, adın sonuna değerlik parantez içinde Roma rakamıyla belirtilir.
Örnekler:
2. Metal + Kök Bileşiğinin Adlandırılması: Metalin adı + kök adı yazılır. Kök'ün birim sayısı "1" değilse parantez içine alınır.
Örnekler:
🔑 Unutma: Değişken değerlikli metallerin (Fe, Cu, Pb gibi) oluşturduğu bileşikleri adlandırırken, metalin değerliğini Roma rakamlarıyla belirtmelisin. Örneğin: Fe(OH)₃ → Demir (III) hidroksit.
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
2
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı