Elektrokimya, kimyasal enerjiyi elektrik enerjisine dönüştüren süreçleri inceleyen bir bilim... Daha fazla göster
AYT Kimya 12. Sınıf Elektrokimya Konu Anlatımı








Redoks Tepkimelerinin Denkleştirilmesi
Redoks tepkimelerini anlamak elektrokimyanın temelini oluşturuyor. Bu tepkimelerde elektronlar bir elementten diğerine transfer oluyor.
Redoks tepkimesi olup olmadığını anlamak için şu yöntemi kullan: Tepkimedeki tüm elementlerin yüklerini bul. Giren ve çıkan şekilde elementlere bak - en az birinin yükü değişmişse redokstır.
Yükseltgenme basamakları grup numaralarına göre belirleniyor. 1A grubu +1, 2A grubu +2, 7A grubu -1/+7 yüklerini alabilir. Bu temel kuralları ezberlemen gerekiyor.
💡 İpucu: Element halinde bir madde varsa kesinlikle redoks tepkimesidir!

Yük Basamağı Kuralları
Yük hesaplamalarında kullanacağın temel kurallar var. Oksijen genellikle -2 yükü alır . Tek başına elementlerin yükü her zaman 0'dır.
Bileşiklerin toplam yükü sıfırdır. Önemli kökler: NO₃⁻ (nitrat) -1, PO₄³⁻ (fosfat) -3, SO₄²⁻ (sülfat) -2, CO₃²⁻ (karbonat) -2, NH₄⁺ (amonyum) +1.
Redoks tepkimelerinin denkleştirilmesinde hangi maddenin elektron verdiğini ve aldığını bul. Elektron veren yükseltgenir (yükü artar), elektron alan indirgenir (yükü azalır).
💡 Hatırla: İndirgenen madde, diğerini yükseltgeyendir!

Redoks Denkleştirme Tipleri
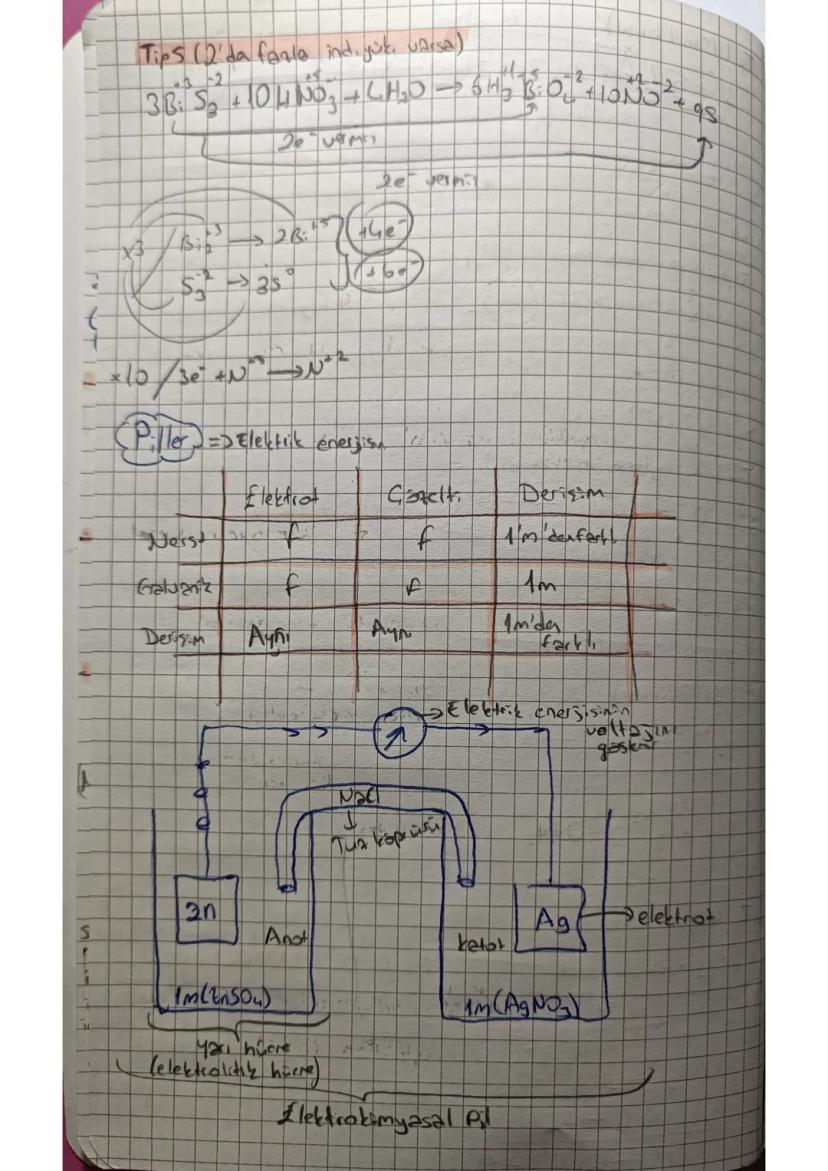
Redoks denkleştirmede farklı tipler var. Tip 1 (basit): Sadece elektron transferini dengeleyerek çöz. Tip 2: Asit ortamda H⁺ ve H₂O ekleyerek denkleştir.
Tip 3: Katsayılara dikkat et ve elektron dengesini sağla. Her zaman elektron veren ve alan miktarları eşit olmalı.
Denkleştirirken önce redoks olan elementleri bul, sonra elektron transferini hesapla. Elektronları eşitlemek için uygun katsayıları kullan.
💡 Püf Noktası: Elektron sayıları eşit olana kadar katsayıları ayarla!
Elektrokimyasal Piller - Temel Kavramlar
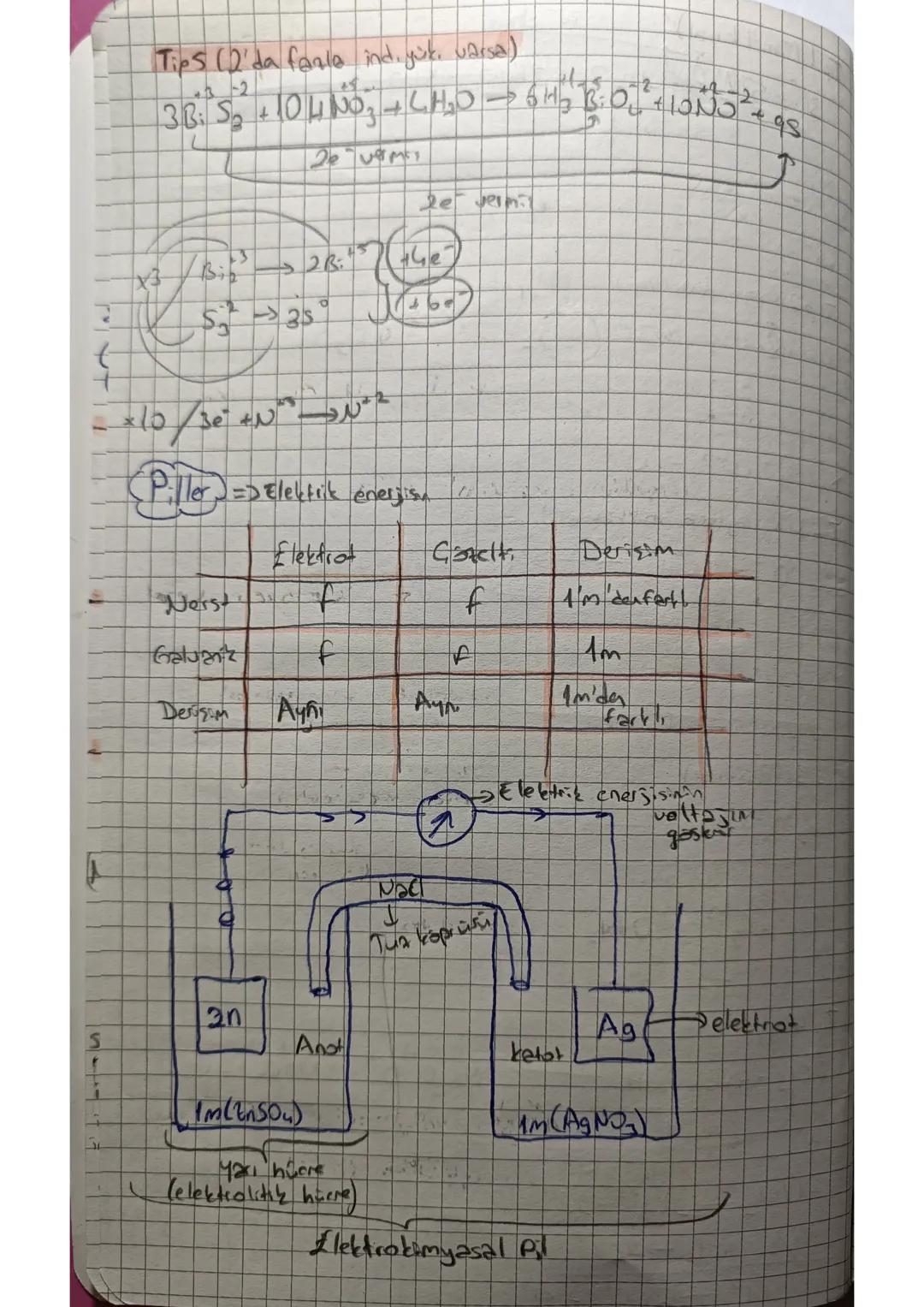
Elektrokimyasal piller kimyasal enerjiyi elektrik enerjisine dönüştürür. İki yarı hücreden oluşur ve tuz köprüsü ile bağlanır.
Elektrotlar önemli: Anot (yükseltgenme olur), Katot (indirgenme olur). Elektronlar her zaman anotan katoda doğru akar.
Galvanik pil kendiliğinden çalışır ve elektrik üretir. İçindeki redoks tepkimeleri sayesinde sürekli elektron akışı sağlar.
💡 Akılda Tut: AnOt = Oksitlenme (yükseltgenme), Red Cat = Redüksiyon (indirgenme)!

Pil Potansiyeli ve Elektrot Belirleme
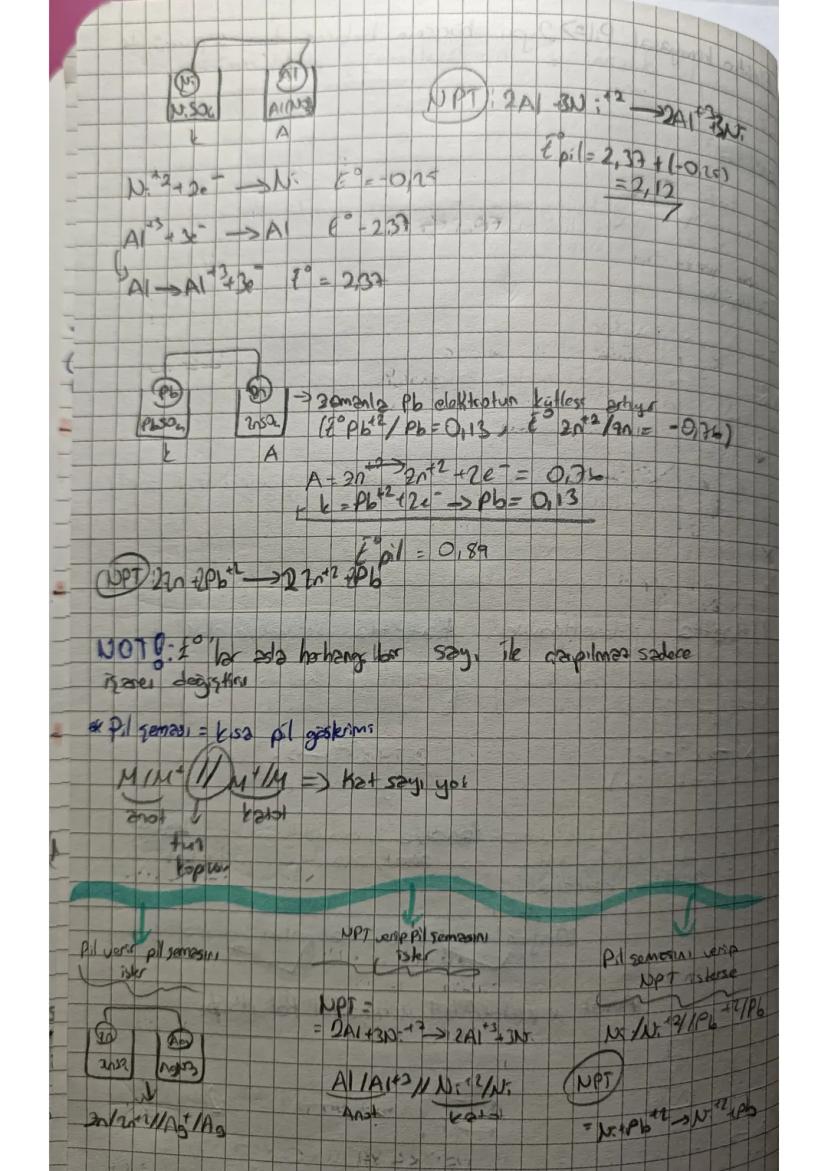
Standart potansiyeller (E°) ile hangi elektrodun anot/katot olacağını belirleyebilirsin. Daha düşük potansiyelli elektrot anot olur.
Pilin yönünü belirlemek için şu ipuçlarını kullan: Kütlesi azalan elektrot anot, kütlesi artan katot. Katyonlar katoda, anyonlar anoda gider.
NPT (Normal Potansiyel Tablosu) kullanarak pil potansiyelini hesapla: E°pil = E°katot - E°anot. Pozitif değer çıkarsa pil kendiliğinden çalışır.
💡 Formül: Her zaman E° değerleri toplanmaz, sadece elektron sayısı artırılır!
Pil Hesaplamaları ve Şemalar
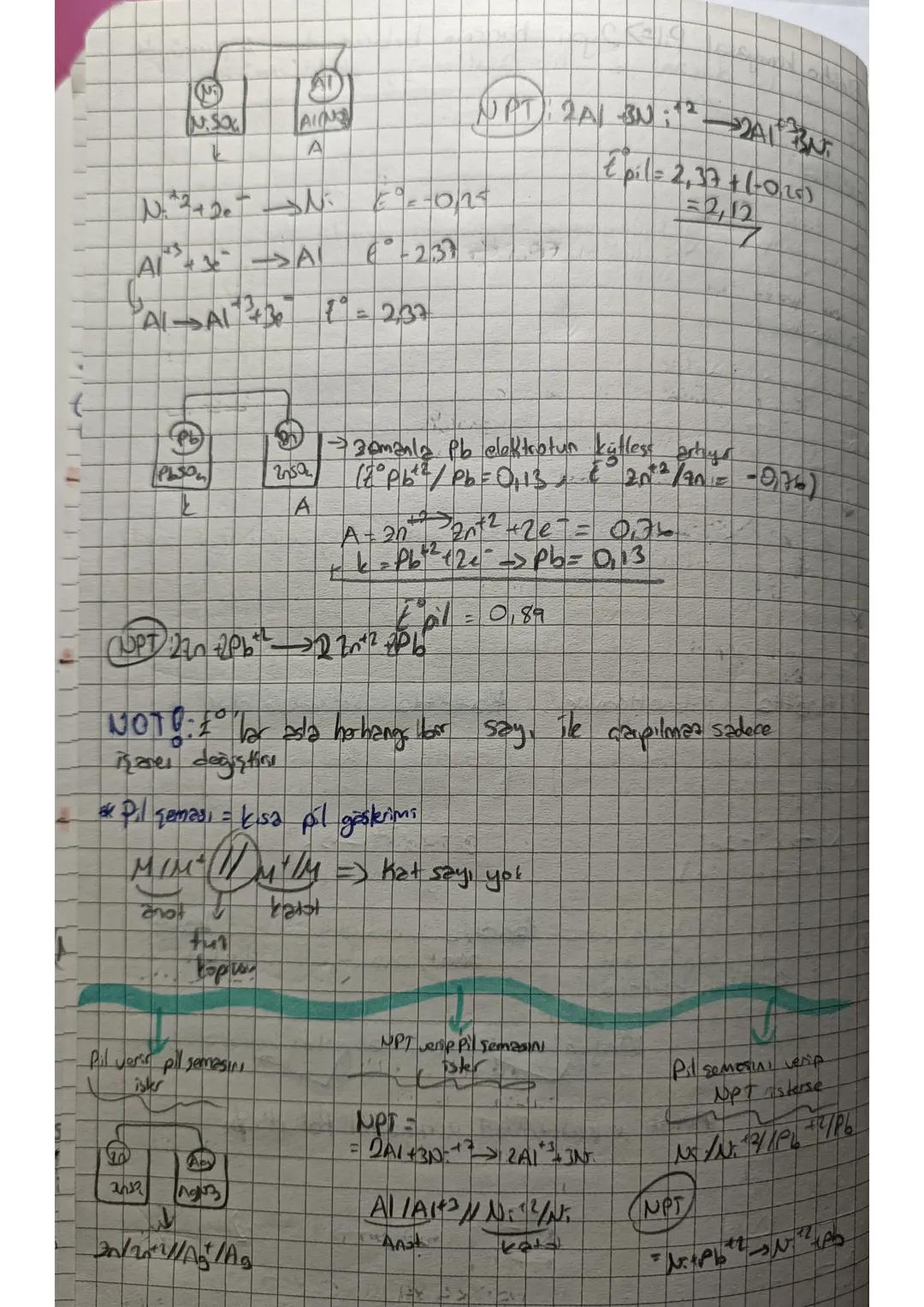
Pil potansiyeli hesaplarken E° değerlerini doğru kullan. E°pil = E°katot - E°anot formülü her zaman geçerli.
Pil şeması yazarken: Anot | Anot çözeltisi || Katot çözeltisi | Katot şeklinde yaz. Çift çizgi tuz köprüsünü gösterir.
NPT tablosunu kullanarak hangi metalin daha kolay yükseltgeneceğini belirleyebilirsin. Düşük potansiyelli metaller daha kolay elektron verir.
💡 Dikkat: Pil şemasında elektron akış yönünü doğru belirlemeyi unutma!

Pil Potansiyeline Etki Eden Faktörler
Sıcaklık ve derişim pil potansiyelini etkiler. Derişim arttıkça o elektrodun potansiyeli değişir. Elektrodun büyüklüğü potansiyeli etkilemez.
Denge prensibi ile sıcaklık etkisini anlayabilirsin. Tepkime endotermikse sıcaklık artışı potansiyeli artırır, eksotermikse azaltır.
Derişim azalırsa o elektrodun potansiyeli azalır. Su eklersen derişim düşer, tuz eklersen artar. Bu da pil potansiyelini değiştirir.
💡 Pratik Kural: Derişim azalırsa potansiyel azalır, artar artar!

Derişim Pilleri
Derişim pilleri aynı elektrotlardan oluşur ama farklı derişimlerde çözelti içerir. Derişimi az olan anot, fazla olan katot olur.
Derişim pilini çalıştırmak için: Anota su ekle (derişimi azalt) veya katota tuz ekle (derişimi artır). Bu potansiyel farkını artırır.
Çalışmayan pili aktifleştirmek için derişim farkı oluşturman gerekiyor. Makas açılıyorsa potansiyel artıyor, kapanıyorsa azalıyor.
💡 Makas Taktiği: Derişim farkı artırarak pil potansiyelini kontrol edebilirsin!

Nernst Denklemi ve Saf Su Elektrolizi
Nernst denklemi ile NPT dışı koşullarda pil potansiyelini hesapla: E = E° - × log. Bu formül derişim etkisini gösterir.
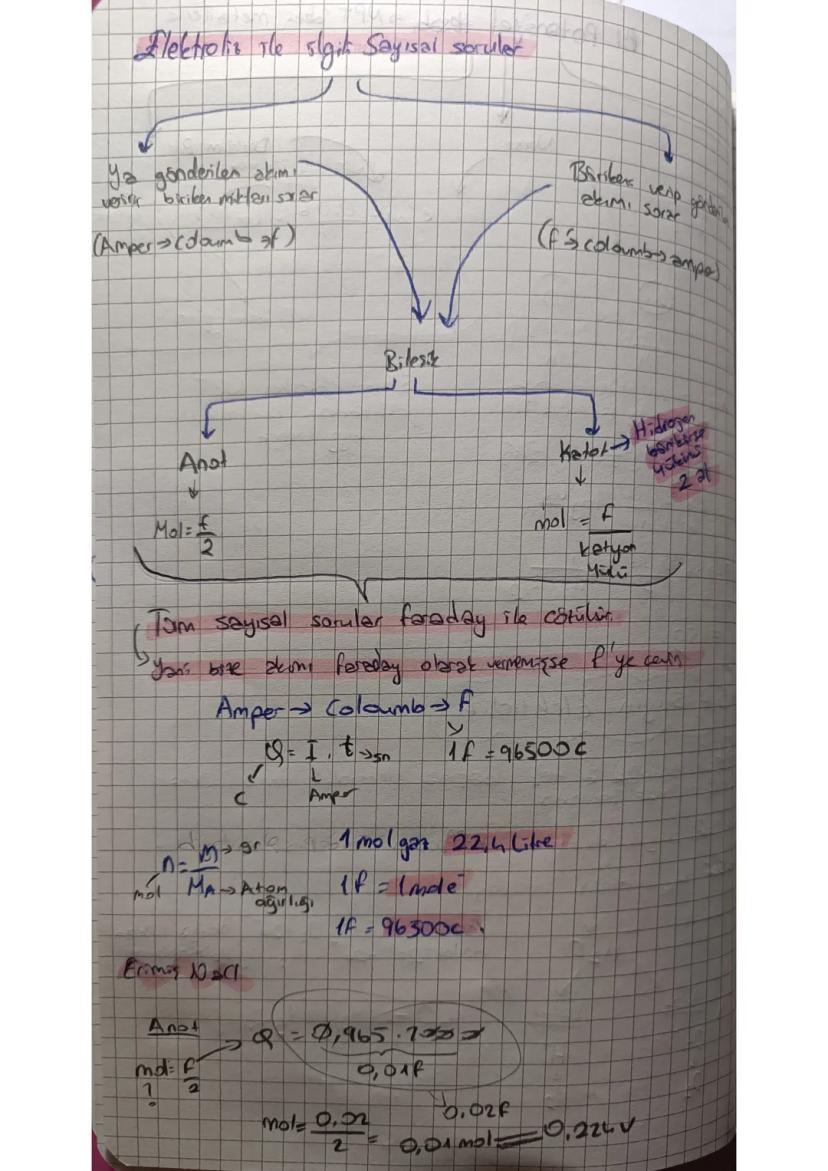
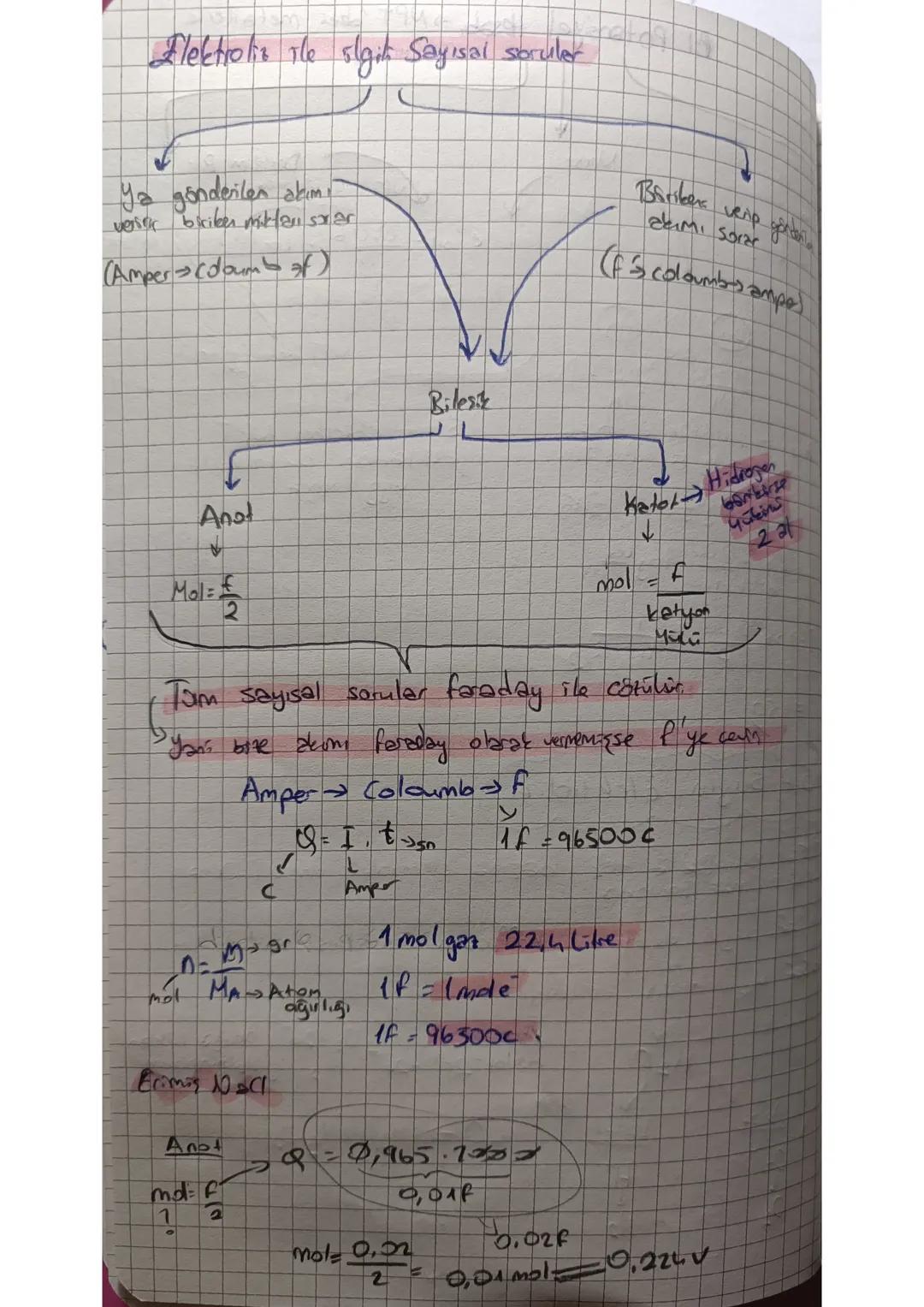
Saf su elektrolizi için asidik ortam şart. Hoffmann voltmetresi kullanılır. Anotta oksijen, katotta hidrojen çıkar.
Elektrolizde çıkan gaz hacimlerinin oranı önemli: H₂ : O₂ = 2 : 1. Bu oran su molekülünün yapısından kaynaklanıyor.
💡 Elektroliz: Elektrik enerjisini kimyasal enerjiye dönüştürme işlemi!
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Electrochemical Cells
4Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
AYT Kimya 12. Sınıf Elektrokimya Konu Anlatımı
Elektrokimya, kimyasal enerjiyi elektrik enerjisine dönüştüren süreçleri inceleyen bir bilim dalı. Günlük hayatımızdaki pillerden elektroliz işlemlerine kadar birçok teknolojinin temelidir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Redoks Tepkimelerinin Denkleştirilmesi
Redoks tepkimelerini anlamak elektrokimyanın temelini oluşturuyor. Bu tepkimelerde elektronlar bir elementten diğerine transfer oluyor.
Redoks tepkimesi olup olmadığını anlamak için şu yöntemi kullan: Tepkimedeki tüm elementlerin yüklerini bul. Giren ve çıkan şekilde elementlere bak - en az birinin yükü değişmişse redokstır.
Yükseltgenme basamakları grup numaralarına göre belirleniyor. 1A grubu +1, 2A grubu +2, 7A grubu -1/+7 yüklerini alabilir. Bu temel kuralları ezberlemen gerekiyor.
💡 İpucu: Element halinde bir madde varsa kesinlikle redoks tepkimesidir!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Yük Basamağı Kuralları
Yük hesaplamalarında kullanacağın temel kurallar var. Oksijen genellikle -2 yükü alır . Tek başına elementlerin yükü her zaman 0'dır.
Bileşiklerin toplam yükü sıfırdır. Önemli kökler: NO₃⁻ (nitrat) -1, PO₄³⁻ (fosfat) -3, SO₄²⁻ (sülfat) -2, CO₃²⁻ (karbonat) -2, NH₄⁺ (amonyum) +1.
Redoks tepkimelerinin denkleştirilmesinde hangi maddenin elektron verdiğini ve aldığını bul. Elektron veren yükseltgenir (yükü artar), elektron alan indirgenir (yükü azalır).
💡 Hatırla: İndirgenen madde, diğerini yükseltgeyendir!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Redoks Denkleştirme Tipleri
Redoks denkleştirmede farklı tipler var. Tip 1 (basit): Sadece elektron transferini dengeleyerek çöz. Tip 2: Asit ortamda H⁺ ve H₂O ekleyerek denkleştir.
Tip 3: Katsayılara dikkat et ve elektron dengesini sağla. Her zaman elektron veren ve alan miktarları eşit olmalı.
Denkleştirirken önce redoks olan elementleri bul, sonra elektron transferini hesapla. Elektronları eşitlemek için uygun katsayıları kullan.
💡 Püf Noktası: Elektron sayıları eşit olana kadar katsayıları ayarla!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektrokimyasal Piller - Temel Kavramlar
Elektrokimyasal piller kimyasal enerjiyi elektrik enerjisine dönüştürür. İki yarı hücreden oluşur ve tuz köprüsü ile bağlanır.
Elektrotlar önemli: Anot (yükseltgenme olur), Katot (indirgenme olur). Elektronlar her zaman anotan katoda doğru akar.
Galvanik pil kendiliğinden çalışır ve elektrik üretir. İçindeki redoks tepkimeleri sayesinde sürekli elektron akışı sağlar.
💡 Akılda Tut: AnOt = Oksitlenme (yükseltgenme), Red Cat = Redüksiyon (indirgenme)!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Pil Potansiyeli ve Elektrot Belirleme
Standart potansiyeller (E°) ile hangi elektrodun anot/katot olacağını belirleyebilirsin. Daha düşük potansiyelli elektrot anot olur.
Pilin yönünü belirlemek için şu ipuçlarını kullan: Kütlesi azalan elektrot anot, kütlesi artan katot. Katyonlar katoda, anyonlar anoda gider.
NPT (Normal Potansiyel Tablosu) kullanarak pil potansiyelini hesapla: E°pil = E°katot - E°anot. Pozitif değer çıkarsa pil kendiliğinden çalışır.
💡 Formül: Her zaman E° değerleri toplanmaz, sadece elektron sayısı artırılır!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Pil Hesaplamaları ve Şemalar
Pil potansiyeli hesaplarken E° değerlerini doğru kullan. E°pil = E°katot - E°anot formülü her zaman geçerli.
Pil şeması yazarken: Anot | Anot çözeltisi || Katot çözeltisi | Katot şeklinde yaz. Çift çizgi tuz köprüsünü gösterir.
NPT tablosunu kullanarak hangi metalin daha kolay yükseltgeneceğini belirleyebilirsin. Düşük potansiyelli metaller daha kolay elektron verir.
💡 Dikkat: Pil şemasında elektron akış yönünü doğru belirlemeyi unutma!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Pil Potansiyeline Etki Eden Faktörler
Sıcaklık ve derişim pil potansiyelini etkiler. Derişim arttıkça o elektrodun potansiyeli değişir. Elektrodun büyüklüğü potansiyeli etkilemez.
Denge prensibi ile sıcaklık etkisini anlayabilirsin. Tepkime endotermikse sıcaklık artışı potansiyeli artırır, eksotermikse azaltır.
Derişim azalırsa o elektrodun potansiyeli azalır. Su eklersen derişim düşer, tuz eklersen artar. Bu da pil potansiyelini değiştirir.
💡 Pratik Kural: Derişim azalırsa potansiyel azalır, artar artar!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Derişim Pilleri
Derişim pilleri aynı elektrotlardan oluşur ama farklı derişimlerde çözelti içerir. Derişimi az olan anot, fazla olan katot olur.
Derişim pilini çalıştırmak için: Anota su ekle (derişimi azalt) veya katota tuz ekle (derişimi artır). Bu potansiyel farkını artırır.
Çalışmayan pili aktifleştirmek için derişim farkı oluşturman gerekiyor. Makas açılıyorsa potansiyel artıyor, kapanıyorsa azalıyor.
💡 Makas Taktiği: Derişim farkı artırarak pil potansiyelini kontrol edebilirsin!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Nernst Denklemi ve Saf Su Elektrolizi
Nernst denklemi ile NPT dışı koşullarda pil potansiyelini hesapla: E = E° - × log. Bu formül derişim etkisini gösterir.
Saf su elektrolizi için asidik ortam şart. Hoffmann voltmetresi kullanılır. Anotta oksijen, katotta hidrojen çıkar.
Elektrolizde çıkan gaz hacimlerinin oranı önemli: H₂ : O₂ = 2 : 1. Bu oran su molekülünün yapısından kaynaklanıyor.
💡 Elektroliz: Elektrik enerjisini kimyasal enerjiye dönüştürme işlemi!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Electrochemical Cells
4Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅