Kimyanın temelini oluşturan atom yapısı, TYT'de karşınıza mutlaka çıkacak konulardan... Daha fazla göster
Atomun Yapısı: TYT Kimya 2. Konu Anlatımı















TYT Atom Yapısı - Giriş ve Sınav Analizi
TYT'de atom yapısı konusu her yıl karşınıza çıkan temel konulardan biri. Son 5 yıla baktığımızda, bu konudan toplam 4 soru sorulmuş - bu da konunun ne kadar önemli olduğunu gösteriyor.
Bu konu kimyanın alfabesi gibi düşünebilirsiniz. Atom konusunu iyi kavramazsanız, periyodik sistem, mol kavramı, kimyasal türler arası etkileşimler gibi diğer konularda ciddi sıkıntılar yaşarsınız. Bazı yıllarda direkt soru çıkmasa bile, diğer konuların içinde mutlaka sorulur.
Konunun %100'ü atomun yapısı başlığı altında toplanmış, atom modelleri kısmından hiç soru gelmemiş. Bu da çalışırken hangi bölümlere odaklanacağınızı gösteriyor.
💡 İpucu: Bu konu ezber değil, öğrenilecek bir konu. Mantığını kavradığınızda hem kolay hem de eğlenceli hale geliyor.

Atom Modelleri - Dalton ve Thomson
Dalton Atom Modeli kimya tarihinin ilk bilimsel atom teorisi. Dalton'a göre maddeler atom denen küçük taneciklerden oluşur ve atomlar kimyasal tepkimelerde parçalanamaz, bölünemez.
Dalton'un temel fikirleri: Atomlar içi dolu küre şeklinde, aynı elementin tüm atomları özdeş, farklı elementlerin atomları farklı. Farklı element atomlarının belirli oranlarda birleşmesiyle bileşikler oluşur.
Thomson Atom Modeli ise elektronu keşfettikten sonra geliştirildi. Thomson'a göre atom, pozitif yüklü bir küre içinde elektronların homojen dağıldığı "üzümlü kek" gibi bir yapıya sahip. Atomdaki negatif yük sayısı pozitif yük sayısına eşit olduğu için atom nötrdür.
Her iki modelin de eksiklikleri var: Dalton atom altı parçacıkları bulamadı, atomların nükleer olaylarda parçalanabileceğini bilmiyordu. Thomson ise yüklerin atomda homojen dağılmadığını açıklayamadı.
💡 Not: Günümüzde Dalton'un sadece "farklı elementlerin belirli oranda birleşmesi" fikri geçerliliğini koruyor.

Rutherford ve Bohr Atom Modelleri
Rutherford altın levha deneyiyle atomun yapısını çözdü. Alfa ışınlarının çoğu altın levhadan geçti, bazıları saptı, çok azı geri döndü. Bundan atomun büyük kısmının boş olduğunu, pozitif yükün küçük bir bölgede (çekirdek) toplandığını anladı.
Rutherford'a göre çekirdek çapı yaklaşık 10⁻¹²-10⁻¹³ cm, elektronlar bu boşlukta çekirdek etrafında döner. Çekirdekteki pozitif yük miktarı elemanı belirler. Çekirdekte kütlesi pozitif yük kütlesine eşit yüksüz tanecikler (nötron) de bulunur.
Bohr Atom Modeli ise elektronların davranışını açıkladı. Elektronlar çekirdekten belirli uzaklıklarda, belirli enerjiye sahip yörüngelerde (enerji düzeyleri) bulunur. Bu düzeyler n=1,2,3... veya K,L,M,N... ile gösterilir.
Elektronun dışarıdan enerji alıp daha yüksek enerji düzeyine geçmesine uyarılma denir. Uyarılmış atom kararsızdir, elektron temel hâle geçerken yörüngeler arası enerji farkına denk ışıma yapar.
⚡ Dikkat: Bohr sadece tek elektronlu atomları (H, He⁺, Li²⁺) açıklayabildi, çok elektronlularda yetersiz kaldı.

Bohr Modeli Soruları ve Çözüm Teknikleri
Bohr modelinin temel özellikleri sınavda sık sorulur. Elektronlar belirli enerji düzeylerinde bulunur, dışarıdan enerji alarak uyarılır ve daha sonra ışın yayarak temel hâle döner.
Soruları çözerken şu noktaları unutmayın: Dalton modelinde günümüzde geçerli olan sadece "farklı elementlerin belirli oranda birleşmesi" kuralı. Thomson "üzümlü kek" modelini geliştirdi, Rutherford çekirdekli atom modelini.
Atom modelleri kronolojik sırası: Dalton → Thomson → Rutherford → Bohr. Her model bir öncekinin eksiklerini gidermeye çalışmış ama yeni eksiklikleri de ortaya çıkmış.
Önemli ayrım: Orbital kavramı Bohr'da değil, modern atom teorisinde var. Bohr'da sadece yörünge kavramı var, orbital farklı bir şey.
🎯 Sınav İpucu: Soruları çözerken hangi modelin hangi özelliğini savunduğunu karıştırmamaya dikkat edin. Her modelin kendine özgü eksiklikleri var.

Rutherford Altın Levha Deneyi ve Model Karşılaştırmaları
Rutherford'un altın levha deneyi atom yapısını anlamamızı sağlayan kritik deney. Pozitif yüklü alfa tanecikleri altın levhaya gönderilir, çoğu geçer, bazıları sapar, çok azı geri döner.
Deneyin sonuçları: Atomun büyük kısmı boş, pozitif yük küçük bir bölgede (çekirdek) toplanmış, protonlar atom kütlesinin yaklaşık yarısını oluşturuyor. Dikkat edin, bu deneyle nötronların varlığı gözlemlenemez çünkü nötronlar yüksüz.
Atom modelleri kronolojik sırası: Dalton (atom bölünmez küre) → Thomson (üzümlü kek, yüklerin eşit dağılımı) → Rutherford (çekirdekli model) → Bohr (enerji düzeyleri).
Soruları çözerken modellerin özelliklerini karıştırmayın: Yörünge kavramı ilk kez Bohr'da, çekirdek kavramı Rutherford'da ortaya çıktı. Thomson yüksüz taneciklerden değil, pozitif-negatif yüklerin dağılımından bahsetti.
⚠️ Dikkat: Soru çözümlerinde dallanmış ağaç sorularında adım adım ilerleyin, aceleci davranmayın.

Modern Atom Teorisi ve Temel Tanecikler
Modern atom teorisine göre atom, bir elementin tüm özelliklerini taşıyan en küçük tanecik. Atomun yapısında proton, nötron, elektron gibi atom altı tanecikler bulunur.
Proton çekirdekte bulunan pozitif yüklü tanecik (kütlesi 1,673×10⁻²⁴ g), nötron çekirdekte bulunan yüksüz tanecik (kütlesi 1,675×10⁻²⁴ g). Elektron çekirdek etrafında bulunan negatif yüklü tanecik (kütlesi 9,109×10⁻²⁸ g).
Elektronun kütlesi proton veya nötronun 1/1836'sı kadar küçük. Bu yüzden atomun kütlesi neredeyse tamamen çekirdekte toplanmış. Çekirdeğin hacmi atomun hacminin yanında çok küçük.
Atom numarası proton sayısını, kütle numarası proton+nötron toplamını gösterir. Bir elementin cinsini proton sayısı belirler. Kimyasal özellik proton ve elektrona, fiziksel özellik her şeye bağlıdır.
📝 Formül: Nötron sayısı = Kütle numarası - Atom numarası

İyon Kavramı ve Hesaplamalar
İyon yüklü taneciğe denir. Kimyasal olaylarda proton alınıp verilmez, atomun yüklenmesi sadece elektron alışverişi ile olur. Elektron alan tanecik negatif, elektron veren tanecik pozitif yüklenir.
Katyon pozitif yüklü iyon (elektron vermiş), anyon negatif yüklü iyon (elektron almış). İyon yükü = Proton sayısı - Elektron sayısı formülüyle hesaplanır.
Soruları çözerken semboldeki konumları ezberleyin: Sol üstte kütle numarası, sol altta atom numarası, sağ üstte iyon yükü. Tüm oksijen taneciklerinde proton sayısı aynı, tüm oksijen atomlarında elektron sayısı aynı.
X²⁻ → X¹⁺ dönüşümünde elektron sayısı azalır, iyon yükü artar ama proton sayısı ve çekirdek yükü değişmez. Grafik sorularında proton-elektron ilişkisine dikkat edin.
⚡ Püf Nokta: İyon yükü pozitifse elektron eksilmiş, negatifse elektron fazlalığı var.
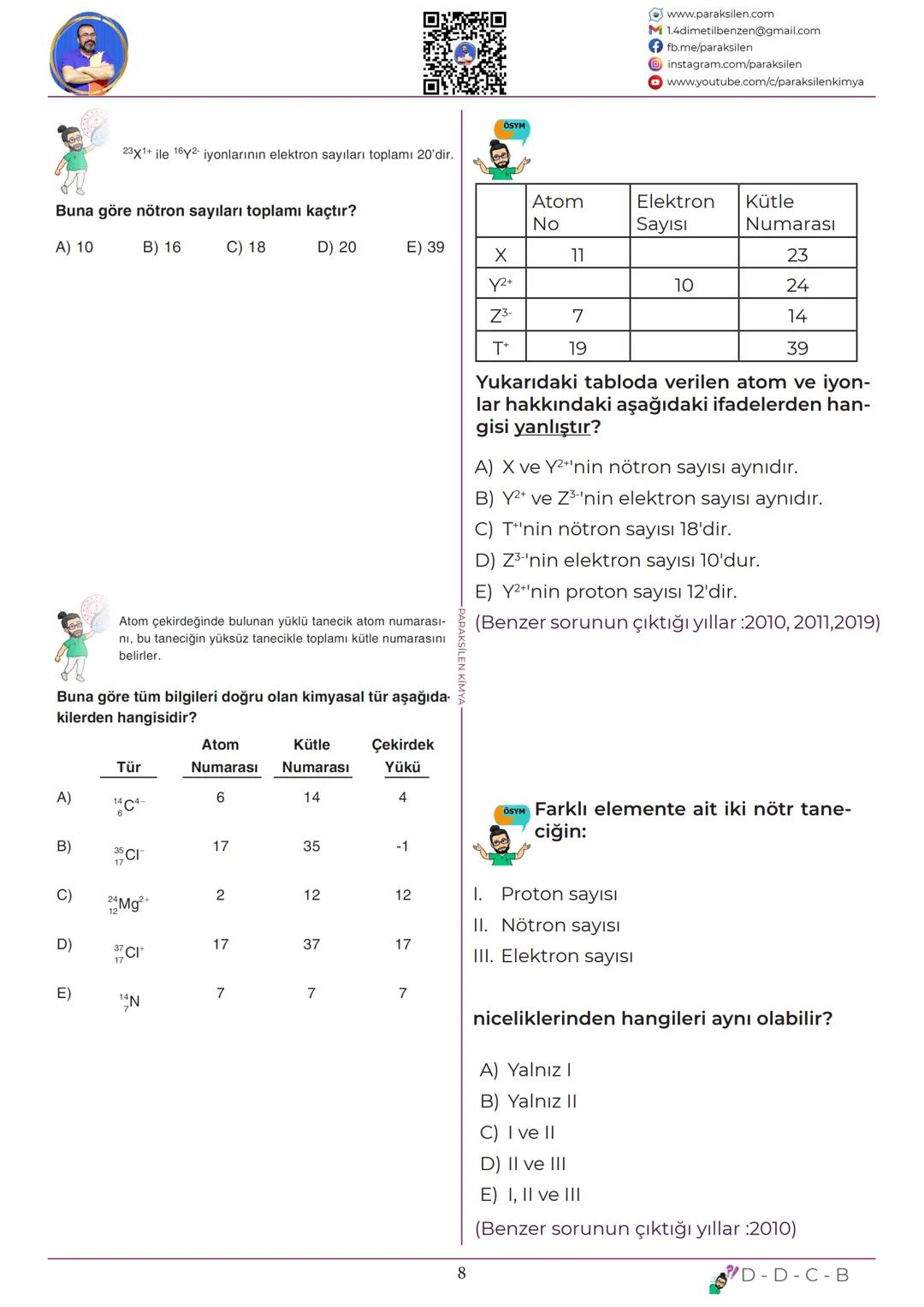
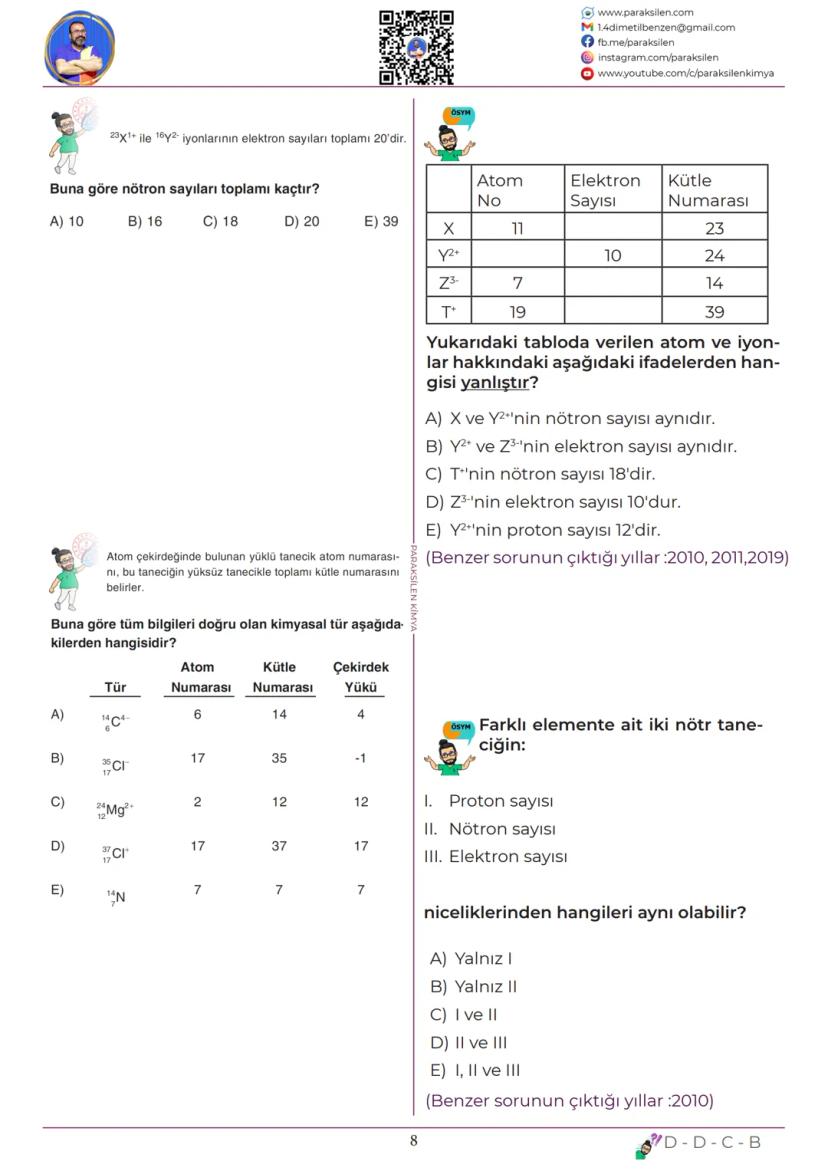
İyon Hesaplamaları ve Çözüm Teknikleri
İyon hesaplamalarında temel formülleri kullanın: Elektron sayısı = Proton sayısı - İyon yükü. Nötron sayısı = Kütle numarası - Proton sayısı.
Sorularda dikkat edilecek noktalar: Atom numarası = Proton sayısı = Çekirdek yükü her zaman eşit. Kütle numarası çekirdekteki tanecik sayısını (nükleon) verir. Farklı elementlerin proton sayıları farklı ama nötron, elektron sayıları aynı olabilir.
Tablo sorularında her satırı ayrı ayrı kontrol edin. Y²⁺ iyonunun proton sayısı = atom numarası, elektron sayısı = proton sayısı - 2. Z³⁻ iyonunun elektron sayısı = proton sayısı + 3.
Kimyasal türleri yazarken doğru format: ᴬₓX^n (A: kütle numarası, Z: atom numarası, n: iyon yükü). Çekirdek yükü atom numarasına eşittir.
🔥 Hızlı Çözüm: ÖSYM sorularında sayısal verilerden eksik olanları sistematik olarak bulun, rastgele deneme yapmayın.

İyonik Taneciklerin Boyutları ve Çekim Kuvvetleri
Tanecik elektron verdiğinde çapı küçülür çünkü aynı sayıda proton daha az elektronu çeker, elektron başına düşen çekim artar. Elektron aldığında çapı büyür çünkü proton başına düşecek elektron sayısı artar, çekim zayıflar.
Aynı elementin taneciklerinin çap sıralaması: X²⁻ > X¹⁻ > X > X¹⁺ > X²⁺ şeklindedir. Anyon çapı > Nötr atom çapı > Katyon çapı.
Aynı elektron sayısına sahip taneciklerde proton sayısı arttıkça çap küçülür: O²⁻ > F⁻ > Ne > Na⁺ > Mg²⁺ (8, 9, 10, 11, 12 proton).
X → X²⁺ dönüşümünde kimyasal özellik değişir (elektron sayısı değişti), elektron başına çekim artar, çap küçülür. Çekirdeğin toplam çekim gücü aynı kalır ama elektron başına düşen artar.
🎯 Kritik Kural: Proton arttıkça çap küçülür, elektron arttıkça çap büyür. Bu mantığı kavrayın, ezberlemeyin.

İzotop Atomlar ve Ortalama Atom Kütlesi
İzotop atomlar proton sayısı aynı, nötron sayısı farklı olan tanecikler. ¹H, ²D, ³T hidrojenin izotopları. Elektron sayıları da aynıysa kimyasal özellikleri aynı, fiziksel özellikleri farklı.
İzotoplar aynı elementle aynı tepkimeye girer, aynı ürünü oluştururlar. H₂ + O₂ → H₂O su yapar, D₂ + O₂ → D₂O ağır su yapar. Her ikisi de sudur ama fiziksel özellikleri farklı.
Ortalama atom kütlesi = / 100 formülüyle hesaplanır.
Grafikle soru çözümünde: Aynı proton, farklı elektron sayısına sahip taneciklerden elektron fazlası olan anyon, elektron eksigi olan katyon. Nötr atomlarda proton = elektron.
⚠️ Unutmayın: Kimyasal özellik proton+elektron, fiziksel özellik proton+nötron+elektron+bağ yapısı gibi her şeye bağlı.





Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Isotope
1Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
Atomun Yapısı: TYT Kimya 2. Konu Anlatımı
Kimyanın temelini oluşturan atom yapısı, TYT'de karşınıza mutlaka çıkacak konulardan biri. Bu konu sadece sınavda değil, kimyanın tüm diğer konularını anlamak için de çok kritik - atom konusunu kaçırırsanız, periyodik sistem, mol hesapları ve birçok AYT konusunda da zorlanırsınız.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
TYT Atom Yapısı - Giriş ve Sınav Analizi
TYT'de atom yapısı konusu her yıl karşınıza çıkan temel konulardan biri. Son 5 yıla baktığımızda, bu konudan toplam 4 soru sorulmuş - bu da konunun ne kadar önemli olduğunu gösteriyor.
Bu konu kimyanın alfabesi gibi düşünebilirsiniz. Atom konusunu iyi kavramazsanız, periyodik sistem, mol kavramı, kimyasal türler arası etkileşimler gibi diğer konularda ciddi sıkıntılar yaşarsınız. Bazı yıllarda direkt soru çıkmasa bile, diğer konuların içinde mutlaka sorulur.
Konunun %100'ü atomun yapısı başlığı altında toplanmış, atom modelleri kısmından hiç soru gelmemiş. Bu da çalışırken hangi bölümlere odaklanacağınızı gösteriyor.
💡 İpucu: Bu konu ezber değil, öğrenilecek bir konu. Mantığını kavradığınızda hem kolay hem de eğlenceli hale geliyor.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Atom Modelleri - Dalton ve Thomson
Dalton Atom Modeli kimya tarihinin ilk bilimsel atom teorisi. Dalton'a göre maddeler atom denen küçük taneciklerden oluşur ve atomlar kimyasal tepkimelerde parçalanamaz, bölünemez.
Dalton'un temel fikirleri: Atomlar içi dolu küre şeklinde, aynı elementin tüm atomları özdeş, farklı elementlerin atomları farklı. Farklı element atomlarının belirli oranlarda birleşmesiyle bileşikler oluşur.
Thomson Atom Modeli ise elektronu keşfettikten sonra geliştirildi. Thomson'a göre atom, pozitif yüklü bir küre içinde elektronların homojen dağıldığı "üzümlü kek" gibi bir yapıya sahip. Atomdaki negatif yük sayısı pozitif yük sayısına eşit olduğu için atom nötrdür.
Her iki modelin de eksiklikleri var: Dalton atom altı parçacıkları bulamadı, atomların nükleer olaylarda parçalanabileceğini bilmiyordu. Thomson ise yüklerin atomda homojen dağılmadığını açıklayamadı.
💡 Not: Günümüzde Dalton'un sadece "farklı elementlerin belirli oranda birleşmesi" fikri geçerliliğini koruyor.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Rutherford ve Bohr Atom Modelleri
Rutherford altın levha deneyiyle atomun yapısını çözdü. Alfa ışınlarının çoğu altın levhadan geçti, bazıları saptı, çok azı geri döndü. Bundan atomun büyük kısmının boş olduğunu, pozitif yükün küçük bir bölgede (çekirdek) toplandığını anladı.
Rutherford'a göre çekirdek çapı yaklaşık 10⁻¹²-10⁻¹³ cm, elektronlar bu boşlukta çekirdek etrafında döner. Çekirdekteki pozitif yük miktarı elemanı belirler. Çekirdekte kütlesi pozitif yük kütlesine eşit yüksüz tanecikler (nötron) de bulunur.
Bohr Atom Modeli ise elektronların davranışını açıkladı. Elektronlar çekirdekten belirli uzaklıklarda, belirli enerjiye sahip yörüngelerde (enerji düzeyleri) bulunur. Bu düzeyler n=1,2,3... veya K,L,M,N... ile gösterilir.
Elektronun dışarıdan enerji alıp daha yüksek enerji düzeyine geçmesine uyarılma denir. Uyarılmış atom kararsızdir, elektron temel hâle geçerken yörüngeler arası enerji farkına denk ışıma yapar.
⚡ Dikkat: Bohr sadece tek elektronlu atomları (H, He⁺, Li²⁺) açıklayabildi, çok elektronlularda yetersiz kaldı.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Bohr Modeli Soruları ve Çözüm Teknikleri
Bohr modelinin temel özellikleri sınavda sık sorulur. Elektronlar belirli enerji düzeylerinde bulunur, dışarıdan enerji alarak uyarılır ve daha sonra ışın yayarak temel hâle döner.
Soruları çözerken şu noktaları unutmayın: Dalton modelinde günümüzde geçerli olan sadece "farklı elementlerin belirli oranda birleşmesi" kuralı. Thomson "üzümlü kek" modelini geliştirdi, Rutherford çekirdekli atom modelini.
Atom modelleri kronolojik sırası: Dalton → Thomson → Rutherford → Bohr. Her model bir öncekinin eksiklerini gidermeye çalışmış ama yeni eksiklikleri de ortaya çıkmış.
Önemli ayrım: Orbital kavramı Bohr'da değil, modern atom teorisinde var. Bohr'da sadece yörünge kavramı var, orbital farklı bir şey.
🎯 Sınav İpucu: Soruları çözerken hangi modelin hangi özelliğini savunduğunu karıştırmamaya dikkat edin. Her modelin kendine özgü eksiklikleri var.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Rutherford Altın Levha Deneyi ve Model Karşılaştırmaları
Rutherford'un altın levha deneyi atom yapısını anlamamızı sağlayan kritik deney. Pozitif yüklü alfa tanecikleri altın levhaya gönderilir, çoğu geçer, bazıları sapar, çok azı geri döner.
Deneyin sonuçları: Atomun büyük kısmı boş, pozitif yük küçük bir bölgede (çekirdek) toplanmış, protonlar atom kütlesinin yaklaşık yarısını oluşturuyor. Dikkat edin, bu deneyle nötronların varlığı gözlemlenemez çünkü nötronlar yüksüz.
Atom modelleri kronolojik sırası: Dalton (atom bölünmez küre) → Thomson (üzümlü kek, yüklerin eşit dağılımı) → Rutherford (çekirdekli model) → Bohr (enerji düzeyleri).
Soruları çözerken modellerin özelliklerini karıştırmayın: Yörünge kavramı ilk kez Bohr'da, çekirdek kavramı Rutherford'da ortaya çıktı. Thomson yüksüz taneciklerden değil, pozitif-negatif yüklerin dağılımından bahsetti.
⚠️ Dikkat: Soru çözümlerinde dallanmış ağaç sorularında adım adım ilerleyin, aceleci davranmayın.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Modern Atom Teorisi ve Temel Tanecikler
Modern atom teorisine göre atom, bir elementin tüm özelliklerini taşıyan en küçük tanecik. Atomun yapısında proton, nötron, elektron gibi atom altı tanecikler bulunur.
Proton çekirdekte bulunan pozitif yüklü tanecik (kütlesi 1,673×10⁻²⁴ g), nötron çekirdekte bulunan yüksüz tanecik (kütlesi 1,675×10⁻²⁴ g). Elektron çekirdek etrafında bulunan negatif yüklü tanecik (kütlesi 9,109×10⁻²⁸ g).
Elektronun kütlesi proton veya nötronun 1/1836'sı kadar küçük. Bu yüzden atomun kütlesi neredeyse tamamen çekirdekte toplanmış. Çekirdeğin hacmi atomun hacminin yanında çok küçük.
Atom numarası proton sayısını, kütle numarası proton+nötron toplamını gösterir. Bir elementin cinsini proton sayısı belirler. Kimyasal özellik proton ve elektrona, fiziksel özellik her şeye bağlıdır.
📝 Formül: Nötron sayısı = Kütle numarası - Atom numarası

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
İyon Kavramı ve Hesaplamalar
İyon yüklü taneciğe denir. Kimyasal olaylarda proton alınıp verilmez, atomun yüklenmesi sadece elektron alışverişi ile olur. Elektron alan tanecik negatif, elektron veren tanecik pozitif yüklenir.
Katyon pozitif yüklü iyon (elektron vermiş), anyon negatif yüklü iyon (elektron almış). İyon yükü = Proton sayısı - Elektron sayısı formülüyle hesaplanır.
Soruları çözerken semboldeki konumları ezberleyin: Sol üstte kütle numarası, sol altta atom numarası, sağ üstte iyon yükü. Tüm oksijen taneciklerinde proton sayısı aynı, tüm oksijen atomlarında elektron sayısı aynı.
X²⁻ → X¹⁺ dönüşümünde elektron sayısı azalır, iyon yükü artar ama proton sayısı ve çekirdek yükü değişmez. Grafik sorularında proton-elektron ilişkisine dikkat edin.
⚡ Püf Nokta: İyon yükü pozitifse elektron eksilmiş, negatifse elektron fazlalığı var.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
İyon Hesaplamaları ve Çözüm Teknikleri
İyon hesaplamalarında temel formülleri kullanın: Elektron sayısı = Proton sayısı - İyon yükü. Nötron sayısı = Kütle numarası - Proton sayısı.
Sorularda dikkat edilecek noktalar: Atom numarası = Proton sayısı = Çekirdek yükü her zaman eşit. Kütle numarası çekirdekteki tanecik sayısını (nükleon) verir. Farklı elementlerin proton sayıları farklı ama nötron, elektron sayıları aynı olabilir.
Tablo sorularında her satırı ayrı ayrı kontrol edin. Y²⁺ iyonunun proton sayısı = atom numarası, elektron sayısı = proton sayısı - 2. Z³⁻ iyonunun elektron sayısı = proton sayısı + 3.
Kimyasal türleri yazarken doğru format: ᴬₓX^n (A: kütle numarası, Z: atom numarası, n: iyon yükü). Çekirdek yükü atom numarasına eşittir.
🔥 Hızlı Çözüm: ÖSYM sorularında sayısal verilerden eksik olanları sistematik olarak bulun, rastgele deneme yapmayın.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
İyonik Taneciklerin Boyutları ve Çekim Kuvvetleri
Tanecik elektron verdiğinde çapı küçülür çünkü aynı sayıda proton daha az elektronu çeker, elektron başına düşen çekim artar. Elektron aldığında çapı büyür çünkü proton başına düşecek elektron sayısı artar, çekim zayıflar.
Aynı elementin taneciklerinin çap sıralaması: X²⁻ > X¹⁻ > X > X¹⁺ > X²⁺ şeklindedir. Anyon çapı > Nötr atom çapı > Katyon çapı.
Aynı elektron sayısına sahip taneciklerde proton sayısı arttıkça çap küçülür: O²⁻ > F⁻ > Ne > Na⁺ > Mg²⁺ (8, 9, 10, 11, 12 proton).
X → X²⁺ dönüşümünde kimyasal özellik değişir (elektron sayısı değişti), elektron başına çekim artar, çap küçülür. Çekirdeğin toplam çekim gücü aynı kalır ama elektron başına düşen artar.
🎯 Kritik Kural: Proton arttıkça çap küçülür, elektron arttıkça çap büyür. Bu mantığı kavrayın, ezberlemeyin.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
İzotop Atomlar ve Ortalama Atom Kütlesi
İzotop atomlar proton sayısı aynı, nötron sayısı farklı olan tanecikler. ¹H, ²D, ³T hidrojenin izotopları. Elektron sayıları da aynıysa kimyasal özellikleri aynı, fiziksel özellikleri farklı.
İzotoplar aynı elementle aynı tepkimeye girer, aynı ürünü oluştururlar. H₂ + O₂ → H₂O su yapar, D₂ + O₂ → D₂O ağır su yapar. Her ikisi de sudur ama fiziksel özellikleri farklı.
Ortalama atom kütlesi = / 100 formülüyle hesaplanır.
Grafikle soru çözümünde: Aynı proton, farklı elektron sayısına sahip taneciklerden elektron fazlası olan anyon, elektron eksigi olan katyon. Nötr atomlarda proton = elektron.
⚠️ Unutmayın: Kimyasal özellik proton+elektron, fiziksel özellik proton+nötron+elektron+bağ yapısı gibi her şeye bağlı.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Isotope
1Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅