Atom modelleri ve periyodik sistem, modern kimyanın temellerini oluşturan en... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
1,745
•
Güncellendi May 15, 2026
•
Esma Melek KARADAĞ
@esmamelekkarada
Atom modelleri ve periyodik sistem, modern kimyanın temellerini oluşturan en... Daha fazla göster




Atom modelleri tarih boyunca sürekli gelişmiştir. Her model, atomun yapısını daha iyi açıklamak için önceki modellerin eksikliklerini gidermeye çalışmıştır. Democritos'tan Modern Atom Modeli'ne kadar uzanan bu yolculuk, bilimin nasıl ilerlediğini gösterir.
Dalton Atom Modeli (1803) kimyada modern çağın başlangıcı kabul edilir. Bu modele göre elementler bölünemez atomlardan oluşur, bir elementin tüm atomları aynıdır ve kimyasal tepkimeler atomların yeniden düzenlenmesinden ibarettir.
Thomson Modeli (1902) atomu, içinde artı ve eksi yüklerin homojen dağıldığı nötr bir küre olarak tanımlar. Bu modelde elektronların kütlesinin atomun yanında çok küçük olduğu kabul edilir. Rutherford Modeli (1911) ise atomun çoğunun boş olduğunu ve kütlenin çekirdekte toplandığını göstermiştir.
💡 Atomla ilgili her yeni model, bir öncekinin açıklayamadığı gözlemleri açıklamak için geliştirilmiştir. Bu bilim dünyasında çok yaygın bir ilerleyiş biçimidir!
Bohr Atom Modeli (1913) elektronu çekirdeğin etrafında belirli yörüngelerde hareket eden parçacıklar olarak tanımlar. Bu modelde elektronlar K, L, M, N... gibi belirli enerji seviyelerinde bulunur. Elektronun enerjisi, çekirdekten uzaklaştıkça artar.
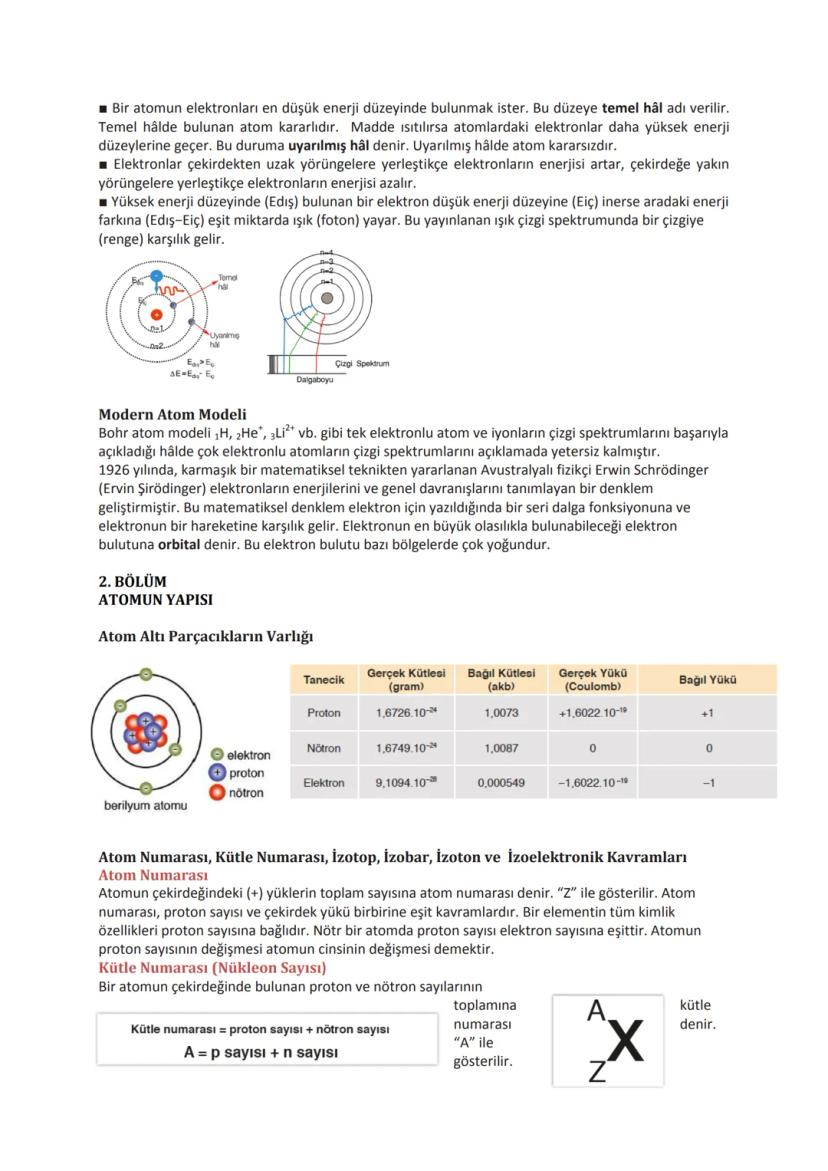
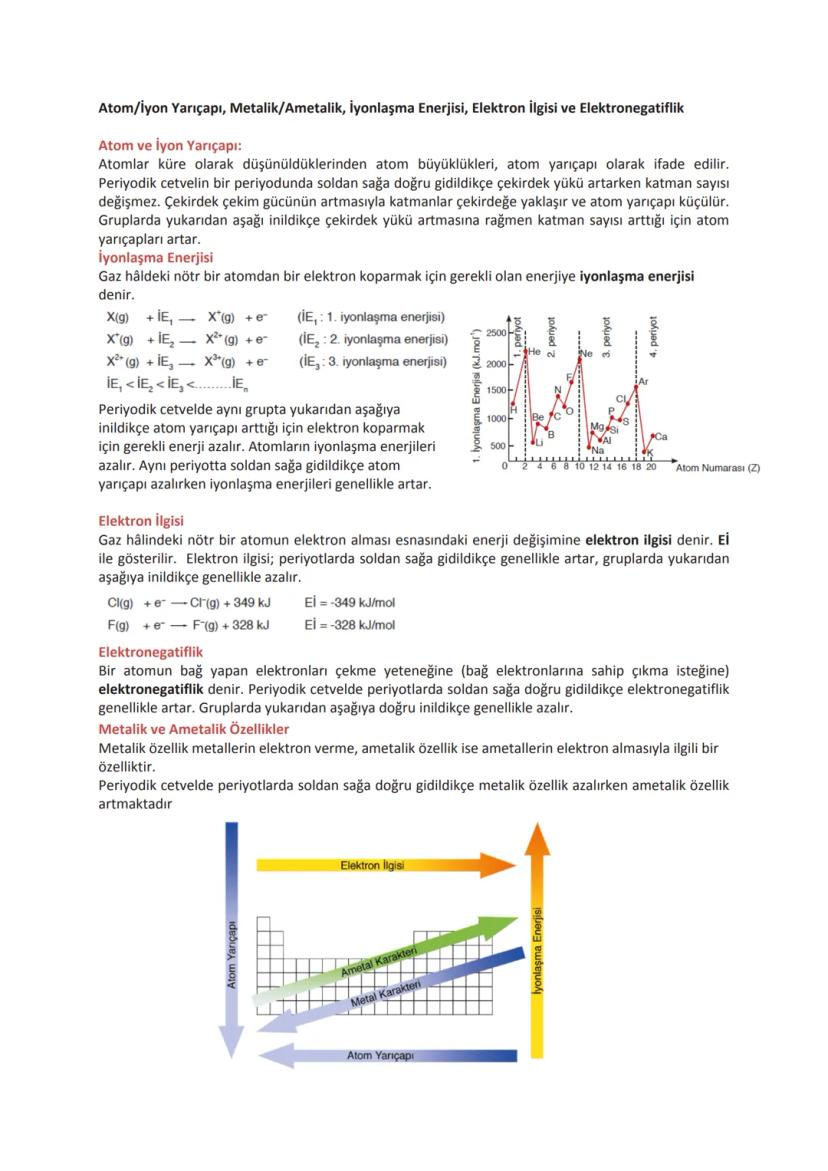
Bohr modelinde atomlar temel hâl ve uyarılmış hâl olmak üzere iki durum gösterir. Temel halde elektronlar en düşük enerji düzeyindedir ve atom kararlıdır. Atomlar ısı aldığında elektronlar yüksek enerji düzeylerine çıkar ve uyarılmış hâle geçer.
Uyarılmış haldeki atom kararsızdır ve tekrar kararlı hale geçmek ister. Bir elektron yüksek enerji seviyesinden düşük enerji seviyesine indiğinde, aradaki enerji farkını ışık (foton) olarak yayar. Bu yayılan ışık, çizgi spektrumunda belirli bir renge karşılık gelir.
💡 Havai fişeklerin renkli ışık saçmasının nedeni budur! Atomlar ısı enerjisiyle uyarılır, sonra temel hale dönerken farklı renklerde ışık yayarlar.
Modern Atom Modeli, Bohr'un modelinin çok elektronlu atomları açıklamadaki yetersizliği üzerine geliştirilmiştir. 1926'da Erwin Schrödinger elektronların davranışlarını tanımlayan matematiksel bir denklem geliştirdi. Bu modele göre elektronların belirli bir yörüngede değil, bir elektron bulutu (orbital) içinde bulunma olasılığı vardır. Bu bulunan elektron, bazı bölgelerde daha yoğun bulunur.

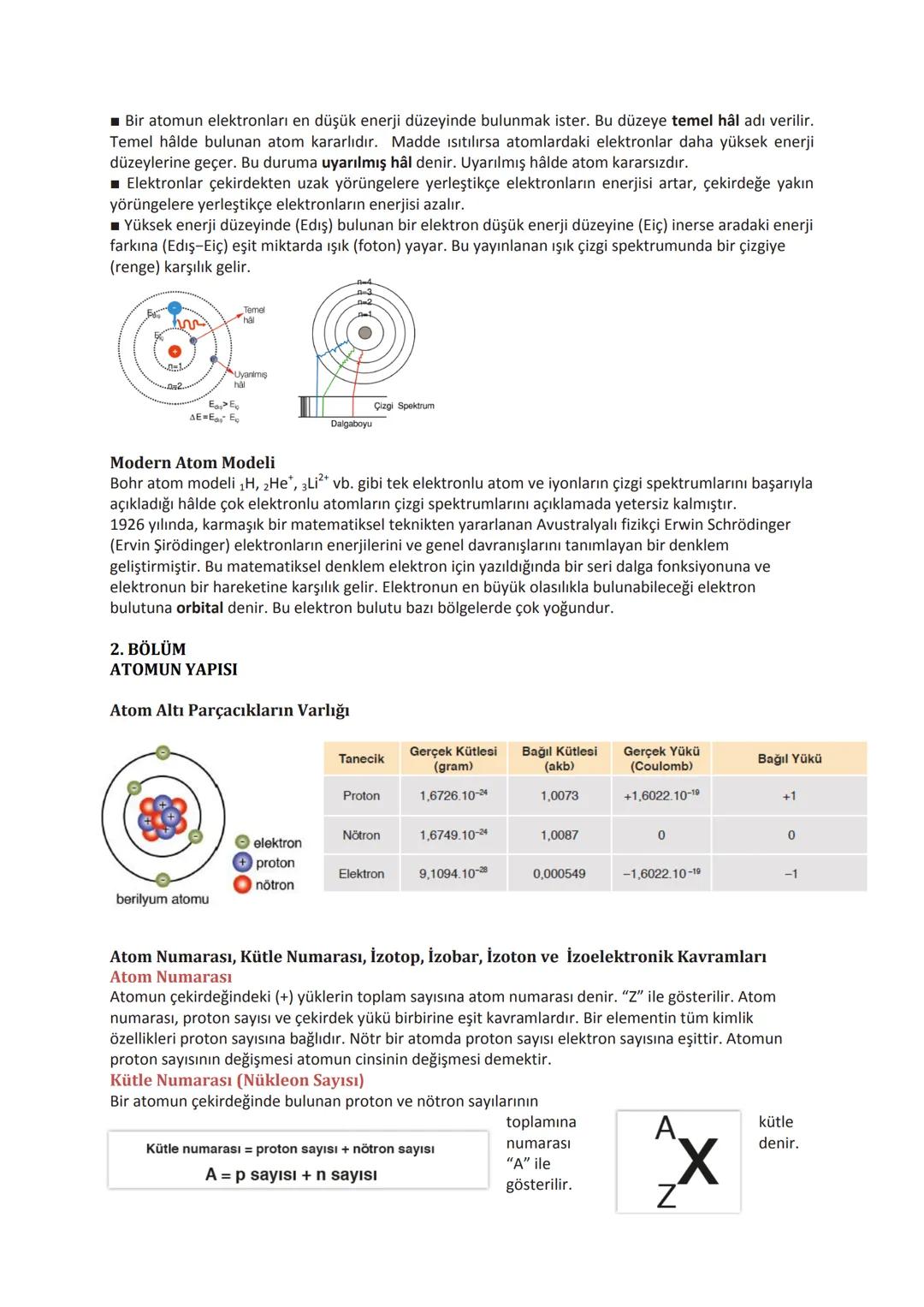
Atomu oluşturan temel parçacıklar proton, nötron ve elektrondur. Protonlar pozitif yüklü, nötronlar yüksüz, elektronlar ise negatif yüklüdür. Proton ve nötron çekirdekte bulunurken, elektronlar çekirdeğin çevresindeki orbitallerde yer alır.
Atom numarası (Z), çekirdekteki proton sayısını gösterir ve elementin kimliğini belirler. Kütle numarası (A) ise proton ve nötron sayılarının toplamıdır . Nötr bir atomda proton ve elektron sayıları birbirine eşittir.
Aynı elementin farklı atomları arasında çeşitli ilişkiler olabilir:
💡 Aynı elementin izotopları kimyasal özellikleri aynı, fiziksel özellikleri farklı olan atomlardır. Örneğin karbon-12, karbon-13 ve karbon-14 izotoplarının hepsi karbon elementi olarak davranır, ama farklı kütlelere sahiptir!

Periyodik cetvelin temelleri 1869'da Rus kimyacı Dimitri Mendeleyev tarafından atılmıştır. Ancak modern periyodik cetvel, Henry Moseley'in elementleri atom numaralarına göre düzenlemesiyle oluşturulmuştur.
Modern periyodik cetvelde 7 periyot (yatay sıra) ve 18 grup (düşey sütun) bulunur. Gruplar iki şekilde adlandırılır: 1A, 2A, 3B gibi harfli sistem veya IUPAC'ın önerdiği 1'den 18'e numaralama sistemi. A grubu elementleri baş grup (ana grup), B grubu elementleri ise yan grup (geçiş elementleri) olarak adlandırılır.
Atomun elektron katman dağılımı ile periyodik cetveldeki konumu arasında doğrudan bir ilişki vardır:
💡 Kimyasal tepkimelerde genellikle değerlik elektronları rol oynar. Bu nedenle aynı grupta bulunan elementler benzer kimyasal özellikler gösterir!
Elementler özelliklerine göre metaller, yarı metaller, ametaller ve soy gazlar olarak sınıflandırılır. Metaller periyodik cetvelin sol tarafında, ametaller sağ tarafında, yarı metaller ise bu ikisi arasındaki çapraz bölgede yer alır. Soy gazlar en sağdaki grubu oluşturur.
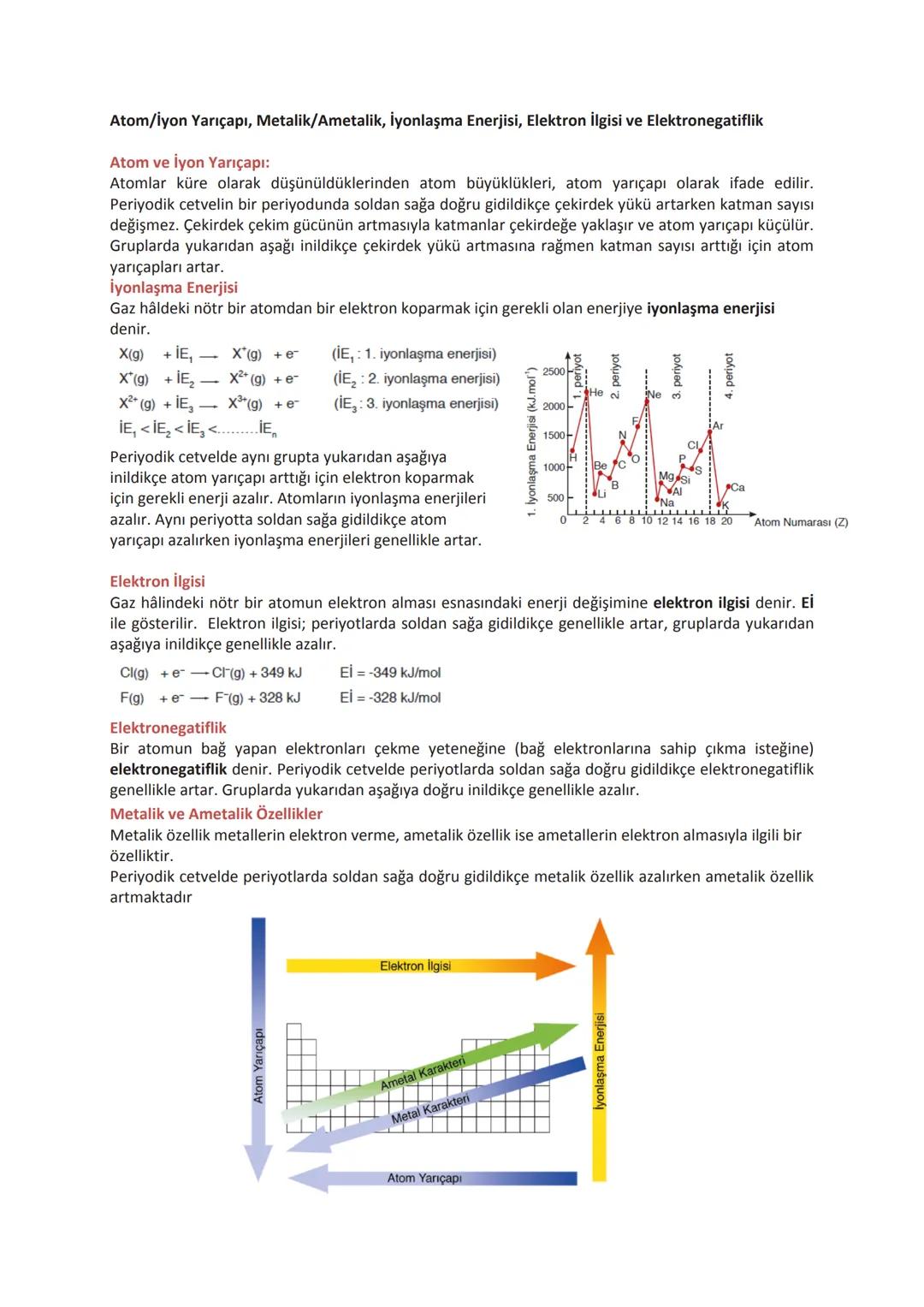
Elementlerin periyodik cetveldeki yerlerine göre gösterdikleri özellikler belirli eğilimler içerir. Bu eğilimleri bilmek, elementlerin davranışlarını tahmin etmemizi sağlar.
Atom yarıçapı, periyotlarda soldan sağa doğru gidildikçe genellikle küçülür. Bunun nedeni artan çekirdek yükünün elektronları daha kuvvetle çekmesidir. Gruplarda yukarıdan aşağıya inildikçe ise atom yarıçapı artar çünkü katman sayısı artar.
İyonlaşma enerjisi, bir atomdan elektron koparmak için gereken enerjidir. Periyotlarda soldan sağa doğru genellikle artar, gruplarda yukarıdan aşağıya doğru azalır. Her bir elektronu koparmak için gereken enerji bir öncekinden daha fazladır (IE₁ < IE₂ < IE₃).
Elektron ilgisi, bir atomun elektron kabul ederken açığa çıkardığı enerjidir. Periyotlarda soldan sağa gidildikçe genellikle artar, gruplarda yukarıdan aşağıya inildikçe azalır.
💡 Flor (F), klor (Cl) gibi halojenler yüksek elektron ilgisine sahiptir ve kolaylıkla elektron alarak negatif yüklü iyonlar oluştururlar!
Elektronegatiflik, bir atomun bağ elektronlarını çekme yeteneğidir. Periyotlarda soldan sağa artar, gruplarda yukarıdan aşağıya azalır. Metalik özellik ise periyotlarda soldan sağa azalırken, ametalik özellik artar. Metalik özellik elektron verme, ametalik özellik ise elektron alma eğilimi ile ilgilidir.
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Esma Melek KARADAĞ
@esmamelekkarada
Atom modelleri ve periyodik sistem, modern kimyanın temellerini oluşturan en önemli konulardır. Bu kavramlar, maddelerin yapısını, elementlerin özelliklerini ve kimyasal bağların nasıl oluştuğunu anlamamızı sağlar. Atomun keşfinden modern atom modeline kadar geçen süreçte bilim insanlarının katkılarıyla bilgilerimiz sürekli gelişmiştir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Atom modelleri tarih boyunca sürekli gelişmiştir. Her model, atomun yapısını daha iyi açıklamak için önceki modellerin eksikliklerini gidermeye çalışmıştır. Democritos'tan Modern Atom Modeli'ne kadar uzanan bu yolculuk, bilimin nasıl ilerlediğini gösterir.
Dalton Atom Modeli (1803) kimyada modern çağın başlangıcı kabul edilir. Bu modele göre elementler bölünemez atomlardan oluşur, bir elementin tüm atomları aynıdır ve kimyasal tepkimeler atomların yeniden düzenlenmesinden ibarettir.
Thomson Modeli (1902) atomu, içinde artı ve eksi yüklerin homojen dağıldığı nötr bir küre olarak tanımlar. Bu modelde elektronların kütlesinin atomun yanında çok küçük olduğu kabul edilir. Rutherford Modeli (1911) ise atomun çoğunun boş olduğunu ve kütlenin çekirdekte toplandığını göstermiştir.
💡 Atomla ilgili her yeni model, bir öncekinin açıklayamadığı gözlemleri açıklamak için geliştirilmiştir. Bu bilim dünyasında çok yaygın bir ilerleyiş biçimidir!
Bohr Atom Modeli (1913) elektronu çekirdeğin etrafında belirli yörüngelerde hareket eden parçacıklar olarak tanımlar. Bu modelde elektronlar K, L, M, N... gibi belirli enerji seviyelerinde bulunur. Elektronun enerjisi, çekirdekten uzaklaştıkça artar.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bohr modelinde atomlar temel hâl ve uyarılmış hâl olmak üzere iki durum gösterir. Temel halde elektronlar en düşük enerji düzeyindedir ve atom kararlıdır. Atomlar ısı aldığında elektronlar yüksek enerji düzeylerine çıkar ve uyarılmış hâle geçer.
Uyarılmış haldeki atom kararsızdır ve tekrar kararlı hale geçmek ister. Bir elektron yüksek enerji seviyesinden düşük enerji seviyesine indiğinde, aradaki enerji farkını ışık (foton) olarak yayar. Bu yayılan ışık, çizgi spektrumunda belirli bir renge karşılık gelir.
💡 Havai fişeklerin renkli ışık saçmasının nedeni budur! Atomlar ısı enerjisiyle uyarılır, sonra temel hale dönerken farklı renklerde ışık yayarlar.
Modern Atom Modeli, Bohr'un modelinin çok elektronlu atomları açıklamadaki yetersizliği üzerine geliştirilmiştir. 1926'da Erwin Schrödinger elektronların davranışlarını tanımlayan matematiksel bir denklem geliştirdi. Bu modele göre elektronların belirli bir yörüngede değil, bir elektron bulutu (orbital) içinde bulunma olasılığı vardır. Bu bulunan elektron, bazı bölgelerde daha yoğun bulunur.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Atomu oluşturan temel parçacıklar proton, nötron ve elektrondur. Protonlar pozitif yüklü, nötronlar yüksüz, elektronlar ise negatif yüklüdür. Proton ve nötron çekirdekte bulunurken, elektronlar çekirdeğin çevresindeki orbitallerde yer alır.
Atom numarası (Z), çekirdekteki proton sayısını gösterir ve elementin kimliğini belirler. Kütle numarası (A) ise proton ve nötron sayılarının toplamıdır . Nötr bir atomda proton ve elektron sayıları birbirine eşittir.
Aynı elementin farklı atomları arasında çeşitli ilişkiler olabilir:
💡 Aynı elementin izotopları kimyasal özellikleri aynı, fiziksel özellikleri farklı olan atomlardır. Örneğin karbon-12, karbon-13 ve karbon-14 izotoplarının hepsi karbon elementi olarak davranır, ama farklı kütlelere sahiptir!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Periyodik cetvelin temelleri 1869'da Rus kimyacı Dimitri Mendeleyev tarafından atılmıştır. Ancak modern periyodik cetvel, Henry Moseley'in elementleri atom numaralarına göre düzenlemesiyle oluşturulmuştur.
Modern periyodik cetvelde 7 periyot (yatay sıra) ve 18 grup (düşey sütun) bulunur. Gruplar iki şekilde adlandırılır: 1A, 2A, 3B gibi harfli sistem veya IUPAC'ın önerdiği 1'den 18'e numaralama sistemi. A grubu elementleri baş grup (ana grup), B grubu elementleri ise yan grup (geçiş elementleri) olarak adlandırılır.
Atomun elektron katman dağılımı ile periyodik cetveldeki konumu arasında doğrudan bir ilişki vardır:
💡 Kimyasal tepkimelerde genellikle değerlik elektronları rol oynar. Bu nedenle aynı grupta bulunan elementler benzer kimyasal özellikler gösterir!
Elementler özelliklerine göre metaller, yarı metaller, ametaller ve soy gazlar olarak sınıflandırılır. Metaller periyodik cetvelin sol tarafında, ametaller sağ tarafında, yarı metaller ise bu ikisi arasındaki çapraz bölgede yer alır. Soy gazlar en sağdaki grubu oluşturur.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Elementlerin periyodik cetveldeki yerlerine göre gösterdikleri özellikler belirli eğilimler içerir. Bu eğilimleri bilmek, elementlerin davranışlarını tahmin etmemizi sağlar.
Atom yarıçapı, periyotlarda soldan sağa doğru gidildikçe genellikle küçülür. Bunun nedeni artan çekirdek yükünün elektronları daha kuvvetle çekmesidir. Gruplarda yukarıdan aşağıya inildikçe ise atom yarıçapı artar çünkü katman sayısı artar.
İyonlaşma enerjisi, bir atomdan elektron koparmak için gereken enerjidir. Periyotlarda soldan sağa doğru genellikle artar, gruplarda yukarıdan aşağıya doğru azalır. Her bir elektronu koparmak için gereken enerji bir öncekinden daha fazladır (IE₁ < IE₂ < IE₃).
Elektron ilgisi, bir atomun elektron kabul ederken açığa çıkardığı enerjidir. Periyotlarda soldan sağa gidildikçe genellikle artar, gruplarda yukarıdan aşağıya inildikçe azalır.
💡 Flor (F), klor (Cl) gibi halojenler yüksek elektron ilgisine sahiptir ve kolaylıkla elektron alarak negatif yüklü iyonlar oluştururlar!
Elektronegatiflik, bir atomun bağ elektronlarını çekme yeteneğidir. Periyotlarda soldan sağa artar, gruplarda yukarıdan aşağıya azalır. Metalik özellik ise periyotlarda soldan sağa azalırken, ametalik özellik artar. Metalik özellik elektron verme, ametalik özellik ise elektron alma eğilimi ile ilgilidir.
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
12
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı