Kimya dersinde atom modelleri, elektron dizilimi ve elementlerin periyodik özellikleri... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
530
•
Güncellendi May 5, 2026
•
Ceydoss
@c3yda_kvk
Kimya dersinde atom modelleri, elektron dizilimi ve elementlerin periyodik özellikleri... Daha fazla göster
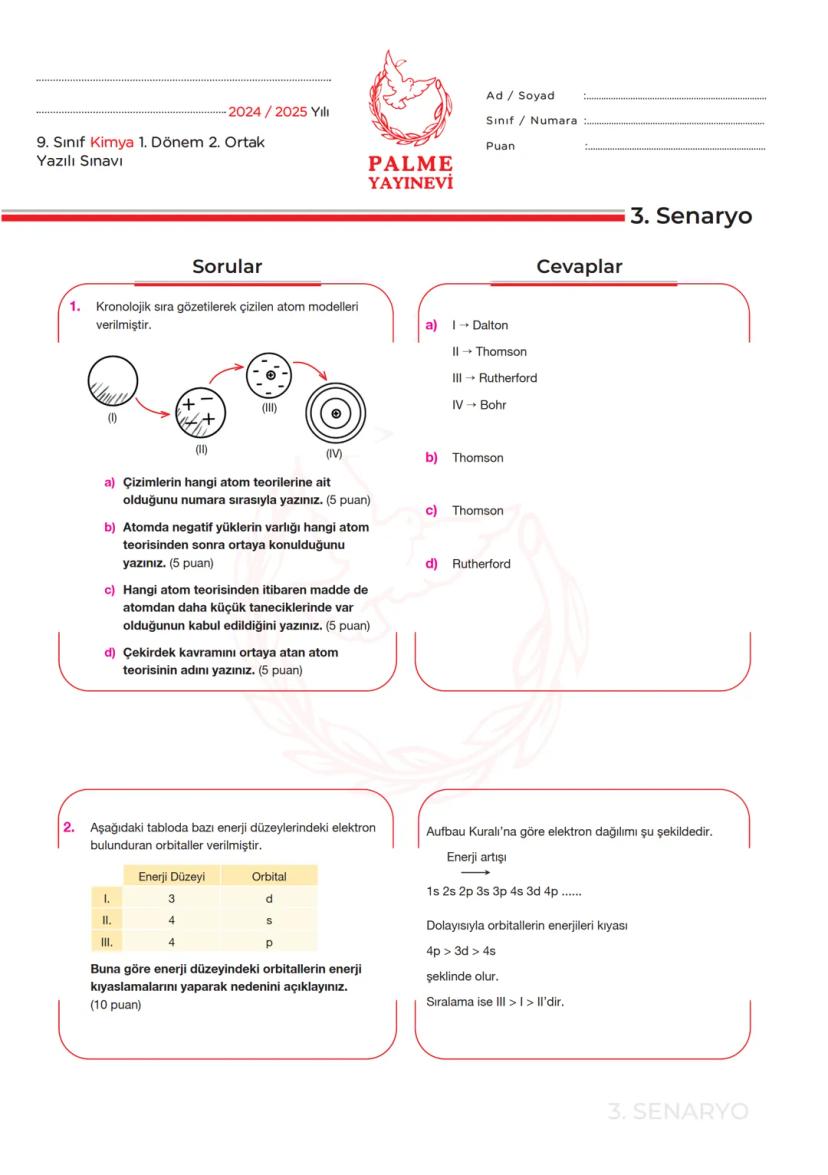






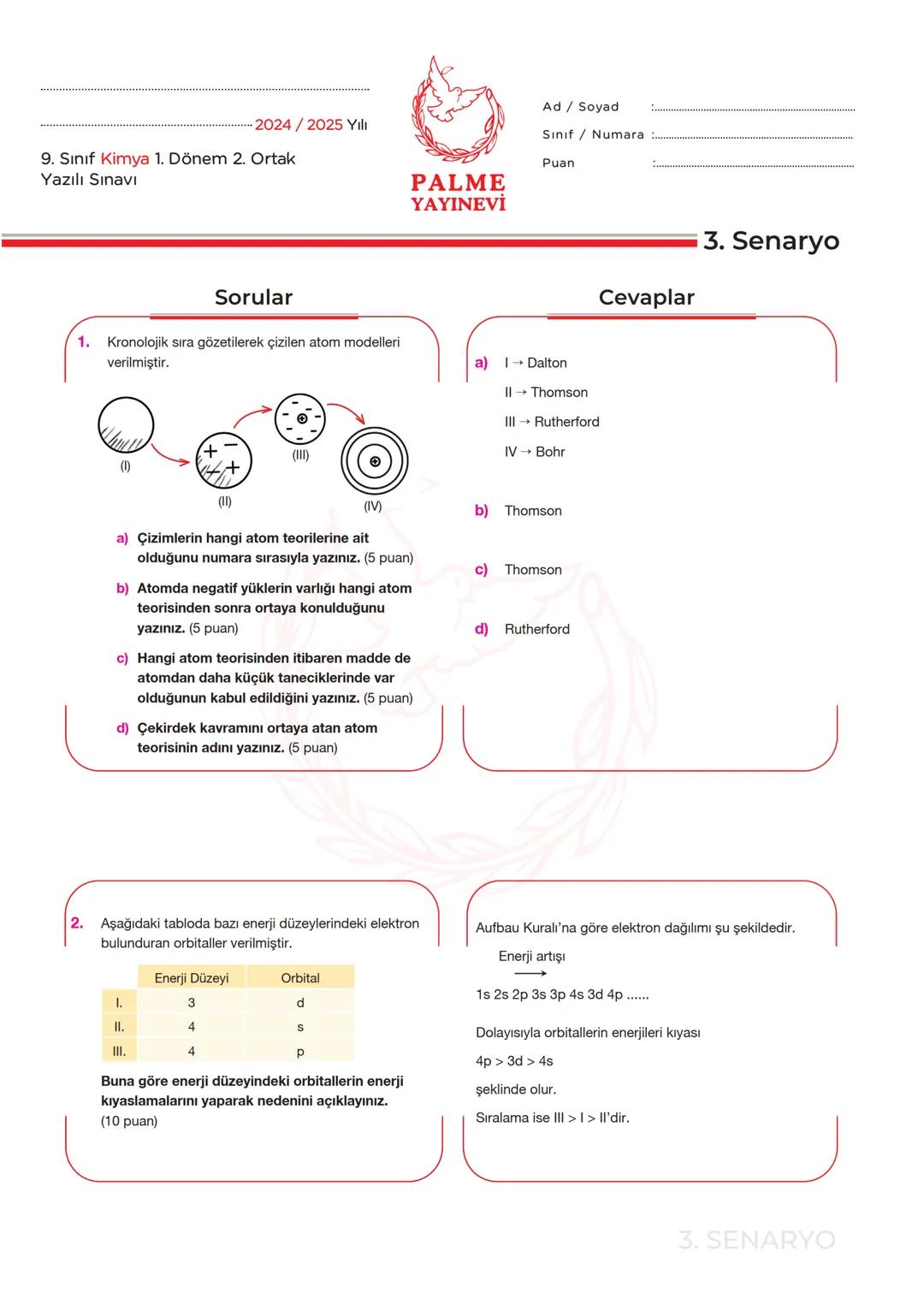
Bilim insanları atomu anlamak için farklı modeller geliştirmişlerdir. Dalton atomu bölünemeyen en küçük parça olarak tanımlarken, Thomson negatif yüklü elektronların keşfiyle "üzümlü kek" modelini ortaya koydu.
Rutherford deneyleriyle atomun çekirdek kavramını ortaya attı ve pozitif yüklerin merkezde toplandığını gösterdi. Bohr ise elektronların belirli enerji seviyelerinde bulunduğunu açıkladı.
Thomson atom modeli, maddenin atomdan daha küçük parçacıklardan oluştuğu fikrini ilk ortaya koyan modeldir. Bu modelden itibaren, atom "bölünemez" kavramından çıkarak daha karmaşık bir yapı olarak kabul edildi.
💡 Hatırlatma: Atom modelleri kronolojik olarak Dalton → Thomson → Rutherford → Bohr şeklinde gelişmiştir ve her yeni model bir öncekinin eksikliklerini gidermiştir.
Farklı atomların elektron dağılımları, Aufbau Kuralı'na göre yapılır. Bu kurala göre elektronlar, enerjisi en düşük orbitalden başlayarak yerleşirler. Enerji artışı 1s→2s→2p→3s→3p→4s→3d→4p şeklinde olur.

Atomlar elektronlarını belirli orbitallere dağıtırlar ve bu dağılım atomların davranışlarını belirler. Küresel simetri, elektronların atom çevresinde dengeli dağılmasıdır ve atom davranışlarını etkiler.
Bir atom, son orbitalinin yarı dolu veya tam dolu olması durumunda küresel simetri özelliği gösterir. Örneğin, Be atomunun $1s^2 2s^2$ elektron dizilimindeki son orbitali tam doludur ve küresel simetridir.
C atomu $1s^2 2s^2 2p^2$ son orbitalindeki tüm orbitaller yarı dolu veya tam dolu olmadığından küresel simetri göstermez. N atomu $1s^2 2s^2 2p^3$ ise $2p$ orbitallerinin tümü yarı dolu olduğundan küresel simetri özelliğine sahiptir.
💡 Püf Nokta: Küresel simetri özelliği gösteren atomlar daha kararlıdır ve kimyasal tepkimelere girme eğilimleri daha düşüktür.
Elementlerin periyodik tablodaki yerleri elektron dizilimlerinden belirlenebilir. Örneğin, He 1. periyot 8A'da, F 2. periyot 7A'da, P 3. periyot 5A'dadır.

Elektronlar bir atomdan ayrıldığında, kalan elektron dağılımı değişir. Bir atomun valans elektron sayısı, onun kimyasal davranışını belirleyen en önemli faktördür.
Periyodik tabloda atom yarıçapı sağdan sola ve yukarıdan aşağıya doğru artar. Bu nedenle Z > Y > X şeklinde sıralanırlar. İyonlaşma enerjisi ise genellikle aşağıdan yukarıya ve soldan sağa doğru artış gösterir.
Soy gazlar, 8A grubu elementleri olup elektron dizilimleri kararlıdır. Dış enerji seviyelerinde 8 elektron (He için 2 elektron) bulundururlar ve kimyasal tepkimelere girme eğilimleri çok düşüktür.
💡 Biliyor muydun? Periyodik tablodaki yerini bildiğin bir elementin, elektron dizilimini, valans elektron sayısını ve diğer fiziksel özelliklerini tahmin edebilirsin!
Elektron dağılımı yapılırken unutma: Aynı enerji düzeyinde, enerjisi eşit olan orbitallere (px, py, pz gibi) elektronlar önce birer birer ve aynı spinle yerleştirilir (Hund Kuralı). Aynı orbitalde ise iki elektron ancak zıt spinle bulunabilir (Pauli İlkesi).

Metalik bağ, metal atomları arasında oluşan güçlü bir kimyasal bağdır. Metal atomlarının dış yörünge elektronlarının ortaklaşa kullanılmasıyla oluşur ve metallerin iletkenlik gibi özelliklerini belirler.
Aynı periyotta bulunan elementlerin metalik bağ kuvvetleri, valans elektron sayısı arttıkça artar. Bu nedenle Li, Be ve B elementleri arasında metalik bağ kuvveti B > Be > Li şeklinde sıralanır.
Periyodik tablodaki konumu bilinen bir elementin fiziksel ve kimyasal özellikleri hakkında tahminler yapabilirsin. Örneğin, alkali metaller (1A grubu) en aktif metallerdir ve kolayca elektron verirler.
💡 Önemli İpucu: Metalik bağ kuvveti, metalin erime ve kaynama noktasını, sertliğini ve iletkenliğini etkiler. Metalik bağı güçlü olan metaller daha yüksek erime noktasına sahiptir.
Benzer şekilde, bir elementin elektron dizilimini biliyorsan, onun hangi grupta ve periyotta olduğunu, metalik veya ametalik özelliklerini ve diğer elementlerle nasıl tepkime vereceğini tahmin edebilirsin.

Elementlerin elektron dağılımları belirli kurallara göre yapılır. Aufbau ilkesi, elektronların düşük enerjili orbitallerden başlayarak yerleştirilmesi gerektiğini söyler.
Hund kuralı, aynı enerjiye sahip orbitallere elektronlar önce tek tek ve aynı spinle yerleştirilmesi gerektiğini belirtir. Pauli ilkesi ise bir orbitalde en fazla iki elektronun bulunabileceğini ve bunların zıt spinli olması gerektiğini ifade eder.
Atom modellerinin tarihsel gelişimi, bilimin ilerleyişini gösterir. Dalton'un bölünemeyen atom fikrinden, Thomson'un elektronları keşfetmesine ve Rutherford'un çekirdek kavramını ortaya atmasına kadar bilgimiz sürekli genişlemiştir.
💡 Sınav İpucu: Elektron dağılımlarında kurallara uygun olmayan dizilimler genellikle sınavlarda sorulur. Bunları tespit edebilmek için Aufbau, Hund ve Pauli ilkelerini iyi anlamalısın!
Yanlış elektron dizilimlerini tespit ederken şunlara dikkat etmelisin: Enerjisi düşük orbitaller dolmadan yüksek enerjili orbitallere elektron yerleşmişse Aufbau ilkesine; eş enerjili orbitallere tek tek elektron yerleşmeden çift elektron yerleşmişse Hund kuralına; aynı orbitalde aynı spinli iki elektron varsa Pauli ilkesine aykırıdır.

Elementlerin periyodik tablodaki yerleri, onların kimyasal ve fiziksel özelliklerini belirler. Alkali metaller (1A) elektron vermeye, halojenler (7A) elektron almaya eğilimlidir.
Elektronegatiflik periyodik tabloda soldan sağa artar ve yukarıdan aşağıya azalır. Bu nedenle, aynı periyotta sağdaki elementler daha elektronegatiftir. Örneğin, Z > Y > X şeklinde sıralanabilir.
Metallerde pozitif yüklü metal iyonları ile serbest dolaşan valans elektronları arasındaki çekim kuvvetine metalik bağ denir. Bu bağ, metallerin elektrik iletkenliği, ısı iletkenliği ve şekil verilebilme özelliklerini belirler.
💡 Biliyor muydun? Metalik bağ kuvveti, metal atomlarının pozitif iyon yükü ve serbest valans elektron sayısı arttıkça güçlenir.
Atom numaraları ardışık elementlerde, atom numarası arttıkça elektronların çekirdeğe olan çekim kuvveti artar. Bu da genellikle atom yarıçapının küçülmesine neden olur. Ancak, yeni bir enerji seviyesine geçildiğinde atom yarıçapı aniden artar.

İyonik bileşikler, katyonlar (pozitif yüklü iyonlar) ve anyonlar (negatif yüklü iyonlar) arasındaki elektrostatik çekim kuvvetleri ile oluşur. Bir bileşiğin formülü, içerdiği iyonların toplam yüklerinin birbirini nötrleştirmesiyle belirlenir.
gibi bir katyon, veya gibi anyonlarla birleşerek kararlı bileşikler oluşturabilir. Bu bileşiklerin formülleri iyonların yüklerini dengeleyecek şekilde yazılır: ve .
Bileşiklerin toplam atom sayısını hesaplarken, formüldeki her bir elementin atom sayısını toplamak gerekir. Örneğin, bileşiğinde 1 Ca, 2 N ve 6 O atomu olmak üzere toplam 9 atom vardır.
💡 Pratik Yöntem: İyonik bileşiklerin formülünü yazarken iyonların yüklerini çapraz yazarak indis olarak kullanabilirsin. Örneğin, ve için formülü elde edilir.
İyonik bileşiklerin özelliklerini, içerdikleri iyonların özellikleri belirler. Metallerin katyonları ve ametallerin anyonları, farklı kimyasal ve fiziksel özelliklere sahip çeşitli bileşikler oluşturabilir.
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Ceydoss
@c3yda_kvk
Kimya dersinde atom modelleri, elektron dizilimi ve elementlerin periyodik özellikleri ile ilgili önemli kavramları göreceğiz. Bu konular, maddenin temel yapısını anlamak ve kimyasal davranışlarını yorumlamak için çok önemlidir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bilim insanları atomu anlamak için farklı modeller geliştirmişlerdir. Dalton atomu bölünemeyen en küçük parça olarak tanımlarken, Thomson negatif yüklü elektronların keşfiyle "üzümlü kek" modelini ortaya koydu.
Rutherford deneyleriyle atomun çekirdek kavramını ortaya attı ve pozitif yüklerin merkezde toplandığını gösterdi. Bohr ise elektronların belirli enerji seviyelerinde bulunduğunu açıkladı.
Thomson atom modeli, maddenin atomdan daha küçük parçacıklardan oluştuğu fikrini ilk ortaya koyan modeldir. Bu modelden itibaren, atom "bölünemez" kavramından çıkarak daha karmaşık bir yapı olarak kabul edildi.
💡 Hatırlatma: Atom modelleri kronolojik olarak Dalton → Thomson → Rutherford → Bohr şeklinde gelişmiştir ve her yeni model bir öncekinin eksikliklerini gidermiştir.
Farklı atomların elektron dağılımları, Aufbau Kuralı'na göre yapılır. Bu kurala göre elektronlar, enerjisi en düşük orbitalden başlayarak yerleşirler. Enerji artışı 1s→2s→2p→3s→3p→4s→3d→4p şeklinde olur.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Atomlar elektronlarını belirli orbitallere dağıtırlar ve bu dağılım atomların davranışlarını belirler. Küresel simetri, elektronların atom çevresinde dengeli dağılmasıdır ve atom davranışlarını etkiler.
Bir atom, son orbitalinin yarı dolu veya tam dolu olması durumunda küresel simetri özelliği gösterir. Örneğin, Be atomunun $1s^2 2s^2$ elektron dizilimindeki son orbitali tam doludur ve küresel simetridir.
C atomu $1s^2 2s^2 2p^2$ son orbitalindeki tüm orbitaller yarı dolu veya tam dolu olmadığından küresel simetri göstermez. N atomu $1s^2 2s^2 2p^3$ ise $2p$ orbitallerinin tümü yarı dolu olduğundan küresel simetri özelliğine sahiptir.
💡 Püf Nokta: Küresel simetri özelliği gösteren atomlar daha kararlıdır ve kimyasal tepkimelere girme eğilimleri daha düşüktür.
Elementlerin periyodik tablodaki yerleri elektron dizilimlerinden belirlenebilir. Örneğin, He 1. periyot 8A'da, F 2. periyot 7A'da, P 3. periyot 5A'dadır.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Elektronlar bir atomdan ayrıldığında, kalan elektron dağılımı değişir. Bir atomun valans elektron sayısı, onun kimyasal davranışını belirleyen en önemli faktördür.
Periyodik tabloda atom yarıçapı sağdan sola ve yukarıdan aşağıya doğru artar. Bu nedenle Z > Y > X şeklinde sıralanırlar. İyonlaşma enerjisi ise genellikle aşağıdan yukarıya ve soldan sağa doğru artış gösterir.
Soy gazlar, 8A grubu elementleri olup elektron dizilimleri kararlıdır. Dış enerji seviyelerinde 8 elektron (He için 2 elektron) bulundururlar ve kimyasal tepkimelere girme eğilimleri çok düşüktür.
💡 Biliyor muydun? Periyodik tablodaki yerini bildiğin bir elementin, elektron dizilimini, valans elektron sayısını ve diğer fiziksel özelliklerini tahmin edebilirsin!
Elektron dağılımı yapılırken unutma: Aynı enerji düzeyinde, enerjisi eşit olan orbitallere (px, py, pz gibi) elektronlar önce birer birer ve aynı spinle yerleştirilir (Hund Kuralı). Aynı orbitalde ise iki elektron ancak zıt spinle bulunabilir (Pauli İlkesi).

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Metalik bağ, metal atomları arasında oluşan güçlü bir kimyasal bağdır. Metal atomlarının dış yörünge elektronlarının ortaklaşa kullanılmasıyla oluşur ve metallerin iletkenlik gibi özelliklerini belirler.
Aynı periyotta bulunan elementlerin metalik bağ kuvvetleri, valans elektron sayısı arttıkça artar. Bu nedenle Li, Be ve B elementleri arasında metalik bağ kuvveti B > Be > Li şeklinde sıralanır.
Periyodik tablodaki konumu bilinen bir elementin fiziksel ve kimyasal özellikleri hakkında tahminler yapabilirsin. Örneğin, alkali metaller (1A grubu) en aktif metallerdir ve kolayca elektron verirler.
💡 Önemli İpucu: Metalik bağ kuvveti, metalin erime ve kaynama noktasını, sertliğini ve iletkenliğini etkiler. Metalik bağı güçlü olan metaller daha yüksek erime noktasına sahiptir.
Benzer şekilde, bir elementin elektron dizilimini biliyorsan, onun hangi grupta ve periyotta olduğunu, metalik veya ametalik özelliklerini ve diğer elementlerle nasıl tepkime vereceğini tahmin edebilirsin.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Elementlerin elektron dağılımları belirli kurallara göre yapılır. Aufbau ilkesi, elektronların düşük enerjili orbitallerden başlayarak yerleştirilmesi gerektiğini söyler.
Hund kuralı, aynı enerjiye sahip orbitallere elektronlar önce tek tek ve aynı spinle yerleştirilmesi gerektiğini belirtir. Pauli ilkesi ise bir orbitalde en fazla iki elektronun bulunabileceğini ve bunların zıt spinli olması gerektiğini ifade eder.
Atom modellerinin tarihsel gelişimi, bilimin ilerleyişini gösterir. Dalton'un bölünemeyen atom fikrinden, Thomson'un elektronları keşfetmesine ve Rutherford'un çekirdek kavramını ortaya atmasına kadar bilgimiz sürekli genişlemiştir.
💡 Sınav İpucu: Elektron dağılımlarında kurallara uygun olmayan dizilimler genellikle sınavlarda sorulur. Bunları tespit edebilmek için Aufbau, Hund ve Pauli ilkelerini iyi anlamalısın!
Yanlış elektron dizilimlerini tespit ederken şunlara dikkat etmelisin: Enerjisi düşük orbitaller dolmadan yüksek enerjili orbitallere elektron yerleşmişse Aufbau ilkesine; eş enerjili orbitallere tek tek elektron yerleşmeden çift elektron yerleşmişse Hund kuralına; aynı orbitalde aynı spinli iki elektron varsa Pauli ilkesine aykırıdır.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Elementlerin periyodik tablodaki yerleri, onların kimyasal ve fiziksel özelliklerini belirler. Alkali metaller (1A) elektron vermeye, halojenler (7A) elektron almaya eğilimlidir.
Elektronegatiflik periyodik tabloda soldan sağa artar ve yukarıdan aşağıya azalır. Bu nedenle, aynı periyotta sağdaki elementler daha elektronegatiftir. Örneğin, Z > Y > X şeklinde sıralanabilir.
Metallerde pozitif yüklü metal iyonları ile serbest dolaşan valans elektronları arasındaki çekim kuvvetine metalik bağ denir. Bu bağ, metallerin elektrik iletkenliği, ısı iletkenliği ve şekil verilebilme özelliklerini belirler.
💡 Biliyor muydun? Metalik bağ kuvveti, metal atomlarının pozitif iyon yükü ve serbest valans elektron sayısı arttıkça güçlenir.
Atom numaraları ardışık elementlerde, atom numarası arttıkça elektronların çekirdeğe olan çekim kuvveti artar. Bu da genellikle atom yarıçapının küçülmesine neden olur. Ancak, yeni bir enerji seviyesine geçildiğinde atom yarıçapı aniden artar.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
İyonik bileşikler, katyonlar (pozitif yüklü iyonlar) ve anyonlar (negatif yüklü iyonlar) arasındaki elektrostatik çekim kuvvetleri ile oluşur. Bir bileşiğin formülü, içerdiği iyonların toplam yüklerinin birbirini nötrleştirmesiyle belirlenir.
gibi bir katyon, veya gibi anyonlarla birleşerek kararlı bileşikler oluşturabilir. Bu bileşiklerin formülleri iyonların yüklerini dengeleyecek şekilde yazılır: ve .
Bileşiklerin toplam atom sayısını hesaplarken, formüldeki her bir elementin atom sayısını toplamak gerekir. Örneğin, bileşiğinde 1 Ca, 2 N ve 6 O atomu olmak üzere toplam 9 atom vardır.
💡 Pratik Yöntem: İyonik bileşiklerin formülünü yazarken iyonların yüklerini çapraz yazarak indis olarak kullanabilirsin. Örneğin, ve için formülü elde edilir.
İyonik bileşiklerin özelliklerini, içerdikleri iyonların özellikleri belirler. Metallerin katyonları ve ametallerin anyonları, farklı kimyasal ve fiziksel özelliklere sahip çeşitli bileşikler oluşturabilir.
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
2
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı