Kimyada atomun yapısını ve davranışını anlamak için atom modellerini ve... Daha fazla göster
9. Sınıf Kimya 2. Ünite: Özellikle Testlerle Dolu Ders Notları






Atom Modelleri ve Atomun Yapısı
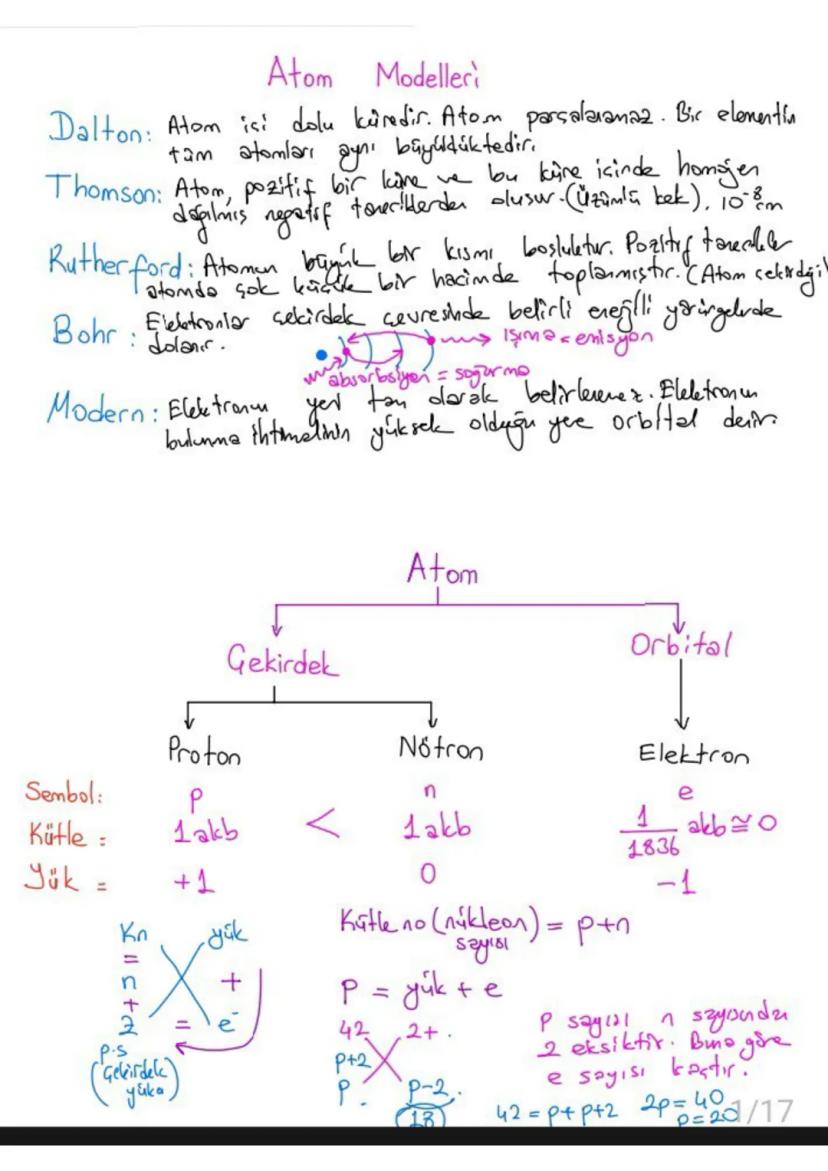
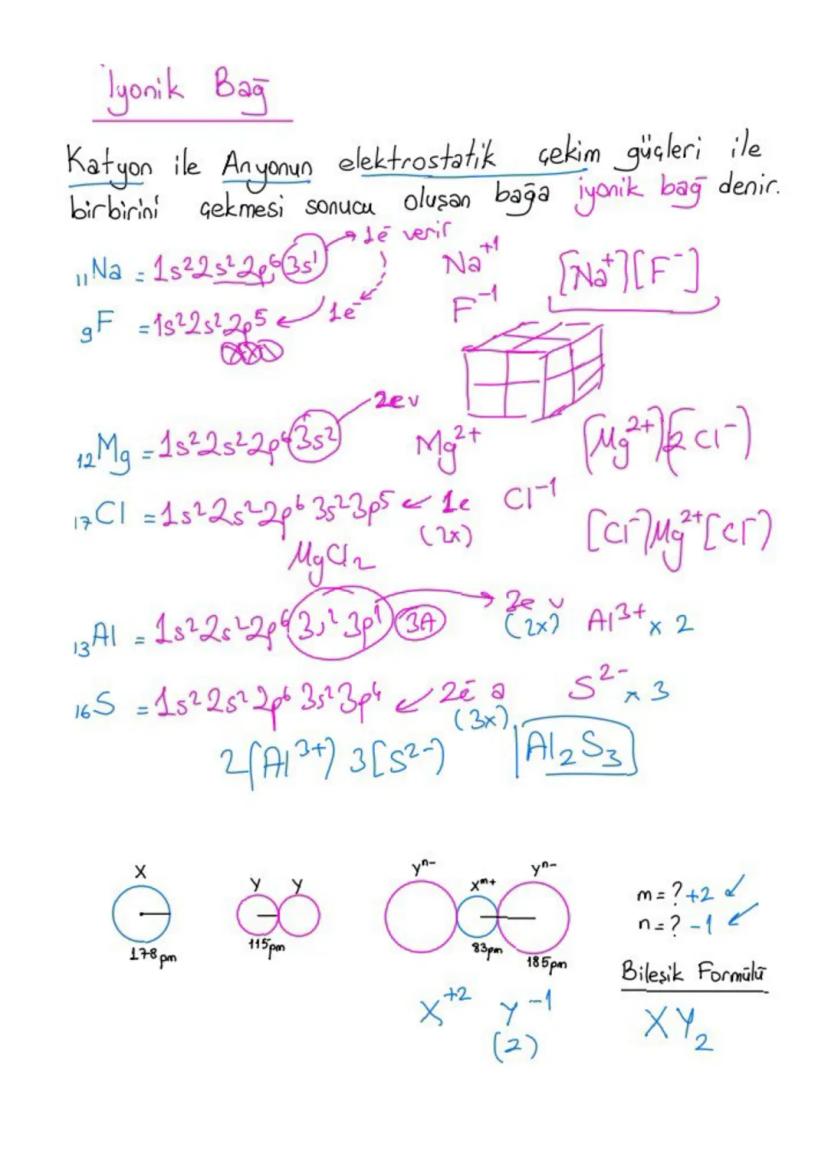
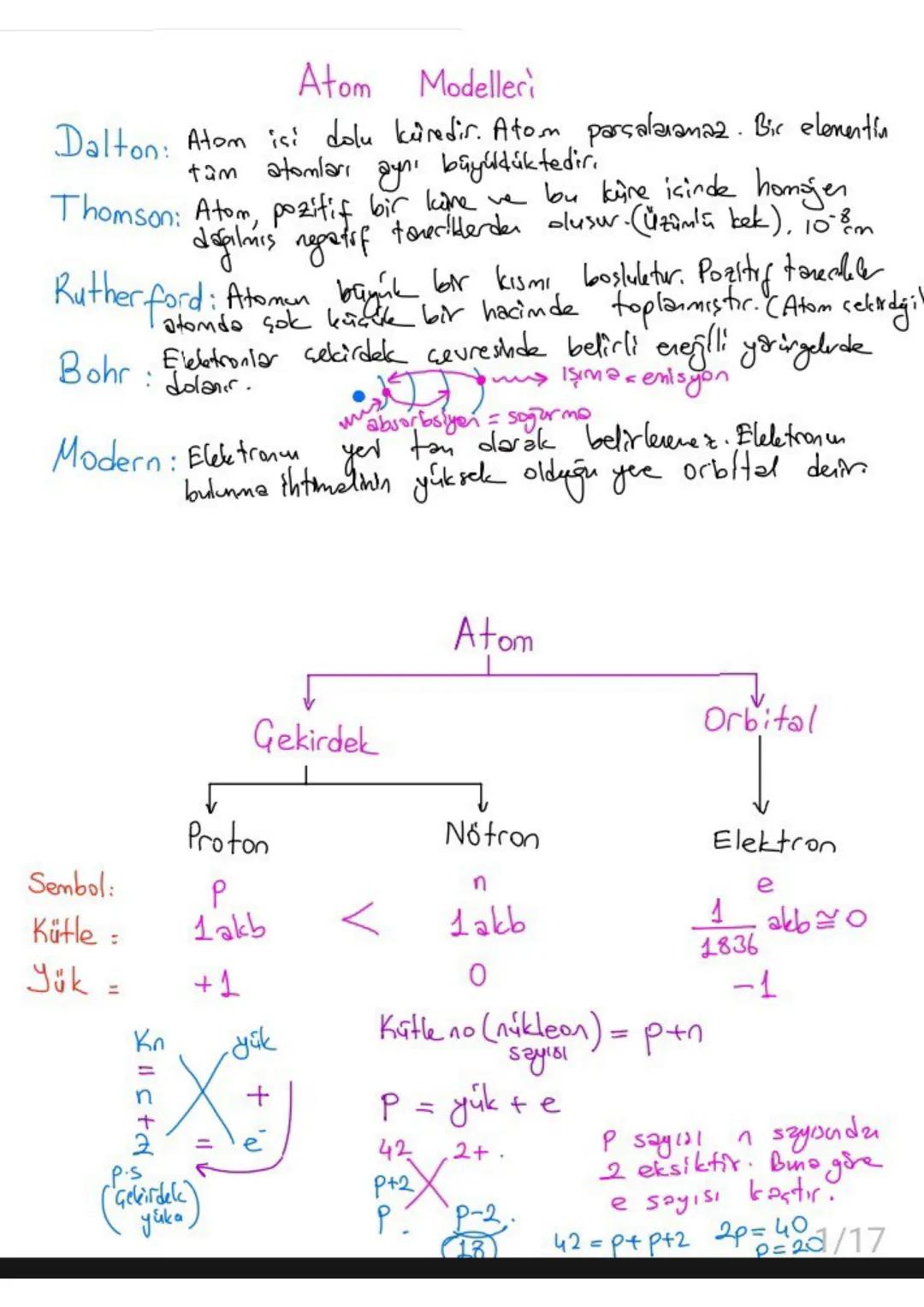
Atomun nasıl göründüğü konusunda bilim insanları farklı fikirler ortaya atmışlar. Dalton atomu bölünmez bir küre olarak düşünürken, Thomson "üzümlü kek" modeliyle elektronları keşfetti. Rutherford atomun çoğunun boş olduğunu ve merkezinde çekirdek bulunduğunu gösterdi.
Modern atom teorisine göre elektronların yeri kesin olarak bilinemez, sadece bulunma ihtimali yüksek olan bölgeler vardır. Bu bölgelere orbital denir.
Atomun temel parçacıkları şunlardır: Proton , nötron (yüksüz, 1 akb kütle) ve elektron . Proton sayısı elementin kimliğini belirler.
💡 Önemli: Kütle numarası = proton sayısı + nötron sayısı formülünü mutlaka hatırla!
Orbitaller ve Elektronların Dizilimi
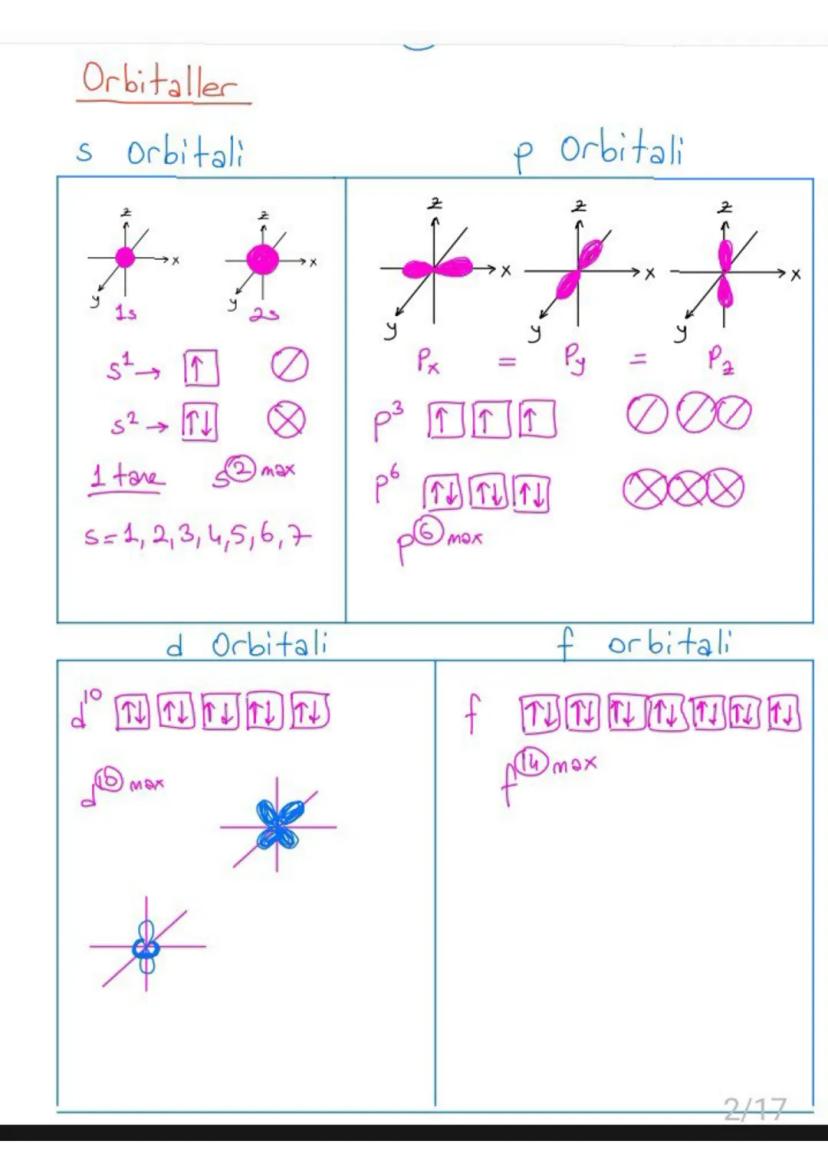
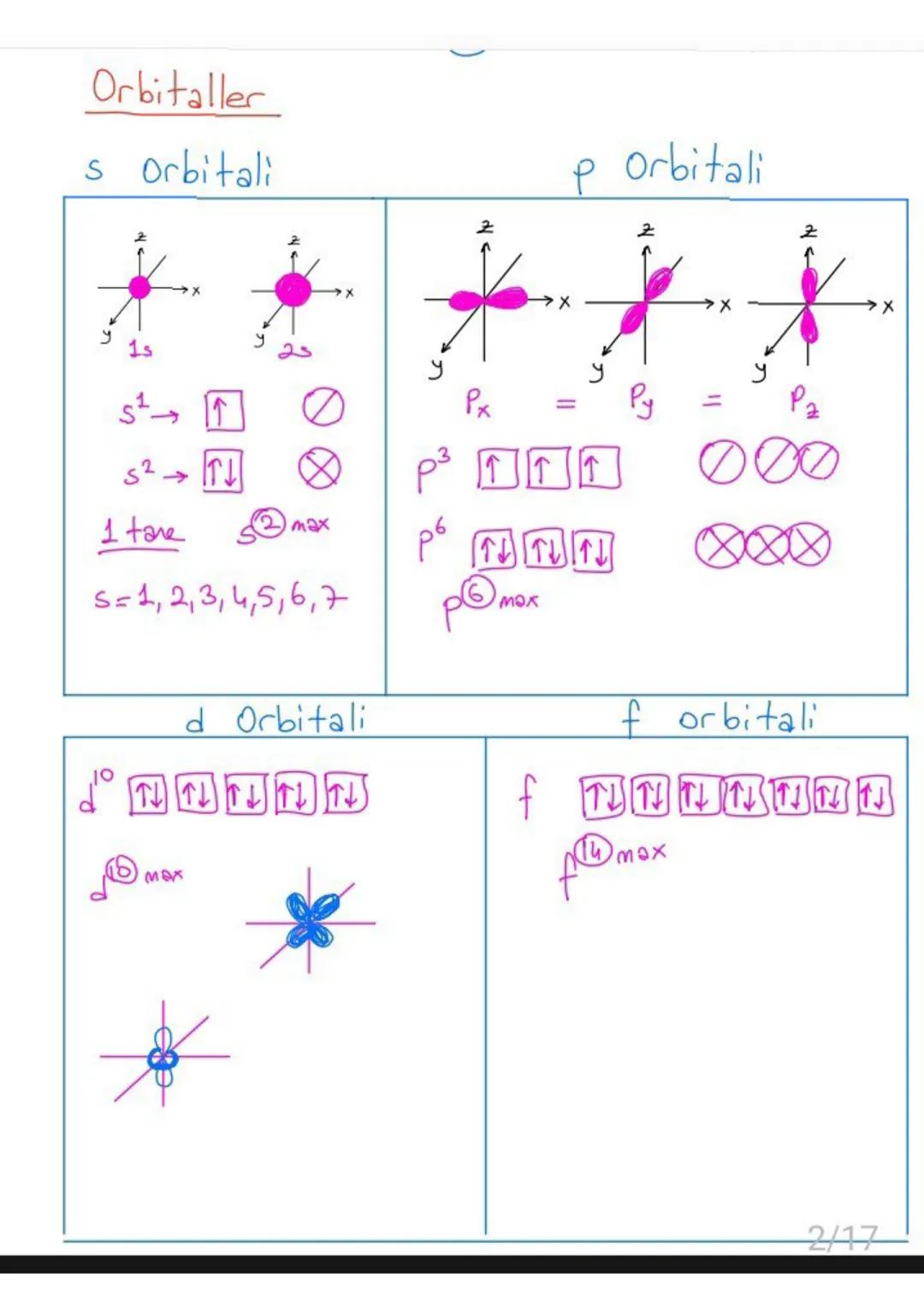
Orbitaller elektronların bulunabileceği enerji seviyelerindeki bölgelerdir. Her orbital tipinin kendine özgü şekli ve elektron kapasitesi vardır.
s orbitali küresel şekillidir ve maksimum 2 elektron alır. p orbitali dambıl şeklinde olup 3 adet bulunur (px, py, pz) ve toplam 6 elektron alabilir. d orbitali 5 adet olup 10 elektron, f orbitali ise 7 adet olup 14 elektron kapasitesi vardır.
Elektronlar orbitallere girerken önce tek tek, sonra çift olarak yerleşirler. Bu Pauli Dışarlama İlkesi gereğidir.
💡 Püf Nokta: Orbital kapasitelerini hatırla: s²p⁶d¹⁰f¹⁴

Elektronik Diziliş Kuralları
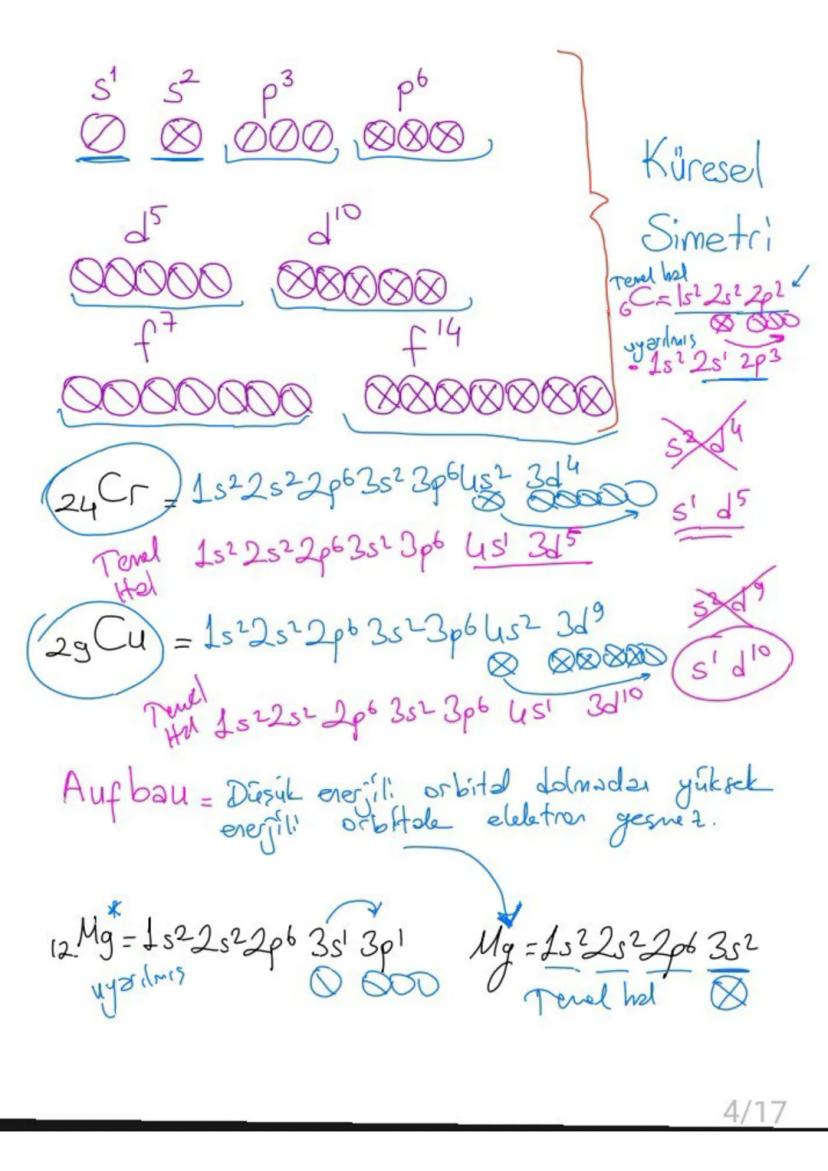
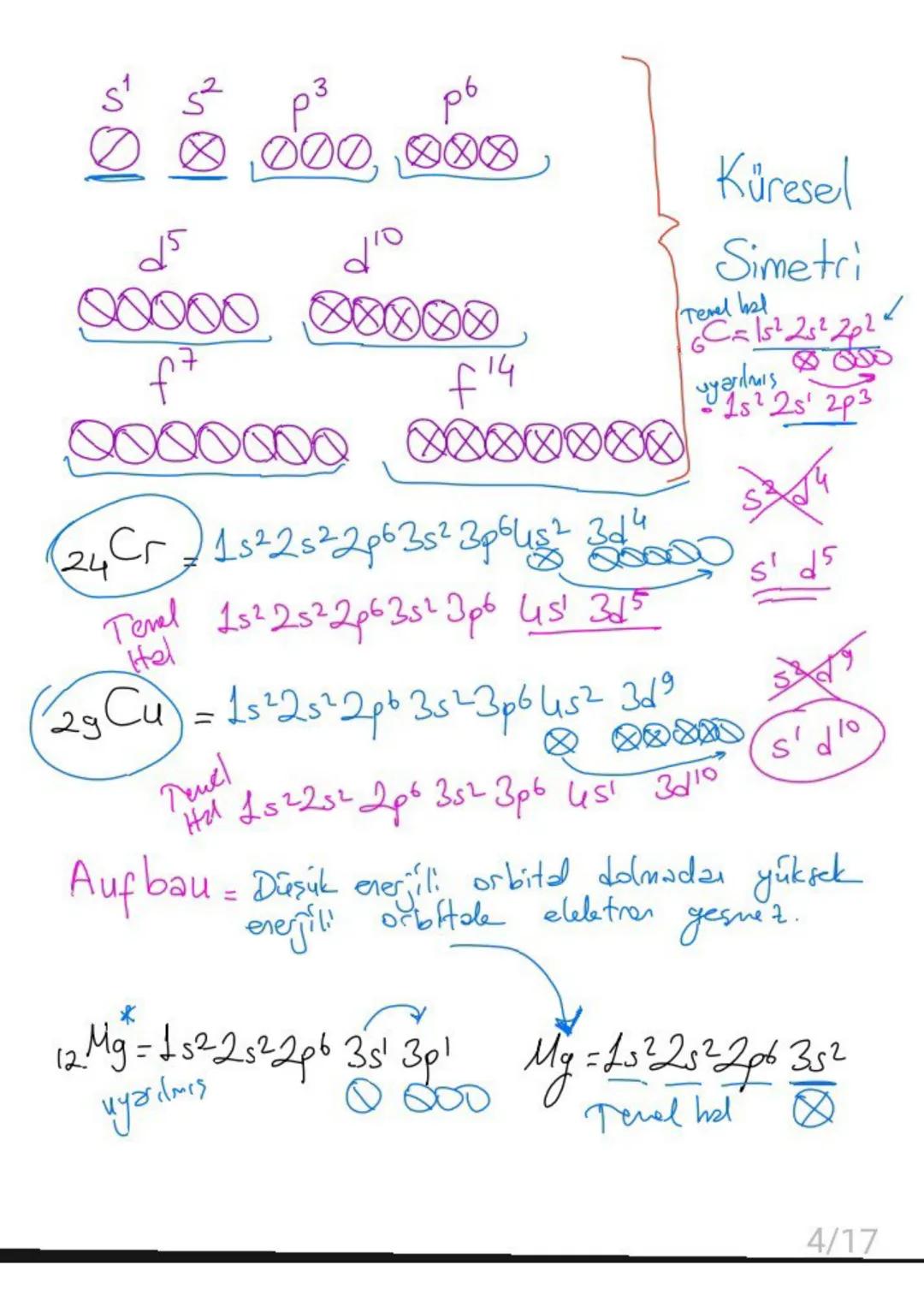
Elektronlar atomda Aufbau ilkesine göre dizilir: önce düşük enerjili orbitaller dolar. Ancak bazı elementlerde (Krom ve Bakır gibi) yarı dolu veya tam dolu d orbitalleri daha kararlı olduğu için elektronik diziliş farklılaşır.
24Cr: Beklenen 4s²3d⁴ yerine 4s¹3d⁵ dizilimi gösterir çünkü yarı dolu d orbitali daha kararlıdır. 29Cu: Beklenen 4s²3d⁹ yerine 4s¹3d¹⁰ dizilimi gösterir çünkü tam dolu d orbitali daha kararlıdır.
Bu istisnalar sınav sorularında sık çıkar, mutlaka ezberle!
💡 Dikkat: s³d⁴ → s¹d⁵ ve s²d⁹ → s¹d¹⁰ dönüşümlerini unutma!
Değerlik Orbitalleri
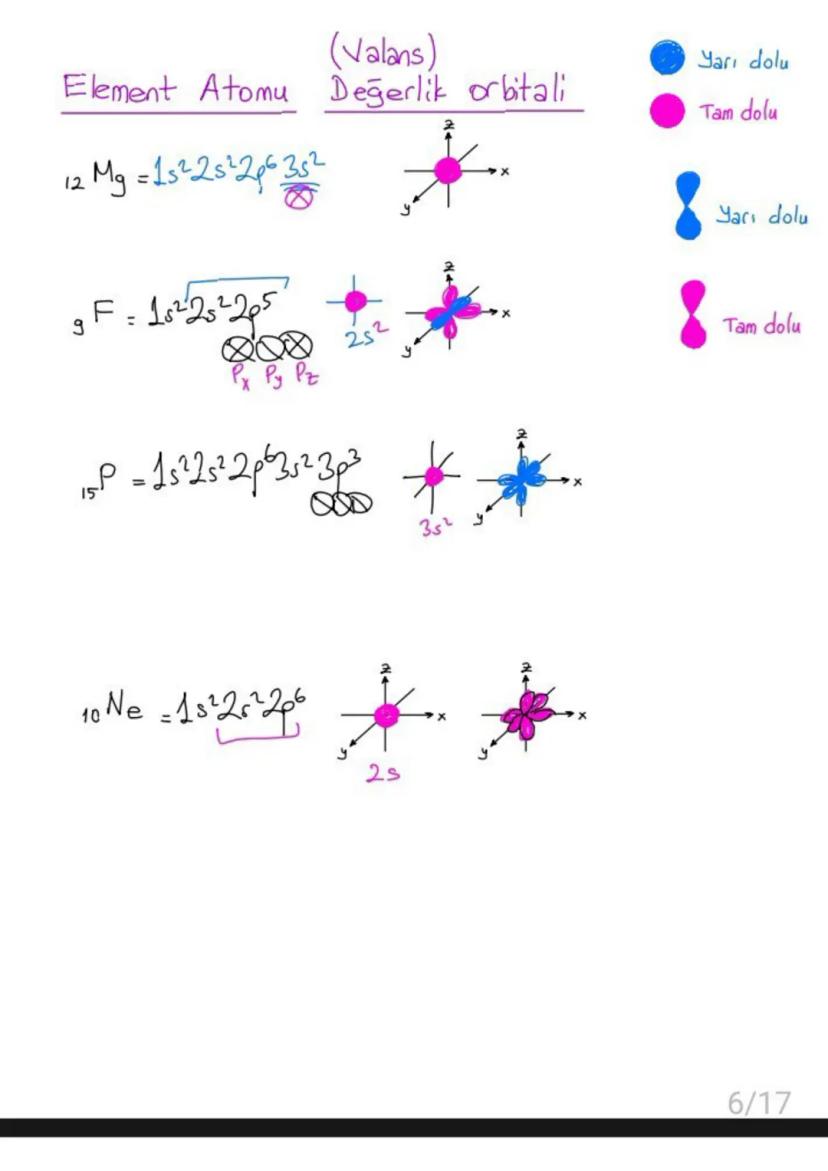
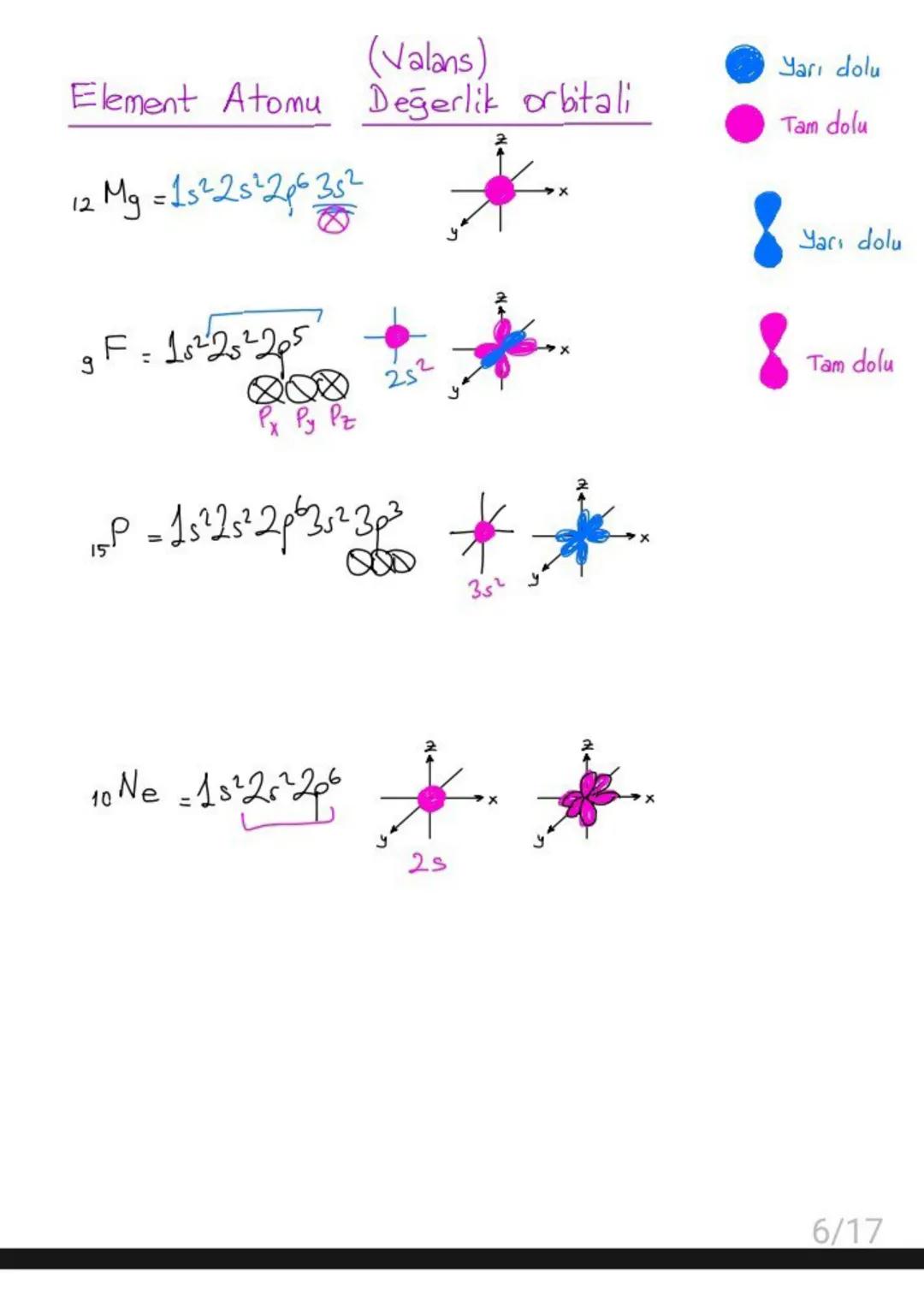
Değerlik orbitalleri atomun en dış katmanındaki elektronları içeren orbitallerdir. Bunlar elementin kimyasal davranışını belirler.
Örneğin 15P'nin elektronik dizilimi 1s²2s²2p⁶3s²3p³'tür. En dış katmandaki 3s²3p³ orbitalleri değerlik orbitallerini oluşturur. p orbitallerindeki 3 elektron tek tek dağılmış durumdadır.
Yarı dolu ve tam dolu orbitaller özel kararlılık gösterir. Bu yüzden kimyasal tepkimelerde elementler bu duruma ulaşmaya çalışır.
💡 Önemli: Değerlik elektronları elementin hangi grubunda olduğunu ve kimyasal özelliklerini belirler.

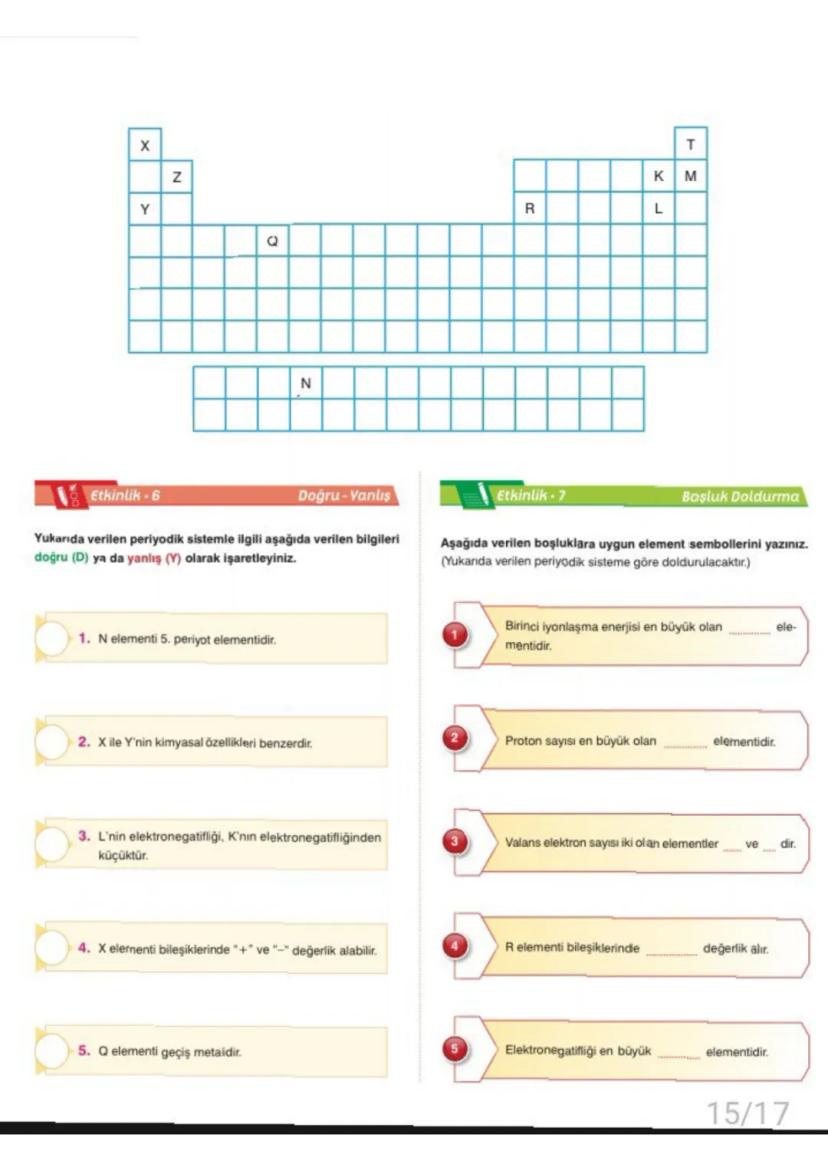
Periyodik Sistem ve Gruplar
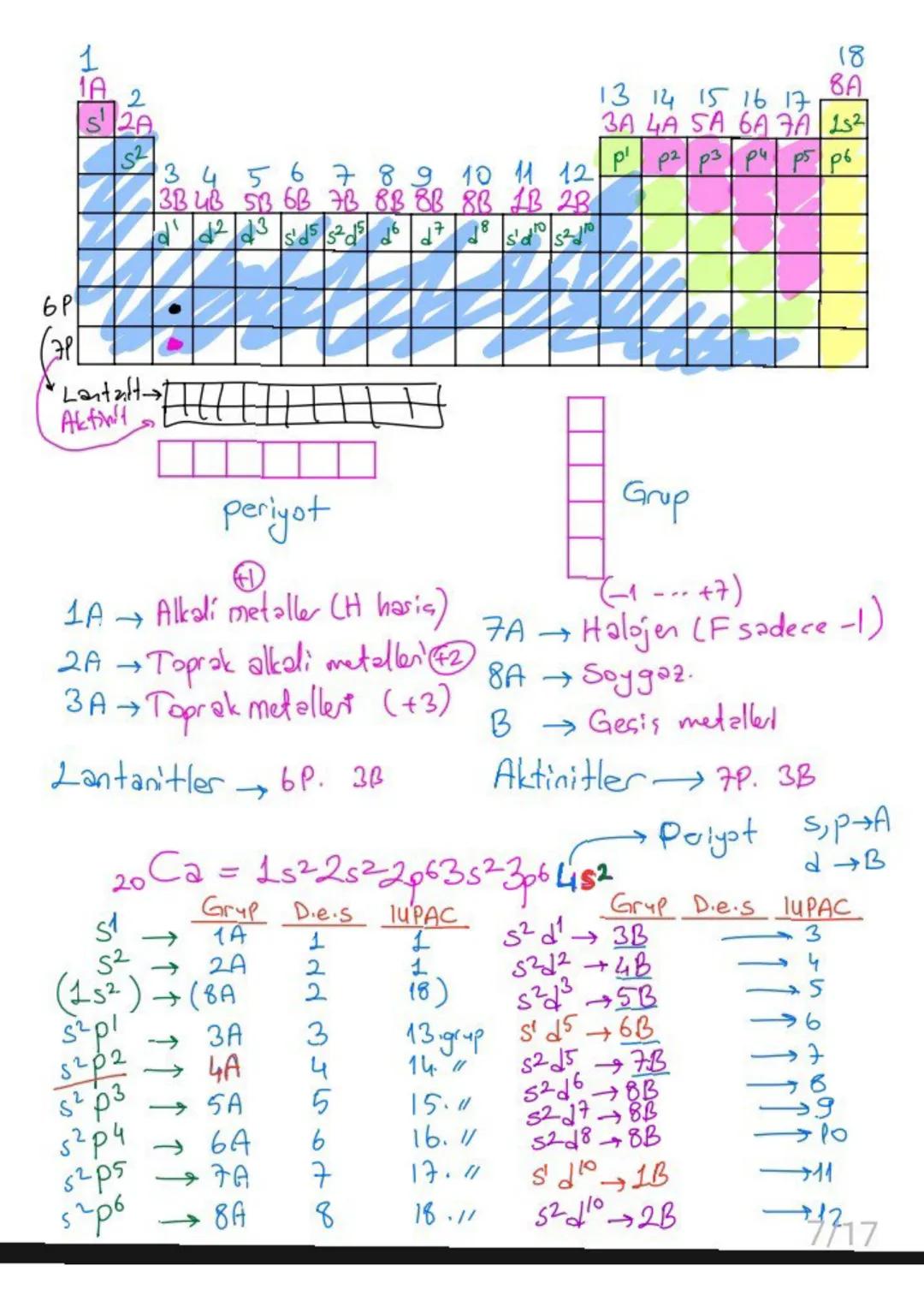
Periyodik sistem elementlerin elektronik dizilişlerine göre düzenlenmiştir. s bloku , p bloku ve d bloku (geçiş metalleri) vardır.
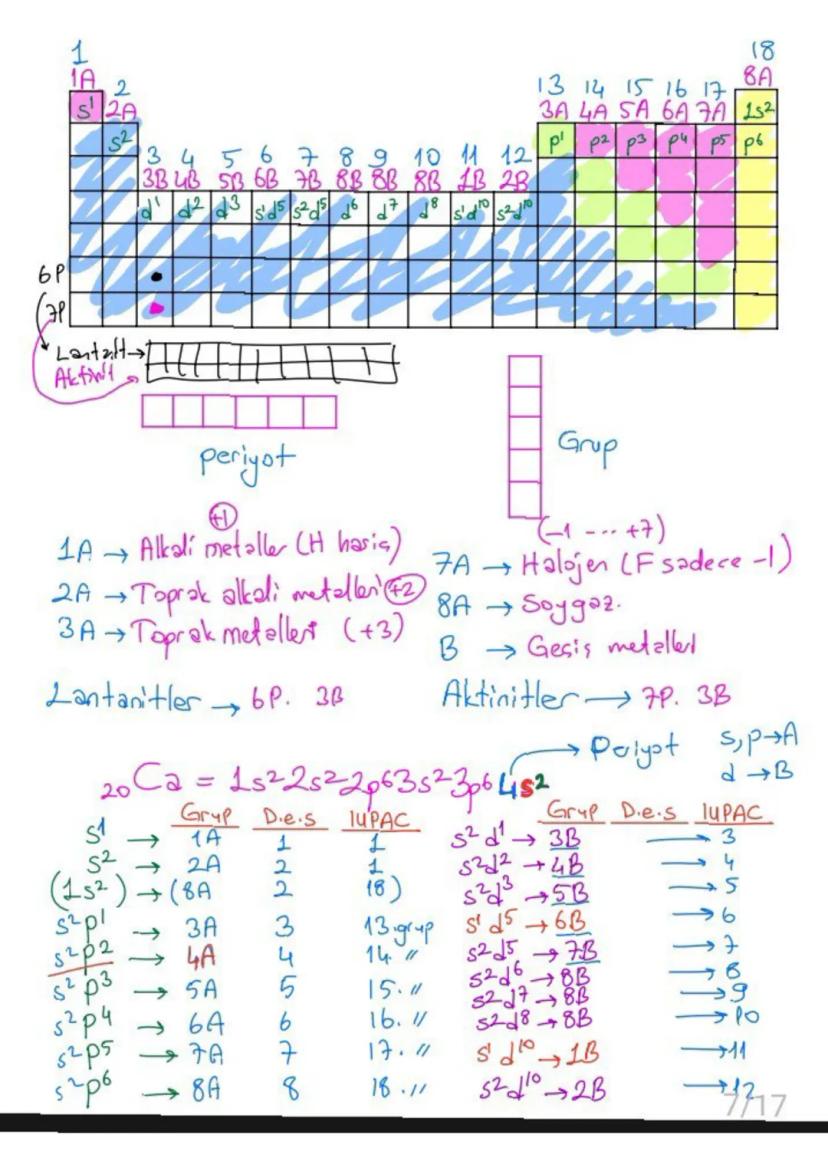
Grup numarasını bulmak için son elektronun bulunduğu orbital tipine bak: s¹→1A, s²→2A, s²p¹→3A gibi. d bloku elementleri için grup numarası = .
1A alkali metaller, 2A toprak alkali metaller, 7A halojenler, 8A soygazlar özel grup isimleridir. Her grubun kendine özgü kimyasal özellikleri vardır.
💡 Pratik İpucu: Elektronik dizilişten grup bulmak için son orbitale odaklan!
Periyodik Özellikler - Atom Yarıçapı
Atom yarıçapı periyodik sistemdeki en önemli özelliklerden biridir. Aynı periyotta soldan sağa gidildikçe proton sayısı arttığı için çekirdek elektronları daha güçlü çeker ve atom yarıçapı azalır.
Aynı grupta yukarıdan aşağı gidildikçe yeni elektron katmanları eklendiği için atom yarıçapı artar.
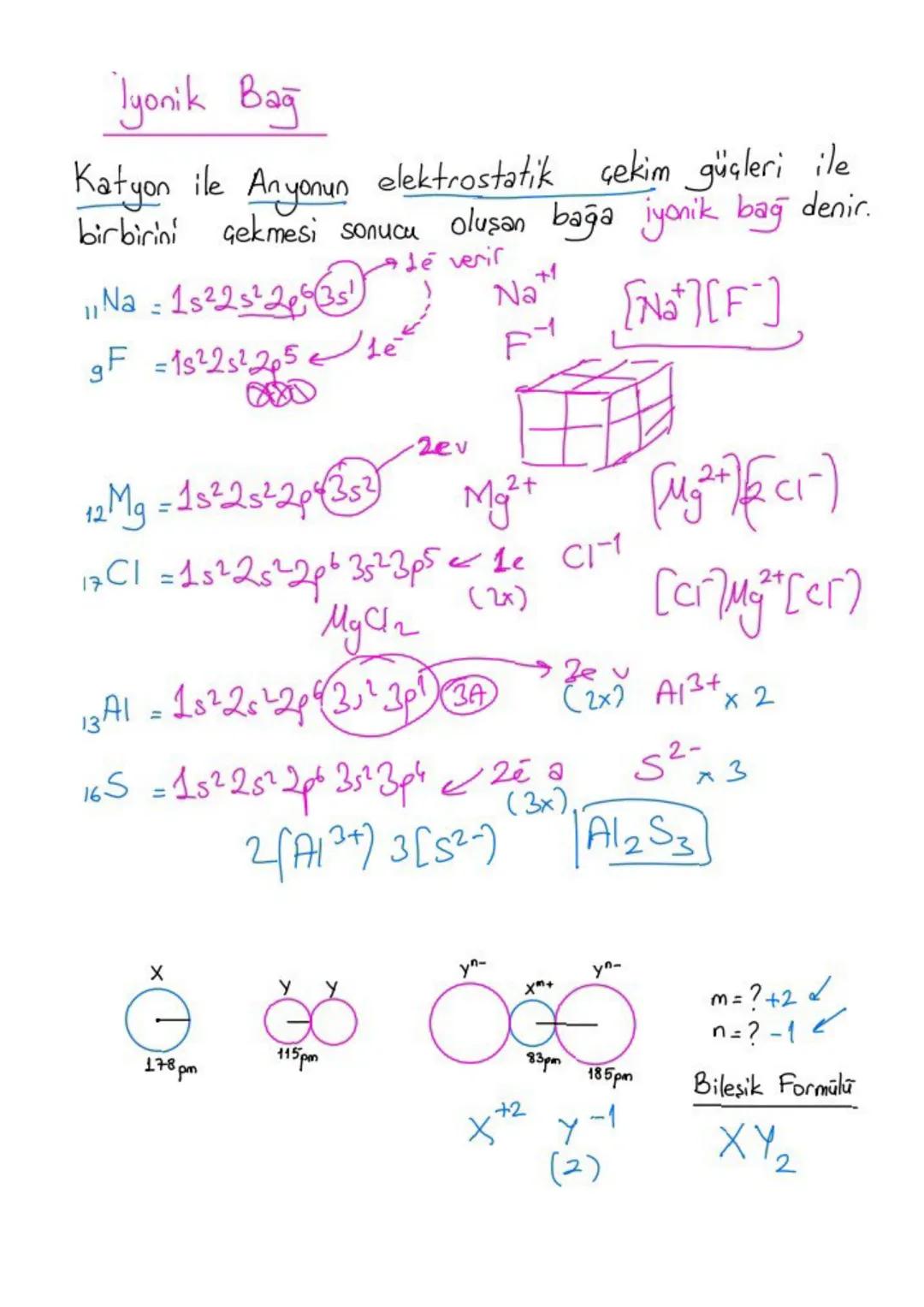
İyon yarıçapı için: Elektron kaybeden atomlar (katyonlar) küçülür, elektron kazanan atomlar (anyonlar) büyür. Aynı elektron sayısına sahip iyonlarda proton sayısı fazla olanın yarıçapı daha küçüktür.
💡 Hatırla: Periyotta sağa doğru küçülme, grupta aşağı doğru büyüme!
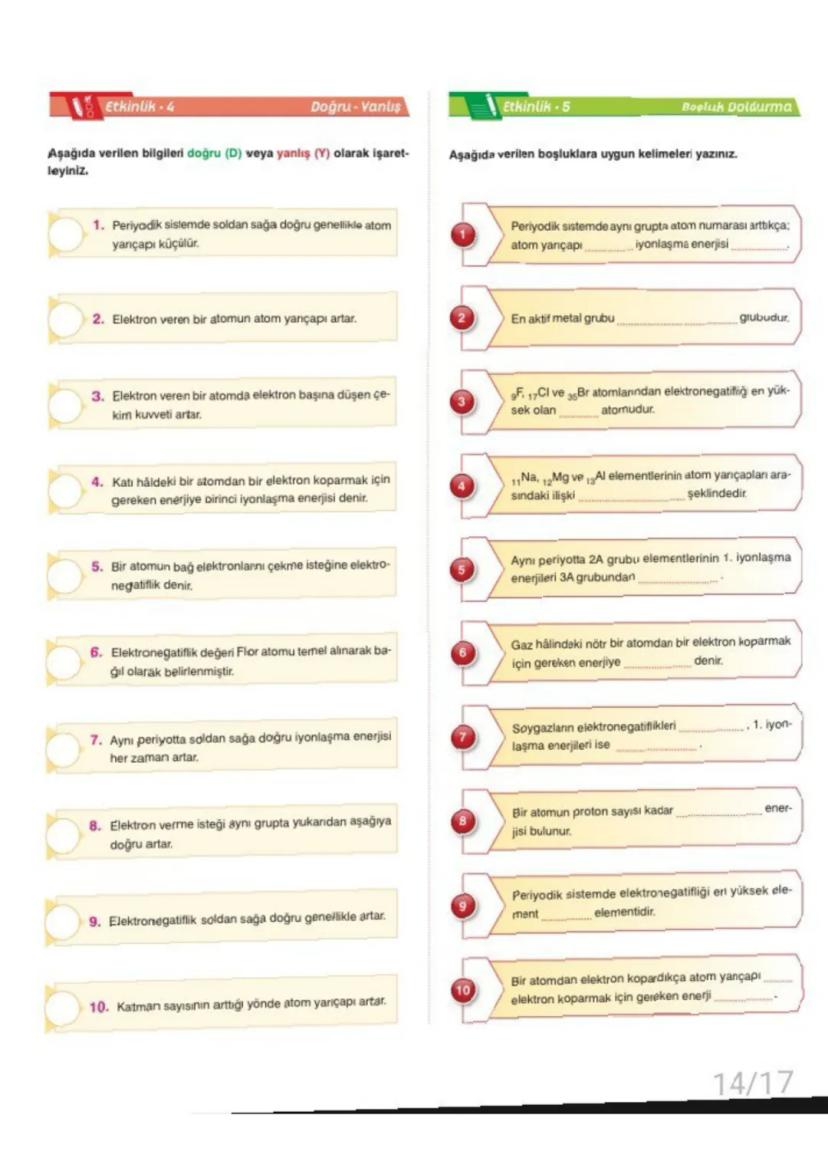
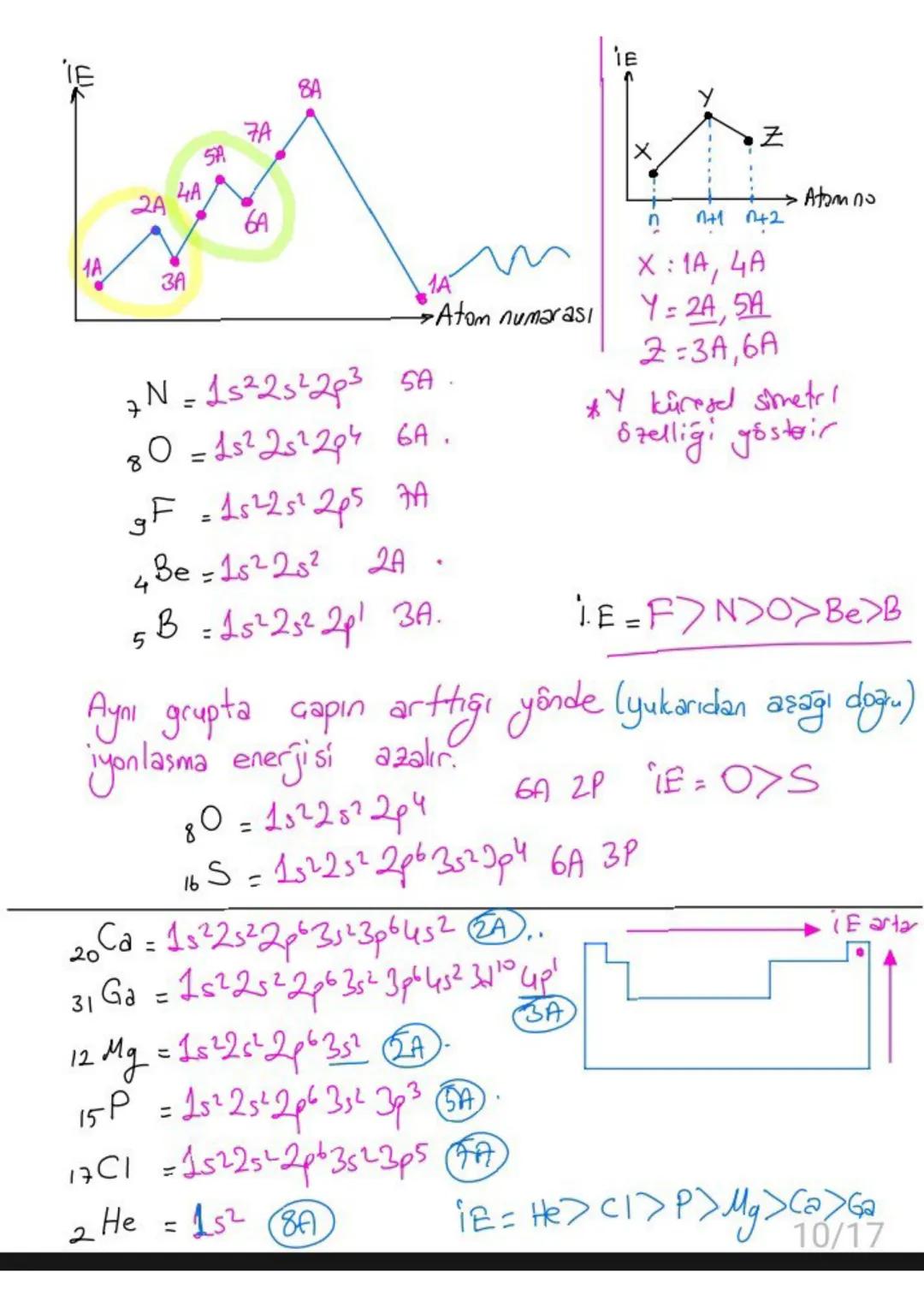
İyonlaşma Enerjisi
İyonlaşma enerjisi bir atomdan elektron koparmak için gereken enerjidir. Atom yarıçapı ile ters orantılıdır: küçük atomlarda elektronlar çekirdeğe daha yakın olduğu için koparılması daha zor.
Aynı periyotta soldan sağa gidildikçe iyonlaşma enerjisi artar. Aynı grupta aşağı gidildikçe iyonlaşma enerjisi azalır.
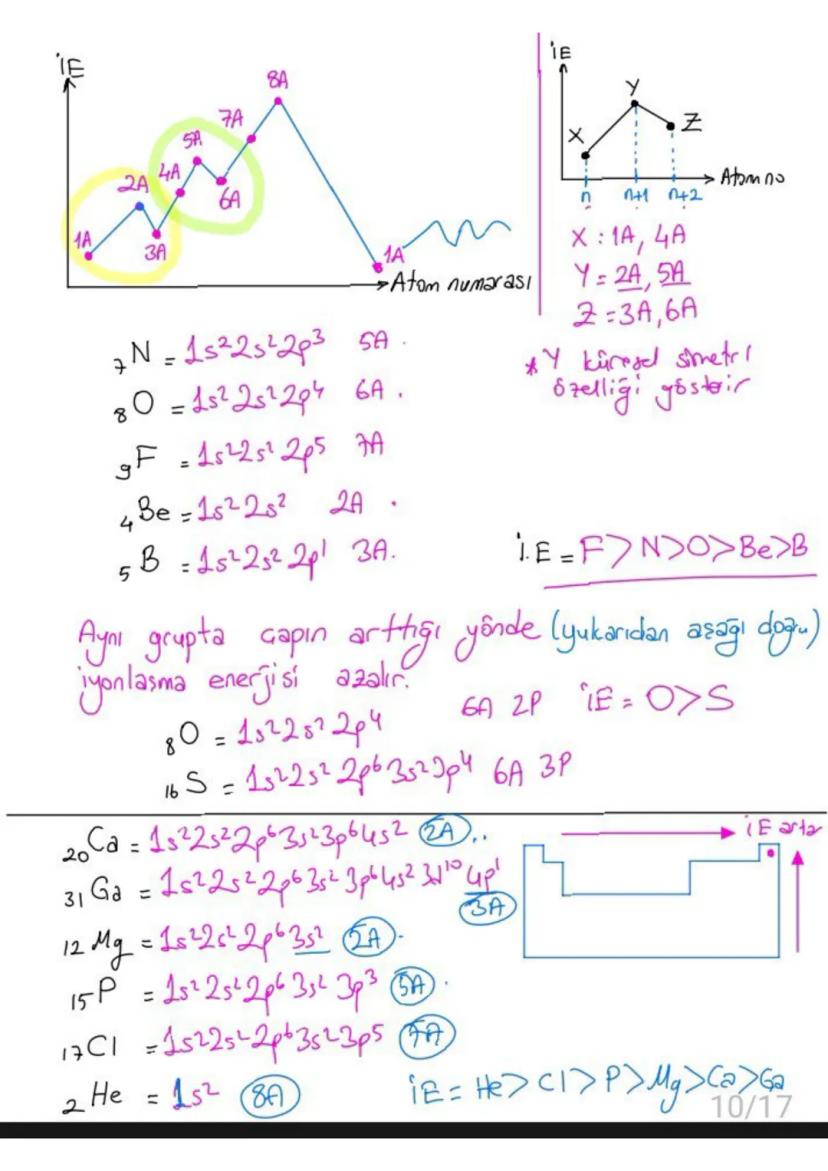
Yarı dolu ve tam dolu orbitaller özel kararlılık gösterdiği için bu durumları bozacak iyonlaşmalar daha zor gerçekleşir. Bu yüzden 2A gruplarının iyonlaşma enerjisi 3A'dan yüksektir.
💡 İpucu: İyonlaşma enerjisi sıralaması yaparken önce periyot, sonra grup etkisini düşün!

Elektronegatiflik ve Metalik Özellikler
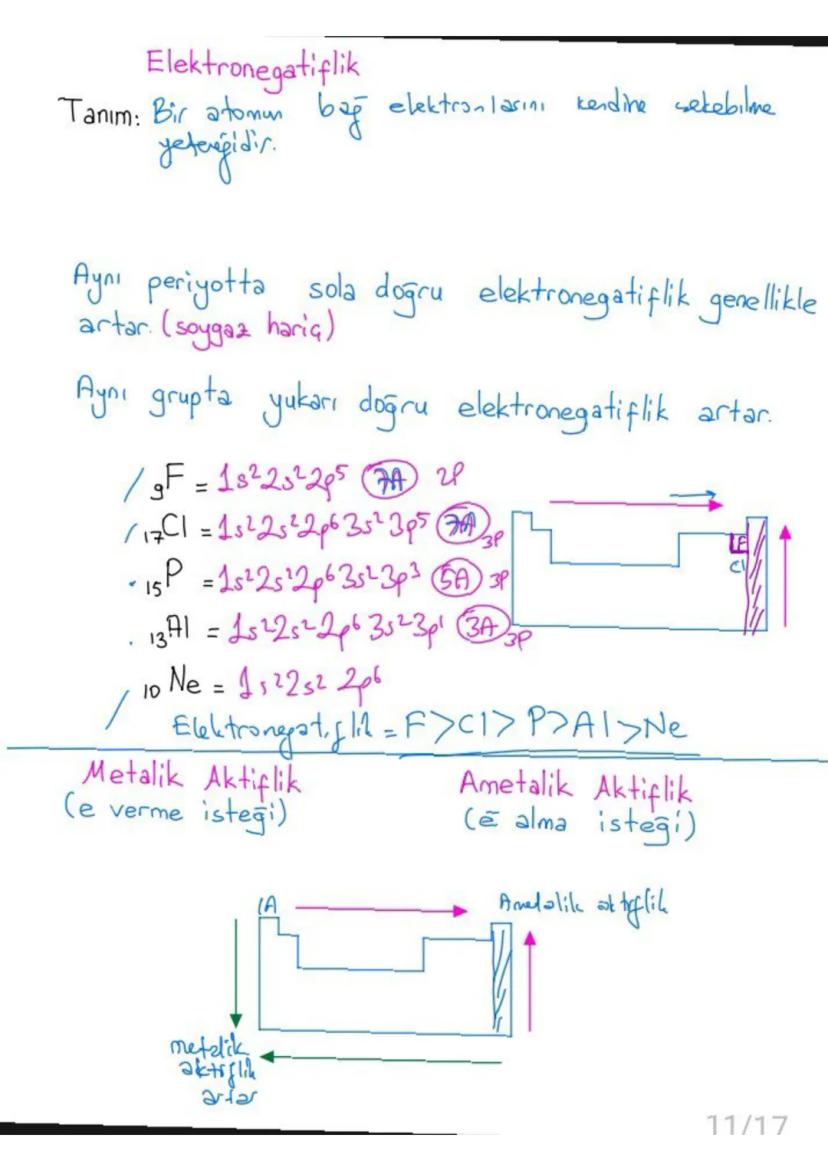
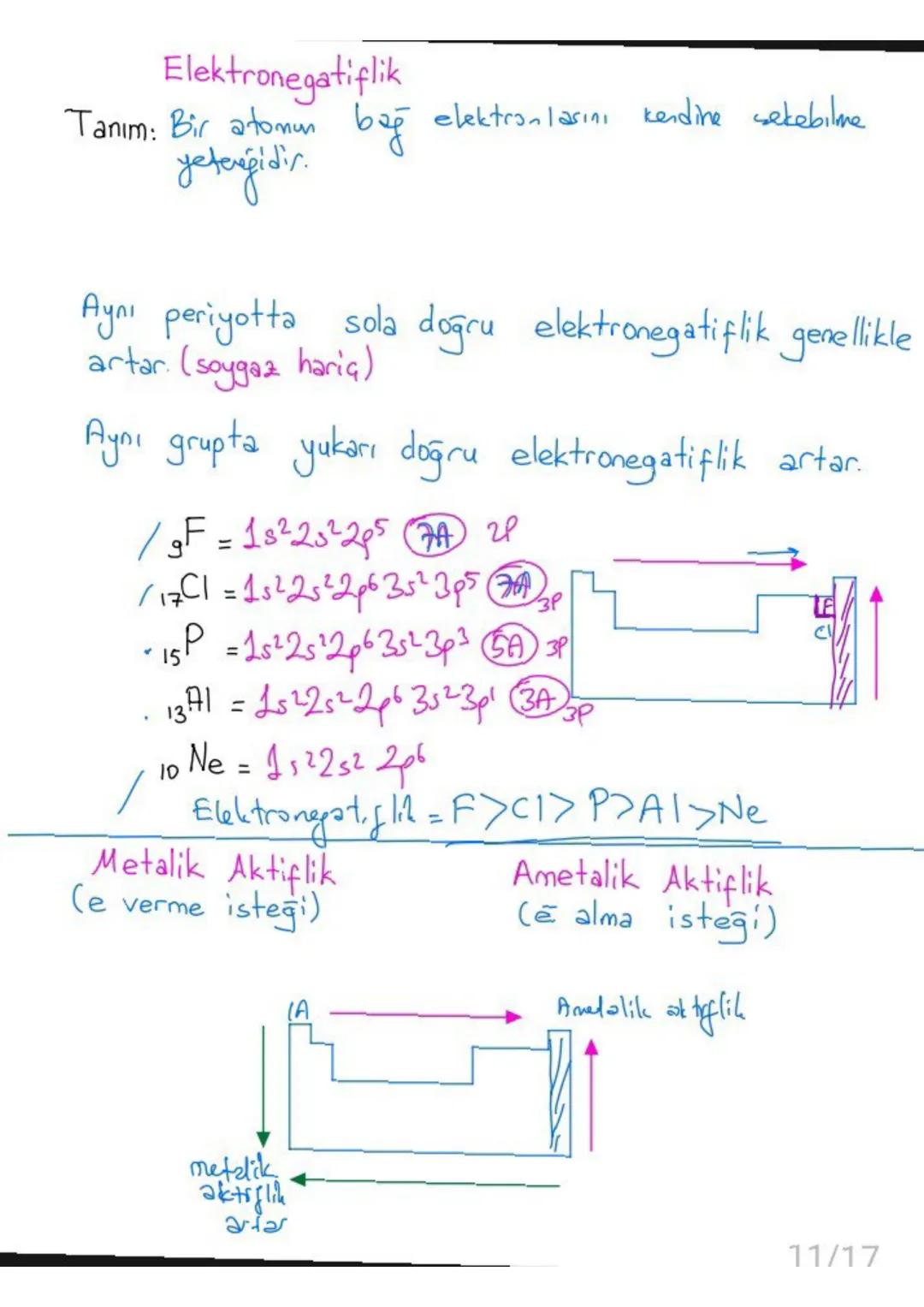
Elektronegatiflik bir atomun bağ elektronlarını kendine çekme yeteneğidir. Periyodik sistemde sağ üst köşeye doğru artar, flor en elektronegatif elementtir.
Aynı periyotta soldan sağa elektronegatiflik artar, aynı grupta yukarı doğru elektronegatiflik artar. Soygazların elektronegatifliği tanımlanmaz çünkü bağ oluşturmazlar.
Metalik karakter elektronegatiflikle ters orantılıdır. Soldaki elementler metal, sağdakiler ametal özellik gösterir. Metal olanlar elektron verme, ametal olanlar elektron alma eğilimindedir.
💡 Kolay Hatırlama: Flor'dan uzaklaştıkça elektronegatiflik azalır!

Metalik Bağ ve Metal Özellikleri
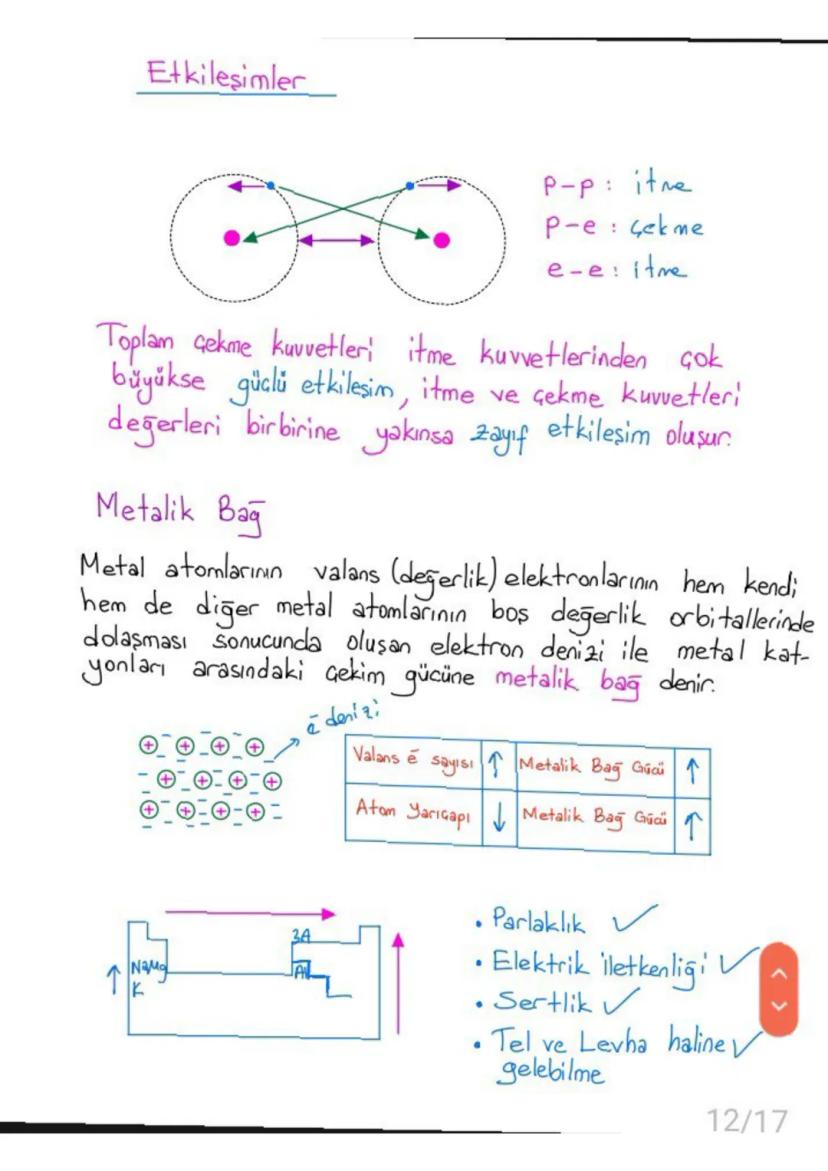
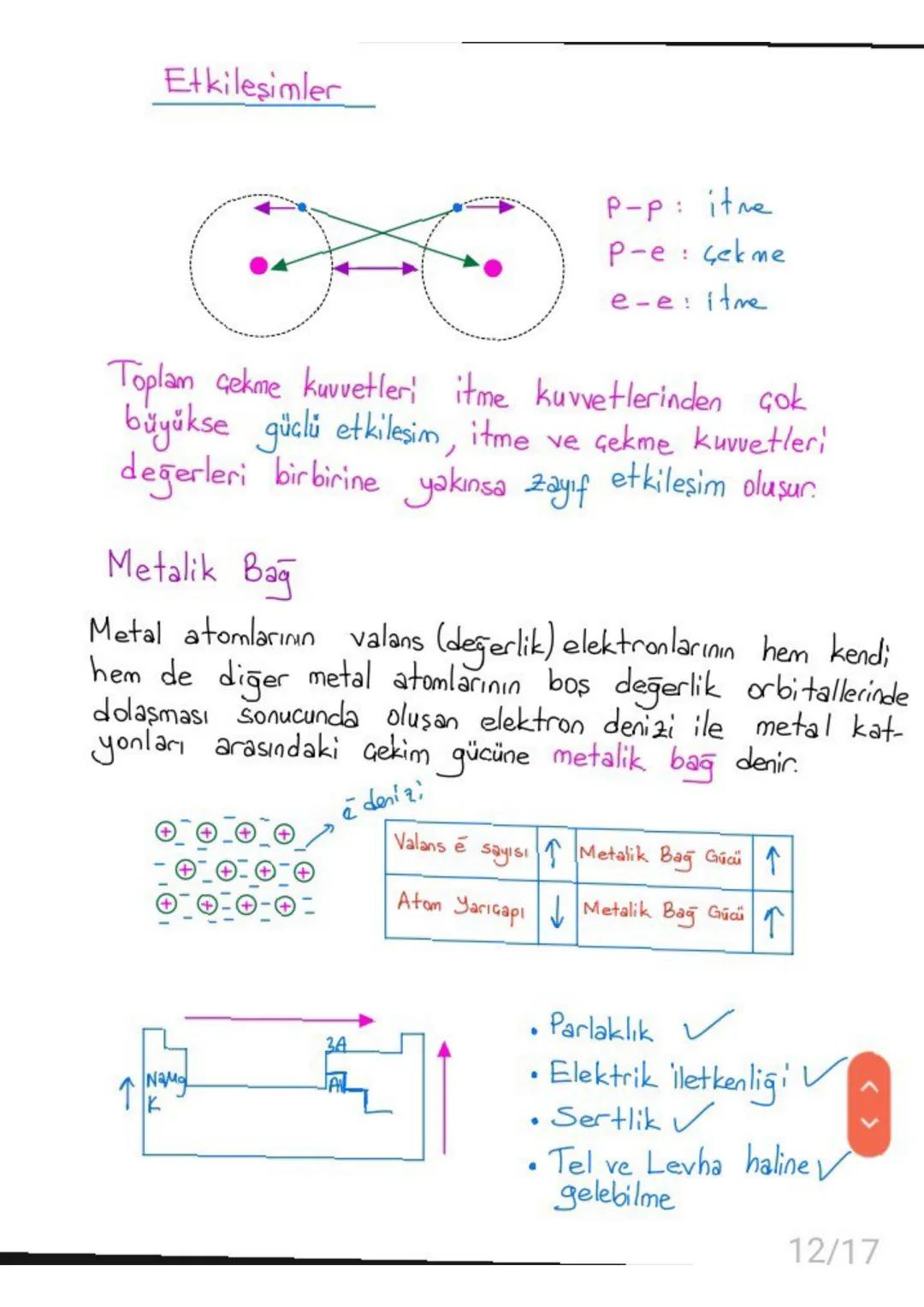
Metalik bağ metal atomlarının değerlik elektronlarının tüm metal kafes boyunca serbestçe hareket etmesiyle oluşur. Bu "elektron denizi" metal katyonlarını bir arada tutar.
Metalik bağın gücü değerlik elektron sayısı arttıkça güçlenir, atom yarıçapı azaldıkça güçlenir. Bu nedenle küçük atomlu, çok değerlik elektronlu metaller daha sert ve yüksek erime noktasına sahiptir.
Metallerin parlaklık, elektrik iletkenliği, tel-levha haline gelebilme gibi özellikleri metalik bağdan kaynaklanır.
💡 Önemli: Metalik bağ gücü = değerlik elektron sayısı / atom yarıçapı oranıyla artar!
Periyodik Özellikler Özeti ve Test Soruları
Periyodik özellikler için genel kurallar: Atom yarıçapı sol alt köşede maksimum, iyonlaşma enerjisi ve elektronegatiflik sağ üst köşede maksimum.
1A alkali metaller en aktif metallerdir. Aynı periyotta 2A grubunun iyonlaşma enerjisi 3A'dan yüksektir (tam dolu s orbitali kararlılığı).
Test sorularında bu özelliklerin periyottaki ve gruptaki değişimini karşılaştırman istenebilir. Her zaman önce atomların periyodik sistemdeki yerini belirle, sonra kuralları uygula.
💡 Sınav İpucu: Periyodik özellik sorularında önce elementleri yerleştir, sonra trendi uygula!


Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Ionic Bond
9Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimya
İyonik bağlı bileşiklerin oluşumu ve adlandırılması kovalent bağlı bileşiklerin adlandırılması
9. Sınıf kimya
Etkiletişimler konu anlatımı içerisinde sorularda mevcuttur.
Türler arası etkileşimler 1
Türler arası etkileşimler 1
kimyasal türler arası etkileşimler; güçlü etkileşimler
güçlü etkileşimler detaylı konu anlatım notları
Kimyasal türler arasi etkileşimler
Bu ders notu kimyasal türler arasi etkileşimler konu anlatımı içerir
Tyt Kimya Kimyasal türler arası etkileşimler
Tyt Kimya özet ders notu
İyonik Bağ
9.Sinif Kimya
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Lewis Nokta Yapısı
Lewis Nokta yapısı
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
En popüler içerikler
98.sınıf matematik
Tüm üniteleri içermektedir!
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
11. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
9.sınıf tarih ders notları
Yeni maarif modele uygundur
İnkılap tarihi
Beğenin
TYT AYT TARİH
Tarih
9. Sınıf edebiyat ders notları.
9. Sınıflar için Türk Dili edebiyatı notları.
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
9. Sınıf Kimya 2. Ünite: Özellikle Testlerle Dolu Ders Notları
Kimyada atomun yapısını ve davranışını anlamak için atom modellerini ve orbitallerini bilmen gerekiyor. Bu konular, periyodik sistemdeki elementlerin özelliklerini ve neden farklı şekillerde davrandıklarını açıklıyor.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Atom Modelleri ve Atomun Yapısı
Atomun nasıl göründüğü konusunda bilim insanları farklı fikirler ortaya atmışlar. Dalton atomu bölünmez bir küre olarak düşünürken, Thomson "üzümlü kek" modeliyle elektronları keşfetti. Rutherford atomun çoğunun boş olduğunu ve merkezinde çekirdek bulunduğunu gösterdi.
Modern atom teorisine göre elektronların yeri kesin olarak bilinemez, sadece bulunma ihtimali yüksek olan bölgeler vardır. Bu bölgelere orbital denir.
Atomun temel parçacıkları şunlardır: Proton , nötron (yüksüz, 1 akb kütle) ve elektron . Proton sayısı elementin kimliğini belirler.
💡 Önemli: Kütle numarası = proton sayısı + nötron sayısı formülünü mutlaka hatırla!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Orbitaller ve Elektronların Dizilimi
Orbitaller elektronların bulunabileceği enerji seviyelerindeki bölgelerdir. Her orbital tipinin kendine özgü şekli ve elektron kapasitesi vardır.
s orbitali küresel şekillidir ve maksimum 2 elektron alır. p orbitali dambıl şeklinde olup 3 adet bulunur (px, py, pz) ve toplam 6 elektron alabilir. d orbitali 5 adet olup 10 elektron, f orbitali ise 7 adet olup 14 elektron kapasitesi vardır.
Elektronlar orbitallere girerken önce tek tek, sonra çift olarak yerleşirler. Bu Pauli Dışarlama İlkesi gereğidir.
💡 Püf Nokta: Orbital kapasitelerini hatırla: s²p⁶d¹⁰f¹⁴

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektronik Diziliş Kuralları
Elektronlar atomda Aufbau ilkesine göre dizilir: önce düşük enerjili orbitaller dolar. Ancak bazı elementlerde (Krom ve Bakır gibi) yarı dolu veya tam dolu d orbitalleri daha kararlı olduğu için elektronik diziliş farklılaşır.
24Cr: Beklenen 4s²3d⁴ yerine 4s¹3d⁵ dizilimi gösterir çünkü yarı dolu d orbitali daha kararlıdır. 29Cu: Beklenen 4s²3d⁹ yerine 4s¹3d¹⁰ dizilimi gösterir çünkü tam dolu d orbitali daha kararlıdır.
Bu istisnalar sınav sorularında sık çıkar, mutlaka ezberle!
💡 Dikkat: s³d⁴ → s¹d⁵ ve s²d⁹ → s¹d¹⁰ dönüşümlerini unutma!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Değerlik Orbitalleri
Değerlik orbitalleri atomun en dış katmanındaki elektronları içeren orbitallerdir. Bunlar elementin kimyasal davranışını belirler.
Örneğin 15P'nin elektronik dizilimi 1s²2s²2p⁶3s²3p³'tür. En dış katmandaki 3s²3p³ orbitalleri değerlik orbitallerini oluşturur. p orbitallerindeki 3 elektron tek tek dağılmış durumdadır.
Yarı dolu ve tam dolu orbitaller özel kararlılık gösterir. Bu yüzden kimyasal tepkimelerde elementler bu duruma ulaşmaya çalışır.
💡 Önemli: Değerlik elektronları elementin hangi grubunda olduğunu ve kimyasal özelliklerini belirler.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Periyodik Sistem ve Gruplar
Periyodik sistem elementlerin elektronik dizilişlerine göre düzenlenmiştir. s bloku , p bloku ve d bloku (geçiş metalleri) vardır.
Grup numarasını bulmak için son elektronun bulunduğu orbital tipine bak: s¹→1A, s²→2A, s²p¹→3A gibi. d bloku elementleri için grup numarası = .
1A alkali metaller, 2A toprak alkali metaller, 7A halojenler, 8A soygazlar özel grup isimleridir. Her grubun kendine özgü kimyasal özellikleri vardır.
💡 Pratik İpucu: Elektronik dizilişten grup bulmak için son orbitale odaklan!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Periyodik Özellikler - Atom Yarıçapı
Atom yarıçapı periyodik sistemdeki en önemli özelliklerden biridir. Aynı periyotta soldan sağa gidildikçe proton sayısı arttığı için çekirdek elektronları daha güçlü çeker ve atom yarıçapı azalır.
Aynı grupta yukarıdan aşağı gidildikçe yeni elektron katmanları eklendiği için atom yarıçapı artar.
İyon yarıçapı için: Elektron kaybeden atomlar (katyonlar) küçülür, elektron kazanan atomlar (anyonlar) büyür. Aynı elektron sayısına sahip iyonlarda proton sayısı fazla olanın yarıçapı daha küçüktür.
💡 Hatırla: Periyotta sağa doğru küçülme, grupta aşağı doğru büyüme!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
İyonlaşma Enerjisi
İyonlaşma enerjisi bir atomdan elektron koparmak için gereken enerjidir. Atom yarıçapı ile ters orantılıdır: küçük atomlarda elektronlar çekirdeğe daha yakın olduğu için koparılması daha zor.
Aynı periyotta soldan sağa gidildikçe iyonlaşma enerjisi artar. Aynı grupta aşağı gidildikçe iyonlaşma enerjisi azalır.
Yarı dolu ve tam dolu orbitaller özel kararlılık gösterdiği için bu durumları bozacak iyonlaşmalar daha zor gerçekleşir. Bu yüzden 2A gruplarının iyonlaşma enerjisi 3A'dan yüksektir.
💡 İpucu: İyonlaşma enerjisi sıralaması yaparken önce periyot, sonra grup etkisini düşün!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektronegatiflik ve Metalik Özellikler
Elektronegatiflik bir atomun bağ elektronlarını kendine çekme yeteneğidir. Periyodik sistemde sağ üst köşeye doğru artar, flor en elektronegatif elementtir.
Aynı periyotta soldan sağa elektronegatiflik artar, aynı grupta yukarı doğru elektronegatiflik artar. Soygazların elektronegatifliği tanımlanmaz çünkü bağ oluşturmazlar.
Metalik karakter elektronegatiflikle ters orantılıdır. Soldaki elementler metal, sağdakiler ametal özellik gösterir. Metal olanlar elektron verme, ametal olanlar elektron alma eğilimindedir.
💡 Kolay Hatırlama: Flor'dan uzaklaştıkça elektronegatiflik azalır!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Metalik Bağ ve Metal Özellikleri
Metalik bağ metal atomlarının değerlik elektronlarının tüm metal kafes boyunca serbestçe hareket etmesiyle oluşur. Bu "elektron denizi" metal katyonlarını bir arada tutar.
Metalik bağın gücü değerlik elektron sayısı arttıkça güçlenir, atom yarıçapı azaldıkça güçlenir. Bu nedenle küçük atomlu, çok değerlik elektronlu metaller daha sert ve yüksek erime noktasına sahiptir.
Metallerin parlaklık, elektrik iletkenliği, tel-levha haline gelebilme gibi özellikleri metalik bağdan kaynaklanır.
💡 Önemli: Metalik bağ gücü = değerlik elektron sayısı / atom yarıçapı oranıyla artar!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Periyodik Özellikler Özeti ve Test Soruları
Periyodik özellikler için genel kurallar: Atom yarıçapı sol alt köşede maksimum, iyonlaşma enerjisi ve elektronegatiflik sağ üst köşede maksimum.
1A alkali metaller en aktif metallerdir. Aynı periyotta 2A grubunun iyonlaşma enerjisi 3A'dan yüksektir (tam dolu s orbitali kararlılığı).
Test sorularında bu özelliklerin periyottaki ve gruptaki değişimini karşılaştırman istenebilir. Her zaman önce atomların periyodik sistemdeki yerini belirle, sonra kuralları uygula.
💡 Sınav İpucu: Periyodik özellik sorularında önce elementleri yerleştir, sonra trendi uygula!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Ionic Bond
9Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimya
İyonik bağlı bileşiklerin oluşumu ve adlandırılması kovalent bağlı bileşiklerin adlandırılması
9. Sınıf kimya
Etkiletişimler konu anlatımı içerisinde sorularda mevcuttur.
Türler arası etkileşimler 1
Türler arası etkileşimler 1
kimyasal türler arası etkileşimler; güçlü etkileşimler
güçlü etkileşimler detaylı konu anlatım notları
Kimyasal türler arasi etkileşimler
Bu ders notu kimyasal türler arasi etkileşimler konu anlatımı içerir
Tyt Kimya Kimyasal türler arası etkileşimler
Tyt Kimya özet ders notu
İyonik Bağ
9.Sinif Kimya
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Lewis Nokta Yapısı
Lewis Nokta yapısı
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
En popüler içerikler
98.sınıf matematik
Tüm üniteleri içermektedir!
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
11. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
9.sınıf tarih ders notları
Yeni maarif modele uygundur
İnkılap tarihi
Beğenin
TYT AYT TARİH
Tarih
9. Sınıf edebiyat ders notları.
9. Sınıflar için Türk Dili edebiyatı notları.
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅