Modern Atom Teorisi ve Periyodik Cetvel, kimyanın temel yapı taşlarını... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
295
•
Güncellendi May 20, 2026
•
Dilara
@dilara_akb7p
Modern Atom Teorisi ve Periyodik Cetvel, kimyanın temel yapı taşlarını... Daha fazla göster
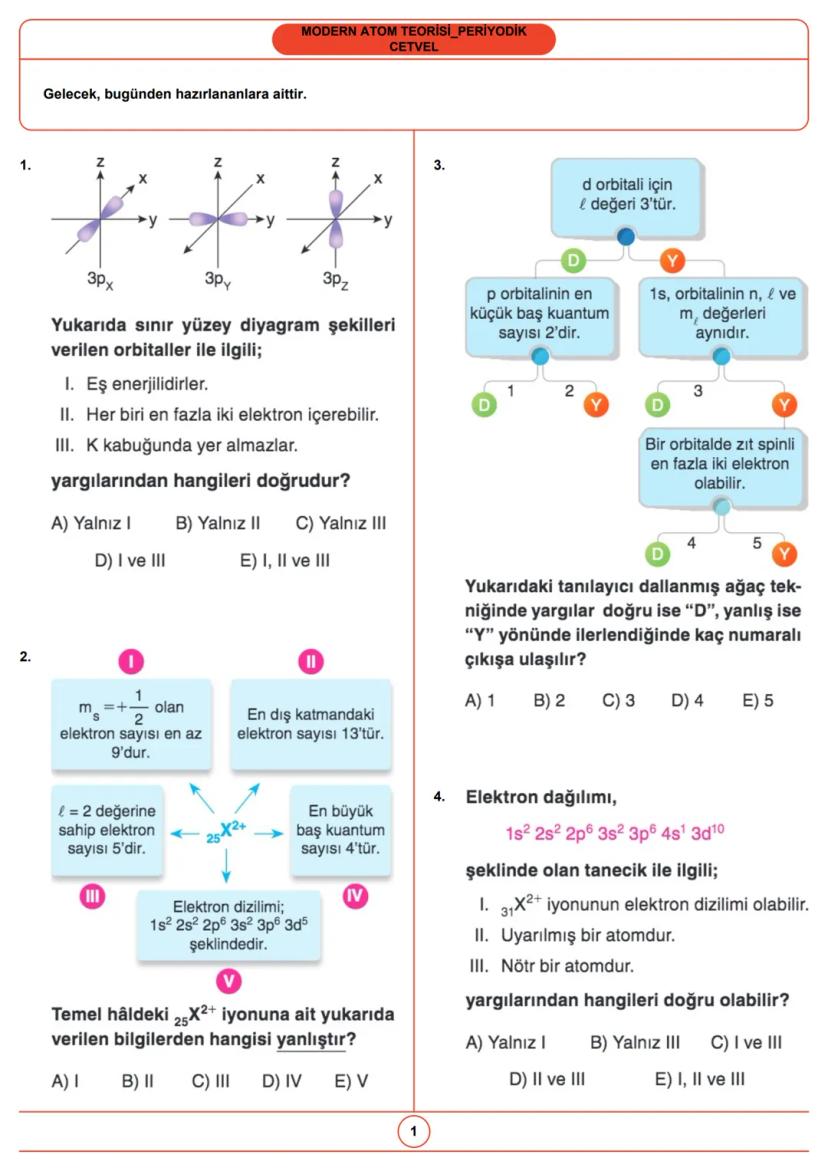


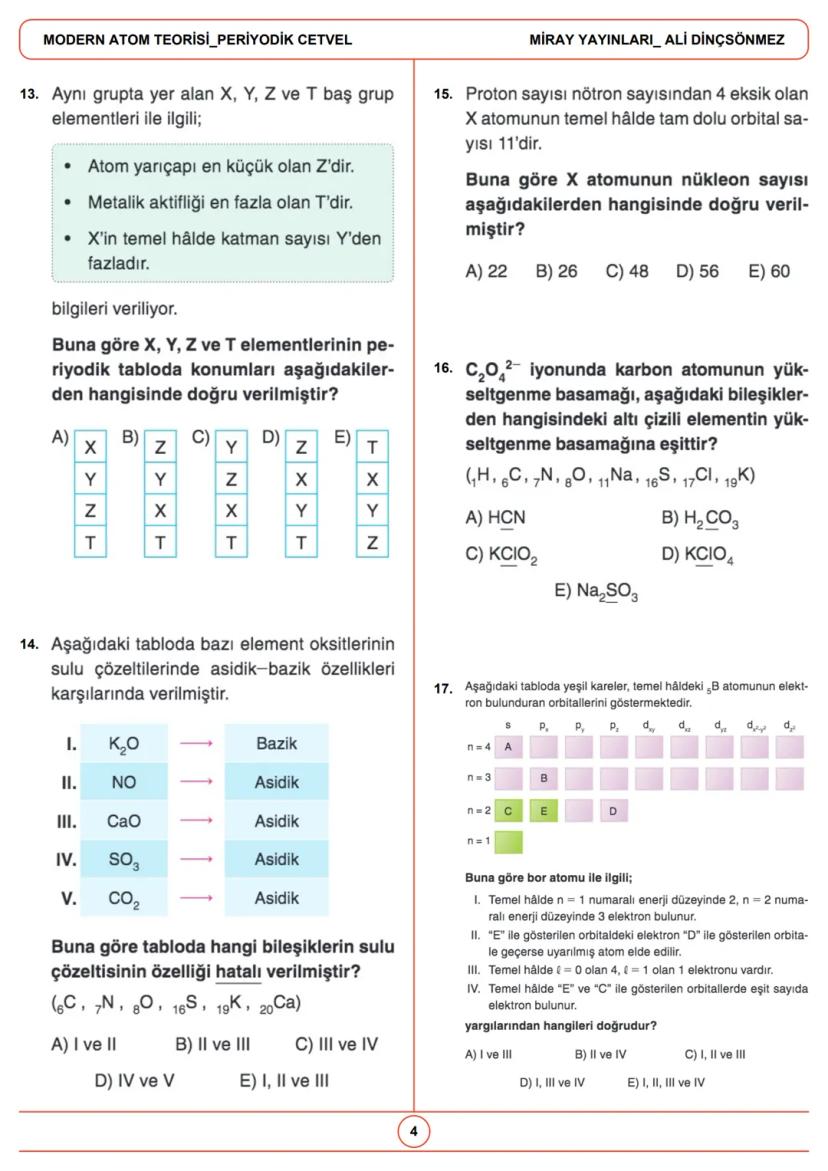






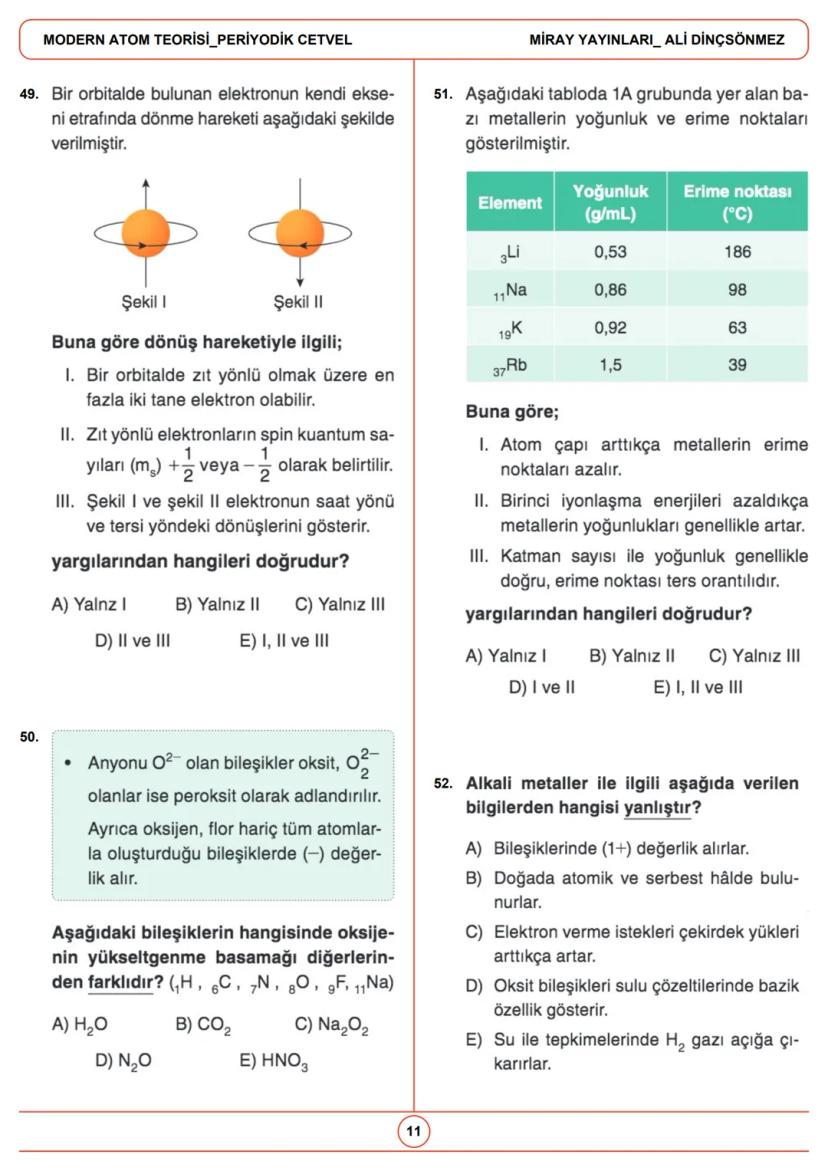
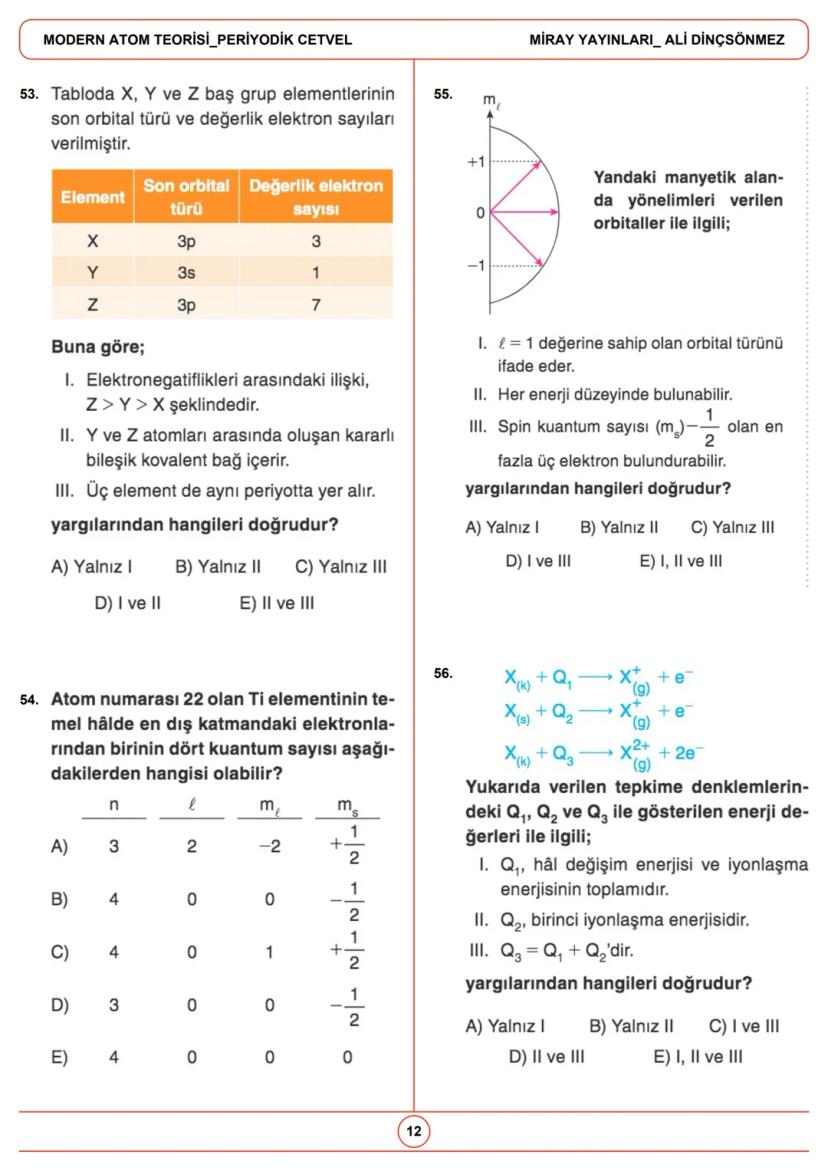
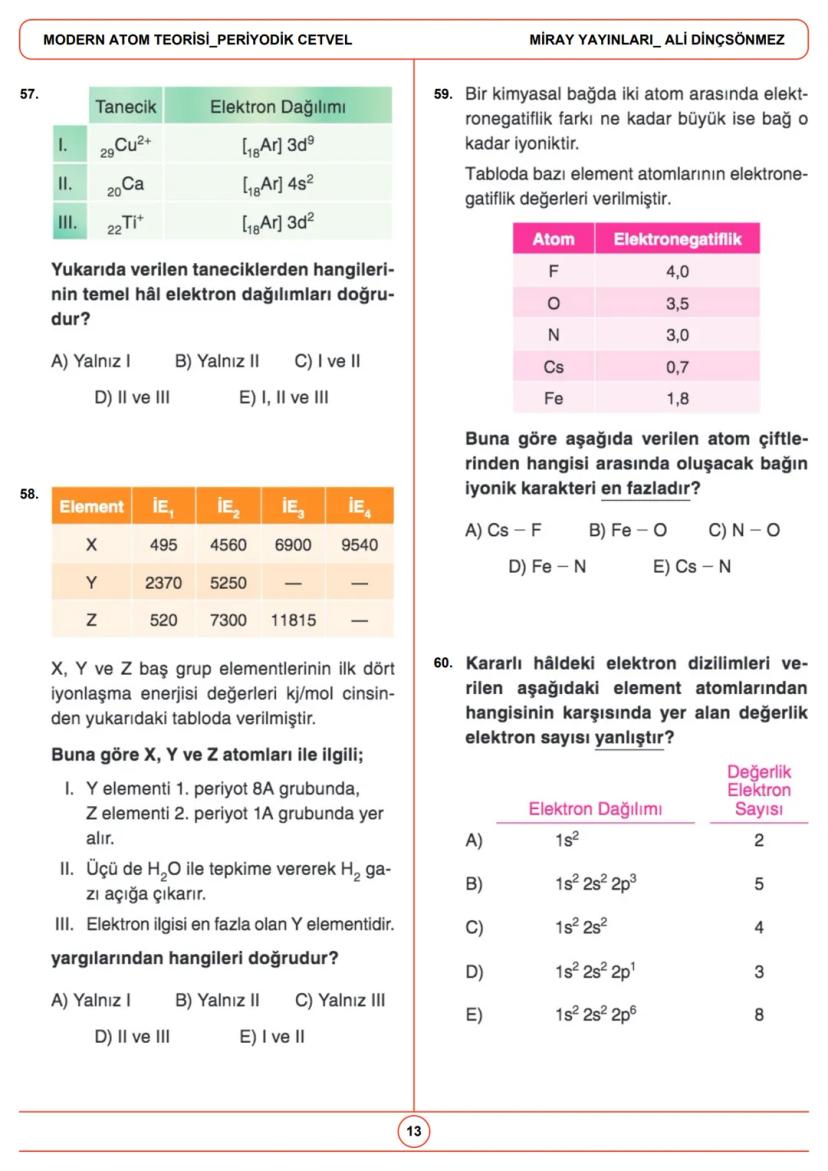

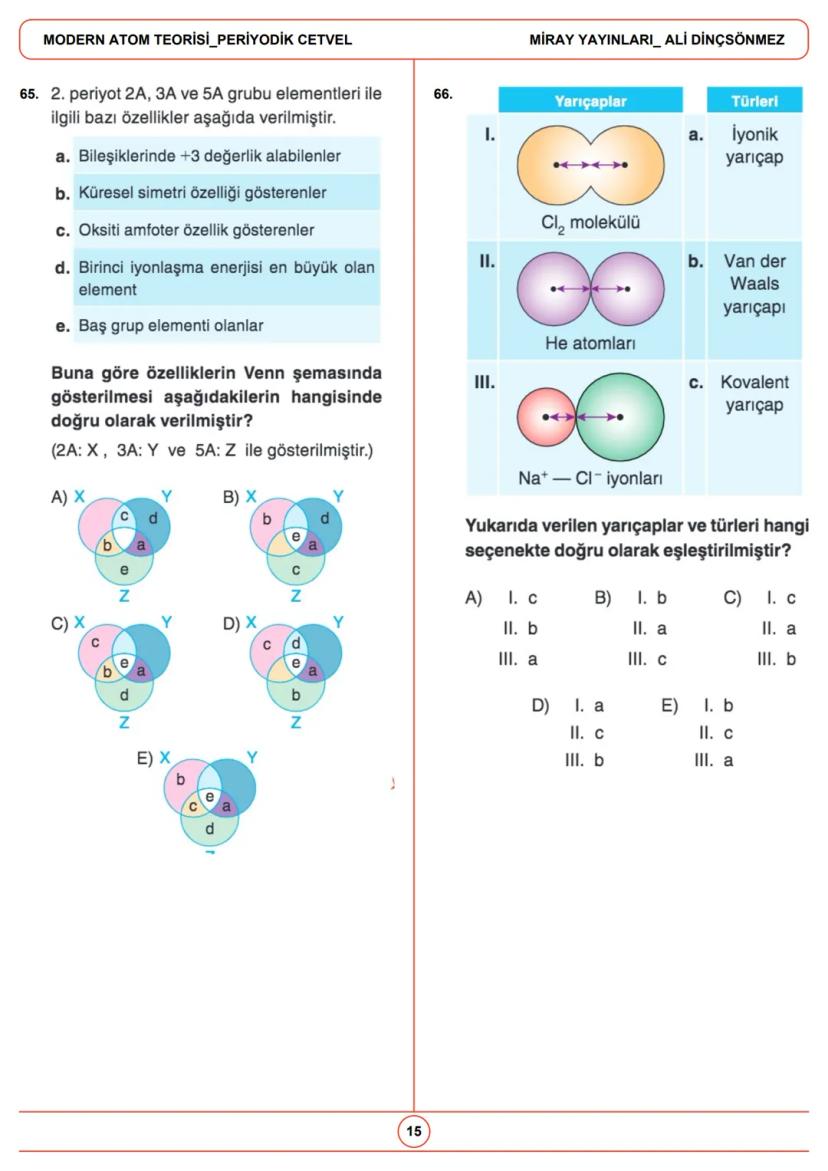
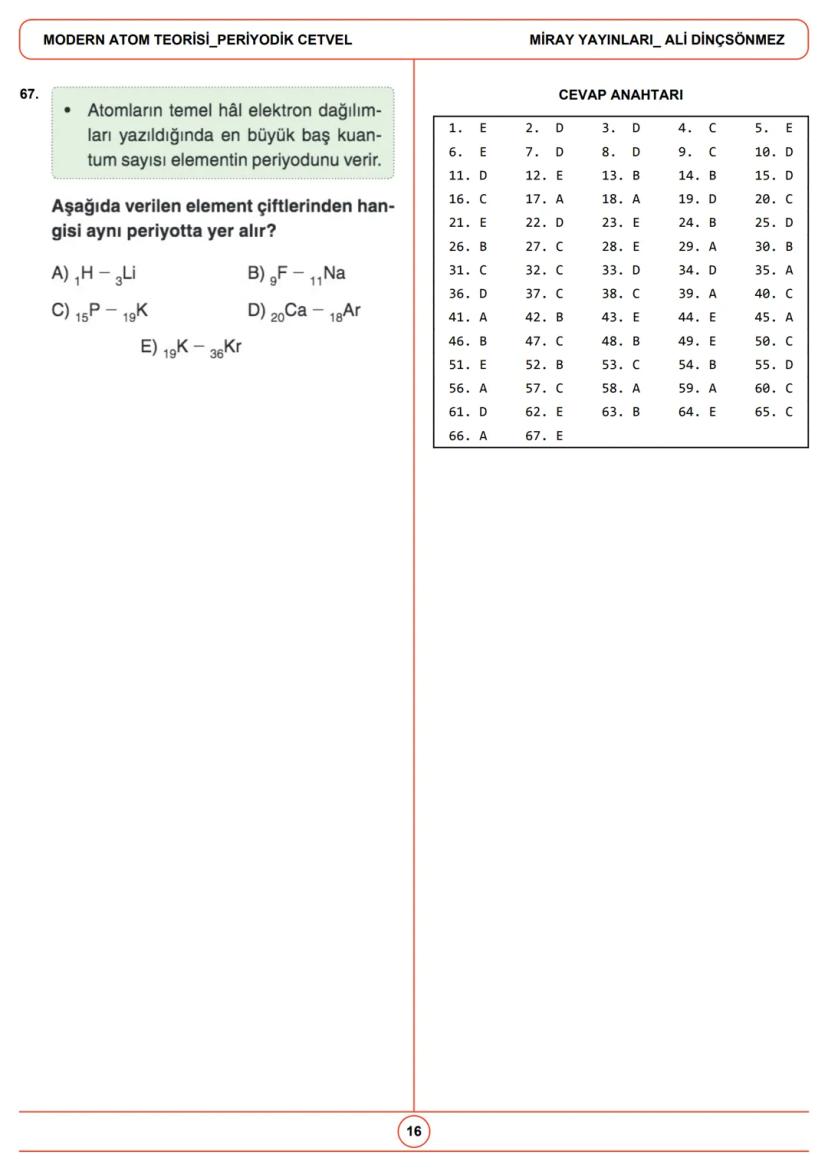
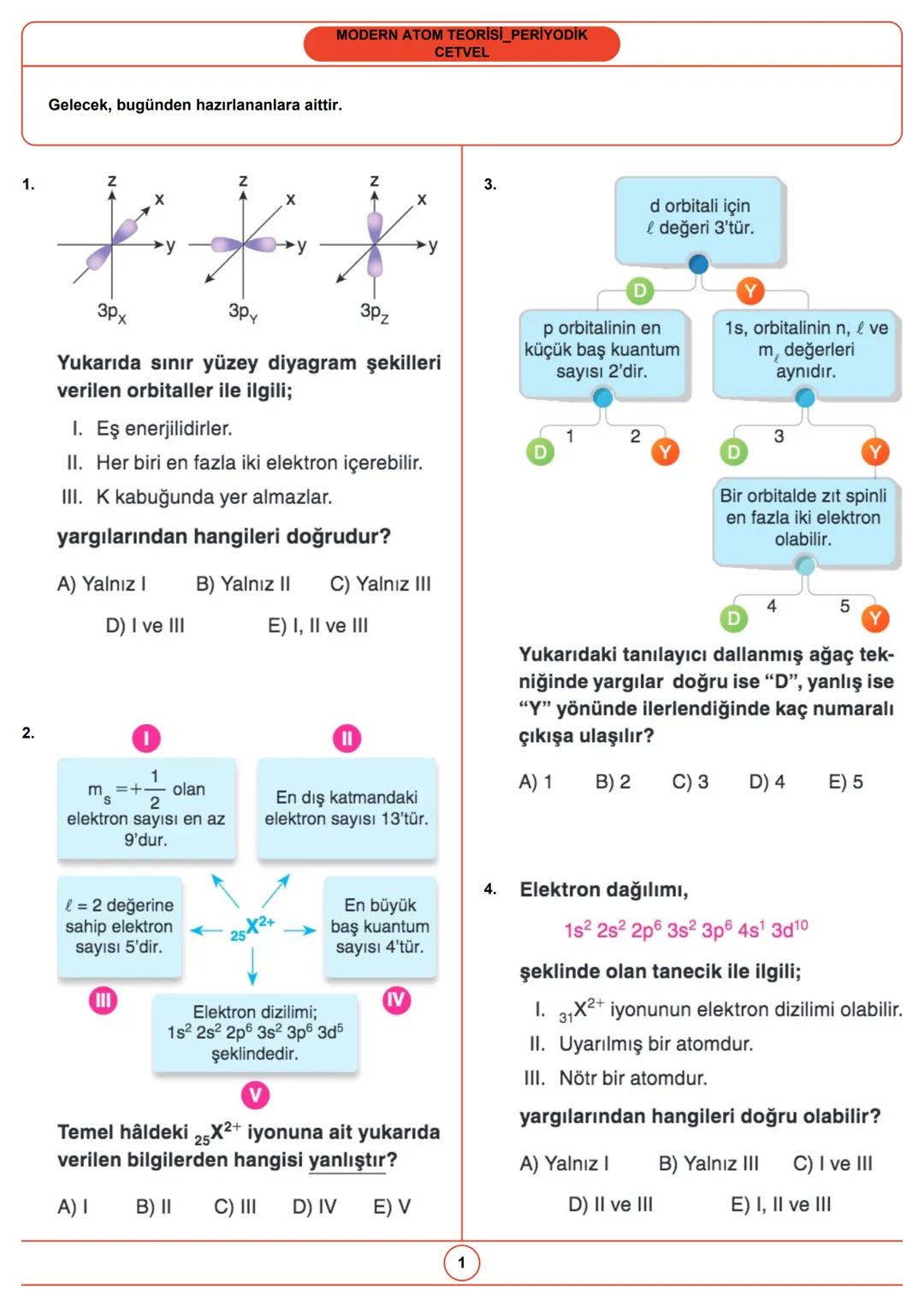
Atomda elektronlar, orbitaller adı verilen belirli enerji seviyelerinde bulunur. Orbitaller, elektronların bulunma olasılığının yüksek olduğu bölgelerdir ve farklı şekillere sahiptir.
p orbitalleri (p<sub>x</sub>, p<sub>y</sub>, p<sub>z</sub>) eş enerjilidir ve her orbital en fazla iki elektron içerebilir. Bu elektronların spinleri (dönüş yönleri) birbirine zıttır. p orbitalleri K kabuğunda bulunmaz, en küçük baş kuantum sayısı 2'dir.
Elektronların yerleştiği orbitallerin enerji seviyesi, baş kuantum sayısı (n), açısal momentum kuantum sayısı (l) ve manyetik kuantum sayısı (m<sub>l</sub>) ile belirlenir. Örneğin, d orbitalinin l değeri 2, p orbitalinin en küçük baş kuantum sayısı 2'dir.
💡 Önemli Not: Bir atom uyarıldığında, elektron daha yüksek enerjili bir orbitale geçer. Elektron temel hâle dönerken dışarıya enerji (ışık) yayar.
Temel hâlden farklı olarak elektron dağılımı değiştirilmiş atomlara uyarılmış atom denir. Uyarılmış bir atomda elektronlar, Aufbau ilkesine göre doldurulmamış orbitallerde bulunabilir.

Modern atom modeline göre elektronlar, çekirdek etrafında belirli yörüngelerde değil orbitallerde bulunur. Bu model, elektronların bulunma olasılığını tanımlayan kuantum mekaniğine dayanır.
Periyodik tabloda elementler, atom numaralarının artışına göre sıralanır. Elementlerin kimyasal ve fiziksel özellikleri, periyodik olarak tekrarlanır. Periyodik tabloda:
Aynı periyotta, atom numarası arttıkça atom yarıçapı azalır. Bunun nedeni, artan çekirdek yükünün elektronları daha kuvvetli çekmesidir. Örneğin, 3. periyottaki Na, Mg, Al, Si, P, S ve Cl elementlerinde atom yarıçapı Na'dan Cl'ye doğru azalır.
💡 Dikkat: Elektronlar, atomda Aufbau (artan enerji) ilkesi, Hund kuralı ve Pauli dışlama ilkesine göre yerleşir.
Bir atomun uyarılmış hâli, temel hâle göre daha yüksek enerjilidir ve daha kararsızdır. Uyarılmış hâldeki atom, enerjisini kaybederek temel hâle dönme eğilimindedir.

İyonlaşma enerjisi, bir atomdan elektron koparmak için gereken enerjidir. Periyodik tabloda, soldan sağa gidildikçe genellikle iyonlaşma enerjisi artar, yukarıdan aşağıya inildikçe azalır.
İyonlaşma enerjisi grafiğinde ani artışlar, katmanların dolmasını gösterir. Örneğin, 3. periyotta yer alan bir X elementinin iyonlaşma enerjisindeki ani artış, değerlik elektronlarının tamamının koptuğunu gösterir.
Elektron dağılımı ve kuantum sayıları, atomların özelliklerini belirler:
💡 Bohr Modeli vs Modern Atom Teorisi: Bohr atom modelinde elektronlar belirli yörüngelerde hareket ederken, modern atom teorisinde elektronların bulunma olasılığının en yüksek olduğu bölgeler (orbitaller) tanımlanır.
Element oksitlerinin özellikleri, elementin metalik veya ametalik karakterine bağlıdır. Metal oksitleri sulu çözeltide bazik, ametal oksitleri ise asidik özellik gösterir.
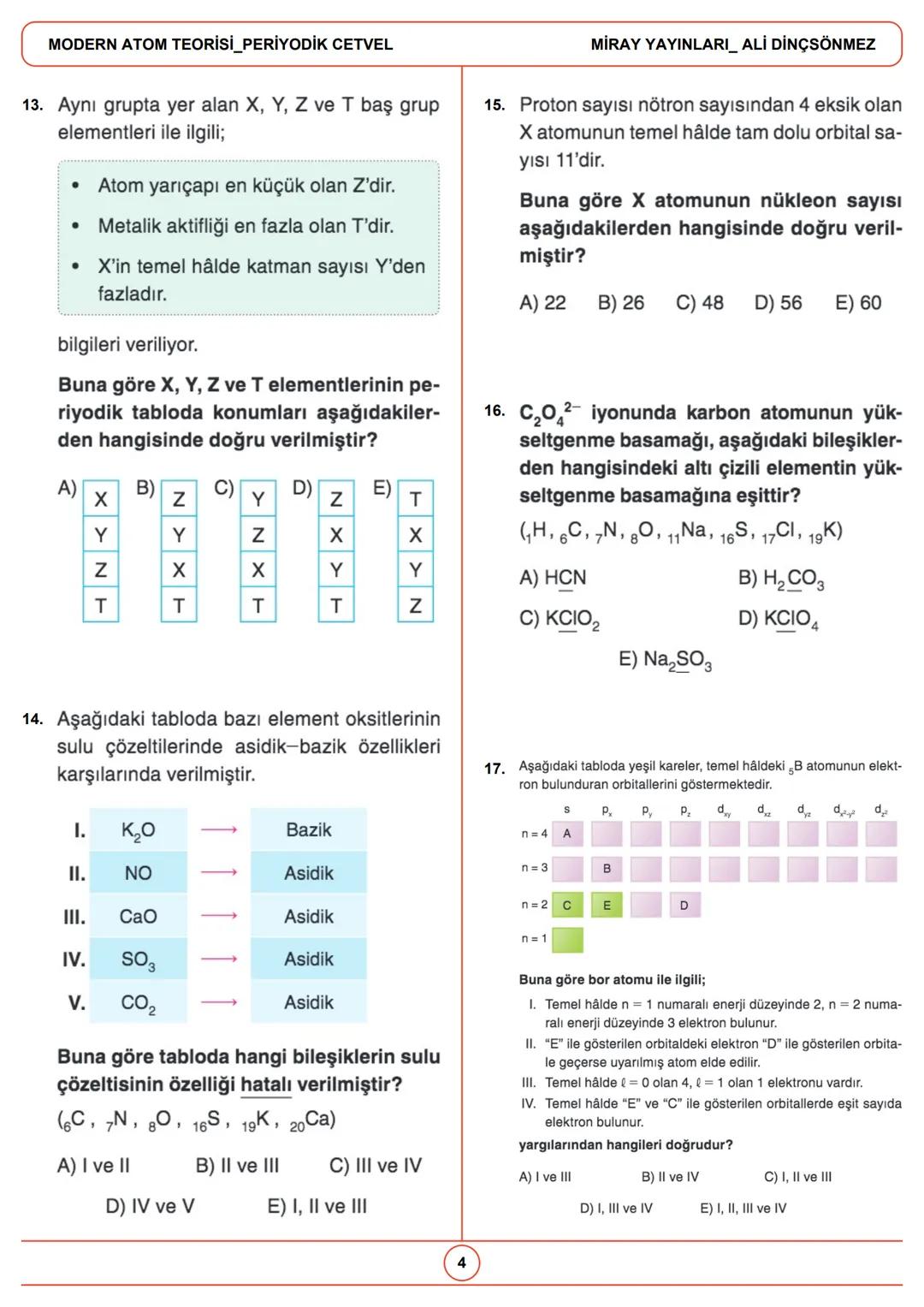
Periyodik tabloda elementlerin konumları, elektron dizilimlerine bağlıdır. Aynı grupta bulunan elementler benzer kimyasal özellikler gösterir çünkü değerlik elektron sayıları aynıdır.
Periyodik özelliklerin değişimi:
Bir elementin nükleon sayısı, proton ve nötron sayılarının toplamıdır. Atomun temel hâlindeki tam dolu orbital sayısı, elektron diziliminden bulunabilir.
💡 Yükseltgenme Basamakları: Elementlerin bileşiklerindeki yükseltgenme basamakları, değerlik elektron sayılarına ve bağ yaptıkları elementlerin özelliklerine bağlıdır.
Elektronların orbitallere yerleşimini gösteren diyagramlarda, bir kare bir orbitali temsil eder. Uyarılmış hâldeki atomda, elektronlar temel hâldekinden farklı orbitallere yerleşir ve bu durum atomun enerji seviyesini yükseltir.

Kuantum sayıları, elektronların atom içindeki durumlarını belirler ve her elektron için dört kuantum sayısı vardır:
Temel hâldeki bir atomun elektron dizilimi, Aufbau ilkesi (artan enerji sırası), Pauli ilkesi (bir orbitalde zıt spinli en fazla iki elektron) ve Hund kuralı (aynı enerji düzeyindeki orbitallere önce tek tek elektron yerleşir) uygulanarak belirlenir.
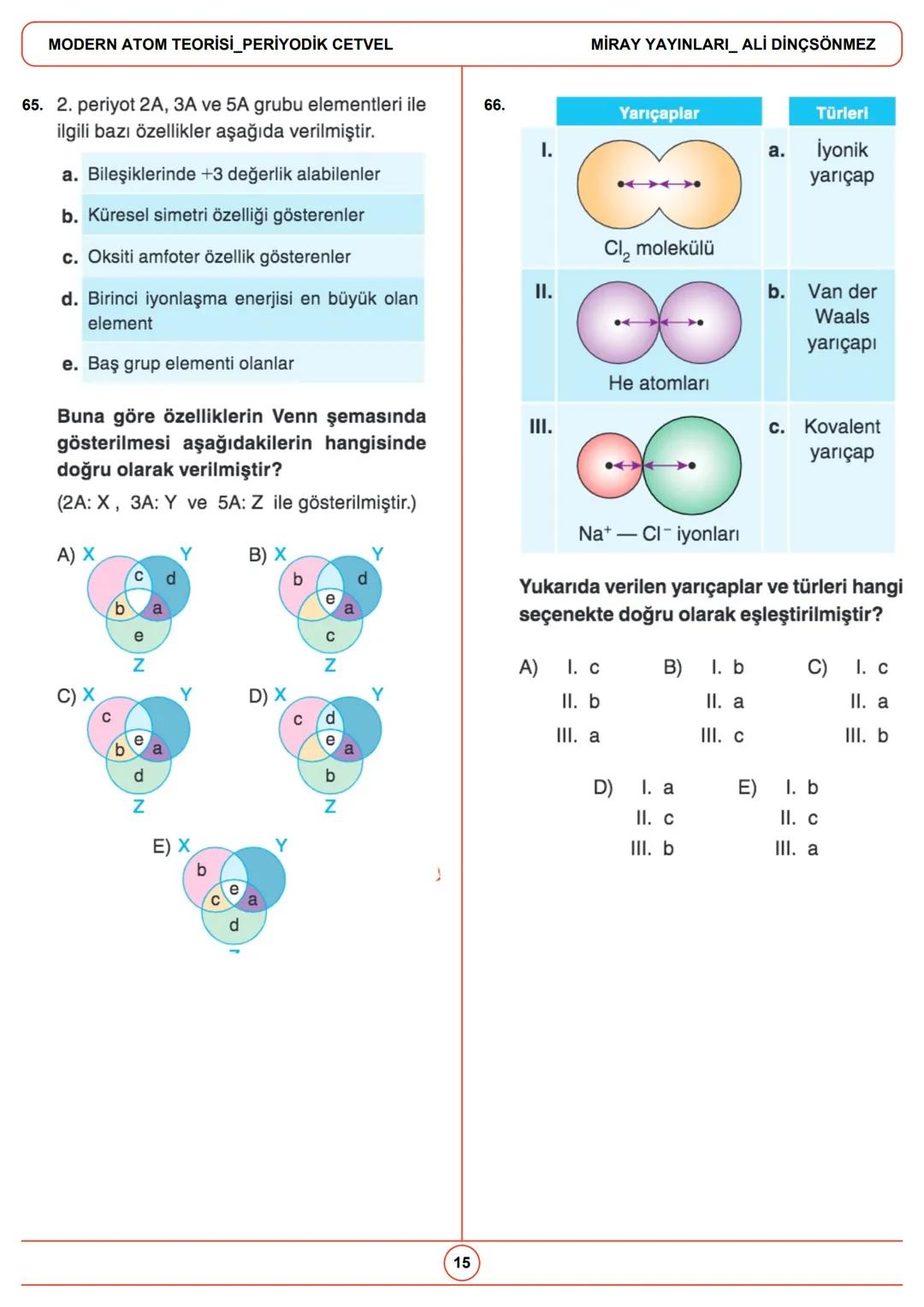
💡 Küresel Simetri: Değerlik orbital ve alt kabuklarının tam dolu veya tamamen boş olması durumunda atom, küresel simetri özelliği gösterir.
Elementler, değerlik elektronlarının sayısına göre periyodik tabloda gruplara ayrılır. Örneğin, periyodik tabloda 4. periyot 3A grubundaki element, değerlik elektron dizilimi 4s<sup>2</sup>4p<sup>1</sup> olan alüminyum benzeri bir elementtir.

Periyodik tabloda elementler, elektron dizilimlerine göre sınıflandırılır. IUPAC sistemine göre periyodik tabloda 18 grup bulunur:
Elementlerin temel hâl elektron diziliminde bazı istisnalar vardır:
Bir atomun periyodik tablodaki yerini belirlemede:
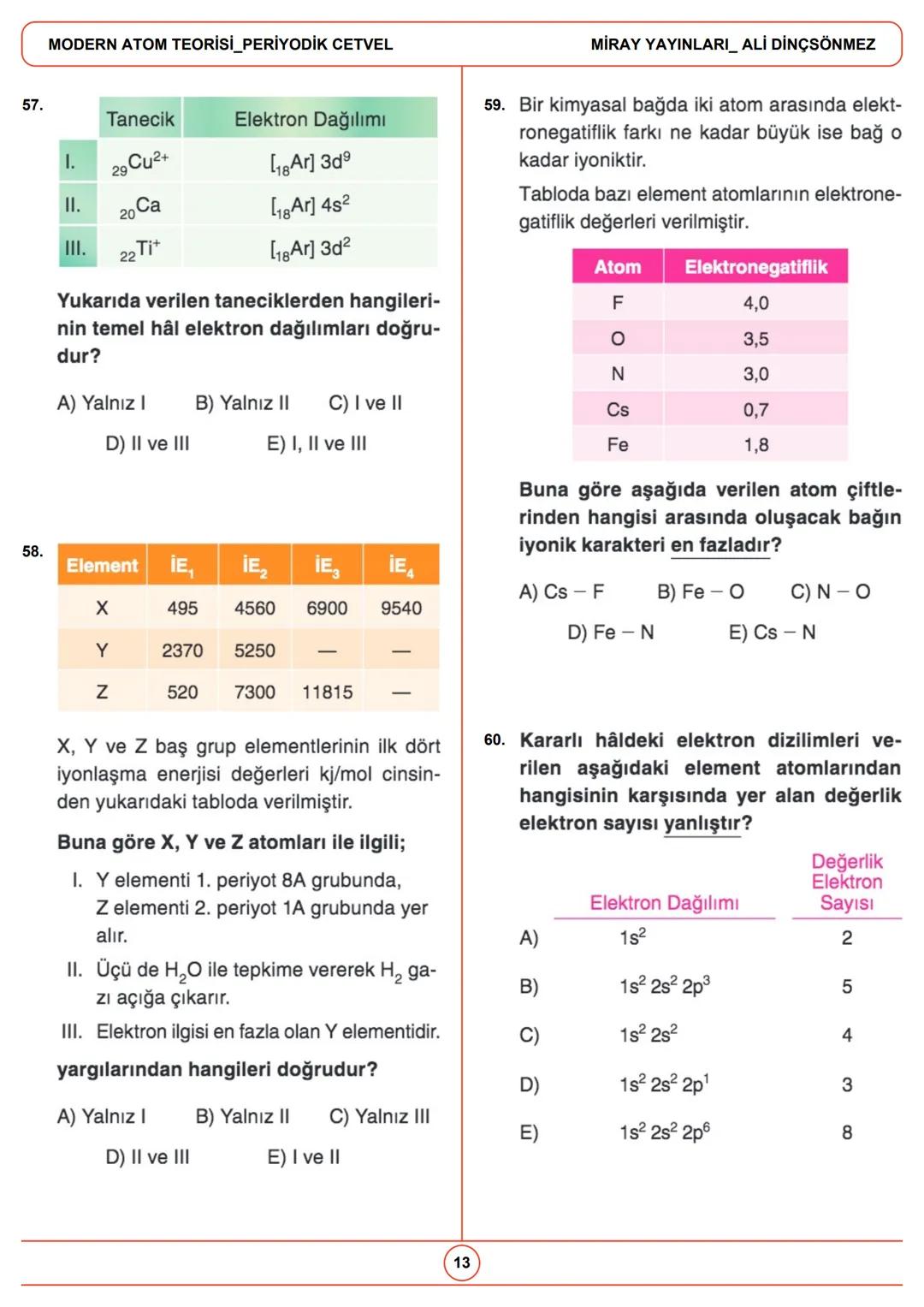
💡 Elektronegatiflik ve Bağ Karakteri: İki atom arasındaki elektronegatiflik farkı arttıkça bağın iyonik karakteri artar. Örneğin, F (4,0) ve Cs (0,7) arasındaki bağ güçlü iyonik karaktere sahiptir.
Periyodik tabloda aynı grupta yer alan elementlerin atom yarıçapları, yukarıdan aşağıya doğru artar. Örneğin, 1A grubunda Li < Na < K < Rb şeklindedir.

Bir atomun temel hâl elektron dizilimini yazarken, elektronlar artan enerji düzeyinde orbitallere yerleştirilir. Bu düzen genellikle:
1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f...
şeklindedir.
Örneğin, temel hâldeki nötr Cu atomu için elektron dizilimi: 1s<sup>2</sup> 2s<sup>2</sup> 2p<sup>6</sup> 3s<sup>2</sup> 3p<sup>6</sup> 4s<sup>1</sup> 3d<sup>10</sup> şeklindedir.
İyon hâlindeki taneciklerin elektron dizilimi yazılırken:
💡 Peroksitler ve Oksitler: Oksijen, genellikle bileşiklerinde -2 değerlikli olurken, peroksitlerde (O<sub>2</sub><sup>2-</sup>) -1 değerlik alır. Örneğin Na<sub>2</sub>O<sub>2</sub>'de oksijenin yükseltgenme basamağı -1'dir.
Elementlerin iyonlaşma enerjileri karşılaştırıldığında, genellikle aynı periyotta soldan sağa doğru artar, aynı grupta yukarıdan aşağıya doğru azalır. İyonlaşma enerjilerindeki ani artışlar, katmanların dolduğunu gösterir.

Elementlerin periyodik özellikleri, elektron dizilimlerine ve özellikle de değerlik elektronlarına bağlıdır. Periyodik tabloda:
Orbitaller, belirli enerji seviyelerinde ve belirli şekillerde bulunur:
💡 Madelung-Kletchkowski Kuralı: Orbitallerin enerji seviyelerini karşılaştırmak için değeri kullanılır. değeri küçük olan orbital daha düşük enerjilidir. Eğer değerleri eşitse, n değeri küçük olan orbital daha düşük enerjilidir.
Elementlerin bileşiklerindeki yükseltgenme basamakları, genellikle değerlik elektron sayılarıyla ilgilidir. Örneğin, CaO<sub>2</sub> bileşiğinde kalsiyum +2, oksijen -1 değerliklidir (peroksit).

Elektronların kendi eksenleri etrafında dönme hareketine spin denir. Bir orbitalde bulunan elektronlar zıt spinli olmak zorundadır. Spin kuantum sayısı (m<sub>s</sub>) +1/2 veya -1/2 değerini alır.
Elektronların spin hareketi, atomların manyetik özelliklerini belirler. Yarı dolu orbitallerdeki elektronlar, atomun paramanyetik özellik göstermesine neden olur.
Alkali metaller (1A grubu), periyodik tablonun en solunda yer alır ve şu özelliklere sahiptir:
💡 Oksit vs. Peroksit: Anyon formülü O<sup>2-</sup> olan bileşikler oksit, O<sub>2</sub><sup>2-</sup> olan bileşikler ise peroksit olarak adlandırılır. Na<sub>2</sub>O<sub>2</sub>'de oksijen -1 değerlik alırken, Na<sub>2</sub>O'da -2 değerlik alır.
Alkali metallerin (Li, Na, K, Rb) fiziksel özellikleri incelendiğinde, atom çapı arttıkça yoğunlukları artar, erime noktaları ise azalır. Bu durum, katman sayısı arttıkça atomlar arası çekim kuvvetlerinin zayıflamasından kaynaklanır.

İyonların elektron dizilimleri yazılırken, katyonlarda en dıştaki elektronlar koparılır, anyonlarda ise dış kabuktaki boş orbitallere elektron eklenir. Örneğin:
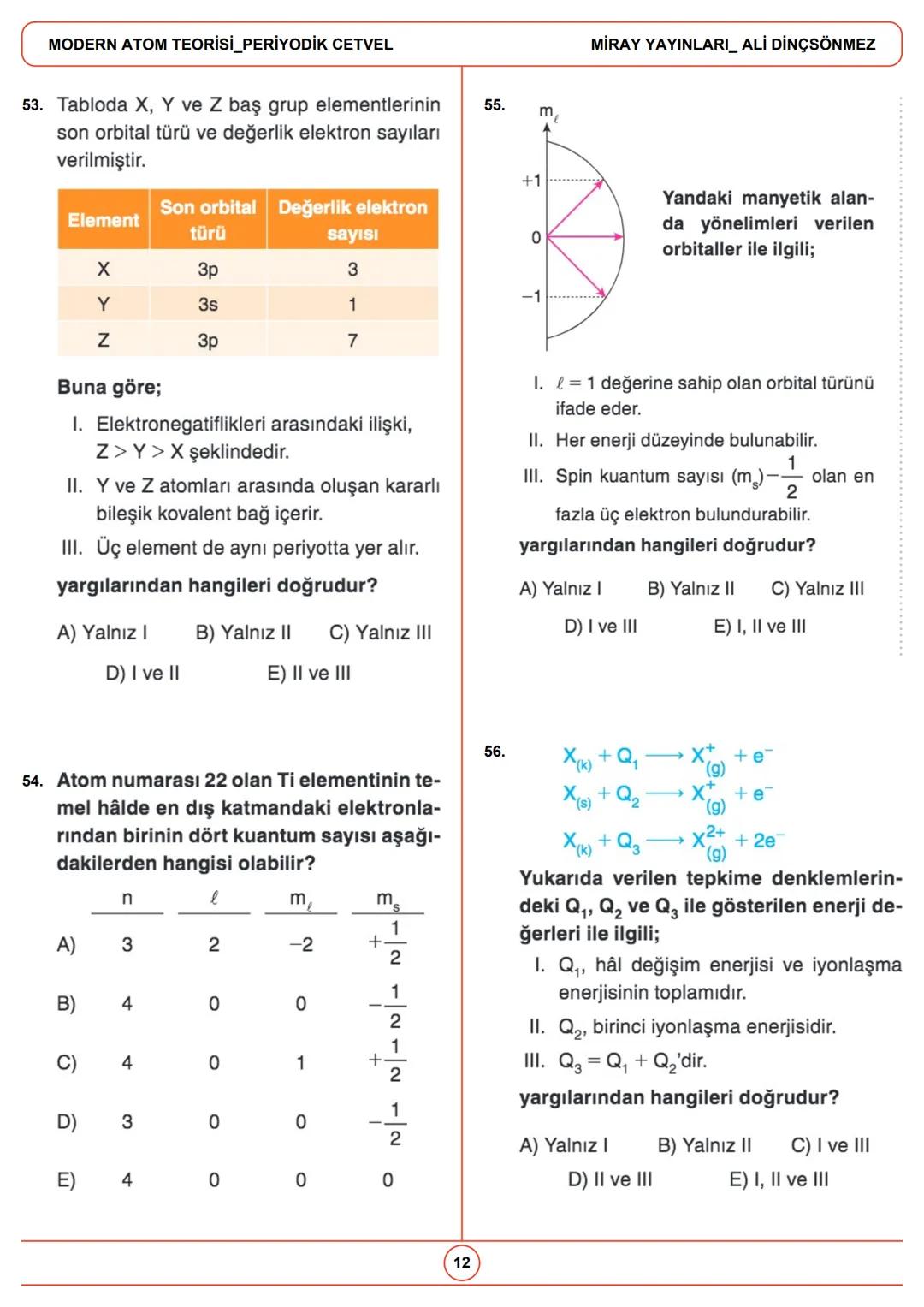
Elementlerin iyonlaşma enerjisi değerleri, atomların elektron verme isteklerini gösterir. Ardışık iyonlaşma enerjilerindeki büyük artışlar, değerlik elektron sayısını ve elementin grubunu belirlemeye yardımcı olur.
Elektronegatiflik, bir atomun bağ elektronlarını kendine çekme yeteneğidir. İki atom arasındaki elektronegatiflik farkı büyüdükçe, bağın iyonik karakteri artar.
Örneğin:
💡 Değerlik Elektron Sayısı: Bir atomun değerlik elektron sayısı, en dış enerji seviyesinde (s ve p orbitallerinde) bulunan elektron sayısıdır. Örneğin, 1s<sup>2</sup> elektron dizilimine sahip He atomu 2 değerlik elektronuna sahiptir.
Elementlerin kararlı bileşiklerinde, atomlar genellikle oktet kuralını sağlamaya çalışır (değerlik kabuğunda 8 elektron bulunması).


Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Dilara
@dilara_akb7p
Modern Atom Teorisi ve Periyodik Cetvel, kimyanın temel yapı taşlarını anlamak için önemli konulardır. Bu konular, atomların yapısını, elektronların düzenlenişini ve elementlerin özelliklerini sınıflandırmayı sağlar. Bu özet, atom teorisi kavramlarını ve periyodik cetveldeki element ilişkilerini daha kolay anlamanıza yardımcı olacaktır.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Atomda elektronlar, orbitaller adı verilen belirli enerji seviyelerinde bulunur. Orbitaller, elektronların bulunma olasılığının yüksek olduğu bölgelerdir ve farklı şekillere sahiptir.
p orbitalleri (p<sub>x</sub>, p<sub>y</sub>, p<sub>z</sub>) eş enerjilidir ve her orbital en fazla iki elektron içerebilir. Bu elektronların spinleri (dönüş yönleri) birbirine zıttır. p orbitalleri K kabuğunda bulunmaz, en küçük baş kuantum sayısı 2'dir.
Elektronların yerleştiği orbitallerin enerji seviyesi, baş kuantum sayısı (n), açısal momentum kuantum sayısı (l) ve manyetik kuantum sayısı (m<sub>l</sub>) ile belirlenir. Örneğin, d orbitalinin l değeri 2, p orbitalinin en küçük baş kuantum sayısı 2'dir.
💡 Önemli Not: Bir atom uyarıldığında, elektron daha yüksek enerjili bir orbitale geçer. Elektron temel hâle dönerken dışarıya enerji (ışık) yayar.
Temel hâlden farklı olarak elektron dağılımı değiştirilmiş atomlara uyarılmış atom denir. Uyarılmış bir atomda elektronlar, Aufbau ilkesine göre doldurulmamış orbitallerde bulunabilir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Modern atom modeline göre elektronlar, çekirdek etrafında belirli yörüngelerde değil orbitallerde bulunur. Bu model, elektronların bulunma olasılığını tanımlayan kuantum mekaniğine dayanır.
Periyodik tabloda elementler, atom numaralarının artışına göre sıralanır. Elementlerin kimyasal ve fiziksel özellikleri, periyodik olarak tekrarlanır. Periyodik tabloda:
Aynı periyotta, atom numarası arttıkça atom yarıçapı azalır. Bunun nedeni, artan çekirdek yükünün elektronları daha kuvvetli çekmesidir. Örneğin, 3. periyottaki Na, Mg, Al, Si, P, S ve Cl elementlerinde atom yarıçapı Na'dan Cl'ye doğru azalır.
💡 Dikkat: Elektronlar, atomda Aufbau (artan enerji) ilkesi, Hund kuralı ve Pauli dışlama ilkesine göre yerleşir.
Bir atomun uyarılmış hâli, temel hâle göre daha yüksek enerjilidir ve daha kararsızdır. Uyarılmış hâldeki atom, enerjisini kaybederek temel hâle dönme eğilimindedir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
İyonlaşma enerjisi, bir atomdan elektron koparmak için gereken enerjidir. Periyodik tabloda, soldan sağa gidildikçe genellikle iyonlaşma enerjisi artar, yukarıdan aşağıya inildikçe azalır.
İyonlaşma enerjisi grafiğinde ani artışlar, katmanların dolmasını gösterir. Örneğin, 3. periyotta yer alan bir X elementinin iyonlaşma enerjisindeki ani artış, değerlik elektronlarının tamamının koptuğunu gösterir.
Elektron dağılımı ve kuantum sayıları, atomların özelliklerini belirler:
💡 Bohr Modeli vs Modern Atom Teorisi: Bohr atom modelinde elektronlar belirli yörüngelerde hareket ederken, modern atom teorisinde elektronların bulunma olasılığının en yüksek olduğu bölgeler (orbitaller) tanımlanır.
Element oksitlerinin özellikleri, elementin metalik veya ametalik karakterine bağlıdır. Metal oksitleri sulu çözeltide bazik, ametal oksitleri ise asidik özellik gösterir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Periyodik tabloda elementlerin konumları, elektron dizilimlerine bağlıdır. Aynı grupta bulunan elementler benzer kimyasal özellikler gösterir çünkü değerlik elektron sayıları aynıdır.
Periyodik özelliklerin değişimi:
Bir elementin nükleon sayısı, proton ve nötron sayılarının toplamıdır. Atomun temel hâlindeki tam dolu orbital sayısı, elektron diziliminden bulunabilir.
💡 Yükseltgenme Basamakları: Elementlerin bileşiklerindeki yükseltgenme basamakları, değerlik elektron sayılarına ve bağ yaptıkları elementlerin özelliklerine bağlıdır.
Elektronların orbitallere yerleşimini gösteren diyagramlarda, bir kare bir orbitali temsil eder. Uyarılmış hâldeki atomda, elektronlar temel hâldekinden farklı orbitallere yerleşir ve bu durum atomun enerji seviyesini yükseltir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kuantum sayıları, elektronların atom içindeki durumlarını belirler ve her elektron için dört kuantum sayısı vardır:
Temel hâldeki bir atomun elektron dizilimi, Aufbau ilkesi (artan enerji sırası), Pauli ilkesi (bir orbitalde zıt spinli en fazla iki elektron) ve Hund kuralı (aynı enerji düzeyindeki orbitallere önce tek tek elektron yerleşir) uygulanarak belirlenir.
💡 Küresel Simetri: Değerlik orbital ve alt kabuklarının tam dolu veya tamamen boş olması durumunda atom, küresel simetri özelliği gösterir.
Elementler, değerlik elektronlarının sayısına göre periyodik tabloda gruplara ayrılır. Örneğin, periyodik tabloda 4. periyot 3A grubundaki element, değerlik elektron dizilimi 4s<sup>2</sup>4p<sup>1</sup> olan alüminyum benzeri bir elementtir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Periyodik tabloda elementler, elektron dizilimlerine göre sınıflandırılır. IUPAC sistemine göre periyodik tabloda 18 grup bulunur:
Elementlerin temel hâl elektron diziliminde bazı istisnalar vardır:
Bir atomun periyodik tablodaki yerini belirlemede:
💡 Elektronegatiflik ve Bağ Karakteri: İki atom arasındaki elektronegatiflik farkı arttıkça bağın iyonik karakteri artar. Örneğin, F (4,0) ve Cs (0,7) arasındaki bağ güçlü iyonik karaktere sahiptir.
Periyodik tabloda aynı grupta yer alan elementlerin atom yarıçapları, yukarıdan aşağıya doğru artar. Örneğin, 1A grubunda Li < Na < K < Rb şeklindedir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bir atomun temel hâl elektron dizilimini yazarken, elektronlar artan enerji düzeyinde orbitallere yerleştirilir. Bu düzen genellikle:
1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f...
şeklindedir.
Örneğin, temel hâldeki nötr Cu atomu için elektron dizilimi: 1s<sup>2</sup> 2s<sup>2</sup> 2p<sup>6</sup> 3s<sup>2</sup> 3p<sup>6</sup> 4s<sup>1</sup> 3d<sup>10</sup> şeklindedir.
İyon hâlindeki taneciklerin elektron dizilimi yazılırken:
💡 Peroksitler ve Oksitler: Oksijen, genellikle bileşiklerinde -2 değerlikli olurken, peroksitlerde (O<sub>2</sub><sup>2-</sup>) -1 değerlik alır. Örneğin Na<sub>2</sub>O<sub>2</sub>'de oksijenin yükseltgenme basamağı -1'dir.
Elementlerin iyonlaşma enerjileri karşılaştırıldığında, genellikle aynı periyotta soldan sağa doğru artar, aynı grupta yukarıdan aşağıya doğru azalır. İyonlaşma enerjilerindeki ani artışlar, katmanların dolduğunu gösterir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Elementlerin periyodik özellikleri, elektron dizilimlerine ve özellikle de değerlik elektronlarına bağlıdır. Periyodik tabloda:
Orbitaller, belirli enerji seviyelerinde ve belirli şekillerde bulunur:
💡 Madelung-Kletchkowski Kuralı: Orbitallerin enerji seviyelerini karşılaştırmak için değeri kullanılır. değeri küçük olan orbital daha düşük enerjilidir. Eğer değerleri eşitse, n değeri küçük olan orbital daha düşük enerjilidir.
Elementlerin bileşiklerindeki yükseltgenme basamakları, genellikle değerlik elektron sayılarıyla ilgilidir. Örneğin, CaO<sub>2</sub> bileşiğinde kalsiyum +2, oksijen -1 değerliklidir (peroksit).

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Elektronların kendi eksenleri etrafında dönme hareketine spin denir. Bir orbitalde bulunan elektronlar zıt spinli olmak zorundadır. Spin kuantum sayısı (m<sub>s</sub>) +1/2 veya -1/2 değerini alır.
Elektronların spin hareketi, atomların manyetik özelliklerini belirler. Yarı dolu orbitallerdeki elektronlar, atomun paramanyetik özellik göstermesine neden olur.
Alkali metaller (1A grubu), periyodik tablonun en solunda yer alır ve şu özelliklere sahiptir:
💡 Oksit vs. Peroksit: Anyon formülü O<sup>2-</sup> olan bileşikler oksit, O<sub>2</sub><sup>2-</sup> olan bileşikler ise peroksit olarak adlandırılır. Na<sub>2</sub>O<sub>2</sub>'de oksijen -1 değerlik alırken, Na<sub>2</sub>O'da -2 değerlik alır.
Alkali metallerin (Li, Na, K, Rb) fiziksel özellikleri incelendiğinde, atom çapı arttıkça yoğunlukları artar, erime noktaları ise azalır. Bu durum, katman sayısı arttıkça atomlar arası çekim kuvvetlerinin zayıflamasından kaynaklanır.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
İyonların elektron dizilimleri yazılırken, katyonlarda en dıştaki elektronlar koparılır, anyonlarda ise dış kabuktaki boş orbitallere elektron eklenir. Örneğin:
Elementlerin iyonlaşma enerjisi değerleri, atomların elektron verme isteklerini gösterir. Ardışık iyonlaşma enerjilerindeki büyük artışlar, değerlik elektron sayısını ve elementin grubunu belirlemeye yardımcı olur.
Elektronegatiflik, bir atomun bağ elektronlarını kendine çekme yeteneğidir. İki atom arasındaki elektronegatiflik farkı büyüdükçe, bağın iyonik karakteri artar.
Örneğin:
💡 Değerlik Elektron Sayısı: Bir atomun değerlik elektron sayısı, en dış enerji seviyesinde (s ve p orbitallerinde) bulunan elektron sayısıdır. Örneğin, 1s<sup>2</sup> elektron dizilimine sahip He atomu 2 değerlik elektronuna sahiptir.
Elementlerin kararlı bileşiklerinde, atomlar genellikle oktet kuralını sağlamaya çalışır (değerlik kabuğunda 8 elektron bulunması).

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
5
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı