Periyodik sistem, elementlerin özelliklerine göre düzenlendiği temel bir kimya konusudur.... Daha fazla göster
AYT Kimya 1. Ünite | Net ve Anlaşılır Anlatım








Elektron Dizilimi ve Periyodik Sistem
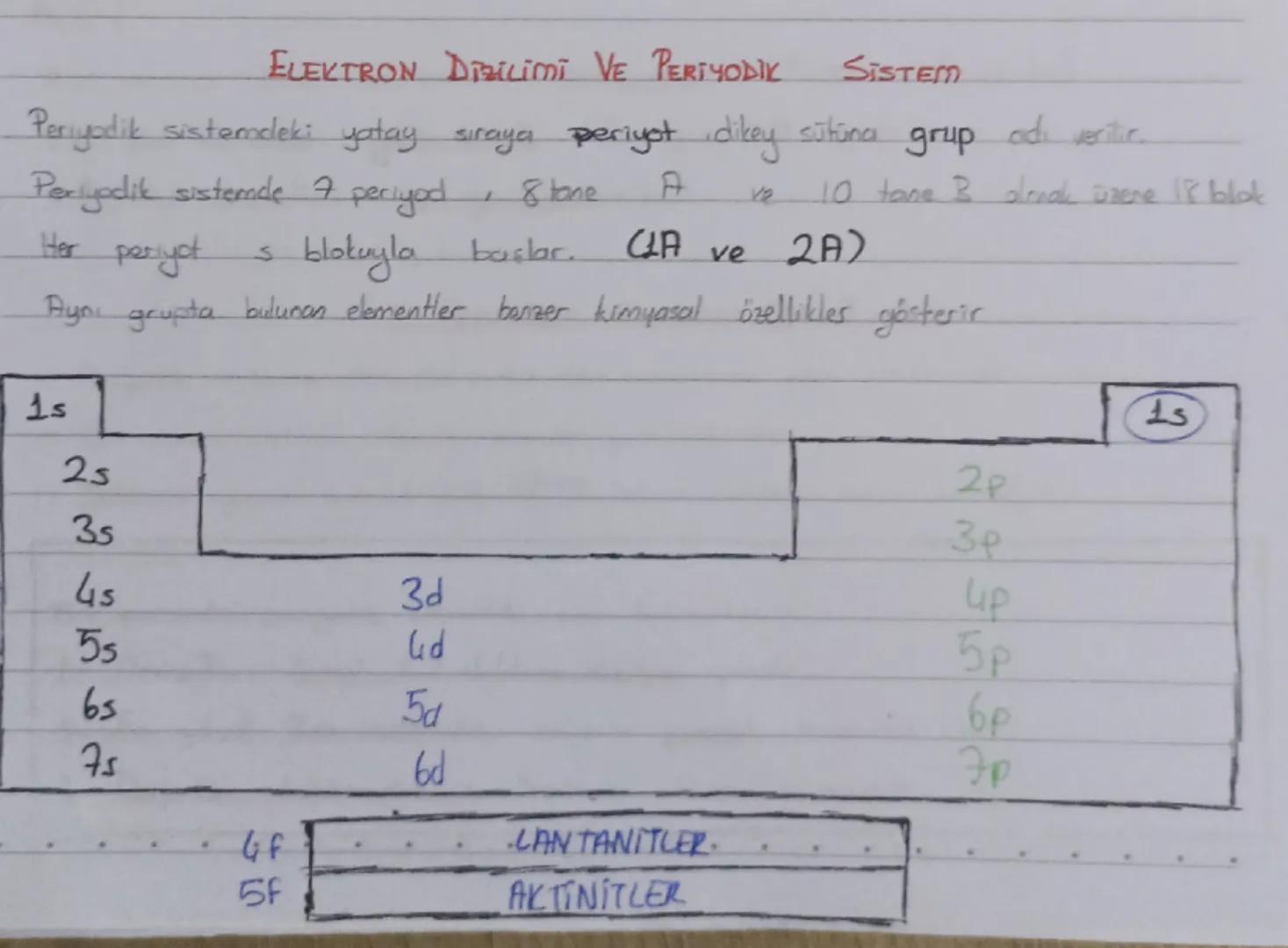
Periyodik sistemde yatay sıralara periyot, dikey sütunlara grup denir. Sistem toplam 7 periyot ve 18 gruptan (8 A grubu, 10 B grubu) oluşur.
Her periyot s bloku (1A ve 2A) ile başlar ve aynı grupta bulunan elementler benzer kimyasal özellikler gösterir. Periyodik tablo s, p, d ve f bloklarından oluşur.
S ve p blok elementleri ana grup (A grubu), d blok elementleri geçiş metalleri (B grubu), f blok elementleri ise iç geçiş metalleridir. Lantanitler ve aktinitler f blokunda yer alır.
💡 Not: Bir elementin periyodik tablodaki yerini bulmak için her zaman nötr haldeki elektron dizilimine bakmalıyız. Atom elektron alsa da verse de periyodik sistemdeki yeri değişmez.

Grupların Özel Adları
Periyodik tablodaki grupların kolayca hatırlanabilmesi için özel adları vardır:
- 1A → Alkali metaller
- 2A → Toprak alkali metaller
- 3A → Toprak metalleri
- 4A → Karbon grubu
- 5A → Azot (nitrojen) grubu
- 6A → Oksijen (kalkojen) grubu
- 7A → Halojenler
- 8A → Soygazlar / Asal gazlar / İnert gazlar
Ayrıca, f blokunda bulunan 4f serisi lantanitler ve 5f serisi aktinitler olarak adlandırılır.
💡 Hatırlatma: Sınav sorularında grup adları sıklıkla karşınıza çıkar. Bu adları ve elementlerin özelliklerini bilmek sorularda büyük avantaj sağlar.

Periyodik Sistemde Yer Bulma
Periyodik sistemde elementler artan atom numarasına göre sıralanmıştır. Bir elementin yerini bulmak için şu adımları izlemelisin:
- Elementin temel hal elektron dizilimini yaz
- En yüksek baş kuantum sayısı sana periyot numarasını verir
- Değerlik elektronlarının toplamı ise grup numarasını gösterir
Örneğin, Sodyum (Na) elementinin elektron dizilimi 1s² 2s² 2p⁶ 3s¹ şeklindedir. En yüksek baş kuantum sayısı 3 olduğu için 3. periyotta, değerlik elektron sayısı 1 olduğu için 1A grubunda yer alır.
💡 Unutma: Bir element iyonlaşsa bile, periyodik sistemdeki yeri değişmez. Çünkü yerini belirleyen faktör, nötr haldeki elektron sayısıdır.

İyonlaşma Enerjisi
İyonlaşma enerjisi, gaz halindeki atom veya iyondan bir elektron koparmak için gereken enerjidir. Bu süreç her zaman endotermiktir yani enerji gerektirir.
Bir atomda kaç tane elektron varsa, o kadar iyonlaşma enerjisi değeri vardır. İyonlaşma enerjisi en büyük olan element helyumdur.
İyonlaşma enerjileri şu şekilde gösterilir:
-
- İyonlaşma: X(g) + IE₁ → X⁺(g) + e⁻
-
- İyonlaşma: X⁺(g) + IE₂ → X²⁺(g) + e⁻
Bir atomdan elektron koparıldıkça, elektron başına düşen çekim kuvveti artar. Bu nedenle, bir sonraki elektronu koparmak için daha fazla enerji gerekir: IE₁ < IE₂ < IE₃ < ... < IEₙ
💡 İpucu: İyonlaşma enerjileri arasındaki büyük sıçramalar, grup numarasını bulmanızı sağlar. Eğer değerler arasında 3-5 kat veya daha fazla bir artış görürseniz, bu bir katmanın bitip diğerine geçildiğinin işaretidir.
İyonlaşma Enerjisinin Değişimi
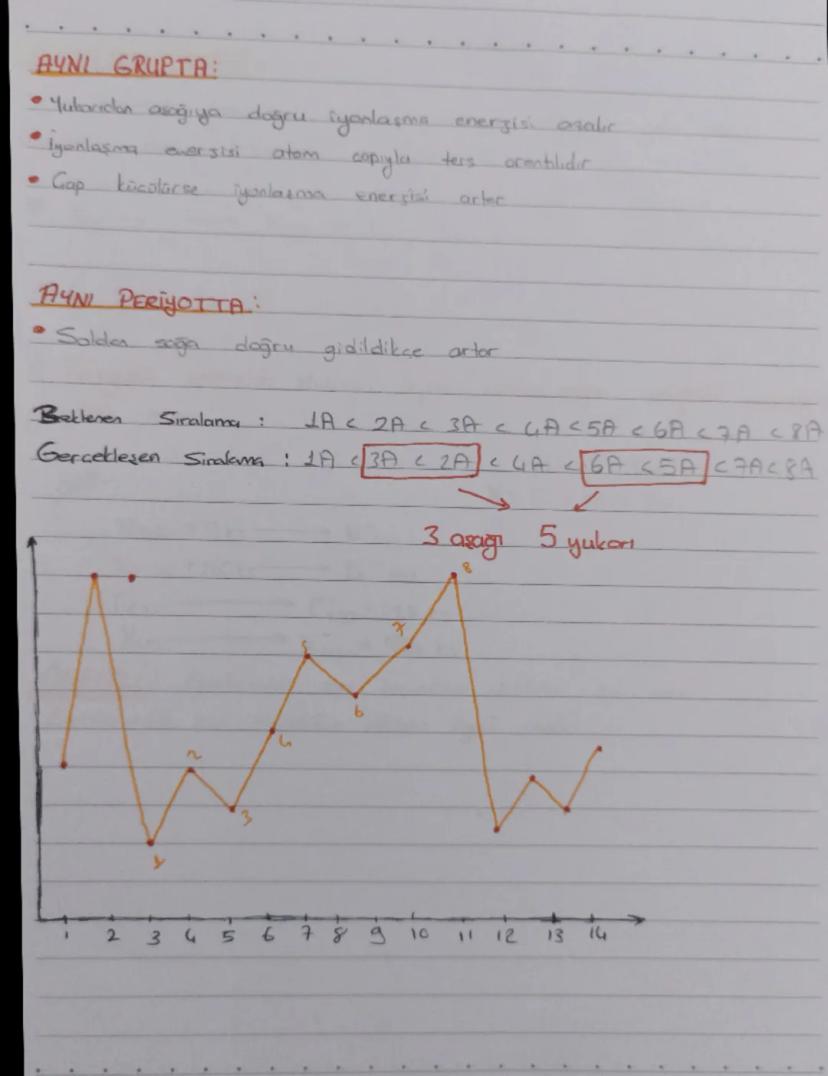
Aynı grupta yukarıdan aşağıya doğru iyonlaşma enerjisi azalır. İyonlaşma enerjisi atom çapıyla ters orantılıdır. Çap büyüdükçe iyonlaşma enerjisi düşer.
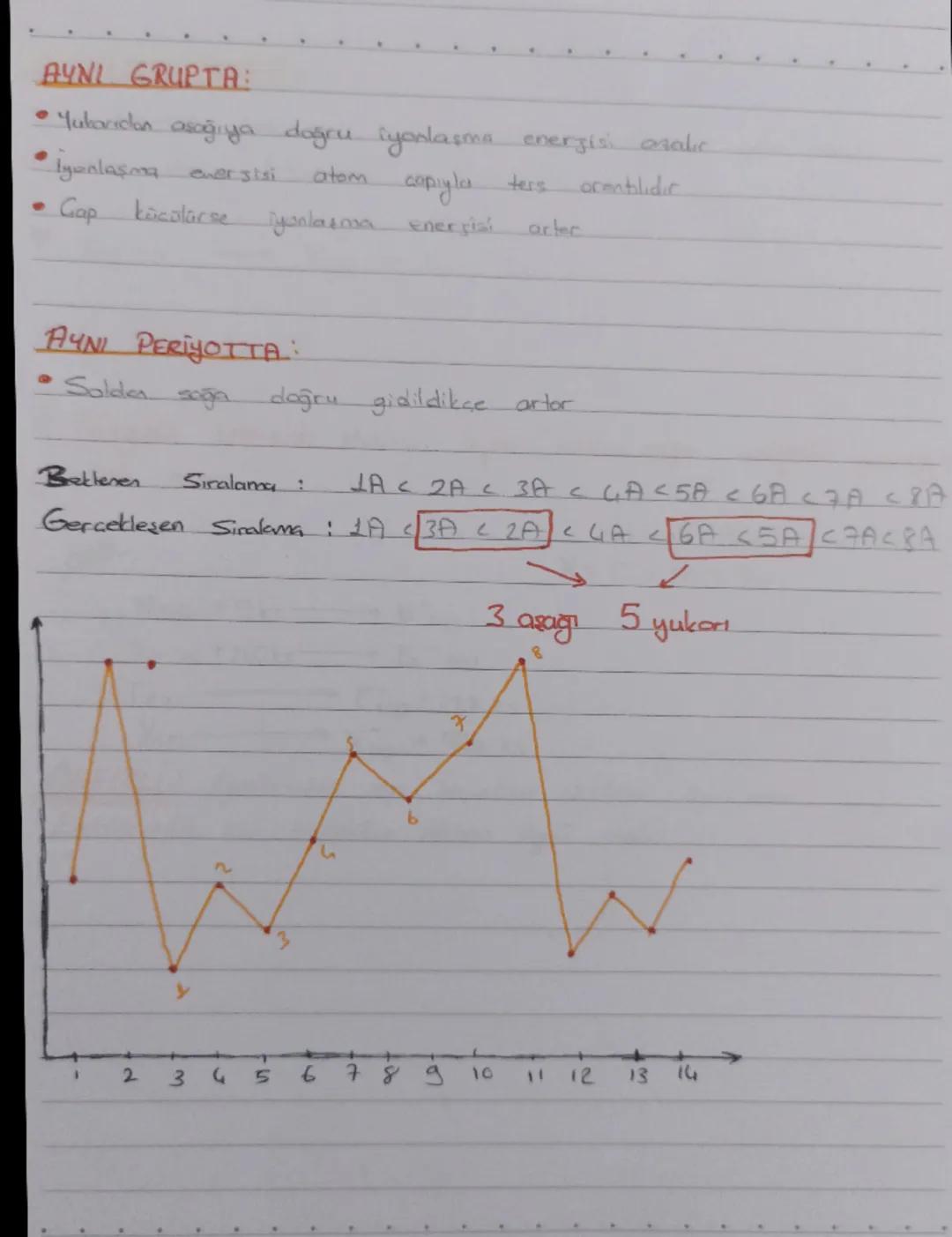
Aynı periyotta soldan sağa doğru gidildikçe genellikle iyonlaşma enerjisi artar. Ancak beklenen sıralama ile gerçekleşen sıralama arasında farklılıklar vardır:
- Beklenen Sıralama: 1A < 2A < 3A < 4A < 5A < 6A < 7A < 8A
- Gerçekleşen Sıralama: 1A < 3A < 2A < 4A < 6A < 5A < 7A < 8A
Bu farklılığın nedeni, atom yapılarındaki elektron-elektron itmeleri ve orbital enerjileridir. 3A, 5A ve 7A gruplarında "dalgalanmalar" görülür.
💡 Kolay Hatırlatma: "3 aşağı, 5 yukarı" şeklinde hatırlayabilirsin. 3A, 5A ve 7A gruplarında iyonlaşma enerjisinde beklenenden farklı değişimler olur.

Elektron İlgisi
Elektron ilgisi, gaz halindeki atom veya iyona bir elektron verildiğinde gerçekleşen enerji değişimidir. Bu süreç endotermik veya ekzotermik olabilir.
X(g) + e⁻ → X⁻(g) + Ei
Periyodik sistemde elektron ilgisi genellikle soldan sağa, aşağıdan yukarıya doğru artar. Elektron ilgisi en fazla olan element klorun (Cl) olduğu düşünülmektedir.
Örnekler:
- N(g) + 9 kJ → N⁻(g) (endotermik)
- Be(g) + 240 kJ → Be⁻(g) (endotermik)
- F(g) → F⁻(g) + 328 kJ (ekzotermik)
- X(g) → X⁻(g) + 596 kJ (ekzotermik)
💡 Dikkat: Ekzotermik olaylarda sayı büyüdükçe elektron ilgisi artar, endotermik olaylarda ise sayı büyüdükçe elektron ilgisi azalır. Karşılaştırmalarda bu farka dikkat etmelisin!

Elektronegatiflik
Elektronegatiflik, bir atomun kimyasal bir bağdaki elektronları çekme yeteneğidir. Atom çapı azaldıkça elektronegatiflik artar. Elektronegatifliği en büyük element flor (F)'dur.
Soygazların bağ yapma eğilimleri olmadığı için elektronegatiflik değerleri yoktur.
Elektronegatiflik farkı, bağın karakterini belirler:
- Fark çok azsa → Apolar kovalent bağ (bağ elektronu ortakta kalır)
- Fark orta düzeydeyse → Polar kovalent bağ (bağ elektronu bir tarafa kayar)
- Fark büyükse → İyonik bağ (bağ elektronu koparılır)
Elektronegatiflik farkı azalırsa kovalent karakter artar, fark artarsa iyonik karakter artar.
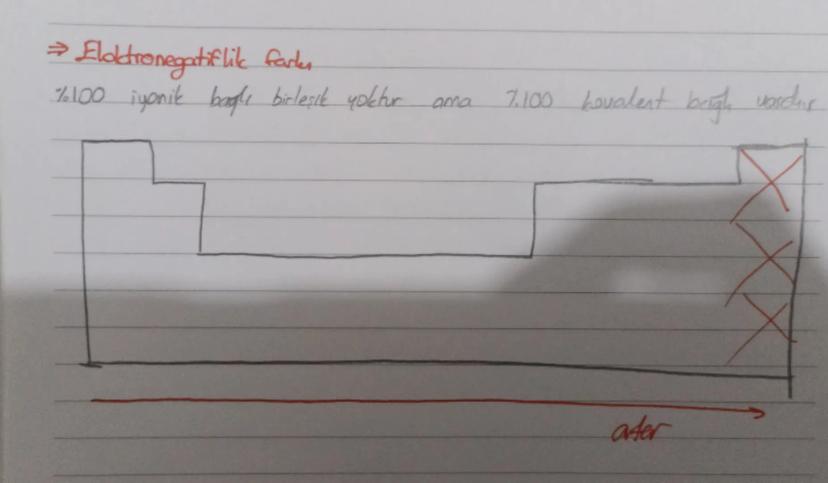
💡 Kimyasal bir gerçek: %100 iyonik bağlı bileşik yoktur, ancak %100 kovalent bağlı bileşikler vardır. En iyonik bağ bile belirli oranda kovalent karakter taşır.

Metalik ve Ametalik Özellikler
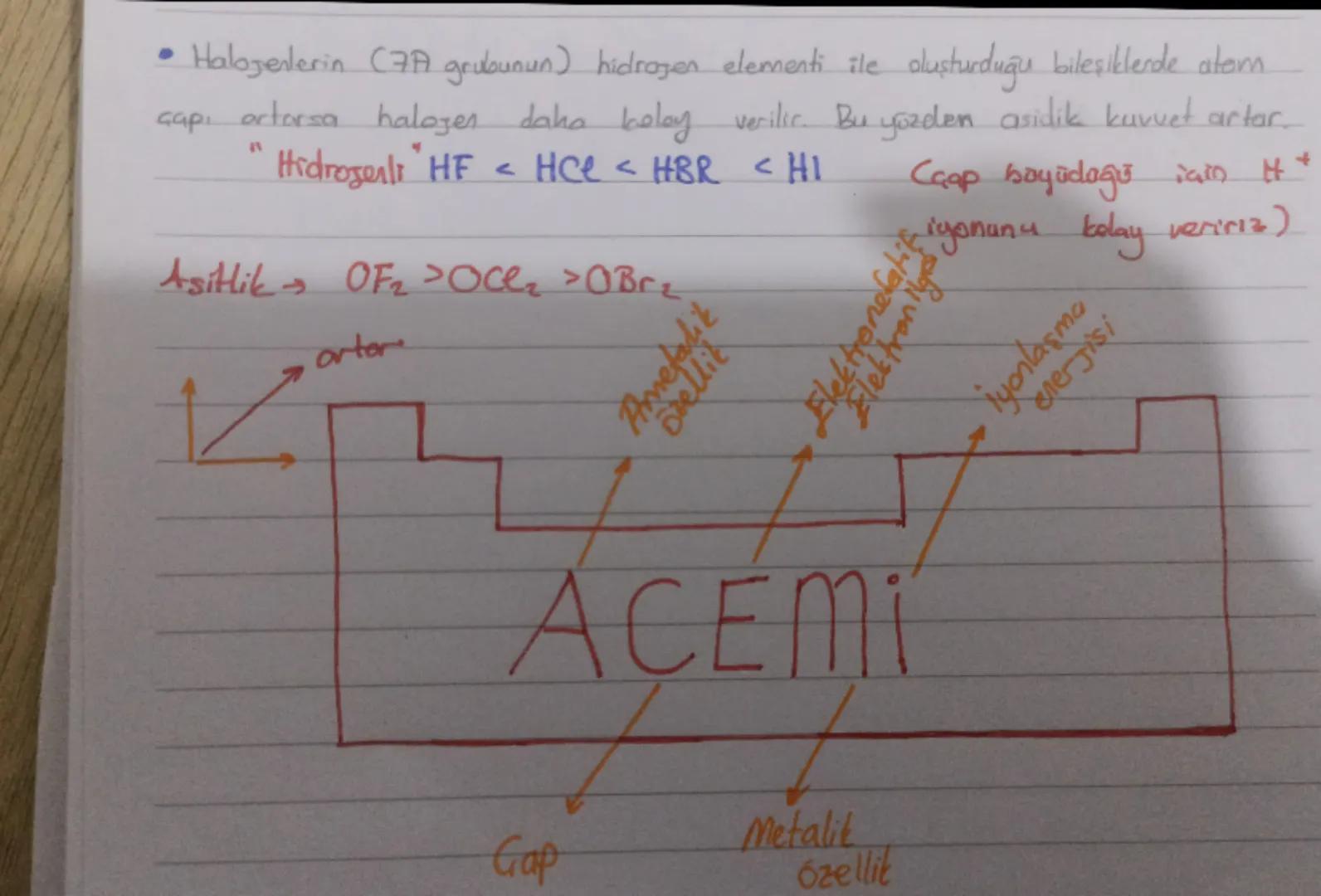
Metaller, elektron verme eğilimi yüksek olan elementlerdir. Atom çapı arttıkça elektron verme eğilimi ve metalik aktiflik artar. Periyodik sistemde aynı periyotta sağdan sola, aynı grupta yukarıdan aşağıya doğru gidildikçe metalik özellik artar.
Ametaller, elektron alma eğilimi yüksek olan elementlerdir. Atom çapı azaldıkça elektron alma eğilimi ve ametalik aktiflik artar. Periyodik sistemde aynı periyotta soldan sağa, aynı grupta aşağıdan yukarıya doğru ametalik özellik artar.
💡 Kolay hatırlama: Metalik ve ametalik özellikler atom çapıyla doğrudan ilişkilidir. Metalik özellikler çapla doğru orantılı, ametalik özellikler ise ters orantılıdır.

Asidik ve Bazik Özellikler
Asit: Suda çözündüğünde H⁺ iyonu veren maddelerdir.
Baz: Suda çözündüğünde OH⁻ iyonu veren maddelerdir.
Oksit: OF₂ birleşiği dışında diğer elementlerin oksijen ile yaptığı bileşiklere oksit denir.
Oksitler üç gruba ayrılır:
- Metal Oksitler: Bazik özellik gösterir (Na₂O, MgO)
- Ametal Oksitler: Asidik özellik gösterir (SO₃, P₂O₅)
- Nötr Oksitler: Ametal sayısı oksijen sayısına eşit veya az ise nötr özellik gösterir (CO, N₂O)
Amfoter metaller (Al, Sn, Pb, Zn, Cr, Be) hem asidik hem de bazik özellik gösterebilir.
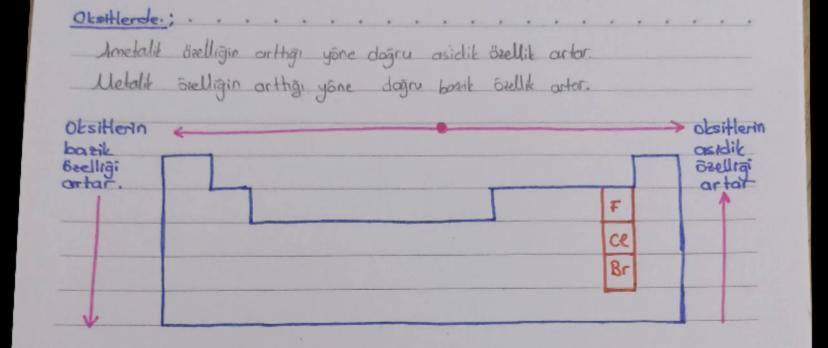
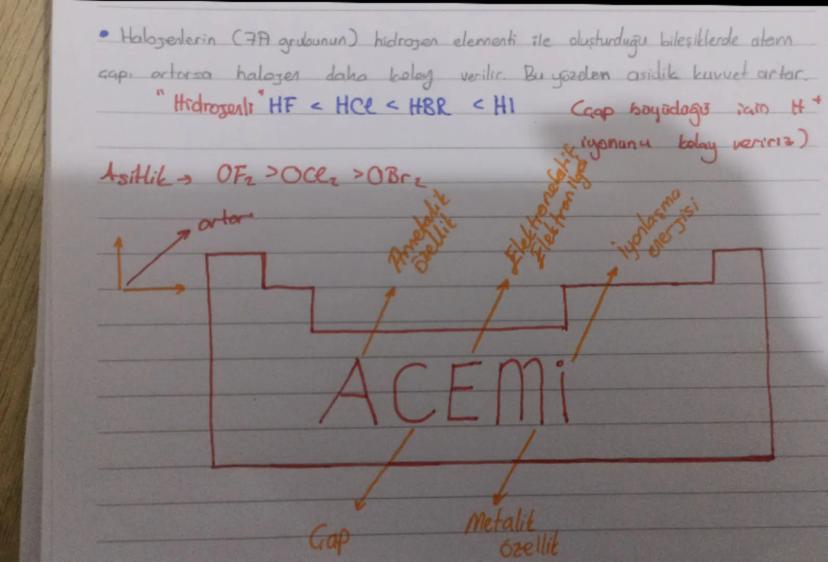
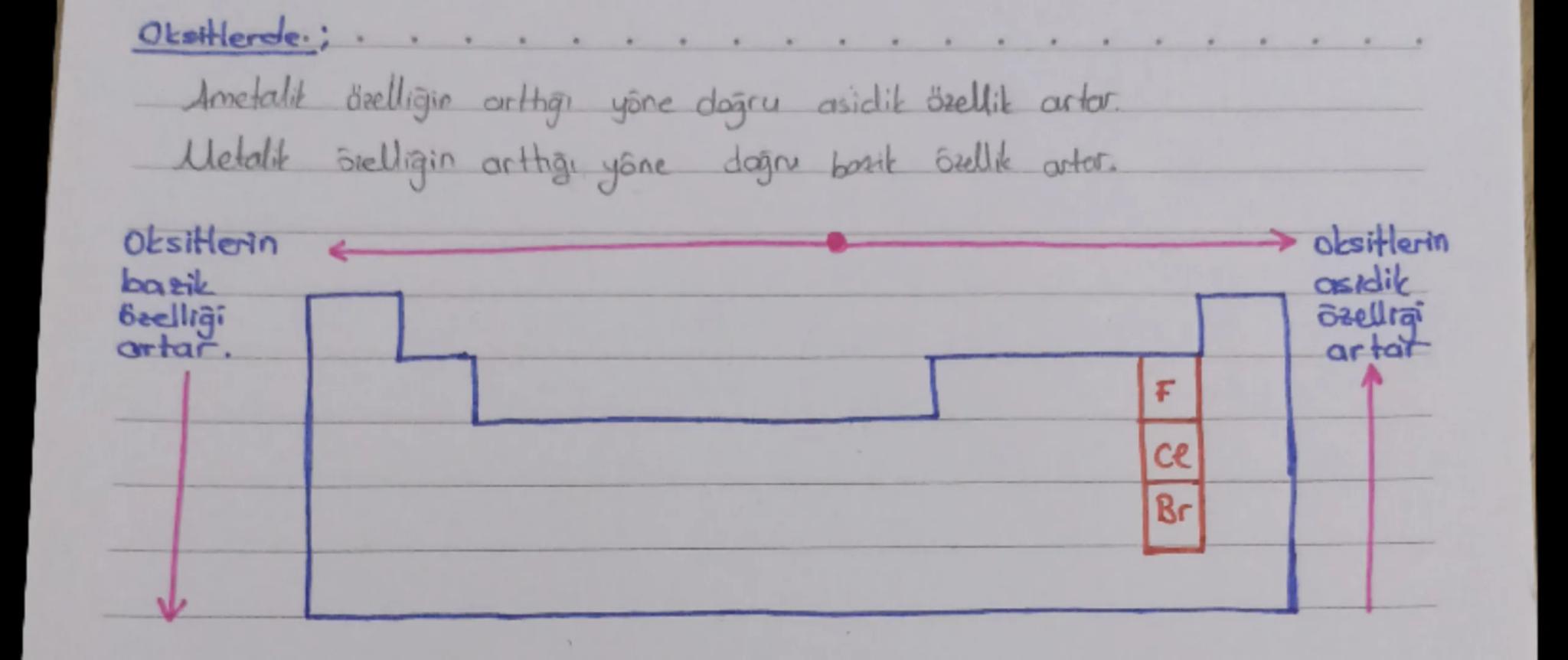
💡 Pratik bilgi: Oksitlerde ametalik özelliğin arttığı yöne doğru asidik özellik, metalik özelliğin arttığı yöne doğru bazik özellik artar. Periyodik tabloda sağa ve yukarı gidildikçe oksitlerin asitliği artar.

Oksitlerin Özellikleri
Metal Oksitler: Amfoter metaller hariç metallerin oksitleri (O⁻²) ve hidroksitleri (OH⁻) bazik özellik gösterir. Örneğin: Na₂O, MgO.
Ametal Oksitler: Ametallerin oksijence zengin bileşikleri asidik özellik gösterir. Bir ametal oksitin (A₁O₍ᵧ₎) asidik olması için y>x olmalıdır. Örneğin: SO₃, P₂O₅.
Nötr Oksitler: Ametal sayısı oksijen sayısına eşit veya az ise nötr özellik gösterir. Örneğin: CO, N₂O.
Periyodik tabloda metal oksitlerin bazikliği aşağıya ve sola doğru artarken, ametal oksitlerin asitliği yukarıya ve sağa doğru artar.
💡 Günlük hayattan örnek: Suda çözündüğünde asit oluşturan CO₂ gazı, havadaki nem ile birleştiğinde asit yağmurlarının oluşumuna katkıda bulunur. Bu, ametal oksitlerin asidik özelliğinin pratik bir sonucudur.
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Periodic Table
5AYT KİMYA KİMYA VE ELEKTRİK
AKTİFLİK
Elementlerin Periyodik Tabloda Yerinin Bulunması | 9. Sınıf Kimya
Elementlerin Periyodik Tabloda Yerinin Bulunması | 9. Sınıf | Kimya | Değerlik Elektron | Orbitaller
Tyt Kimya Periyodik Sistem
Beleş Tyt notu
11. sınıf kimya
1. ünite
2. Ünite Ders Notu: PERİYODİK TABLO VE ELEMENTLERİN ÖZELLİKLERİ
Derste çıkardığım slayt notudur. Kendi özetlerim hesabımda mevcut.
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
AYT Kimya 1. Ünite | Net ve Anlaşılır Anlatım
Periyodik sistem, elementlerin özelliklerine göre düzenlendiği temel bir kimya konusudur. Bu sistemde elementler, atom numaralarına göre sıralanmış ve elektron dizilimlerine dayalı olarak gruplandırılmıştır. Periyodik sistemin anlaşılması, elementlerin fiziksel ve kimyasal özelliklerini tahmin etmemize yardımcı olur.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektron Dizilimi ve Periyodik Sistem
Periyodik sistemde yatay sıralara periyot, dikey sütunlara grup denir. Sistem toplam 7 periyot ve 18 gruptan (8 A grubu, 10 B grubu) oluşur.
Her periyot s bloku (1A ve 2A) ile başlar ve aynı grupta bulunan elementler benzer kimyasal özellikler gösterir. Periyodik tablo s, p, d ve f bloklarından oluşur.
S ve p blok elementleri ana grup (A grubu), d blok elementleri geçiş metalleri (B grubu), f blok elementleri ise iç geçiş metalleridir. Lantanitler ve aktinitler f blokunda yer alır.
💡 Not: Bir elementin periyodik tablodaki yerini bulmak için her zaman nötr haldeki elektron dizilimine bakmalıyız. Atom elektron alsa da verse de periyodik sistemdeki yeri değişmez.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Grupların Özel Adları
Periyodik tablodaki grupların kolayca hatırlanabilmesi için özel adları vardır:
- 1A → Alkali metaller
- 2A → Toprak alkali metaller
- 3A → Toprak metalleri
- 4A → Karbon grubu
- 5A → Azot (nitrojen) grubu
- 6A → Oksijen (kalkojen) grubu
- 7A → Halojenler
- 8A → Soygazlar / Asal gazlar / İnert gazlar
Ayrıca, f blokunda bulunan 4f serisi lantanitler ve 5f serisi aktinitler olarak adlandırılır.
💡 Hatırlatma: Sınav sorularında grup adları sıklıkla karşınıza çıkar. Bu adları ve elementlerin özelliklerini bilmek sorularda büyük avantaj sağlar.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Periyodik Sistemde Yer Bulma
Periyodik sistemde elementler artan atom numarasına göre sıralanmıştır. Bir elementin yerini bulmak için şu adımları izlemelisin:
- Elementin temel hal elektron dizilimini yaz
- En yüksek baş kuantum sayısı sana periyot numarasını verir
- Değerlik elektronlarının toplamı ise grup numarasını gösterir
Örneğin, Sodyum (Na) elementinin elektron dizilimi 1s² 2s² 2p⁶ 3s¹ şeklindedir. En yüksek baş kuantum sayısı 3 olduğu için 3. periyotta, değerlik elektron sayısı 1 olduğu için 1A grubunda yer alır.
💡 Unutma: Bir element iyonlaşsa bile, periyodik sistemdeki yeri değişmez. Çünkü yerini belirleyen faktör, nötr haldeki elektron sayısıdır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
İyonlaşma Enerjisi
İyonlaşma enerjisi, gaz halindeki atom veya iyondan bir elektron koparmak için gereken enerjidir. Bu süreç her zaman endotermiktir yani enerji gerektirir.
Bir atomda kaç tane elektron varsa, o kadar iyonlaşma enerjisi değeri vardır. İyonlaşma enerjisi en büyük olan element helyumdur.
İyonlaşma enerjileri şu şekilde gösterilir:
-
- İyonlaşma: X(g) + IE₁ → X⁺(g) + e⁻
-
- İyonlaşma: X⁺(g) + IE₂ → X²⁺(g) + e⁻
Bir atomdan elektron koparıldıkça, elektron başına düşen çekim kuvveti artar. Bu nedenle, bir sonraki elektronu koparmak için daha fazla enerji gerekir: IE₁ < IE₂ < IE₃ < ... < IEₙ
💡 İpucu: İyonlaşma enerjileri arasındaki büyük sıçramalar, grup numarasını bulmanızı sağlar. Eğer değerler arasında 3-5 kat veya daha fazla bir artış görürseniz, bu bir katmanın bitip diğerine geçildiğinin işaretidir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
İyonlaşma Enerjisinin Değişimi
Aynı grupta yukarıdan aşağıya doğru iyonlaşma enerjisi azalır. İyonlaşma enerjisi atom çapıyla ters orantılıdır. Çap büyüdükçe iyonlaşma enerjisi düşer.
Aynı periyotta soldan sağa doğru gidildikçe genellikle iyonlaşma enerjisi artar. Ancak beklenen sıralama ile gerçekleşen sıralama arasında farklılıklar vardır:
- Beklenen Sıralama: 1A < 2A < 3A < 4A < 5A < 6A < 7A < 8A
- Gerçekleşen Sıralama: 1A < 3A < 2A < 4A < 6A < 5A < 7A < 8A
Bu farklılığın nedeni, atom yapılarındaki elektron-elektron itmeleri ve orbital enerjileridir. 3A, 5A ve 7A gruplarında "dalgalanmalar" görülür.
💡 Kolay Hatırlatma: "3 aşağı, 5 yukarı" şeklinde hatırlayabilirsin. 3A, 5A ve 7A gruplarında iyonlaşma enerjisinde beklenenden farklı değişimler olur.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektron İlgisi
Elektron ilgisi, gaz halindeki atom veya iyona bir elektron verildiğinde gerçekleşen enerji değişimidir. Bu süreç endotermik veya ekzotermik olabilir.
X(g) + e⁻ → X⁻(g) + Ei
Periyodik sistemde elektron ilgisi genellikle soldan sağa, aşağıdan yukarıya doğru artar. Elektron ilgisi en fazla olan element klorun (Cl) olduğu düşünülmektedir.
Örnekler:
- N(g) + 9 kJ → N⁻(g) (endotermik)
- Be(g) + 240 kJ → Be⁻(g) (endotermik)
- F(g) → F⁻(g) + 328 kJ (ekzotermik)
- X(g) → X⁻(g) + 596 kJ (ekzotermik)
💡 Dikkat: Ekzotermik olaylarda sayı büyüdükçe elektron ilgisi artar, endotermik olaylarda ise sayı büyüdükçe elektron ilgisi azalır. Karşılaştırmalarda bu farka dikkat etmelisin!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Elektronegatiflik
Elektronegatiflik, bir atomun kimyasal bir bağdaki elektronları çekme yeteneğidir. Atom çapı azaldıkça elektronegatiflik artar. Elektronegatifliği en büyük element flor (F)'dur.
Soygazların bağ yapma eğilimleri olmadığı için elektronegatiflik değerleri yoktur.
Elektronegatiflik farkı, bağın karakterini belirler:
- Fark çok azsa → Apolar kovalent bağ (bağ elektronu ortakta kalır)
- Fark orta düzeydeyse → Polar kovalent bağ (bağ elektronu bir tarafa kayar)
- Fark büyükse → İyonik bağ (bağ elektronu koparılır)
Elektronegatiflik farkı azalırsa kovalent karakter artar, fark artarsa iyonik karakter artar.
💡 Kimyasal bir gerçek: %100 iyonik bağlı bileşik yoktur, ancak %100 kovalent bağlı bileşikler vardır. En iyonik bağ bile belirli oranda kovalent karakter taşır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Metalik ve Ametalik Özellikler
Metaller, elektron verme eğilimi yüksek olan elementlerdir. Atom çapı arttıkça elektron verme eğilimi ve metalik aktiflik artar. Periyodik sistemde aynı periyotta sağdan sola, aynı grupta yukarıdan aşağıya doğru gidildikçe metalik özellik artar.
Ametaller, elektron alma eğilimi yüksek olan elementlerdir. Atom çapı azaldıkça elektron alma eğilimi ve ametalik aktiflik artar. Periyodik sistemde aynı periyotta soldan sağa, aynı grupta aşağıdan yukarıya doğru ametalik özellik artar.
💡 Kolay hatırlama: Metalik ve ametalik özellikler atom çapıyla doğrudan ilişkilidir. Metalik özellikler çapla doğru orantılı, ametalik özellikler ise ters orantılıdır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Asidik ve Bazik Özellikler
Asit: Suda çözündüğünde H⁺ iyonu veren maddelerdir.
Baz: Suda çözündüğünde OH⁻ iyonu veren maddelerdir.
Oksit: OF₂ birleşiği dışında diğer elementlerin oksijen ile yaptığı bileşiklere oksit denir.
Oksitler üç gruba ayrılır:
- Metal Oksitler: Bazik özellik gösterir (Na₂O, MgO)
- Ametal Oksitler: Asidik özellik gösterir (SO₃, P₂O₅)
- Nötr Oksitler: Ametal sayısı oksijen sayısına eşit veya az ise nötr özellik gösterir (CO, N₂O)
Amfoter metaller (Al, Sn, Pb, Zn, Cr, Be) hem asidik hem de bazik özellik gösterebilir.
💡 Pratik bilgi: Oksitlerde ametalik özelliğin arttığı yöne doğru asidik özellik, metalik özelliğin arttığı yöne doğru bazik özellik artar. Periyodik tabloda sağa ve yukarı gidildikçe oksitlerin asitliği artar.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Oksitlerin Özellikleri
Metal Oksitler: Amfoter metaller hariç metallerin oksitleri (O⁻²) ve hidroksitleri (OH⁻) bazik özellik gösterir. Örneğin: Na₂O, MgO.
Ametal Oksitler: Ametallerin oksijence zengin bileşikleri asidik özellik gösterir. Bir ametal oksitin (A₁O₍ᵧ₎) asidik olması için y>x olmalıdır. Örneğin: SO₃, P₂O₅.
Nötr Oksitler: Ametal sayısı oksijen sayısına eşit veya az ise nötr özellik gösterir. Örneğin: CO, N₂O.
Periyodik tabloda metal oksitlerin bazikliği aşağıya ve sola doğru artarken, ametal oksitlerin asitliği yukarıya ve sağa doğru artar.
💡 Günlük hayattan örnek: Suda çözündüğünde asit oluşturan CO₂ gazı, havadaki nem ile birleştiğinde asit yağmurlarının oluşumuna katkıda bulunur. Bu, ametal oksitlerin asidik özelliğinin pratik bir sonucudur.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Periodic Table
5AYT KİMYA KİMYA VE ELEKTRİK
AKTİFLİK
Elementlerin Periyodik Tabloda Yerinin Bulunması | 9. Sınıf Kimya
Elementlerin Periyodik Tabloda Yerinin Bulunması | 9. Sınıf | Kimya | Değerlik Elektron | Orbitaller
Tyt Kimya Periyodik Sistem
Beleş Tyt notu
11. sınıf kimya
1. ünite
2. Ünite Ders Notu: PERİYODİK TABLO VE ELEMENTLERİN ÖZELLİKLERİ
Derste çıkardığım slayt notudur. Kendi özetlerim hesabımda mevcut.
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅