Kimya dersinin temel konularını öğrenmek, çevremizdeki maddeleri ve günlük hayatta... Daha fazla göster
10. Sınıf Kimya Konuları ve Ders Notları



























Kimyanın Temel Kanunları ve Kimyasal Hesaplamalar
Kimya, maddelerin yapısını, özelliklerini ve birbirleriyle etkileşimlerini inceleyen bilim dalıdır. Bu derste maddelerin davranışlarını anlamamızı sağlayan temel kanunları öğreneceğiz.
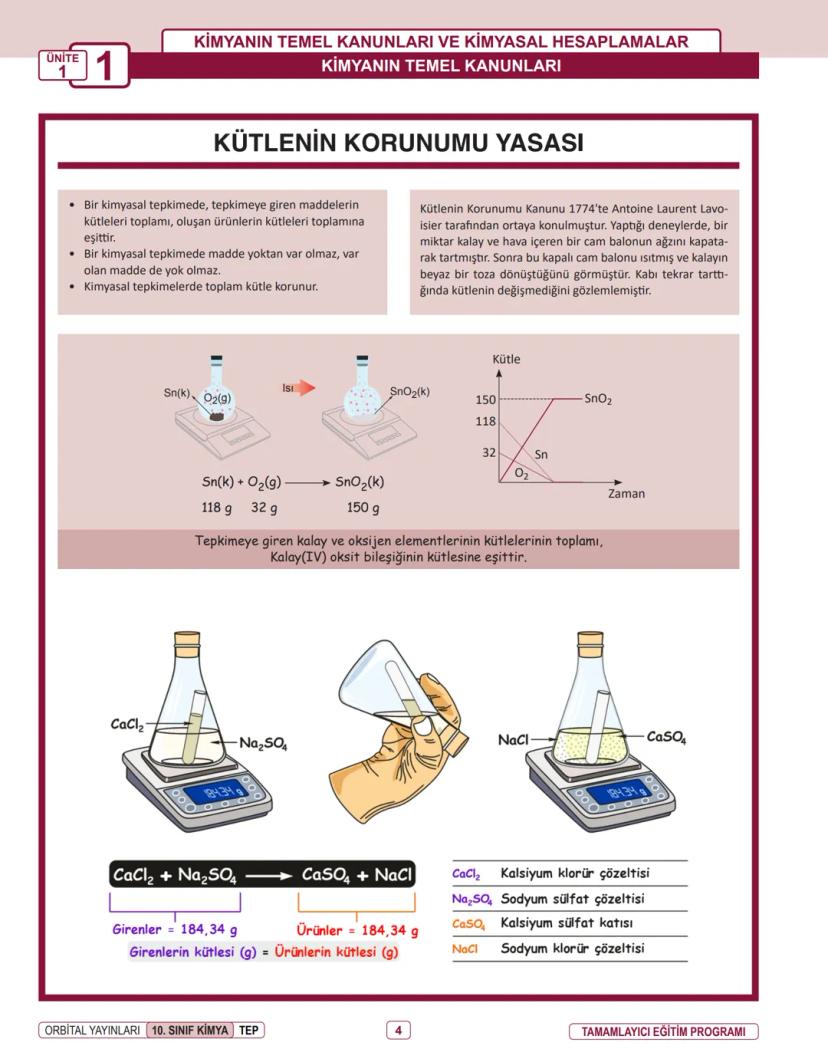
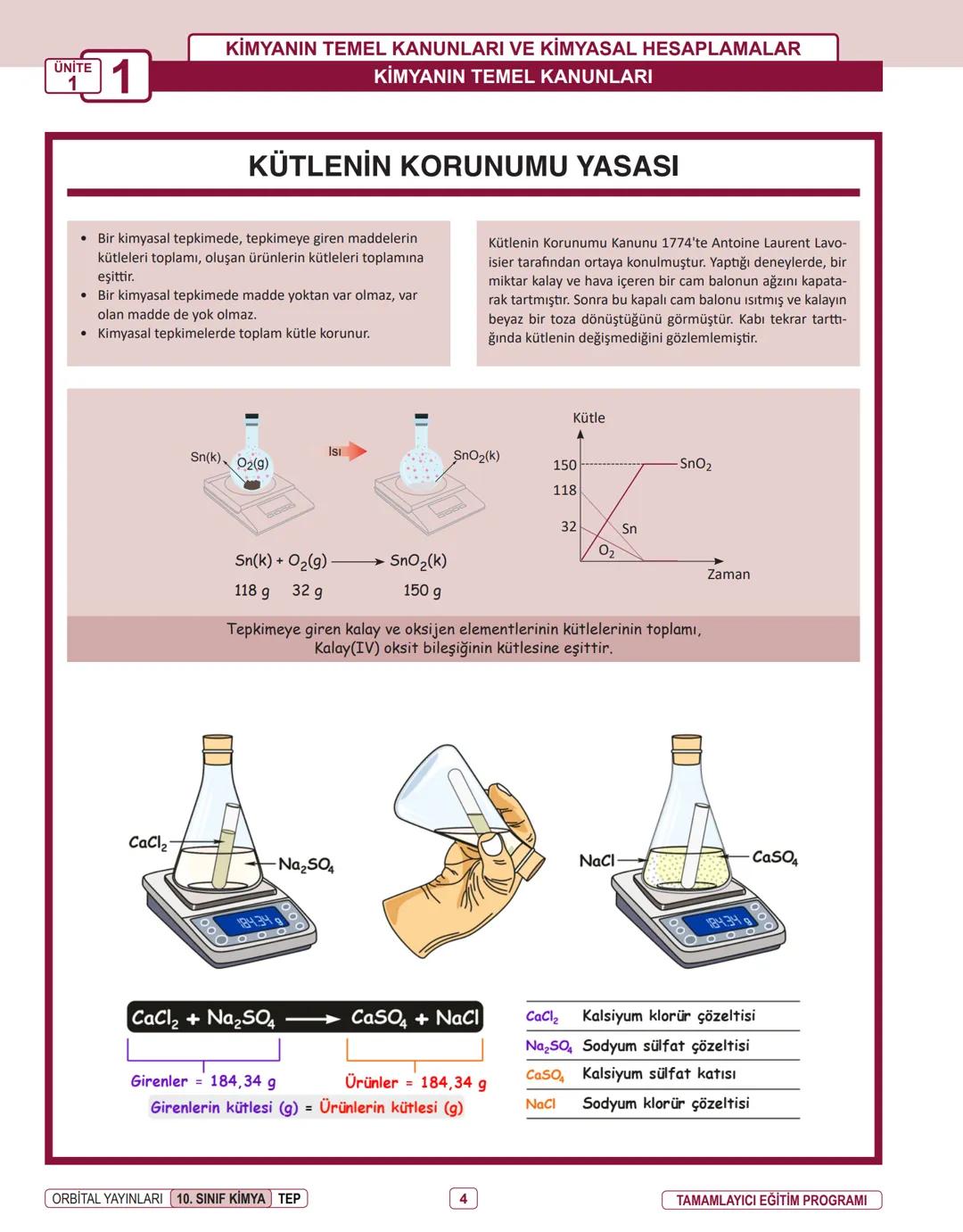
Kütlenin korunumu yasası, kimyanın en temel kanunlarından biridir. Bu yasaya göre bir kimyasal tepkimede, giren maddelerin kütleleri toplamı, oluşan ürünlerin kütleleri toplamına eşittir. Yani madde yoktan var olmaz, var olan da yok olmaz.
Antoine Lavoisier 1774'te bu yasayı keşfetmiştir. Kalay ve havanın bulunduğu kapalı bir kapta, kalayın oksitlenmesi sonucu kütlede değişim olmadığını gözlemlemiştir.
Önemli Not: Kimyasal tepkimelerde atomlar yok olmaz, sadece yeniden düzenlenirler. Bu nedenle kütle her zaman korunur.
Tepkimelerde kütlenin korunduğunu şu örnekle görebiliriz:
CaCl₂ + Na₂SO₄ → CaSO₄ + NaCl
Girenlerin kütlesi = 184,34 g = Ürünlerin kütlesi
Sabit Oranlar Yasası
Maddelerin davranışlarını anlamak için bilmeniz gereken bir başka temel yasa da sabit oranlar yasasıdır. Bu yasa, 1799'da Joseph Proust tarafından ortaya atılmıştır.
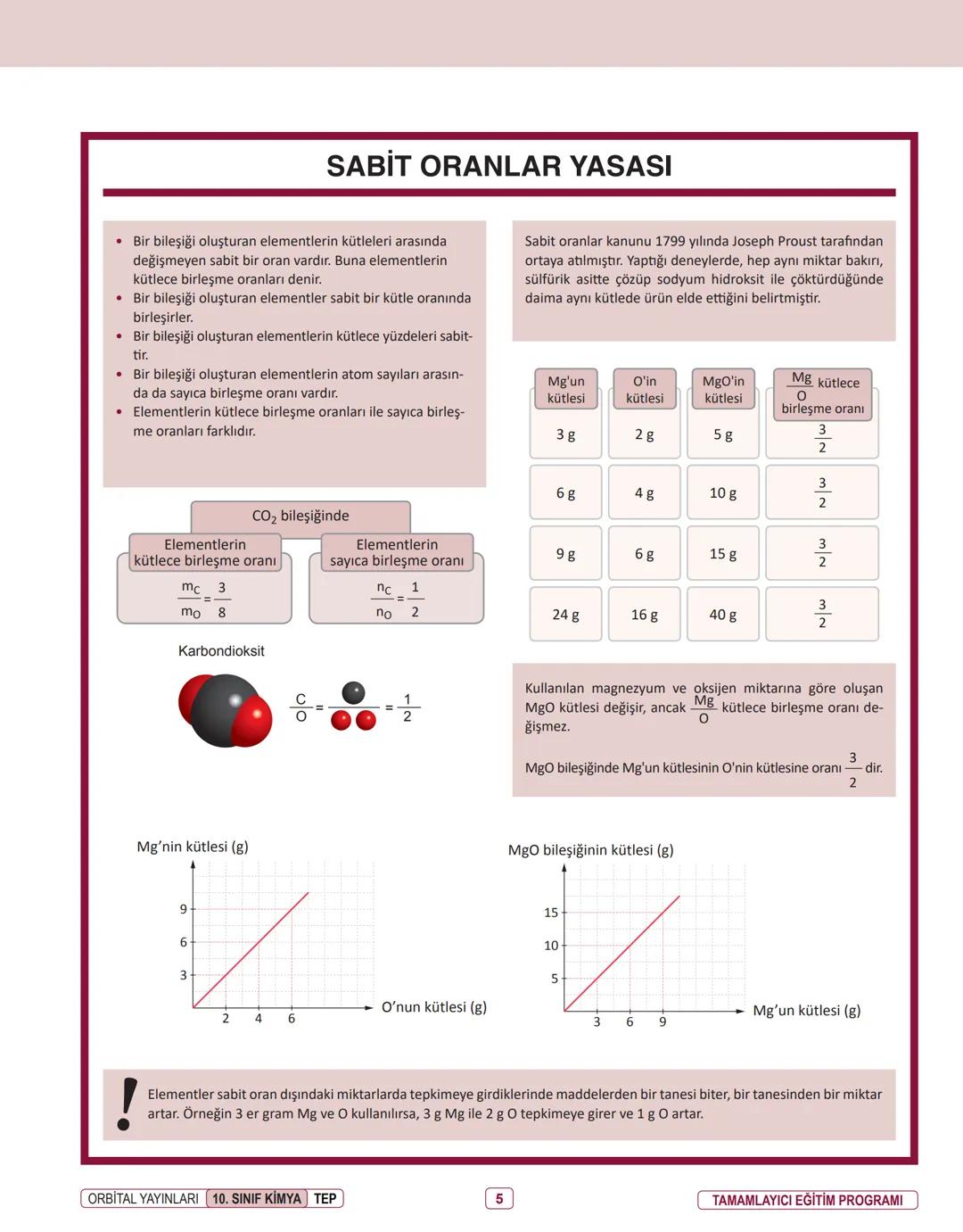
Sabit oranlar yasasına göre bir bileşiği oluşturan elementler her zaman sabit bir kütle oranında birleşirler. Örneğin, karbondioksit (CO₂) molekülünde karbon ve oksijenin kütlece birleşme oranı daima 3/8'dir.
Bileşiklerde elementlerin kütlece yüzdeleri ve atom sayıları arasındaki oran sabittir. Ancak dikkat edin, kütlece birleşme oranı ile sayıca birleşme oranı farklıdır. CO₂'de karbon ve oksijenin sayıca oranı 1/2 iken, kütlece oranı 3/8'dir.
Bu yasayı MgO örneğiyle daha iyi anlayabilirsiniz. Farklı miktarlarda magnezyum ve oksijen kullanılarak MgO oluşturulduğunda, oluşan bileşiğin kütlesi değişir ancak Mg/O kütlece birleşme oranı her zaman 3/2'dir.
| Mg kütlesi | O kütlesi | MgO kütlesi | Mg/O oranı |
|---|---|---|---|
| 3 g | 2 g | 5 g | 3/2 |
| 6 g | 4 g | 10 g | 3/2 |
| 24 g | 16 g | 40 g | 3/2 |
Hatırlatma: Elementler sabit oran dışında tepkimeye girdiklerinde, bir element bittiğinde tepkime durur ve diğer elementten artar. Örneğin 3 g Mg ve 3 g O kullanırsak, 3 g Mg ile 2 g O tepkimeye girer ve 1 g O artar.
Mol Tanecik Sayısı İlişkisi
Kimyada sıkça karşılaşacağımız bir kavram olan "mol", çok küçük tanecikler için kullanılan bir grup adıdır. Latince "büyük yığın" anlamına gelir.
Nasıl ki 1 düzine 12 tane, 1 deste 10 tane anlamına geliyorsa, 1 mol de 6,02x10²³ tane anlamına gelir. Bu sayı Avogadro sayısı olarak bilinir ve kısaca N₀ veya N₍A₎ ile gösterilir.
1 mol tanecik her zaman 6,02x10²³ taneye eşittir. Örneğin:
- 1 mol Fe elementi 6,02x10²³ tane Fe atomundan
- 2 mol He elementi 12,04x10²³ tane He atomundan
- 1 mol H₂O bileşiği 6,02x10²³ tane H₂O molekülünden oluşur
Tanecik sayısı (N) ile mol sayısı (n) arasındaki matematiksel ilişki şu şekildedir:
n = N/N₀
Burada:
- n = Mol sayısı
- N = Tanecik sayısı
- N₀ = Avogadro sayısı
İyi Anla: 1 molekül CO₂, 1 tane CO₂ molekülü demektir. 1 mol CO₂ ise 6,02x10²³ tane CO₂ molekülü anlamına gelir. Bu farkı anlamak, kimyasal hesaplamalarda başarılı olmanın anahtarıdır.

Mol Kütle İlişkisi
Mol kavramı anlaşıldıktan sonra, molün kütleyle ilişkisini de bilmeniz gerekir. Bu ilişki kimyasal hesaplamalar yapmanıza yardımcı olacak.
Bir elementin 1 mol atomu, gram türünden ne kadar kütle gelir? Bu değere o elementin mol kütlesi (atom kütlesi, MA) denir. Örneğin, Helyum (He) elementinin mol kütlesi 4 g/mol'dür. Bu şu anlama gelir:
- 1 mol He elementi = 4 gram
- 2 mol He elementi = 8 gram
- 0,2 mol He elementi = 0,8 gram
Elementlerin atom kütleleri konusunda merak etmeyin, bunlar genellikle sorularda verilecektir, ezberlemenize gerek yoktur.
Bağıl Atom Kütlesi kavramını da öğrenelim. 1 tane ¹²C izotopunun kütlesinin 1/12'sine 1 atomik kütle birimi (1 akb) denir. Akb, gram veya kg gibi bir kütle birimidir, ancak onlardan çok daha küçüktür.
Kütle ile mol sayısı arasındaki matematiksel ilişki şu formülle gösterilir:
n = m/MA
Burada:
- n = Mol sayısı
- m = Kütle (g)
- MA = Mol kütlesi
Pratik Bilgi: Bir bileşiğin mol kütlesi, onu oluşturan elementlerin atom kütlelerinin toplamına eşittir. Örneğin, 1 mol H₂O bileşiği = (2×1) + 16 = 18 gram eder .

Mol - Hacim İlişkisi
Kimyada gazlarla çalışırken, mol sayısı ile gazların hacmi arasındaki ilişkiyi bilmek çok önemlidir.
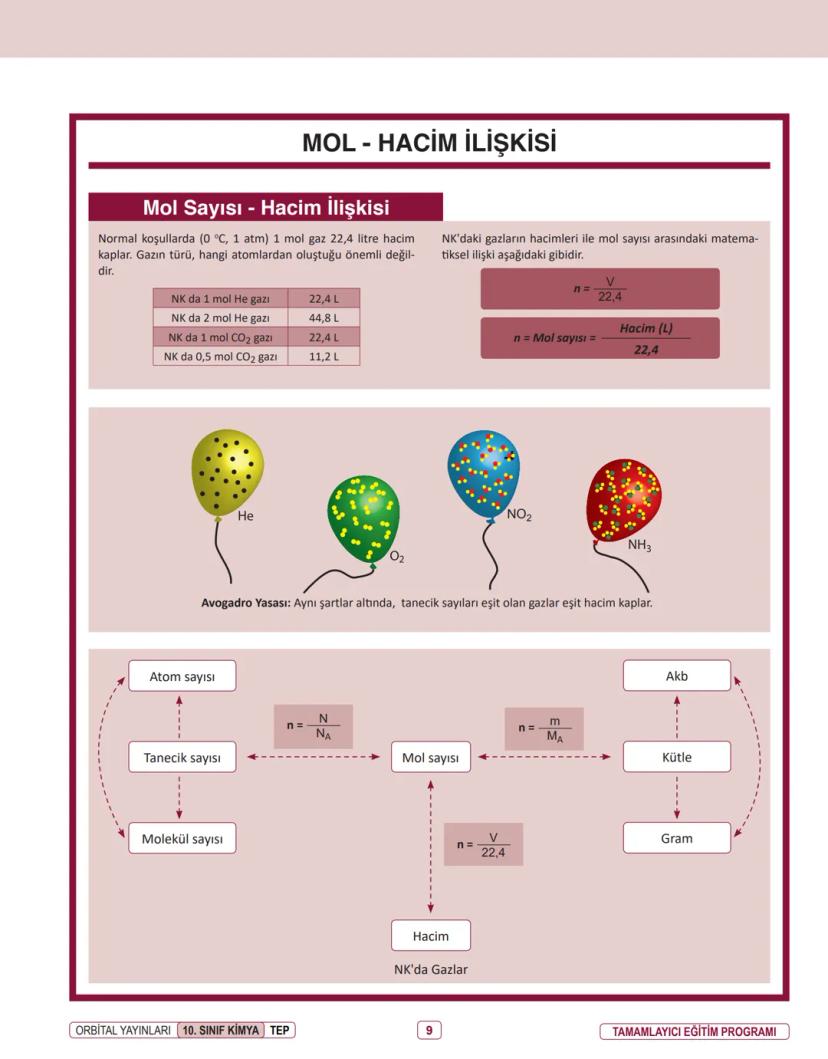
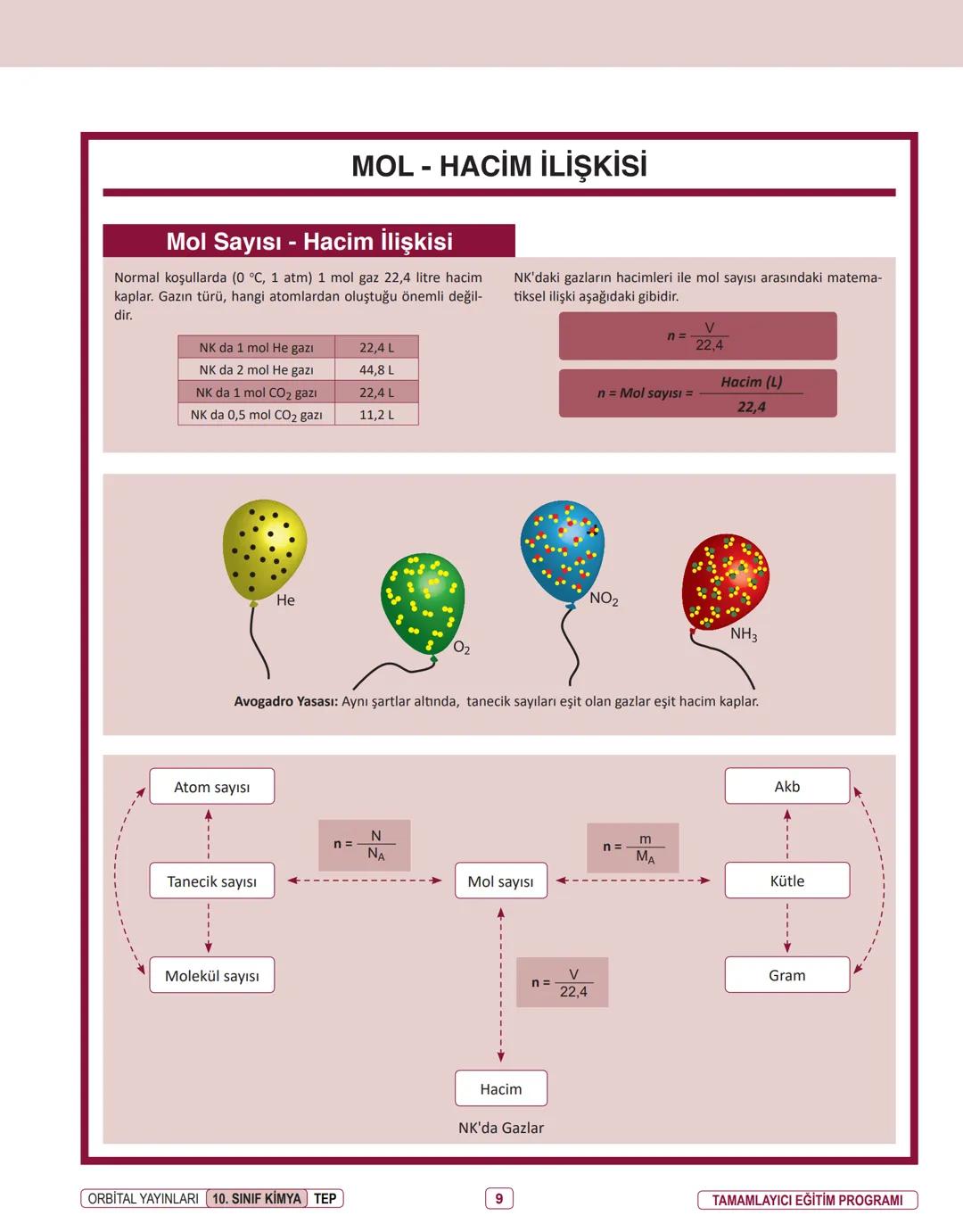
Normal koşullarda (0°C, 1 atm) 1 mol gaz 22,4 litre hacim kaplar. Bu özellik bütün gazlar için geçerlidir, gazın türü veya hangi atomlardan oluştuğu önemli değildir.
Örneğin:
- NK'da 1 mol He gazı = 22,4 L
- NK'da 2 mol He gazı = 44,8 L
- NK'da 0,5 mol CO₂ gazı = 11,2 L
Normal koşullardaki gazların hacimleri ile mol sayısı arasındaki matematiksel ilişki:
n = V/22,4
Burada:
- n = Mol sayısı
- V = Hacim (L)
- 22,4 = 1 mol gazın NK'daki hacmi (L)
Bu ilişki, Avogadro Yasası ile de ilgilidir: Aynı şartlar altında, tanecik sayıları eşit olan gazlar eşit hacim kaplar.
Kimyada mol kavramını anlamak, farklı birimler arasında geçiş yapabilmenizi sağlar:
- Tanecik sayısı ↔ Mol sayısı: n = N/N₀
- Kütle ↔ Mol sayısı: n = m/MA
- Hacim ↔ Mol sayısı: n = V/22,4
Unutma: Normal koşullarda gazların türü ne olursa olsun, 1 mol her zaman 22,4 L hacim kaplar. Bu, gaz hesaplamalarında kolaylık sağlayan önemli bir bilgidir.

Kimyasal Tepkimeler ve Denklemler
Kimyasal tepkime, bir veya birkaç saf maddenin belirli koşullarda kimyasal değişime uğrayarak başka maddelere dönüşmesidir. Bu tepkimelere genellikle enerji değişimleri eşlik eder.
Kimyasal tepkimelerde değişmeyen özellikler şunlardır:
- Toplam atom sayısı ve cinsi
- Toplam tanecik sayısı (proton, nötron, elektron)
- Çekirdek kütlesi
- Toplam kütle
- Toplam elektriksel yük
- Toplam enerji
Değişebilen özellikler ise:
- Atom hacmi veya çapı
- Atomların elektron sayıları ve dizilişleri
- Toplam potansiyel enerji
- Maddelerin fiziksel ve kimyasal özellikleri
- Toplam mol sayısı, molekül sayısı ve hacim
Kimyasal Tepkime Türleri:
-
Sentez Tepkimeleri: İki veya daha fazla maddenin birleşerek yeni bir bileşik oluşturması.
A + B → ABÖrneğin: C + O₂ → CO₂
-
Ayrışma (Analiz) Tepkimeleri: Bir bileşiğin daha basit maddelere ayrılması.
AB → A + BÖrneğin: 2KClO₃ → 2KCl + 3O₂
Kimyasal Denklem Yazarken: Tepkime okunun solundaki maddeler girenler, sağındakiler ise ürünlerdir. Maddelerin fiziksel halleri parantez içine yazılır: gaz için (g), sıvı için (s), katı için (k), suda çözünmüş maddeler için (suda) veya (aq) ifadeleri kullanılır.
Kimyasal Tepkime Türleri ve Denkleştirme
Kimyasal tepkimeleri daha iyi anlamak için, farklı tepkime türlerini bilmek ve denklemleri doğru yazmak önemlidir.
Yanma Tepkimeleri: Bir maddenin oksijen (O₂) ile verdiği tepkimedir. Metaller, ametaller veya bileşikler yanma tepkimesi verebilir.
- Metal yanması: 2Fe(k) + 3/2O₂(g) → Fe₂O₃(k)
- Ametal yanması: C(k) + O₂(g) → CO₂(g)
- Bileşik yanması: CH₄(g) + 2O₂(g) → CO₂(g) + 2H₂O(g)
Yanma tepkimesi için üç şart gereklidir: oksijen, yanacak madde ve tutuşma sıcaklığı. Azot gazının yanması hariç, tüm yanma tepkimeleri ısı açığa çıkarır (ekzotermik).
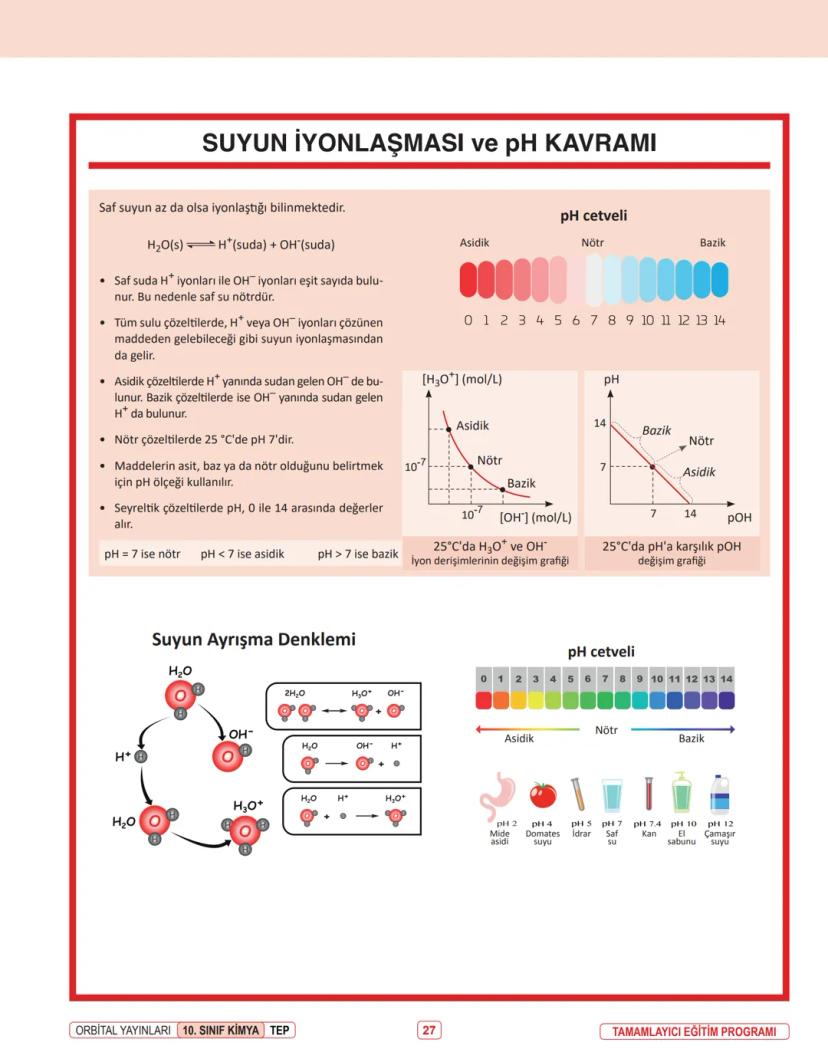
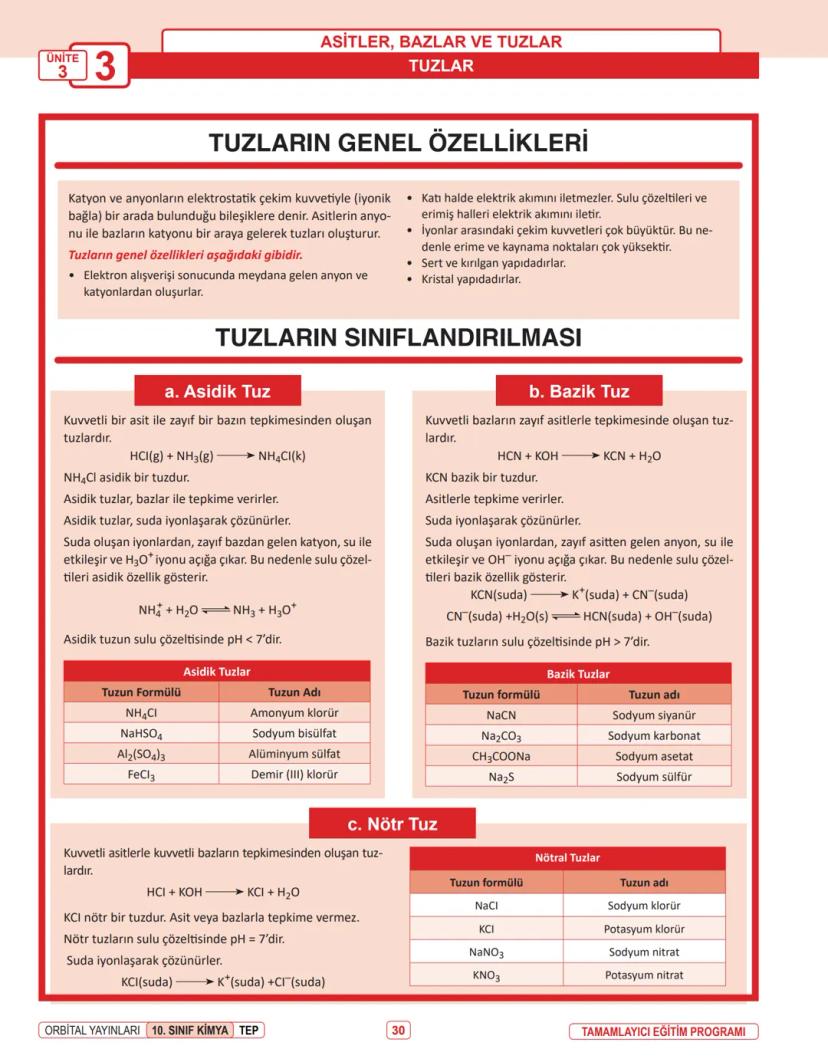
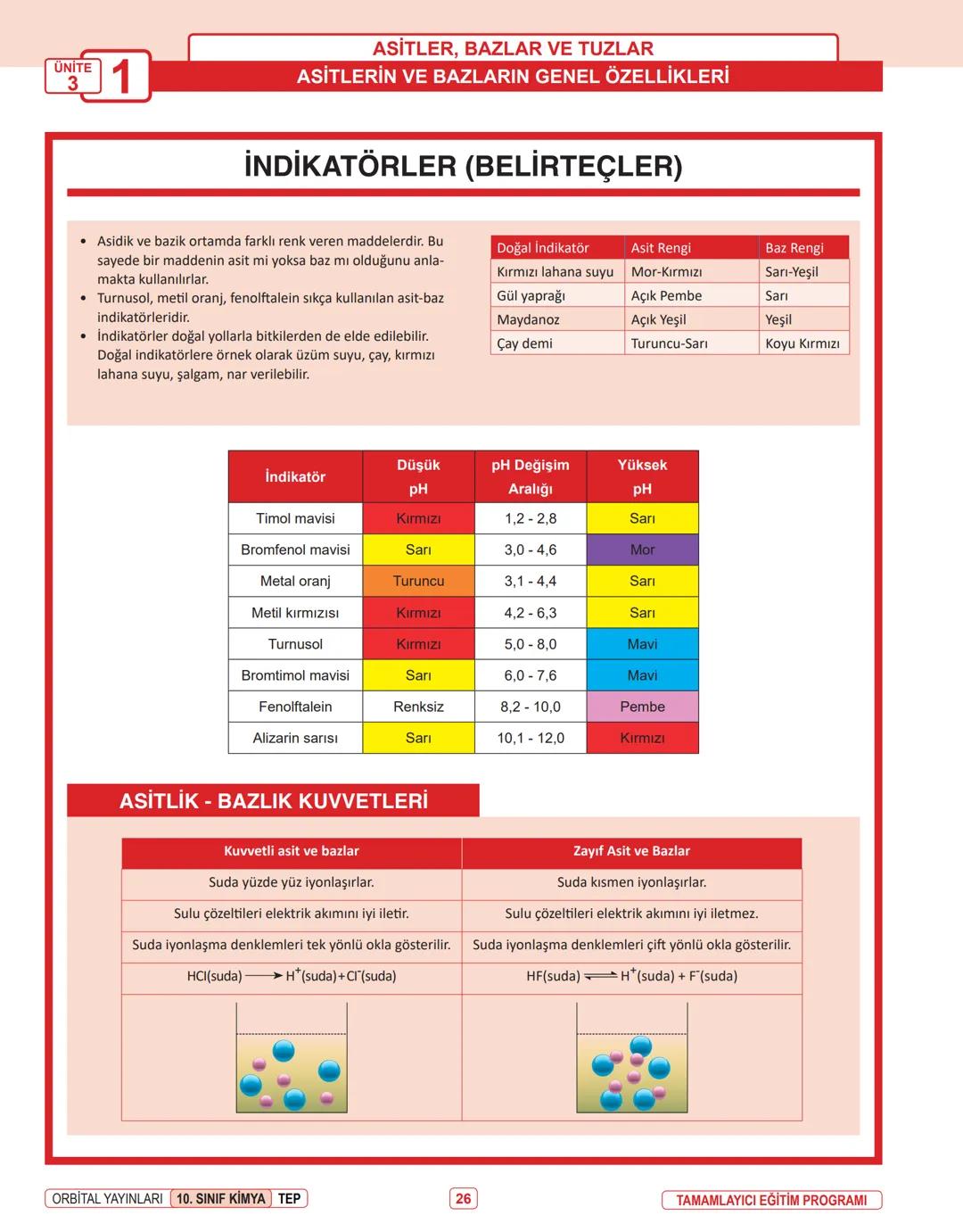
Asit-Baz Tepkimeleri: Asitler H⁺ iyonu verirken, bazlar OH⁻ iyonu verir. Bir asit ile baz karşılaştığında, H⁺ ve OH⁻ iyonları birleşerek su oluşturur ve geriye tuz kalır.
Asit + Baz → Tuz + Su
Örnek: HNO₃ + NaOH → NaNO₃ + H₂O
Çözünme-Çökelme Tepkimeleri: Suda iyi çözünen iki farklı tuzun çözeltileri karıştırıldığında, suda az çözünen yeni bir tuz oluşabilir.
AgNO₃(suda) + NaCl(suda) → AgCl(k) + NaNO₃(suda)
Net İyon Denklemi: Çökelme tepkimelerinde, çözeltide kalan iyonlar "seyirci iyonlar" olarak adlandırılır. Gerçekte tepkimeye giren iyonlar arasındaki denkleme "net iyon denklemi" denir. Örneğin: Ag⁺(suda) + Cl⁻(suda) → AgCl(k)

Verim ve Yüzde Problemleri
Kimyasal tepkimelerde gerçek hayatta karşılaştığımız önemli konulardan biri de verim hesaplamalarıdır. Tepkimeler her zaman %100 verimle gerçekleşmez.
Bir tepkimenin % verimi şu formülle hesaplanır:
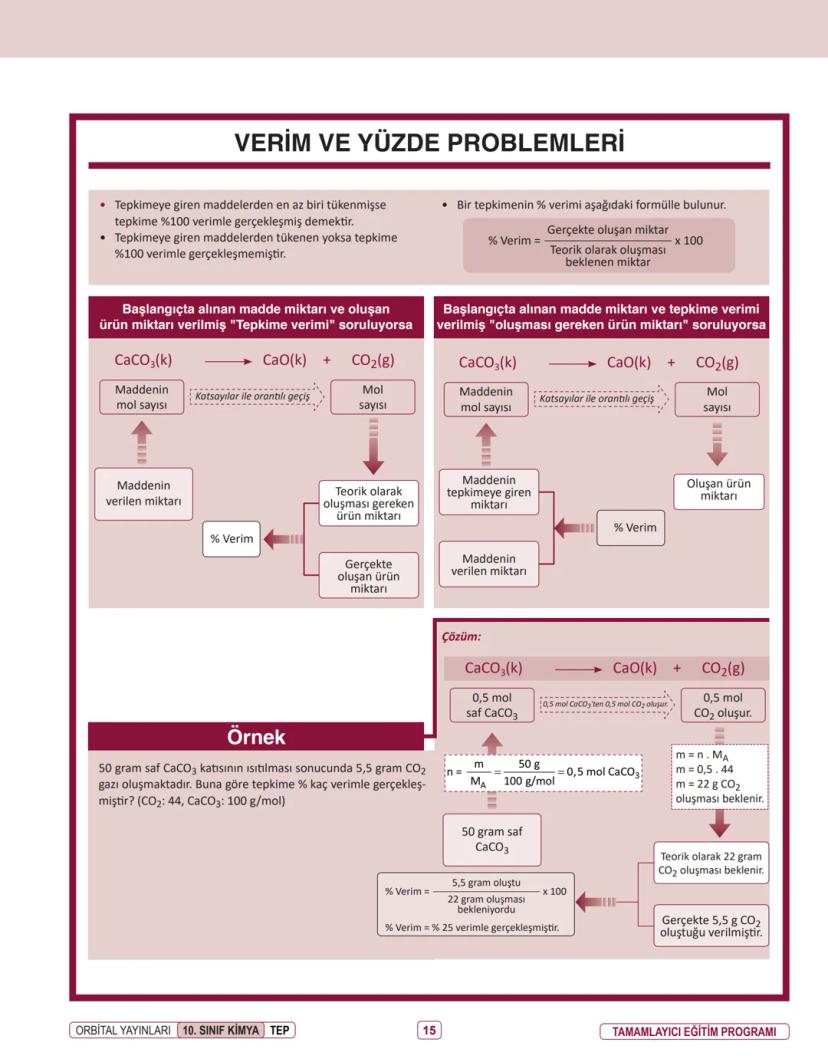
% Verim = (Gerçekte oluşan miktar / Teorik olarak oluşması beklenen miktar) × 100
Tepkimeye giren maddelerden en az biri tükenmişse, tepkime %100 verimle gerçekleşmiş demektir. Ancak tepkimeye giren maddelerden hiçbiri tükenmemişse, tepkime %100 verimle gerçekleşmemiştir.
Bir örnek üzerinden anlamaya çalışalım:
50 gram saf CaCO₃ kütlesinin ısıtılması sonucunda 5,5 gram CO₂ gazı oluşmaktadır. Tepkime % kaç verimle gerçekleşmiştir?
Çözüm:
- Tepkime denklemini yazalım: CaCO₃(k) → CaO(k) + CO₂(g)
- 50 g CaCO₃'ün mol sayısını bulalım: n = m/MA = 50/100 = 0,5 mol CaCO₃
- Teorik olarak oluşması beklenen CO₂ miktarını hesaplayalım: 0,5 mol CaCO₃'ten 0,5 mol CO₂ oluşur. m = n × MA = 0,5 × 44 = 22 g CO₂ oluşması beklenir.
- Gerçekte oluşan miktar 5,5 g CO₂ olduğu için: % Verim = (5,5/22) × 100 = %25
Yani tepkime %25 verimle gerçekleşmiştir.
İpucu: Verim hesaplamalarında önce tepkimeyi yazın, sonra mol sayılarını bulun, daha sonra katsayılara göre oluşması beklenen ürün miktarını hesaplayın ve son olarak gerçekte oluşan miktarla karşılaştırın.

Mol Kütlesi Bulma Problemleri
Kimyasal tepkimelerde bilinmeyen maddelerin mol kütlesini bulabilmek, kimya problemlerini çözmenin önemli bir parçasıdır.
Mol kütlesi bilinmeyen bir maddenin mol kütlesini (MA) bulmak için, o maddeye ait bir mol sayısı (n) ve kütle (m) değerine ihtiyacımız vardır. Bu değerler kullanılarak:
n = m/MA
formülünden MA çözülebilir.
Örnek bir problem çözerek konuyu daha iyi anlayalım:
XO + 2HCl → XCl₂ + H₂O denklemine göre 16 gram XO'nun yeterli miktardaki HCl ile tepkimesinden 7,2 gram H₂O oluşmaktadır. Buna göre, X elementinin mol kütlesi kaç gram/mol'dür?
Çözüm:
- Tepkime denklemine göre 1 mol XO'dan 1 mol H₂O oluşur.
- Oluşan H₂O'nun mol sayısını bulalım: n(H₂O) = m/MA = 7,2/18 = 0,4 mol
- Tepkimeye giren XO'nun mol sayısı da 0,4 mol olmalıdır.
- XO'nun mol kütlesini bulalım: n = m/MA → 0,4 = 16/MA → MA = 16/0,4 = 40 g/mol
- XO'nun mol kütlesi 40 g/mol olduğuna göre: X + 16 = 40 → X = 24 g/mol
X elementinin mol kütlesi 24 g/mol'dür.
Formül Bulma: Bir bileşiğin formülünü bulmak için önce kaba (basit) formül bulunur. Bunun için bileşiği oluşturan elementlerin mol sayıları belirlenir ve en küçük tam sayı oranlarına dönüştürülür. Gerçek formül için ise mol kütlesi ya da toplam atom sayısı bilgisi gereklidir.

Karışımlar
Karışımlar, günlük hayatımızda sıkça karşılaştığımız maddelerdir. İki veya daha fazla maddenin, kendi özelliklerini kaybetmeden bir araya gelmesiyle oluşan sistemlere karışım denir.
Karışımların Özellikleri:
- Homojen veya heterojen olabilirler
- Sabit bir erime, kaynama, donma noktaları ve özkütleleri yoktur
- Belirli bir sembol ya da formülleri yoktur
- Fiziksel yöntemlerle bileşenlerine ayrılırlar
- Bileşenler arasında belirli bir kütle oranı yoktur
Karışımların Sınıflandırılması:
-
Homojen Karışımlar (Çözeltiler):
- Bileşim ve fiziksel özellikleri her noktasında aynı
- Tanecik boyutu 10⁻⁹ m'den küçük
- Örnek: Tuzlu su, kolonya, hava
- Çözücü ve çözünenden oluşur (şekerli suda su çözücü, şeker çözünendir)
-
Kolloidler:
- Çıplak gözle homojen görünür ancak mikroskopla bakıldığında heterojen
- Tanecik boyutu 10⁻⁹ m ile 10⁻⁶ m arasında
- Örnek: Süt, jöle, kan
-
Heterojen Karışımlar:
- Her noktasında farklı özellik gösteren karışımlar
- Tanecik boyutu 10⁻⁶ m'den büyük
- Örnek: Tebeşir tozu-su, zeytinyağı-su
Karışım Çeşitleri: Heterojen karışımların kendi içinde türleri vardır. Süspansiyon , emülsiyon ve aerosol bunlardan bazılarıdır.





















Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Nanoparticles
2Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
10. Sınıf Kimya Konuları ve Ders Notları
Kimya dersinin temel konularını öğrenmek, çevremizdeki maddeleri ve günlük hayatta karşılaştığımız olayları anlamamıza yardımcı olur. Kimyanın temel kanunlarından başlayarak, asitler, bazlar, karışımlar ve günlük hayatta kullandığımız kimyasallar hakkında bilgi edinmek, dünyayı daha iyi anlamamızı sağlar.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Kimyanın Temel Kanunları ve Kimyasal Hesaplamalar
Kimya, maddelerin yapısını, özelliklerini ve birbirleriyle etkileşimlerini inceleyen bilim dalıdır. Bu derste maddelerin davranışlarını anlamamızı sağlayan temel kanunları öğreneceğiz.
Kütlenin korunumu yasası, kimyanın en temel kanunlarından biridir. Bu yasaya göre bir kimyasal tepkimede, giren maddelerin kütleleri toplamı, oluşan ürünlerin kütleleri toplamına eşittir. Yani madde yoktan var olmaz, var olan da yok olmaz.
Antoine Lavoisier 1774'te bu yasayı keşfetmiştir. Kalay ve havanın bulunduğu kapalı bir kapta, kalayın oksitlenmesi sonucu kütlede değişim olmadığını gözlemlemiştir.
Önemli Not: Kimyasal tepkimelerde atomlar yok olmaz, sadece yeniden düzenlenirler. Bu nedenle kütle her zaman korunur.
Tepkimelerde kütlenin korunduğunu şu örnekle görebiliriz:
CaCl₂ + Na₂SO₄ → CaSO₄ + NaCl
Girenlerin kütlesi = 184,34 g = Ürünlerin kütlesi

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Sabit Oranlar Yasası
Maddelerin davranışlarını anlamak için bilmeniz gereken bir başka temel yasa da sabit oranlar yasasıdır. Bu yasa, 1799'da Joseph Proust tarafından ortaya atılmıştır.
Sabit oranlar yasasına göre bir bileşiği oluşturan elementler her zaman sabit bir kütle oranında birleşirler. Örneğin, karbondioksit (CO₂) molekülünde karbon ve oksijenin kütlece birleşme oranı daima 3/8'dir.
Bileşiklerde elementlerin kütlece yüzdeleri ve atom sayıları arasındaki oran sabittir. Ancak dikkat edin, kütlece birleşme oranı ile sayıca birleşme oranı farklıdır. CO₂'de karbon ve oksijenin sayıca oranı 1/2 iken, kütlece oranı 3/8'dir.
Bu yasayı MgO örneğiyle daha iyi anlayabilirsiniz. Farklı miktarlarda magnezyum ve oksijen kullanılarak MgO oluşturulduğunda, oluşan bileşiğin kütlesi değişir ancak Mg/O kütlece birleşme oranı her zaman 3/2'dir.
| Mg kütlesi | O kütlesi | MgO kütlesi | Mg/O oranı |
|---|---|---|---|
| 3 g | 2 g | 5 g | 3/2 |
| 6 g | 4 g | 10 g | 3/2 |
| 24 g | 16 g | 40 g | 3/2 |
Hatırlatma: Elementler sabit oran dışında tepkimeye girdiklerinde, bir element bittiğinde tepkime durur ve diğer elementten artar. Örneğin 3 g Mg ve 3 g O kullanırsak, 3 g Mg ile 2 g O tepkimeye girer ve 1 g O artar.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Mol Tanecik Sayısı İlişkisi
Kimyada sıkça karşılaşacağımız bir kavram olan "mol", çok küçük tanecikler için kullanılan bir grup adıdır. Latince "büyük yığın" anlamına gelir.
Nasıl ki 1 düzine 12 tane, 1 deste 10 tane anlamına geliyorsa, 1 mol de 6,02x10²³ tane anlamına gelir. Bu sayı Avogadro sayısı olarak bilinir ve kısaca N₀ veya N₍A₎ ile gösterilir.
1 mol tanecik her zaman 6,02x10²³ taneye eşittir. Örneğin:
- 1 mol Fe elementi 6,02x10²³ tane Fe atomundan
- 2 mol He elementi 12,04x10²³ tane He atomundan
- 1 mol H₂O bileşiği 6,02x10²³ tane H₂O molekülünden oluşur
Tanecik sayısı (N) ile mol sayısı (n) arasındaki matematiksel ilişki şu şekildedir:
n = N/N₀
Burada:
- n = Mol sayısı
- N = Tanecik sayısı
- N₀ = Avogadro sayısı
İyi Anla: 1 molekül CO₂, 1 tane CO₂ molekülü demektir. 1 mol CO₂ ise 6,02x10²³ tane CO₂ molekülü anlamına gelir. Bu farkı anlamak, kimyasal hesaplamalarda başarılı olmanın anahtarıdır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Mol Kütle İlişkisi
Mol kavramı anlaşıldıktan sonra, molün kütleyle ilişkisini de bilmeniz gerekir. Bu ilişki kimyasal hesaplamalar yapmanıza yardımcı olacak.
Bir elementin 1 mol atomu, gram türünden ne kadar kütle gelir? Bu değere o elementin mol kütlesi (atom kütlesi, MA) denir. Örneğin, Helyum (He) elementinin mol kütlesi 4 g/mol'dür. Bu şu anlama gelir:
- 1 mol He elementi = 4 gram
- 2 mol He elementi = 8 gram
- 0,2 mol He elementi = 0,8 gram
Elementlerin atom kütleleri konusunda merak etmeyin, bunlar genellikle sorularda verilecektir, ezberlemenize gerek yoktur.
Bağıl Atom Kütlesi kavramını da öğrenelim. 1 tane ¹²C izotopunun kütlesinin 1/12'sine 1 atomik kütle birimi (1 akb) denir. Akb, gram veya kg gibi bir kütle birimidir, ancak onlardan çok daha küçüktür.
Kütle ile mol sayısı arasındaki matematiksel ilişki şu formülle gösterilir:
n = m/MA
Burada:
- n = Mol sayısı
- m = Kütle (g)
- MA = Mol kütlesi
Pratik Bilgi: Bir bileşiğin mol kütlesi, onu oluşturan elementlerin atom kütlelerinin toplamına eşittir. Örneğin, 1 mol H₂O bileşiği = (2×1) + 16 = 18 gram eder .

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Mol - Hacim İlişkisi
Kimyada gazlarla çalışırken, mol sayısı ile gazların hacmi arasındaki ilişkiyi bilmek çok önemlidir.
Normal koşullarda (0°C, 1 atm) 1 mol gaz 22,4 litre hacim kaplar. Bu özellik bütün gazlar için geçerlidir, gazın türü veya hangi atomlardan oluştuğu önemli değildir.
Örneğin:
- NK'da 1 mol He gazı = 22,4 L
- NK'da 2 mol He gazı = 44,8 L
- NK'da 0,5 mol CO₂ gazı = 11,2 L
Normal koşullardaki gazların hacimleri ile mol sayısı arasındaki matematiksel ilişki:
n = V/22,4
Burada:
- n = Mol sayısı
- V = Hacim (L)
- 22,4 = 1 mol gazın NK'daki hacmi (L)
Bu ilişki, Avogadro Yasası ile de ilgilidir: Aynı şartlar altında, tanecik sayıları eşit olan gazlar eşit hacim kaplar.
Kimyada mol kavramını anlamak, farklı birimler arasında geçiş yapabilmenizi sağlar:
- Tanecik sayısı ↔ Mol sayısı: n = N/N₀
- Kütle ↔ Mol sayısı: n = m/MA
- Hacim ↔ Mol sayısı: n = V/22,4
Unutma: Normal koşullarda gazların türü ne olursa olsun, 1 mol her zaman 22,4 L hacim kaplar. Bu, gaz hesaplamalarında kolaylık sağlayan önemli bir bilgidir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Kimyasal Tepkimeler ve Denklemler
Kimyasal tepkime, bir veya birkaç saf maddenin belirli koşullarda kimyasal değişime uğrayarak başka maddelere dönüşmesidir. Bu tepkimelere genellikle enerji değişimleri eşlik eder.
Kimyasal tepkimelerde değişmeyen özellikler şunlardır:
- Toplam atom sayısı ve cinsi
- Toplam tanecik sayısı (proton, nötron, elektron)
- Çekirdek kütlesi
- Toplam kütle
- Toplam elektriksel yük
- Toplam enerji
Değişebilen özellikler ise:
- Atom hacmi veya çapı
- Atomların elektron sayıları ve dizilişleri
- Toplam potansiyel enerji
- Maddelerin fiziksel ve kimyasal özellikleri
- Toplam mol sayısı, molekül sayısı ve hacim
Kimyasal Tepkime Türleri:
-
Sentez Tepkimeleri: İki veya daha fazla maddenin birleşerek yeni bir bileşik oluşturması.
A + B → ABÖrneğin: C + O₂ → CO₂
-
Ayrışma (Analiz) Tepkimeleri: Bir bileşiğin daha basit maddelere ayrılması.
AB → A + BÖrneğin: 2KClO₃ → 2KCl + 3O₂
Kimyasal Denklem Yazarken: Tepkime okunun solundaki maddeler girenler, sağındakiler ise ürünlerdir. Maddelerin fiziksel halleri parantez içine yazılır: gaz için (g), sıvı için (s), katı için (k), suda çözünmüş maddeler için (suda) veya (aq) ifadeleri kullanılır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Kimyasal Tepkime Türleri ve Denkleştirme
Kimyasal tepkimeleri daha iyi anlamak için, farklı tepkime türlerini bilmek ve denklemleri doğru yazmak önemlidir.
Yanma Tepkimeleri: Bir maddenin oksijen (O₂) ile verdiği tepkimedir. Metaller, ametaller veya bileşikler yanma tepkimesi verebilir.
- Metal yanması: 2Fe(k) + 3/2O₂(g) → Fe₂O₃(k)
- Ametal yanması: C(k) + O₂(g) → CO₂(g)
- Bileşik yanması: CH₄(g) + 2O₂(g) → CO₂(g) + 2H₂O(g)
Yanma tepkimesi için üç şart gereklidir: oksijen, yanacak madde ve tutuşma sıcaklığı. Azot gazının yanması hariç, tüm yanma tepkimeleri ısı açığa çıkarır (ekzotermik).
Asit-Baz Tepkimeleri: Asitler H⁺ iyonu verirken, bazlar OH⁻ iyonu verir. Bir asit ile baz karşılaştığında, H⁺ ve OH⁻ iyonları birleşerek su oluşturur ve geriye tuz kalır.
Asit + Baz → Tuz + Su
Örnek: HNO₃ + NaOH → NaNO₃ + H₂O
Çözünme-Çökelme Tepkimeleri: Suda iyi çözünen iki farklı tuzun çözeltileri karıştırıldığında, suda az çözünen yeni bir tuz oluşabilir.
AgNO₃(suda) + NaCl(suda) → AgCl(k) + NaNO₃(suda)
Net İyon Denklemi: Çökelme tepkimelerinde, çözeltide kalan iyonlar "seyirci iyonlar" olarak adlandırılır. Gerçekte tepkimeye giren iyonlar arasındaki denkleme "net iyon denklemi" denir. Örneğin: Ag⁺(suda) + Cl⁻(suda) → AgCl(k)

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Verim ve Yüzde Problemleri
Kimyasal tepkimelerde gerçek hayatta karşılaştığımız önemli konulardan biri de verim hesaplamalarıdır. Tepkimeler her zaman %100 verimle gerçekleşmez.
Bir tepkimenin % verimi şu formülle hesaplanır:
% Verim = (Gerçekte oluşan miktar / Teorik olarak oluşması beklenen miktar) × 100
Tepkimeye giren maddelerden en az biri tükenmişse, tepkime %100 verimle gerçekleşmiş demektir. Ancak tepkimeye giren maddelerden hiçbiri tükenmemişse, tepkime %100 verimle gerçekleşmemiştir.
Bir örnek üzerinden anlamaya çalışalım:
50 gram saf CaCO₃ kütlesinin ısıtılması sonucunda 5,5 gram CO₂ gazı oluşmaktadır. Tepkime % kaç verimle gerçekleşmiştir?
Çözüm:
- Tepkime denklemini yazalım: CaCO₃(k) → CaO(k) + CO₂(g)
- 50 g CaCO₃'ün mol sayısını bulalım: n = m/MA = 50/100 = 0,5 mol CaCO₃
- Teorik olarak oluşması beklenen CO₂ miktarını hesaplayalım: 0,5 mol CaCO₃'ten 0,5 mol CO₂ oluşur. m = n × MA = 0,5 × 44 = 22 g CO₂ oluşması beklenir.
- Gerçekte oluşan miktar 5,5 g CO₂ olduğu için: % Verim = (5,5/22) × 100 = %25
Yani tepkime %25 verimle gerçekleşmiştir.
İpucu: Verim hesaplamalarında önce tepkimeyi yazın, sonra mol sayılarını bulun, daha sonra katsayılara göre oluşması beklenen ürün miktarını hesaplayın ve son olarak gerçekte oluşan miktarla karşılaştırın.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Mol Kütlesi Bulma Problemleri
Kimyasal tepkimelerde bilinmeyen maddelerin mol kütlesini bulabilmek, kimya problemlerini çözmenin önemli bir parçasıdır.
Mol kütlesi bilinmeyen bir maddenin mol kütlesini (MA) bulmak için, o maddeye ait bir mol sayısı (n) ve kütle (m) değerine ihtiyacımız vardır. Bu değerler kullanılarak:
n = m/MA
formülünden MA çözülebilir.
Örnek bir problem çözerek konuyu daha iyi anlayalım:
XO + 2HCl → XCl₂ + H₂O denklemine göre 16 gram XO'nun yeterli miktardaki HCl ile tepkimesinden 7,2 gram H₂O oluşmaktadır. Buna göre, X elementinin mol kütlesi kaç gram/mol'dür?
Çözüm:
- Tepkime denklemine göre 1 mol XO'dan 1 mol H₂O oluşur.
- Oluşan H₂O'nun mol sayısını bulalım: n(H₂O) = m/MA = 7,2/18 = 0,4 mol
- Tepkimeye giren XO'nun mol sayısı da 0,4 mol olmalıdır.
- XO'nun mol kütlesini bulalım: n = m/MA → 0,4 = 16/MA → MA = 16/0,4 = 40 g/mol
- XO'nun mol kütlesi 40 g/mol olduğuna göre: X + 16 = 40 → X = 24 g/mol
X elementinin mol kütlesi 24 g/mol'dür.
Formül Bulma: Bir bileşiğin formülünü bulmak için önce kaba (basit) formül bulunur. Bunun için bileşiği oluşturan elementlerin mol sayıları belirlenir ve en küçük tam sayı oranlarına dönüştürülür. Gerçek formül için ise mol kütlesi ya da toplam atom sayısı bilgisi gereklidir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Karışımlar
Karışımlar, günlük hayatımızda sıkça karşılaştığımız maddelerdir. İki veya daha fazla maddenin, kendi özelliklerini kaybetmeden bir araya gelmesiyle oluşan sistemlere karışım denir.
Karışımların Özellikleri:
- Homojen veya heterojen olabilirler
- Sabit bir erime, kaynama, donma noktaları ve özkütleleri yoktur
- Belirli bir sembol ya da formülleri yoktur
- Fiziksel yöntemlerle bileşenlerine ayrılırlar
- Bileşenler arasında belirli bir kütle oranı yoktur
Karışımların Sınıflandırılması:
-
Homojen Karışımlar (Çözeltiler):
- Bileşim ve fiziksel özellikleri her noktasında aynı
- Tanecik boyutu 10⁻⁹ m'den küçük
- Örnek: Tuzlu su, kolonya, hava
- Çözücü ve çözünenden oluşur (şekerli suda su çözücü, şeker çözünendir)
-
Kolloidler:
- Çıplak gözle homojen görünür ancak mikroskopla bakıldığında heterojen
- Tanecik boyutu 10⁻⁹ m ile 10⁻⁶ m arasında
- Örnek: Süt, jöle, kan
-
Heterojen Karışımlar:
- Her noktasında farklı özellik gösteren karışımlar
- Tanecik boyutu 10⁻⁶ m'den büyük
- Örnek: Tebeşir tozu-su, zeytinyağı-su
Karışım Çeşitleri: Heterojen karışımların kendi içinde türleri vardır. Süspansiyon , emülsiyon ve aerosol bunlardan bazılarıdır.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Nanoparticles
2Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅