Kimya dersinde mol kavramı, madde miktarlarını ölçmenin temel yoludur. Bu... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
497
•
Güncellendi May 15, 2026
•
Yağmur Tunç
@yamurtun_x40b1
Kimya dersinde mol kavramı, madde miktarlarını ölçmenin temel yoludur. Bu... Daha fazla göster

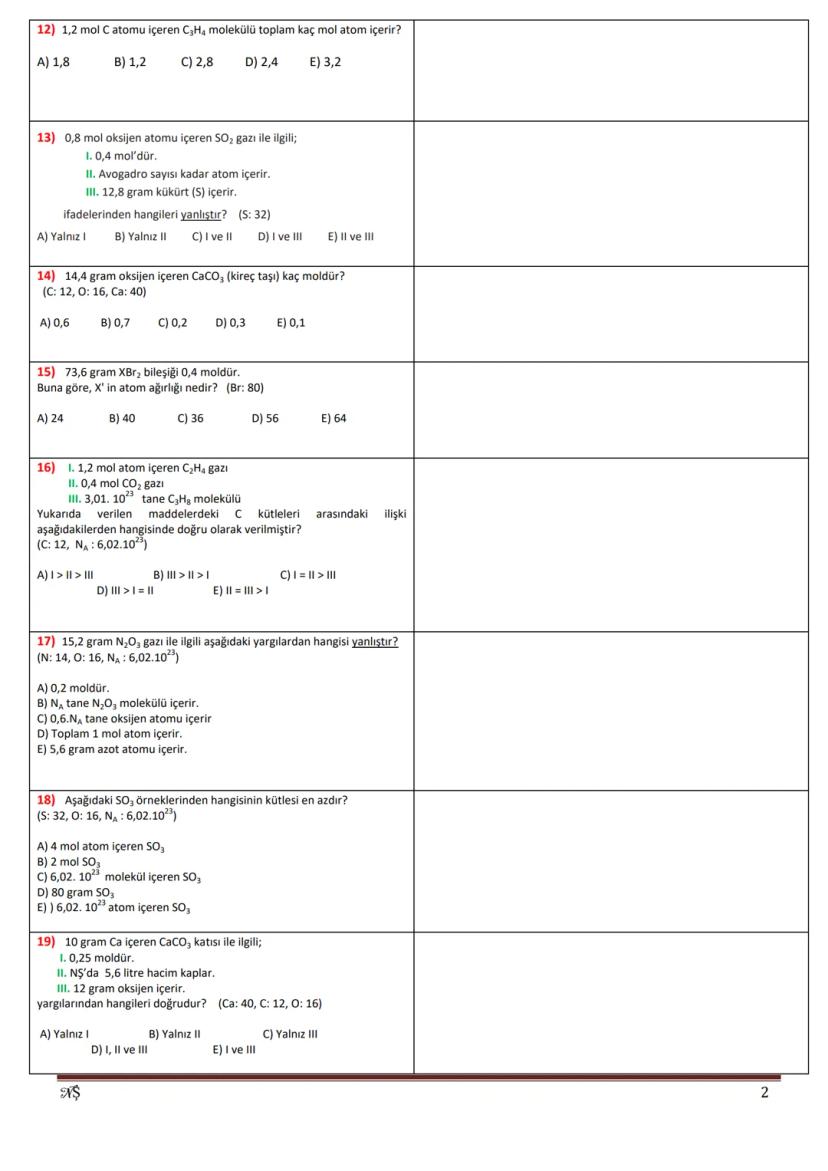





Mol hesaplamalarını yaparken bir maddenin mol sayısını bulmak için kütlesini molekül ağırlığına bölmemiz gerekir. Örneğin, 19,6 gram H₂SO₄'ün mol sayısını bulmak için önce molekül ağırlığını hesaplamamız gerekir: (2×1) + (1×32) + (4×16) = 98 g/mol. Böylece 19,6 g / 98 g/mol = 0,2 mol bulunur.
Bir molekülün kütlesini hesaplamak istediğimizde ise mol sayısını molekül ağırlığı ile çarpmalıyız. Örneğin 0,4 mol SO₃ gazının kütlesi: 0,4 mol × 80 g/mol = 32 gram olur.
Mol sayısı ile molekül sayısı arasındaki ilişkiyi Avogadro sayısı (6,02×10²³) ile kurarız. Örneğin 0,5 mol N₂O₅ molekülü içindeki molekül sayısı: 0,5 mol × 6,02×10²³ molekül/mol = 3,01×10²³ moleküldür.
Hatırla! Normal şartlarda (NŞ) her gaz 1 mol = 22,4 litre hacim kaplar. Bu yüzden 8,96 litre SO₂ gazı, 8,96 ÷ 22,4 = 0,4 mol demektir.
Bir bileşikte belirli bir atom türünün mol sayısını hesaplamak için formüldeki atom katsayılarına dikkat edilmelidir. Örneğin, 0,2 mol (NH₄)₂CO₃ bileşiğinde toplam atom sayısı: 0,2 × [(2×5) + (1×1) + (3×1)] × 6,02×10²³ = 16,8×10²² atomdur.
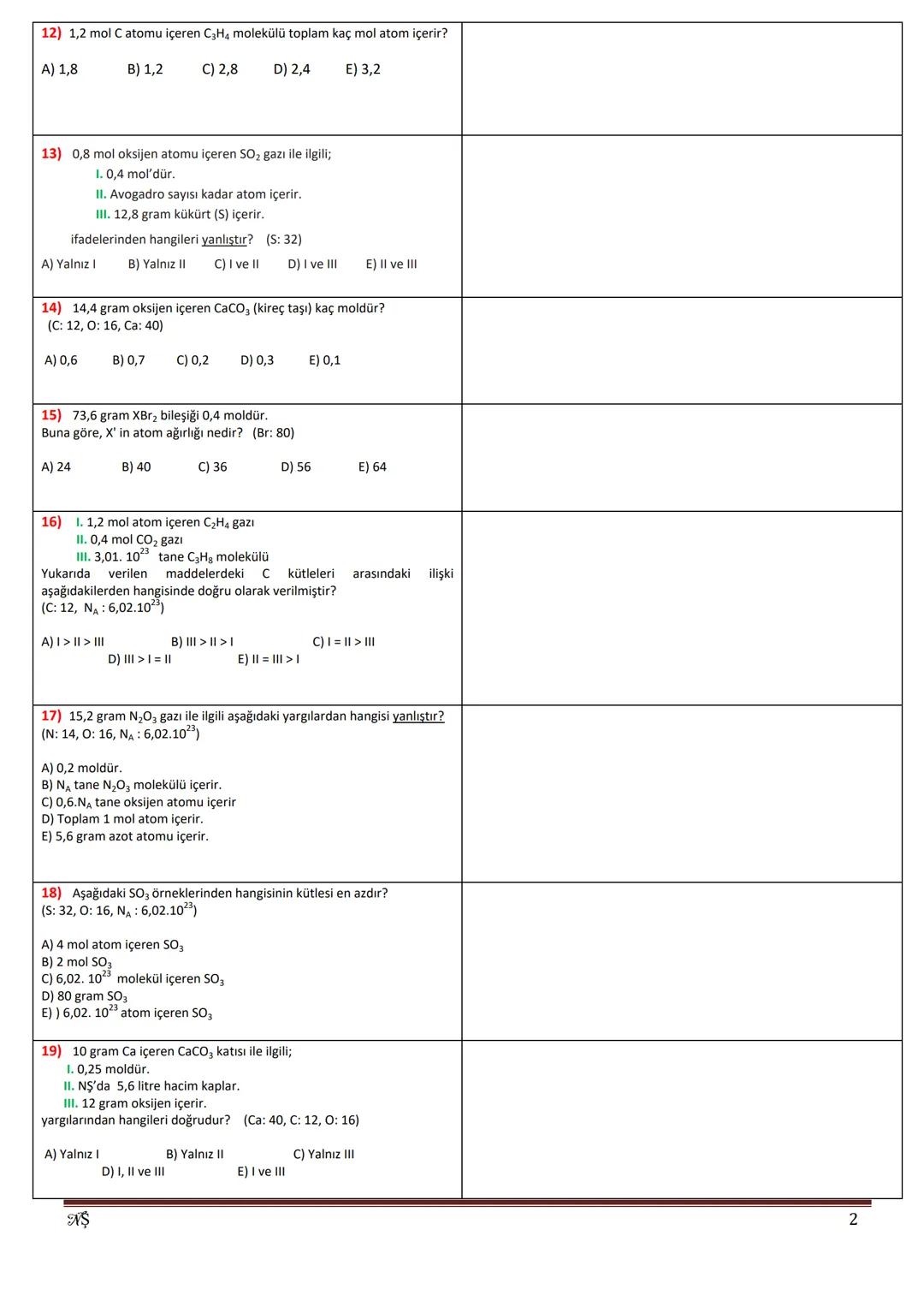
Bir bileşiğin içindeki toplam atom sayısını hesaplarken, bileşikteki her elementin mol sayısını Avogadro sayısıyla çarparız. Örneğin, 1,2 mol C atomu içeren C₃H₄ molekülünde toplam mol atomu: [(1,2 ÷ 3) × 3] + [(1,2 ÷ 3) × 4] = 1,2 + 1,6 = 2,8 mol atom bulunur.
Bir bileşikteki belirli bir atomun mol sayısını bulmak için, o atomun formüldeki katsayısını bileşiğin mol sayısıyla çarparız. Örneğin, 0,4 mol SO₃ gazında oksijen atomlarının mol sayısı: 0,4 × 3 = 1,2 mol olur.
Bir bileşiğin kütlesinden yola çıkarak mol sayısını bulmak için, bileşiğin molekül ağırlığını kullanırız. 73,6 gram XBr₄ bileşiği 0,4 mol olduğuna göre: 73,6 = 0,4 × → X = 24 g/mol bulunur.
İpucu: Maddelerin kütlelerini karşılaştırırken mol sayılarını ve molekül ağırlıklarını dikkate almalısın. Mol sayısı aynıysa, molekül ağırlığı büyük olan maddenin kütlesi daha büyük olur!
Bir bileşik içindeki elementlerin yüzde miktarlarını hesaplarken, o elementin kütlesini toplam bileşik kütlesine böleriz. Örneğin, 0,25 mol CaCO₃ katısında 10 gram Ca bulunur ve bu bileşik: 0,25 × [(40) + (12) + (3×16)] = 25 gram gelir.

Mol kavramı, maddenin tanecik sayısıyla kütlesi arasında köprü kurar. 3,01×10²³ tane CO₂ molekülü, Avogadro sayısının yarısı kadar tanecik içerdiğinden 0,5 mol demektir. 2,4 gram karbon içeren C₂H₄ gazında ise C atomunun mol sayısı: 2,4 ÷ 12 = 0,2 mol olur.
Atomik kütle ile moleküler kütle arasındaki fark önemlidir. 1 tane flor atomu ve 1 mol flor gazı (F₂) kıyaslandığında, 1 mol F₂ gazı (38 gram) en büyük kütleye sahiptir. Bu, Avogadro sayısı kadar F₂ molekülü içermesinden kaynaklanır.
Farklı bileşiklerdeki aynı elementin kütlesini hesaplamak için mol-kütle ilişkisini kullanırız. Örneğin, 0,25 mol X₃O₄ bileşiği 58 gram ise: 58 = 0,25 × → 3X = 168 → X = 56 g/mol bulunur.
Dikkat! Molekül formülündeki indisler (alt sayılar), o elementten kaç tane atom bulunduğunu gösterir. C₄H₈ molekülünün 0,2 molü, 0,2 × 4 = 0,8 mol C atomu ve 0,2 × 8 = 1,6 mol H atomu içerir.
Gazların normal şartlardaki hacimleriyle mol sayıları doğru orantılıdır. 0,5 mol C₂H₂ gazı, normal şartlarda 0,5 × 22,4 = 11,2 litre hacim kaplar. Mol sayılarını bildiğimizde, atomların toplam sayısını hesaplamak için formüldeki atom sayılarını toplayıp mol sayısıyla çarparız.

Gazların mol sayıları ile hacimleri arasında doğrudan bir ilişki vardır. Eşit sayıda oksijen atomu içeren NO, NO₂ ve N₂O₃ moleküllerini karşılaştırdığımızda, aynı sayıda oksijen atomu için gereken NO molekül sayısı daha fazla olacağından, normal şartlarda hacmi en büyük olan NO'dur.
Avogadro sayısı kavramı, moleküllerin sayısını anlamada çok önemlidir. 1,204×10²³ tane atom içeren SO₃ gazında, molekül sayısı atom sayısının 1/4'ü kadardır, yani 1,204×10²³ ÷ 4 = 3,01×10²² molekül bulunur. Bu da 0,05 moldür.
Bir maddenin bir gramında bulunan molekül sayısı, molekül ağırlığının tersine Avogadro sayısının çarpımıyla bulunur. Oksijen (O₂) için bu değer: N/32 moleküldür (N: Avogadro sayısı).
Önemli Not: Kimyasal formüller, bir bileşikteki elementlerin oranını gösterir. CH₃COOH gibi karmaşık bir formülde de toplam atom sayısını bulmak için tüm atomları saymalısın: 2C + 4H + 2O = 8 atom.
Moleküllerin kütleleri karşılaştırılırken, mol sayısı ve molekül ağırlığı birlikte düşünülmelidir. 0,2 mol O₂ molekülü 6,4 gram, 32 akb (atomik kütle birimi) oksijen ise sadece 32/N₁ gram (N₁: Avogadro sayısı) gelir. Bu yüzden 0,2 mol > 32 akb'dir.

Aynı koşullarda gazların hacimleri, mol sayılarıyla doğru orantılıdır. 20 gram neon gazı 1 mol, 32 gram oksijen gazı 1 mol ve 32 gram kükürt dioksit gazı 0,5 mol olduğundan, hacimleri Ne = O₂ > SO₂ şeklinde sıralanır.
Moleküllerin atom içeriğine göre hesaplamalar yapmak önemlidir. Avogadro sayısı kadar atom içerebilmesi için, bir gazın ya tek atomlu olması ya da Avogadro sayısı kadar molekül içermesi gerekir. 35 gram SF₂ bileşiği 0,5 mol olduğundan, 0,5 × 3 × N₁ = 1,5N₁ atom içerir.
Atom sayıları eşit olan O₂, O₃ ve CO gazlarını karşılaştırdığımızda, molekül başına düşen atom sayıları sırasıyla 2, 3 ve 2'dir. Eşit sayıda atom için gereken molekül sayıları ise O₂ = CO > O₃ şeklinde sıralanır.
Püf Noktası: Eşit kütlede maddelerin mol sayılarını karşılaştırırken, molekül ağırlığı küçük olanın mol sayısı daha büyüktür. Bu yüzden eşit kütlede O₂ ve O₃ gazlarından O₂'nin mol sayısı daha büyüktür.
Moleküller içindeki atomların sayısını hesaplarken, atom sayılarını toplayıp mol sayısıyla çarpmalıyız. 17 gram NH₃ (1 mol) 4N₁ atom, 11,2 litre C₂H₂ (0,5 mol) 2N₁ atom ve 1,806×10²³ tane Cl₂ (0,3 mol) 0,6N₁ atom içerdiğinden, atom sayıları sıralaması NH₃ > C₂H₂ > Cl₂ şeklindedir.

Farklı bileşiklerin içerdikleri toplam atom sayılarını karşılaştırabilmek için, formüldeki atom sayılarını toplayıp mol sayısıyla çarparız. 0,3 mol X bileşiğindeki atomların mol sayısı 0,75 mol Y bileşiğindeki atomların mol sayısına eşitse, X ve Y için uygun kombinasyon CH₄ ve CO olabilir. Çünkü 0,3 × 5 = 0,75 × 2 = 1,5 mol atom içerirler.
İki farklı bileşikteki aynı elementin miktarlarını eşitlemek için oran kurmalıyız. 0,4 mol N₂O₅ bileşiğinde 0,4 × 5 = 2 mol oksijen vardır. NO₂ bileşiğinde ise her molde 2 mol oksijen olduğundan, m = 46 gram NO₂ gerekir.
Atom ve moleküllerin kütle karşılaştırmaları yaparken ölçeklere dikkat etmeliyiz. 0,05 molekül-gram O₂, 0,05 atom-gram O, 1 tane O atomu ve 64 akb oksijen kütlelerinin doğru karşılaştırması: atom < akb < atom-gram < molekül-gram şeklindedir.
Formül Hatırlatması: Gazların normal şartlardaki hacimleri V = 22,4 × n (mol) ile bulunur. 4,48 litre hacimli SO₂ gazı 0,2 mol olup, 0,2 × 64 = 12,8 gram gelir.
Avogadro sayısı bir sabittir ve değiştirildiğinde bile bazı nicelikler etkilenmez. Eğer Avogadro sayısı değişseydi, H₂ gazının bağıl molekül kütlesi (2) değişmezdi, ancak 1 molünün gram olarak kütlesi ve normal şartlardaki hacmi değişirdi.
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Yağmur Tunç
@yamurtun_x40b1
Kimya dersinde mol kavramı, madde miktarlarını ölçmenin temel yoludur. Bu özette, mol hesaplamaları, atomlar ve moleküller arasındaki ilişkiler ve günlük hayatta kullandığımız kimyasal maddelerin mol hesaplamaları üzerinde durulacaktır. Mol kavramını anlamak, kimyasal tepkimelerin özünü anlamak demektir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Mol hesaplamalarını yaparken bir maddenin mol sayısını bulmak için kütlesini molekül ağırlığına bölmemiz gerekir. Örneğin, 19,6 gram H₂SO₄'ün mol sayısını bulmak için önce molekül ağırlığını hesaplamamız gerekir: (2×1) + (1×32) + (4×16) = 98 g/mol. Böylece 19,6 g / 98 g/mol = 0,2 mol bulunur.
Bir molekülün kütlesini hesaplamak istediğimizde ise mol sayısını molekül ağırlığı ile çarpmalıyız. Örneğin 0,4 mol SO₃ gazının kütlesi: 0,4 mol × 80 g/mol = 32 gram olur.
Mol sayısı ile molekül sayısı arasındaki ilişkiyi Avogadro sayısı (6,02×10²³) ile kurarız. Örneğin 0,5 mol N₂O₅ molekülü içindeki molekül sayısı: 0,5 mol × 6,02×10²³ molekül/mol = 3,01×10²³ moleküldür.
Hatırla! Normal şartlarda (NŞ) her gaz 1 mol = 22,4 litre hacim kaplar. Bu yüzden 8,96 litre SO₂ gazı, 8,96 ÷ 22,4 = 0,4 mol demektir.
Bir bileşikte belirli bir atom türünün mol sayısını hesaplamak için formüldeki atom katsayılarına dikkat edilmelidir. Örneğin, 0,2 mol (NH₄)₂CO₃ bileşiğinde toplam atom sayısı: 0,2 × [(2×5) + (1×1) + (3×1)] × 6,02×10²³ = 16,8×10²² atomdur.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bir bileşiğin içindeki toplam atom sayısını hesaplarken, bileşikteki her elementin mol sayısını Avogadro sayısıyla çarparız. Örneğin, 1,2 mol C atomu içeren C₃H₄ molekülünde toplam mol atomu: [(1,2 ÷ 3) × 3] + [(1,2 ÷ 3) × 4] = 1,2 + 1,6 = 2,8 mol atom bulunur.
Bir bileşikteki belirli bir atomun mol sayısını bulmak için, o atomun formüldeki katsayısını bileşiğin mol sayısıyla çarparız. Örneğin, 0,4 mol SO₃ gazında oksijen atomlarının mol sayısı: 0,4 × 3 = 1,2 mol olur.
Bir bileşiğin kütlesinden yola çıkarak mol sayısını bulmak için, bileşiğin molekül ağırlığını kullanırız. 73,6 gram XBr₄ bileşiği 0,4 mol olduğuna göre: 73,6 = 0,4 × → X = 24 g/mol bulunur.
İpucu: Maddelerin kütlelerini karşılaştırırken mol sayılarını ve molekül ağırlıklarını dikkate almalısın. Mol sayısı aynıysa, molekül ağırlığı büyük olan maddenin kütlesi daha büyük olur!
Bir bileşik içindeki elementlerin yüzde miktarlarını hesaplarken, o elementin kütlesini toplam bileşik kütlesine böleriz. Örneğin, 0,25 mol CaCO₃ katısında 10 gram Ca bulunur ve bu bileşik: 0,25 × [(40) + (12) + (3×16)] = 25 gram gelir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Mol kavramı, maddenin tanecik sayısıyla kütlesi arasında köprü kurar. 3,01×10²³ tane CO₂ molekülü, Avogadro sayısının yarısı kadar tanecik içerdiğinden 0,5 mol demektir. 2,4 gram karbon içeren C₂H₄ gazında ise C atomunun mol sayısı: 2,4 ÷ 12 = 0,2 mol olur.
Atomik kütle ile moleküler kütle arasındaki fark önemlidir. 1 tane flor atomu ve 1 mol flor gazı (F₂) kıyaslandığında, 1 mol F₂ gazı (38 gram) en büyük kütleye sahiptir. Bu, Avogadro sayısı kadar F₂ molekülü içermesinden kaynaklanır.
Farklı bileşiklerdeki aynı elementin kütlesini hesaplamak için mol-kütle ilişkisini kullanırız. Örneğin, 0,25 mol X₃O₄ bileşiği 58 gram ise: 58 = 0,25 × → 3X = 168 → X = 56 g/mol bulunur.
Dikkat! Molekül formülündeki indisler (alt sayılar), o elementten kaç tane atom bulunduğunu gösterir. C₄H₈ molekülünün 0,2 molü, 0,2 × 4 = 0,8 mol C atomu ve 0,2 × 8 = 1,6 mol H atomu içerir.
Gazların normal şartlardaki hacimleriyle mol sayıları doğru orantılıdır. 0,5 mol C₂H₂ gazı, normal şartlarda 0,5 × 22,4 = 11,2 litre hacim kaplar. Mol sayılarını bildiğimizde, atomların toplam sayısını hesaplamak için formüldeki atom sayılarını toplayıp mol sayısıyla çarparız.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Gazların mol sayıları ile hacimleri arasında doğrudan bir ilişki vardır. Eşit sayıda oksijen atomu içeren NO, NO₂ ve N₂O₃ moleküllerini karşılaştırdığımızda, aynı sayıda oksijen atomu için gereken NO molekül sayısı daha fazla olacağından, normal şartlarda hacmi en büyük olan NO'dur.
Avogadro sayısı kavramı, moleküllerin sayısını anlamada çok önemlidir. 1,204×10²³ tane atom içeren SO₃ gazında, molekül sayısı atom sayısının 1/4'ü kadardır, yani 1,204×10²³ ÷ 4 = 3,01×10²² molekül bulunur. Bu da 0,05 moldür.
Bir maddenin bir gramında bulunan molekül sayısı, molekül ağırlığının tersine Avogadro sayısının çarpımıyla bulunur. Oksijen (O₂) için bu değer: N/32 moleküldür (N: Avogadro sayısı).
Önemli Not: Kimyasal formüller, bir bileşikteki elementlerin oranını gösterir. CH₃COOH gibi karmaşık bir formülde de toplam atom sayısını bulmak için tüm atomları saymalısın: 2C + 4H + 2O = 8 atom.
Moleküllerin kütleleri karşılaştırılırken, mol sayısı ve molekül ağırlığı birlikte düşünülmelidir. 0,2 mol O₂ molekülü 6,4 gram, 32 akb (atomik kütle birimi) oksijen ise sadece 32/N₁ gram (N₁: Avogadro sayısı) gelir. Bu yüzden 0,2 mol > 32 akb'dir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Aynı koşullarda gazların hacimleri, mol sayılarıyla doğru orantılıdır. 20 gram neon gazı 1 mol, 32 gram oksijen gazı 1 mol ve 32 gram kükürt dioksit gazı 0,5 mol olduğundan, hacimleri Ne = O₂ > SO₂ şeklinde sıralanır.
Moleküllerin atom içeriğine göre hesaplamalar yapmak önemlidir. Avogadro sayısı kadar atom içerebilmesi için, bir gazın ya tek atomlu olması ya da Avogadro sayısı kadar molekül içermesi gerekir. 35 gram SF₂ bileşiği 0,5 mol olduğundan, 0,5 × 3 × N₁ = 1,5N₁ atom içerir.
Atom sayıları eşit olan O₂, O₃ ve CO gazlarını karşılaştırdığımızda, molekül başına düşen atom sayıları sırasıyla 2, 3 ve 2'dir. Eşit sayıda atom için gereken molekül sayıları ise O₂ = CO > O₃ şeklinde sıralanır.
Püf Noktası: Eşit kütlede maddelerin mol sayılarını karşılaştırırken, molekül ağırlığı küçük olanın mol sayısı daha büyüktür. Bu yüzden eşit kütlede O₂ ve O₃ gazlarından O₂'nin mol sayısı daha büyüktür.
Moleküller içindeki atomların sayısını hesaplarken, atom sayılarını toplayıp mol sayısıyla çarpmalıyız. 17 gram NH₃ (1 mol) 4N₁ atom, 11,2 litre C₂H₂ (0,5 mol) 2N₁ atom ve 1,806×10²³ tane Cl₂ (0,3 mol) 0,6N₁ atom içerdiğinden, atom sayıları sıralaması NH₃ > C₂H₂ > Cl₂ şeklindedir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Farklı bileşiklerin içerdikleri toplam atom sayılarını karşılaştırabilmek için, formüldeki atom sayılarını toplayıp mol sayısıyla çarparız. 0,3 mol X bileşiğindeki atomların mol sayısı 0,75 mol Y bileşiğindeki atomların mol sayısına eşitse, X ve Y için uygun kombinasyon CH₄ ve CO olabilir. Çünkü 0,3 × 5 = 0,75 × 2 = 1,5 mol atom içerirler.
İki farklı bileşikteki aynı elementin miktarlarını eşitlemek için oran kurmalıyız. 0,4 mol N₂O₅ bileşiğinde 0,4 × 5 = 2 mol oksijen vardır. NO₂ bileşiğinde ise her molde 2 mol oksijen olduğundan, m = 46 gram NO₂ gerekir.
Atom ve moleküllerin kütle karşılaştırmaları yaparken ölçeklere dikkat etmeliyiz. 0,05 molekül-gram O₂, 0,05 atom-gram O, 1 tane O atomu ve 64 akb oksijen kütlelerinin doğru karşılaştırması: atom < akb < atom-gram < molekül-gram şeklindedir.
Formül Hatırlatması: Gazların normal şartlardaki hacimleri V = 22,4 × n (mol) ile bulunur. 4,48 litre hacimli SO₂ gazı 0,2 mol olup, 0,2 × 64 = 12,8 gram gelir.
Avogadro sayısı bir sabittir ve değiştirildiğinde bile bazı nicelikler etkilenmez. Eğer Avogadro sayısı değişseydi, H₂ gazının bağıl molekül kütlesi (2) değişmezdi, ancak 1 molünün gram olarak kütlesi ve normal şartlardaki hacmi değişirdi.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
4
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı