TYT Kimya, kimya biliminin temellerinden atom yapısına, periyodik sistemden kimyasal... Daha fazla göster
TYT Kimya Konuları
Kimya Bilimi
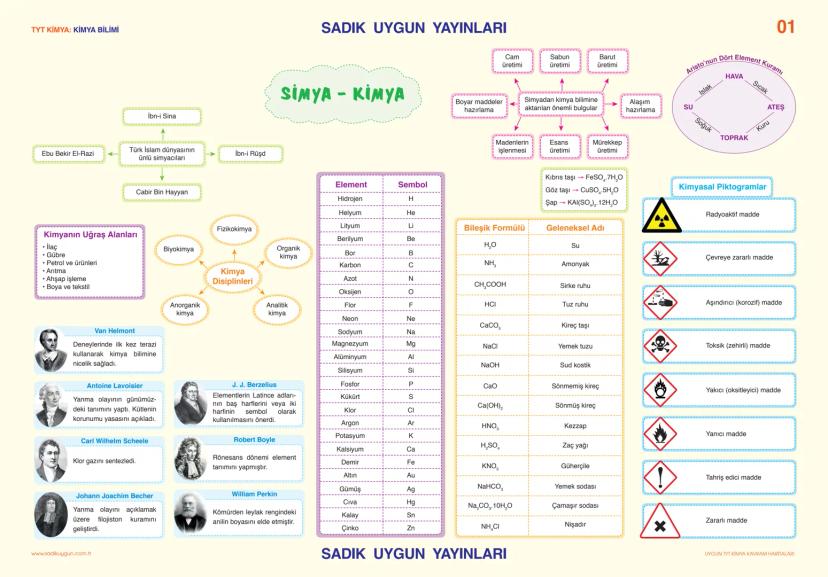
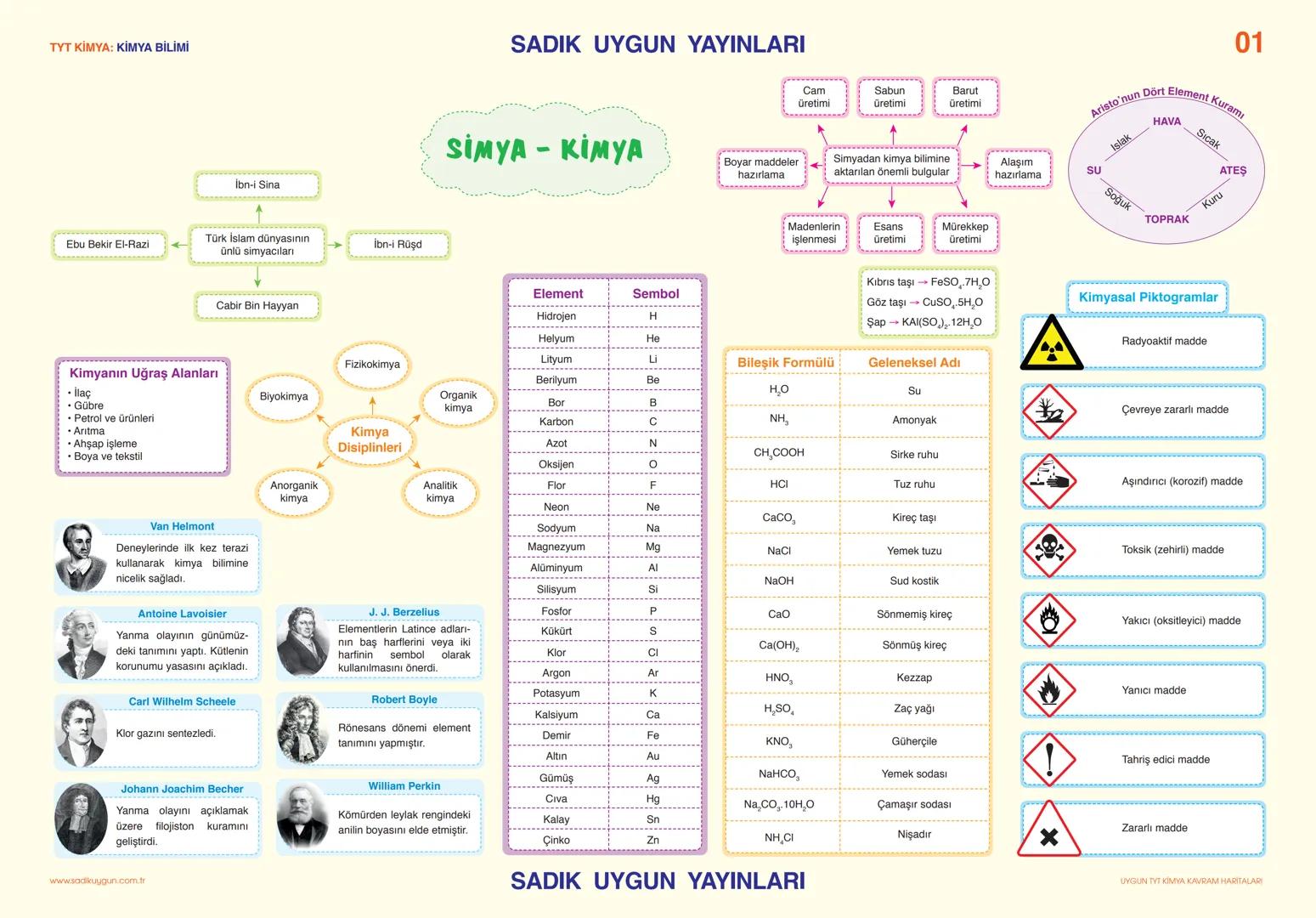
Kimya tarihi aslında simyadan başlıyor ve İbn-i Sina, Ebu Bekir El-Razi gibi Türk-İslam bilginleri bu alanda önemli çalışmalar yapmış. Simyacılar cam, sabun, barut üretimi gibi günümüzde hala kullandığımız pek çok tekniği geliştirmiş.
Modern kimyanın gelişiminde Antoine Lavoisier yanma olayını açıklayarak, Van Helmont teraziyi kullanarak, Robert Boyle element tanımını yaparak önemli katkılar sağlamış. Bu bilginler sayesinde bugün kimyanın dört ana dalı var: organik kimya, anorganik kimya, fizikokimya ve biyokimya.
Elementlerin sembollerini J.J. Berzelius önermiş ve bugün hala kullanıyoruz. Örneğin H (hidrojen), O (oksijen), Na (sodyum) gibi. Kimyasal piktogramlar da güvenlik için çok önemli - radyoaktif, toksik, yanıcı madde işaretlerini mutlaka bilmelisin.
Dikkat: Geleneksel adlar sınavda çıkabilir. Kıbrıs taşı (FeSO₄.7H₂O), göz taşı (CuSO₄.5H₂O), şap gibi isimleri unutma!
Atom ve Yapısı
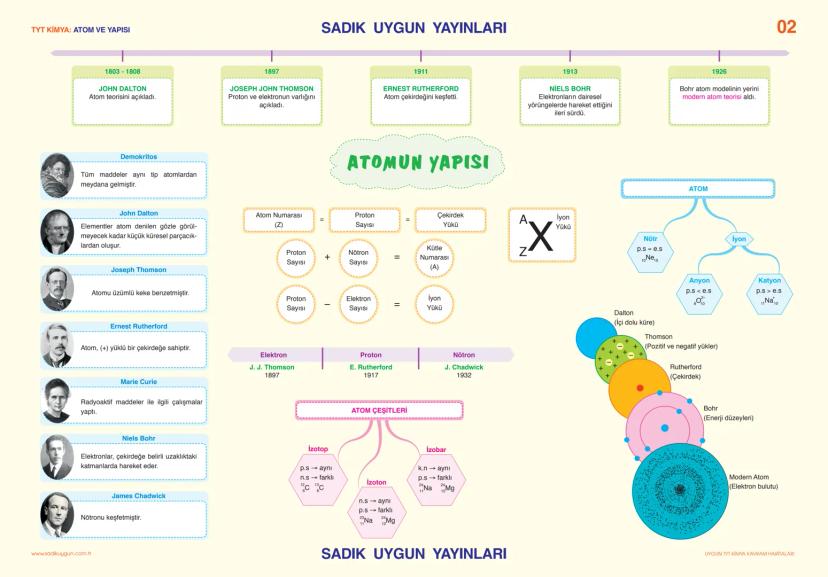
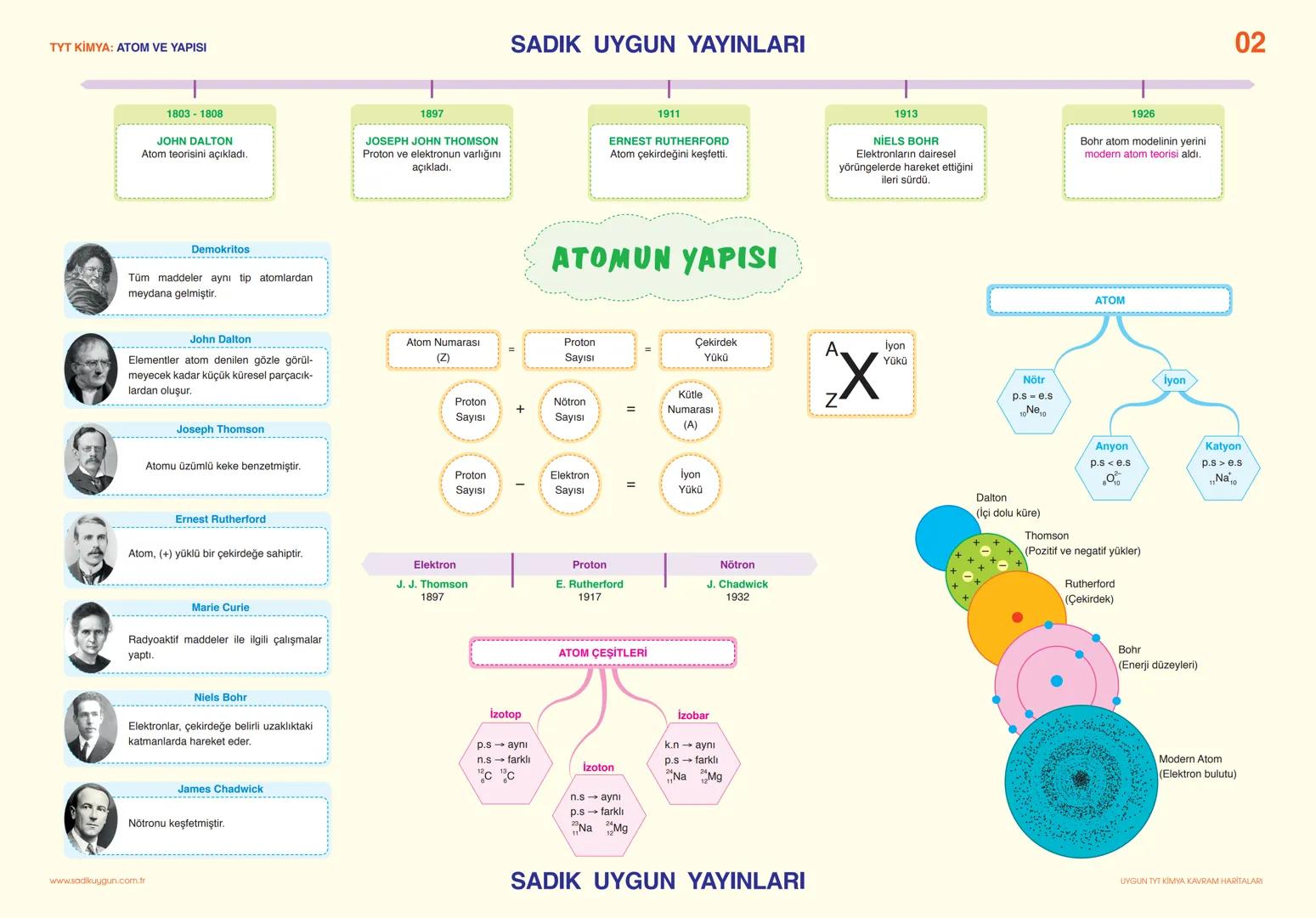
Atom teorisi 1803'te John Dalton ile başlayıp günümüzde modern atom teorisine kadar gelmiş. Her bilgin atomun farklı bir yönünü keşfetmiş: Thomson elektronu, Rutherford çekirdeği, Bohr enerji düzeylerini bulmuş.
Atomun yapısında proton (+), elektron (-) ve nötron (yüksüz) var. Atom numarası (Z) proton sayısına eşit. Kütle numarası (A) ise proton + nötron sayısının toplamı. Bu formülleri ezberle: Z = proton sayısı, A = proton + nötron, iyon yükü = proton - elektron.
İzotop, izoton, izobar kavramları sınavda çok çıkıyor. İzotoplar aynı proton sayısına sahip ama farklı nötron sayısına sahip atomlar. ¹²C ve ¹³C gibi. İzotonlar nötron sayısı aynı, izobarlar kütle numarası aynı atomlar.
İpucu: Atom modelleri tarihsel sırayla öğren - Dalton'dan modern atomya kadar. Bu kronoloji sınavda sıkça sorulur.
Periyodik Sistem
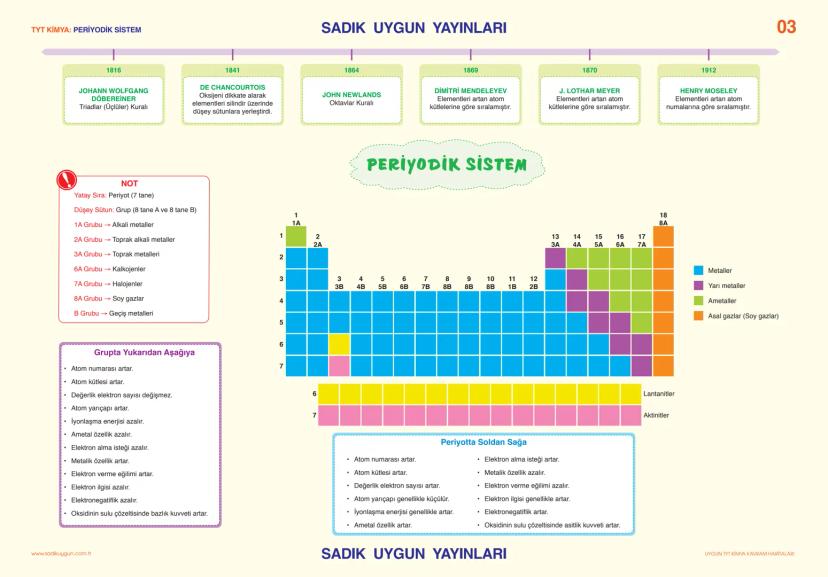
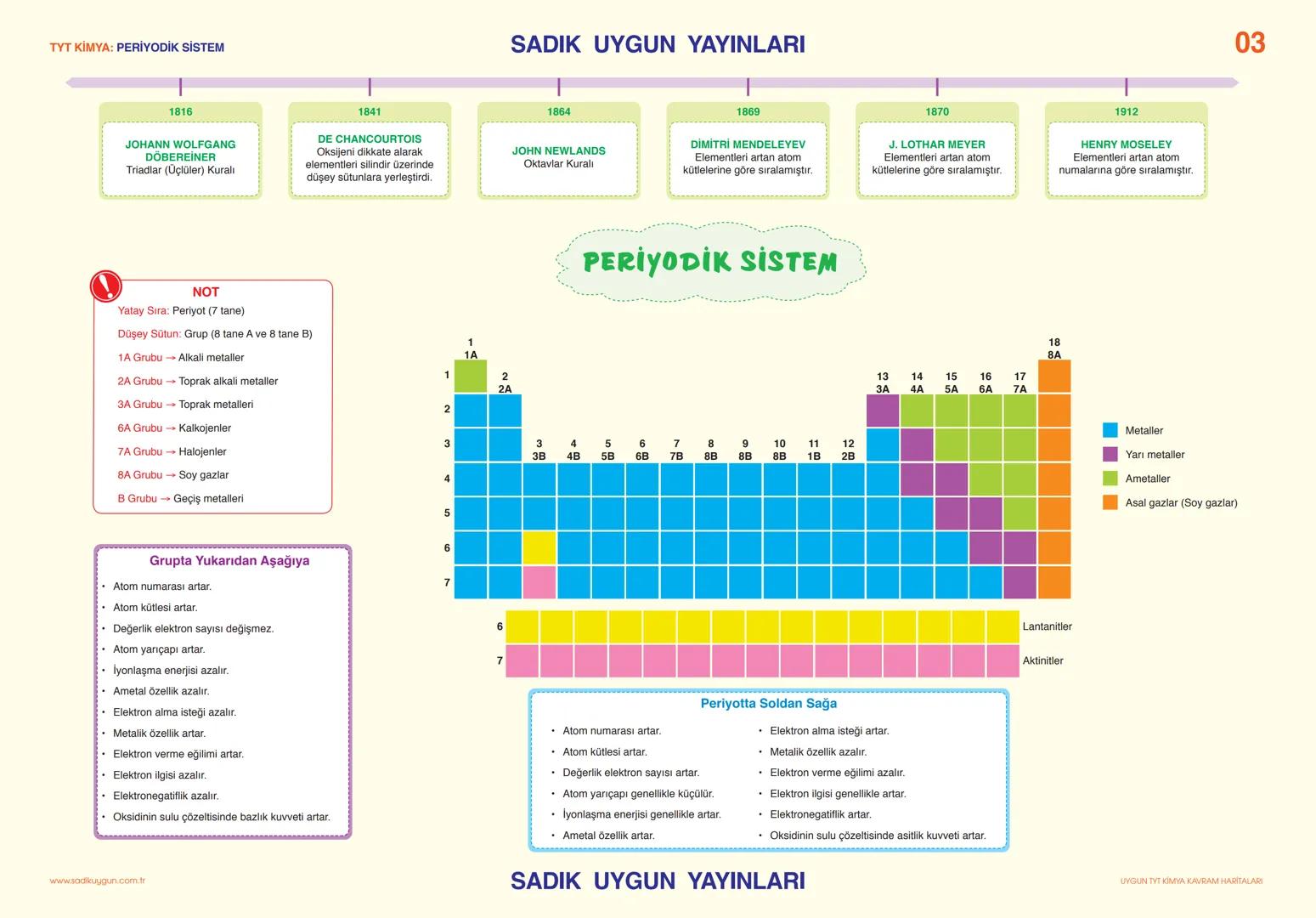
Mendeleyev elementleri atom kütlelerine göre sıralarken, Moseley atom numaralarına göre sıralamış. Bugün kullandığımız periyodik sistem Moseley'in çalışmasına dayanıyor.
Periyodik sistemde 7 periyot (yatay) ve 18 grup (düşey) var. 1A grubu alkali metaller, 2A grubu toprak alkali metaller, 7A grubu halojenler, 8A grubu soy gazlar olarak adlandırılıyor. Bu grupların özelliklerini mutlaka bil.
Periyodik özellikler şu şekilde değişir: Grupta aşağı indikçe atom yarıçapı artar, iyonlaşma enerjisi azalır, metalik özellik artar. Periyotta soldan sağa gidildikçe atom yarıçapı küçülür, iyonlaşma enerjisi artar, ametal özellik artar.
Pratik İpucu: "GASA" formülünü kullan - Grupta Aşağı, Soldan sAğa periyodik özellikler böyle değişir. Bu sınavda çok işine yarayacak!
Kimyasal Türler Arası Etkileşimler
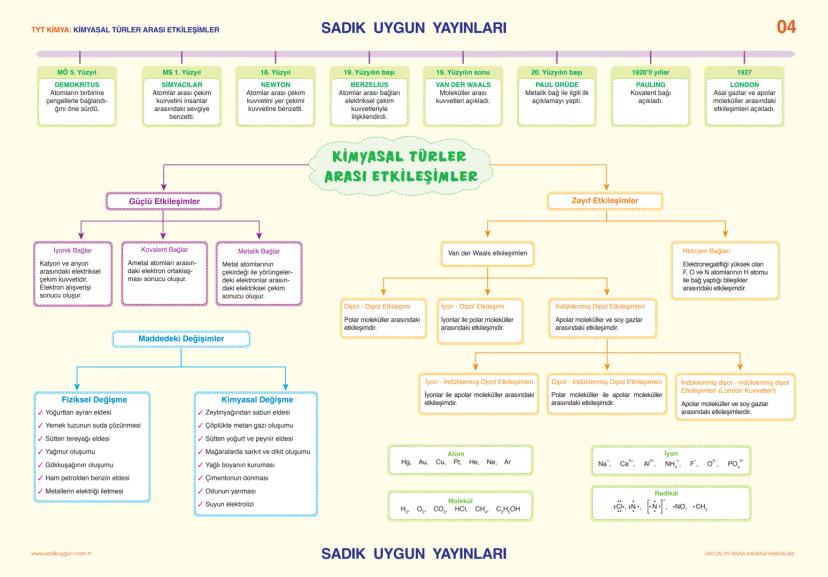
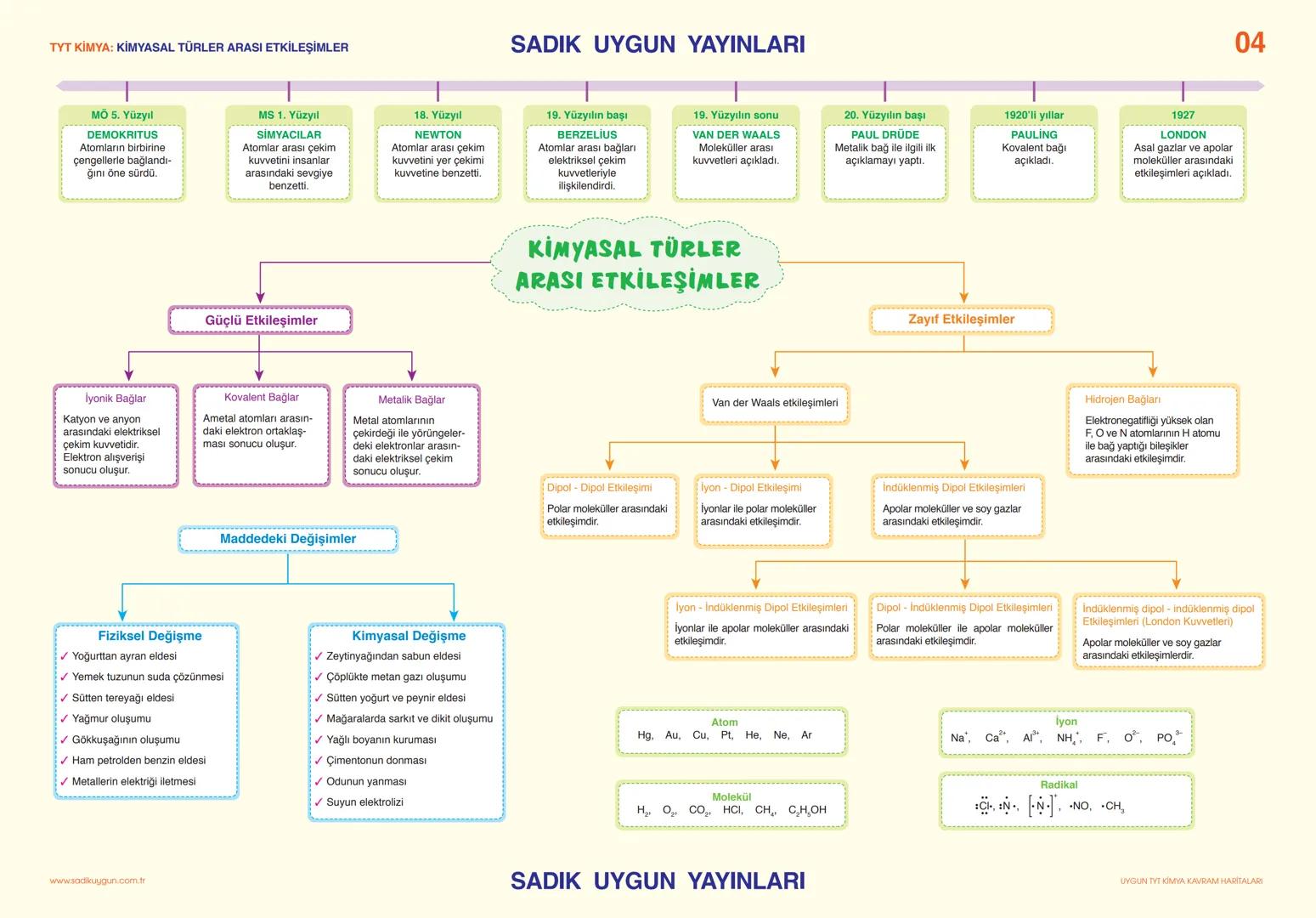
Atomlar arası bağları Demokritos çengellerle açıklamaya çalışmışken, günümüzde Pauling kovalent bağı, London zayıf etkileşimleri açıklamış. Bu bağları iki ana grupta inceleyebiliriz: güçlü ve zayıf etkileşimler.
Güçlü etkileşimler arasında iyonik bağ (elektron alışverişi), kovalent bağ (elektron ortaklaşması) ve metalik bağ var. Zayıf etkileşimler ise Van der Waals kuvvetleri içinde dipol-dipol, London kuvvetleri ve hidrojen bağı bulunur.
Maddelerde fiziksel değişme ve kimyasal değişme var. Yoğurttan ayran eldesi fiziksel, zeytinyağından sabun eldesi kimyasal değişme. Fiziksel değişmede molekül yapısı korunur, kimyasalda değişir.
Dikkat: Hidrojen bağları sadece F, O, N atomlarıyla H arasında oluşur. Bu çok önemli bir detay!
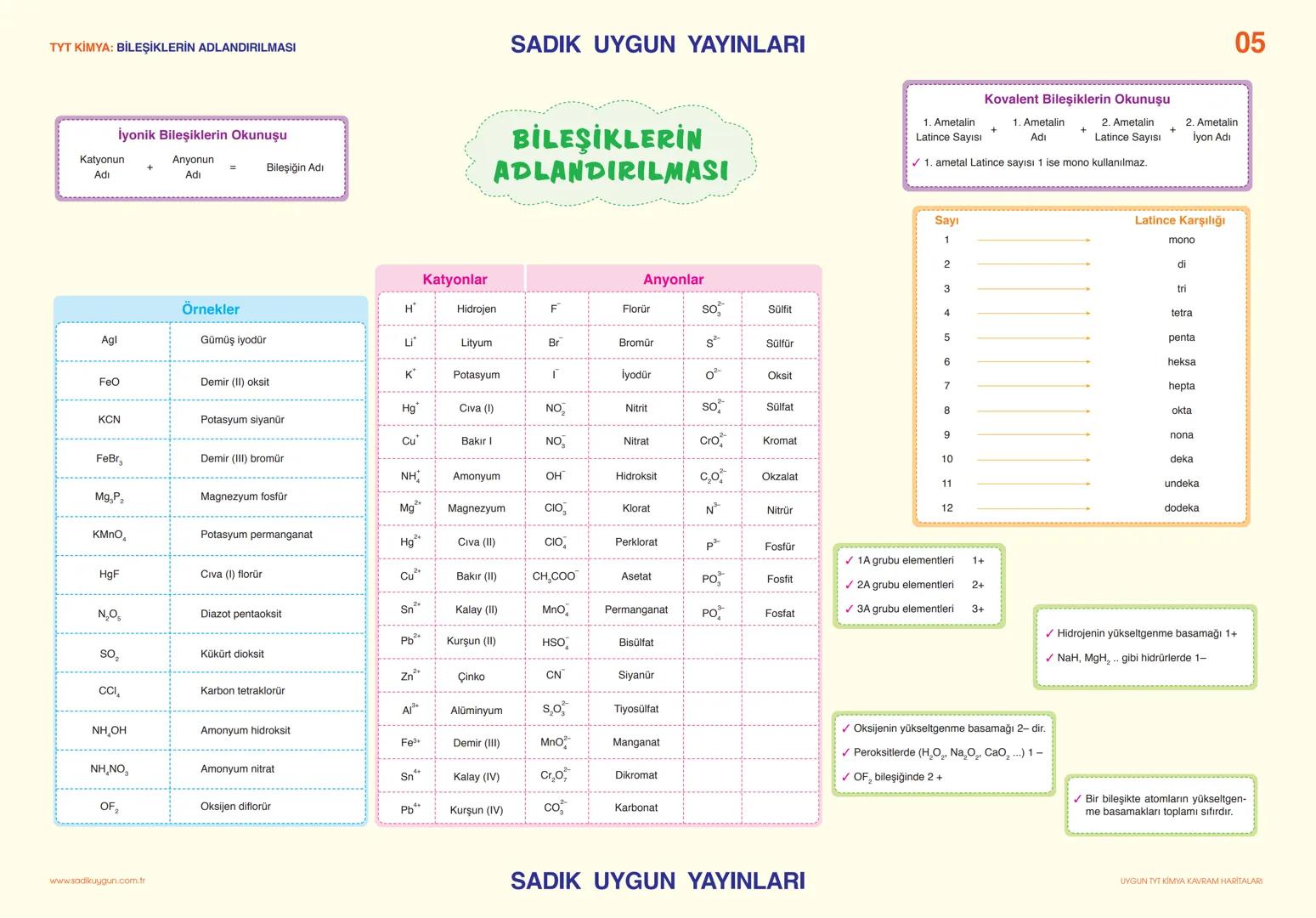
Bileşiklerin Adlandırılması
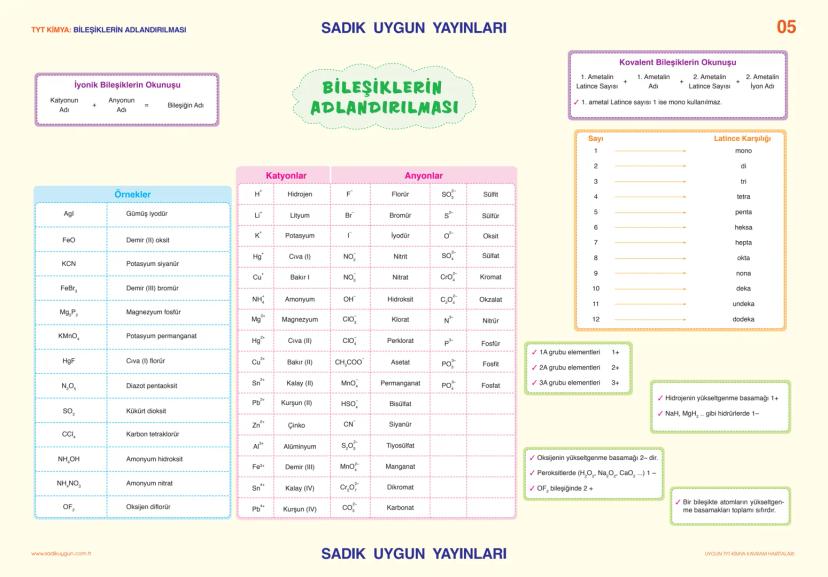
İyonik bileşikler adlandırılırken önce katyonun adı, sonra anyonun adı söylenir. Örneğin NaCl = sodyum klorür. Değişken değerlikli metallerde değerlik Roma rakamıyla belirtilir: FeO = demir (II) oksit.
Kovalent bileşiklerde Latince sayılar kullanılır: mono, di, tri, tetra... N₂O₅ = diazot pentaoksit gibi. İlk ametalin sayısı 1 ise mono kullanılmaz.
Yükseltgenme basamakları çok önemli: 1A grubu +1, 2A grubu +2, 3A grubu +3 değerlikte. Hidrojen genellikle +1, oksijen -2 değerlikli. Bir bileşikteki tüm yükseltgenme basamakları toplamı sıfır olmalı.
Ezber İpucu: Çok kullanılan iyonların adlarını ezberle - NH₄⁺ (amonyum), SO₄²⁻ (sülfat), CO₃²⁻ (karbonat) gibi.
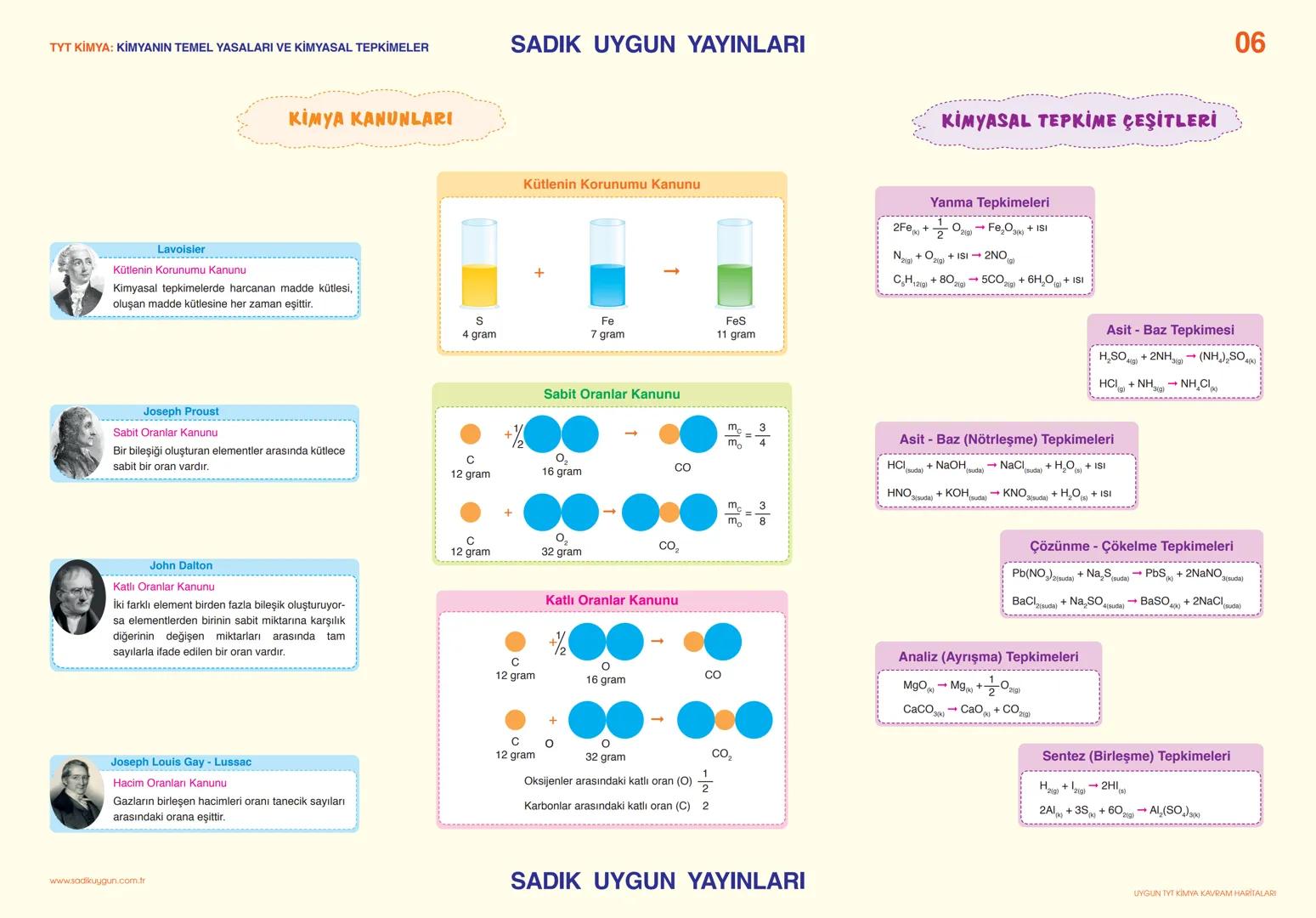
Kimyanin Temel Yasaları ve Kimyasal Tepkimeler
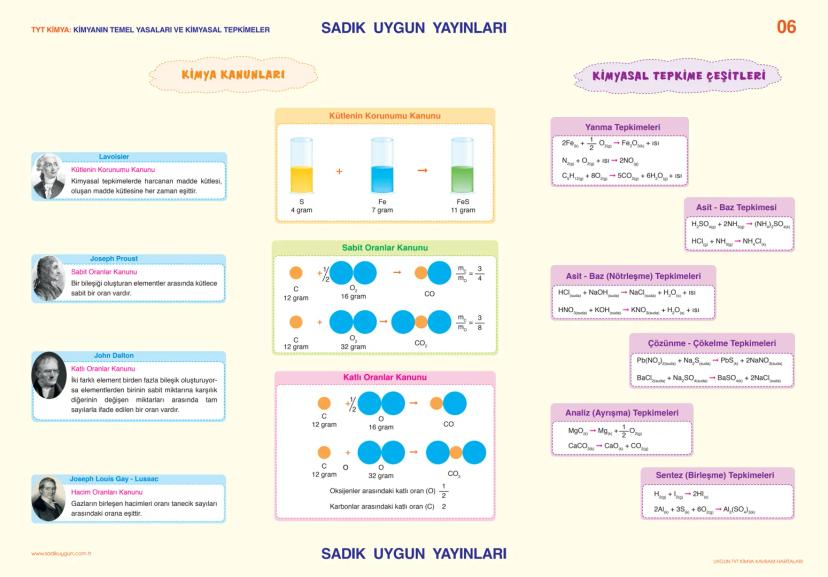
Lavoisier'in Kütlenin Korunumu Kanunu: Kimyasal tepkimelerde harcanan madde kütlesi = oluşan madde kütlesi. Bu temel prensip tüm kimyasal hesaplamalarda kullanılır.
Proust'un Sabit Oranlar Kanunu: Bir bileşiği oluşturan elementler arasında kütlece sabit oran vardır. Dalton'un Katlı Oranlar Kanunu ise iki element birden fazla bileşik oluşturuyorsa, değişen miktarları arasında tam sayı oranı olduğunu söyler.
Kimyasal tepkime çeşitleri beş ana grupta toplanır: yanma, asit-baz, çözünme-çökelme, analiz (ayrışma) ve sentez (birleşme) tepkimeleri. Her birinin karakteristik özellikleri var ve sınavda mutlaka çıkıyor.
Formül İpucu: Gay-Lussac'ın Hacim Oranları Kanunu'nu unutma - gazların birleşen hacimleri oranı, tanecik sayıları oranına eşit!
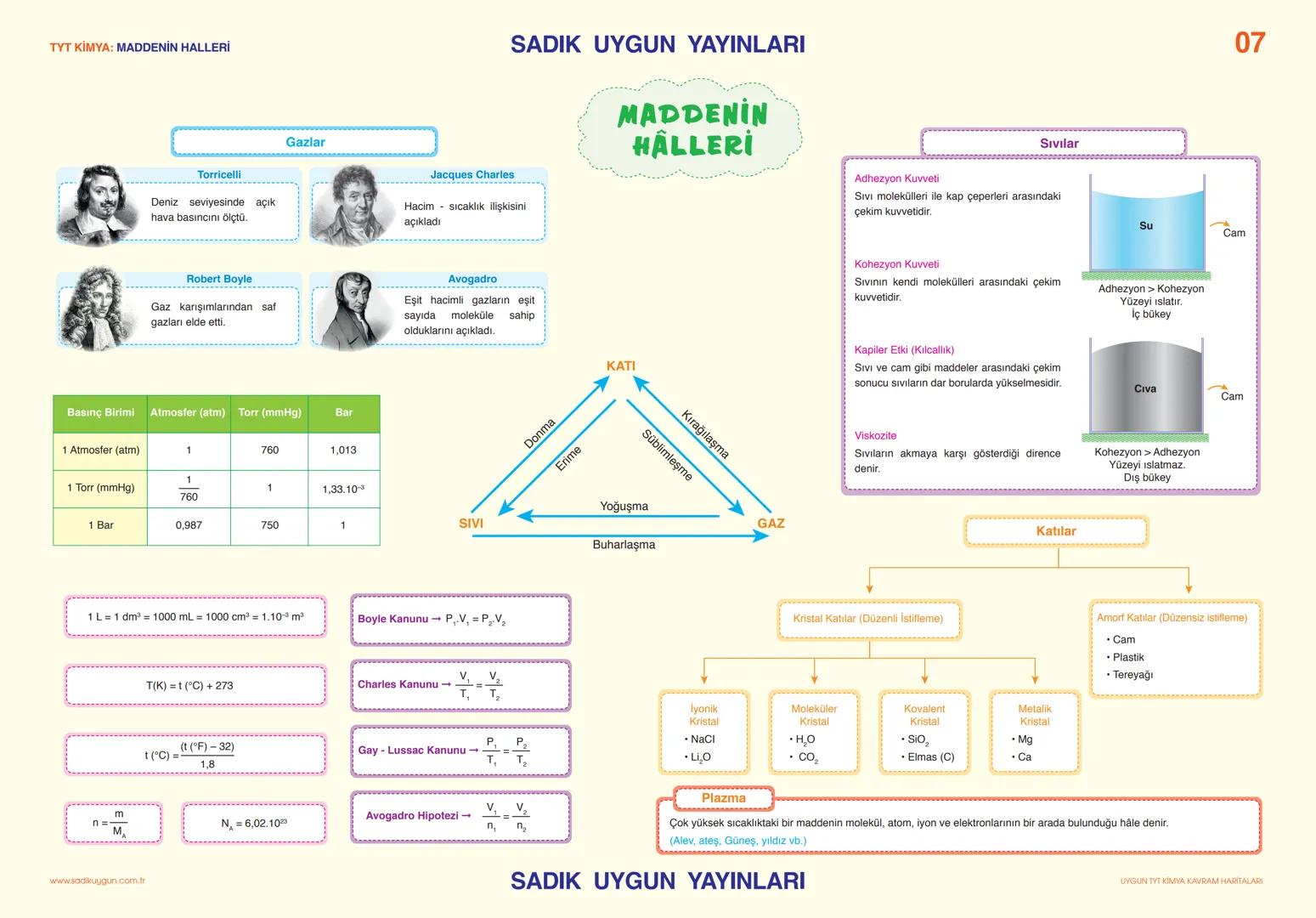
Maddenin Halleri
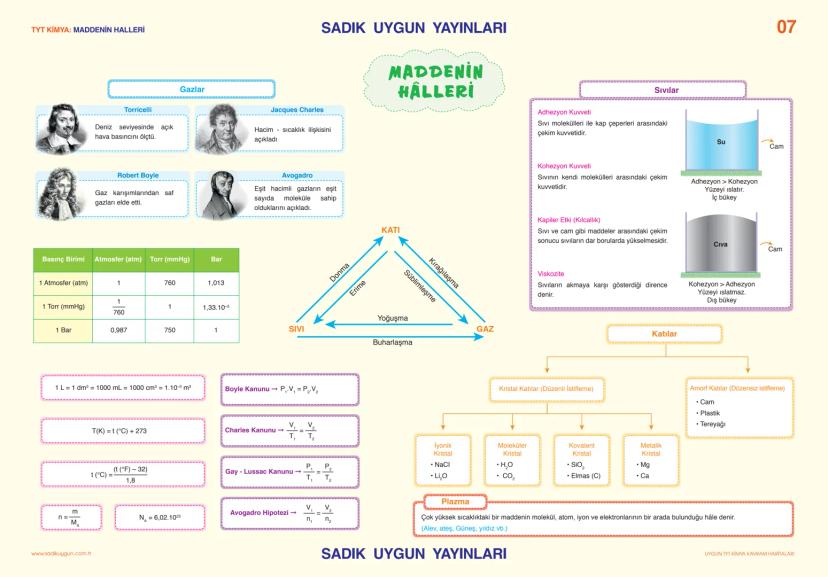
Katı, sıvı, gaz ve plazma olmak üzere dört hal var. Boyle Kanunu , Charles Kanunu ve Gay-Lussac Kanunu gaz yasalarının temeli.
Sıvılarda kohezyon (sıvının kendi molekülleri arası çekim) ve adhezyon kuvvetleri önemli. Su camda iç bükey, cıva dış bükey menisküs oluşturur. Kapiler etki de bu kuvvetlerle açıklanır.
Kristal katılar düzenli diziliş gösterirken, amorf katılar düzensiz. Cam, plastik amorf; tuz, metal kristal katılardır. Kristal katılar iyonik, moleküler, kovalent ve metalik olmak üzere dört türde sınıflandırılır.
Birim Dönüşümü: 1 L = 1000 mL = 1000 cm³, T(K) = t(°C) + 273 formüllerini ezberle!
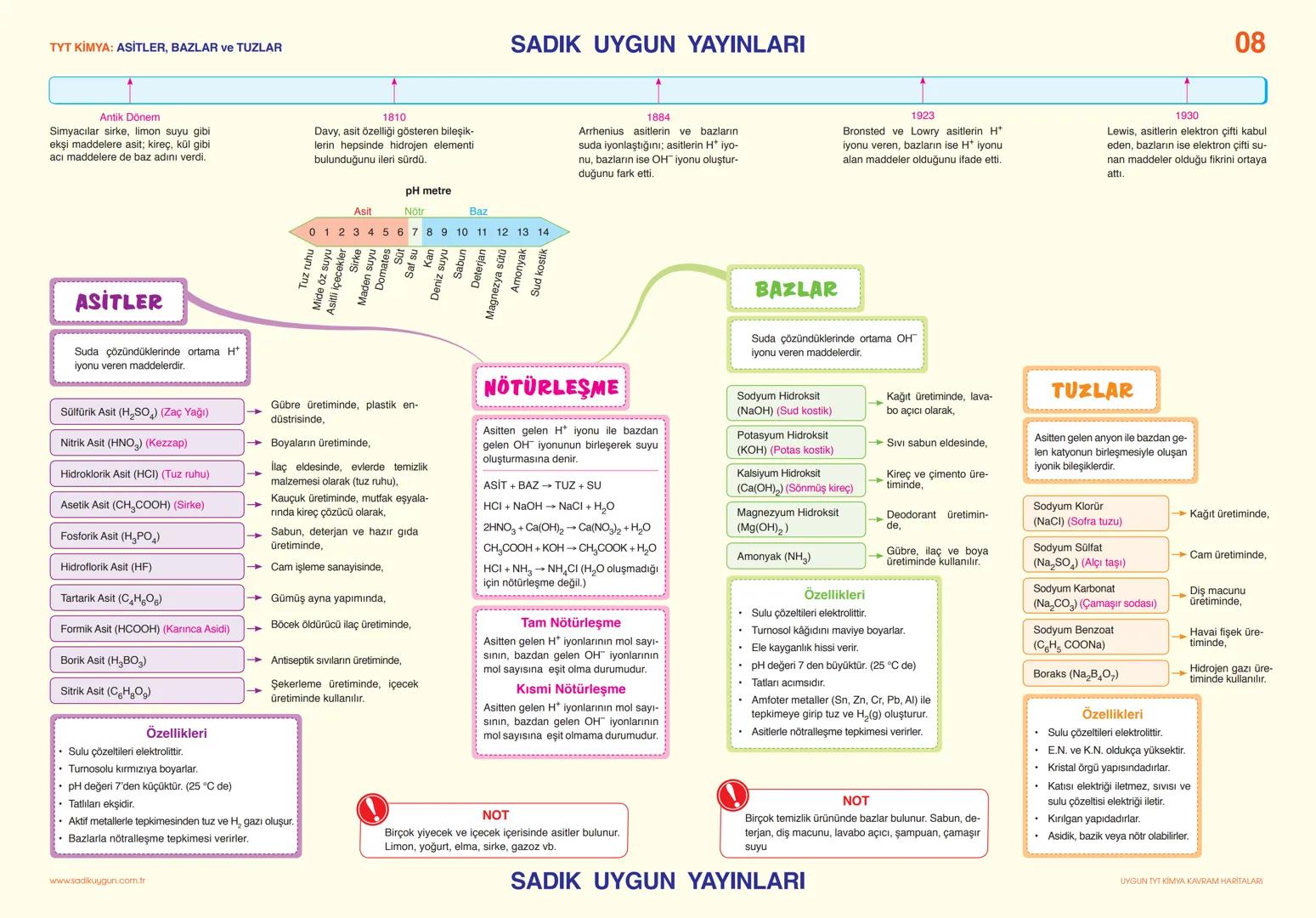
Asitler, Bazlar ve Tuzlar
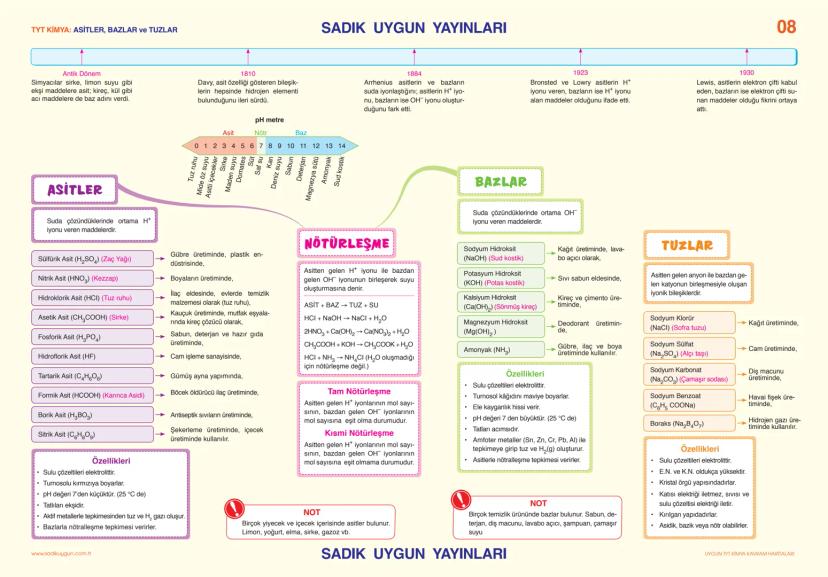
Asitler suda çözündüklerinde H⁺ iyonu veren maddeler. Bazlar ise OH⁻ iyonu veren maddeler (Arrhenius tanımı). pH ölçeği 0-14 arası, 7'den küçük asit, 7'den büyük baz, 7 nötr.
Nötrleşme tepkimesi: Asit + Baz → Tuz + Su. HCl + NaOH → NaCl + H₂O gibi. Tam nötrleşmede H⁺ ve OH⁻ mol sayıları eşit, kısmi nötrleşmede eşit değil.
Asitlerin kullanım alanları: H₂SO₄ (gübre, plastik), HNO₃ (patlayıcı), HCl (temizlik). Bazların kullanım alanları: NaOH (sabun, lavabo açıcı), Ca(OH)₂ (kireç, çimento). Tuzlar ise gıda, cam, deterjan sanayisinde kullanılır.
Günlük Yaşam: Limon, sirke, yoğurt asitli; sabun, deterjan, diş macunu bazlı maddelerdir!
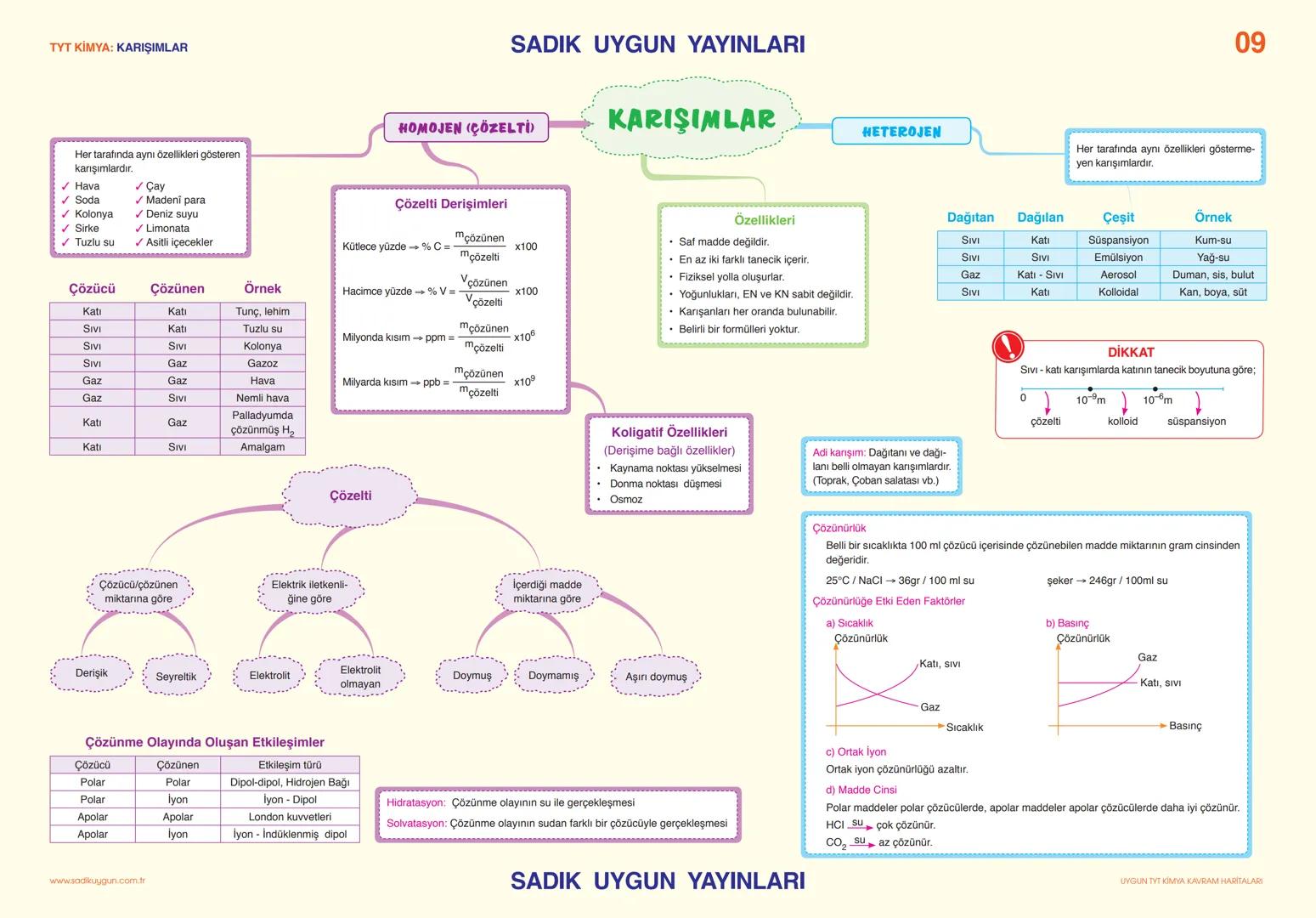
Karışımlar
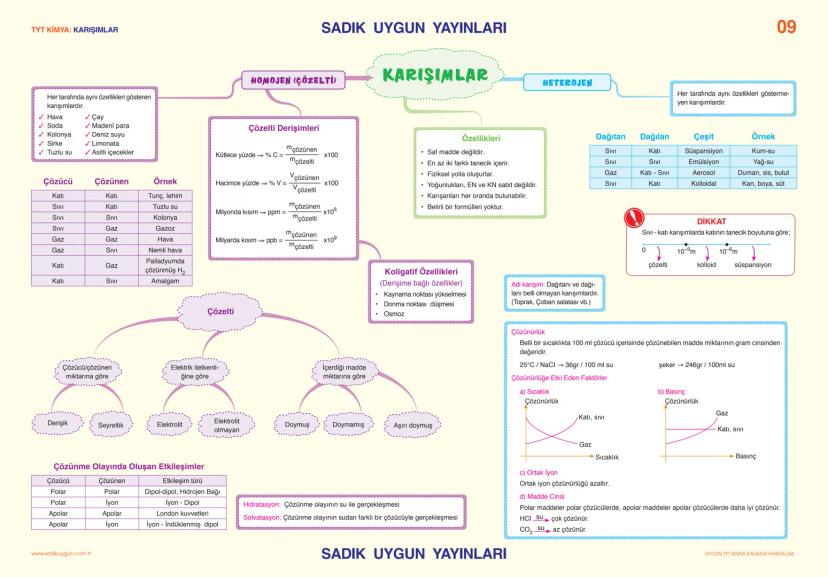
Homojen karışımlar (çözeltiler) her tarafta aynı özellik gösterir: hava, soda, tuzlu su. Heterojen karışımlar farklı özellik gösterir: kum-su, yağ-su, kan.
Çözelti derişimi kütlece yüzde , hacimce yüzde ve ppm/ppb olarak ifade edilir. Koligatif özellikler derişime bağlıdır: kaynama noktası yükselmesi, donma noktası düşmesi, osmoz.
Çözünürlük 100 ml çözücüdeki çözünen madde miktarı (gram). Sıcaklık katı-sıvılarda çözünürlüğü artırır, gazlarda azaltır. Basınç gazlarda çözünürlüğü artırır, katı-sıvılarda etkisizdir.
"Benzer benzeri çözer" Kuralı: Polar maddeler polar çözücülerde, apolar maddeler apolar çözücülerde iyi çözünür!
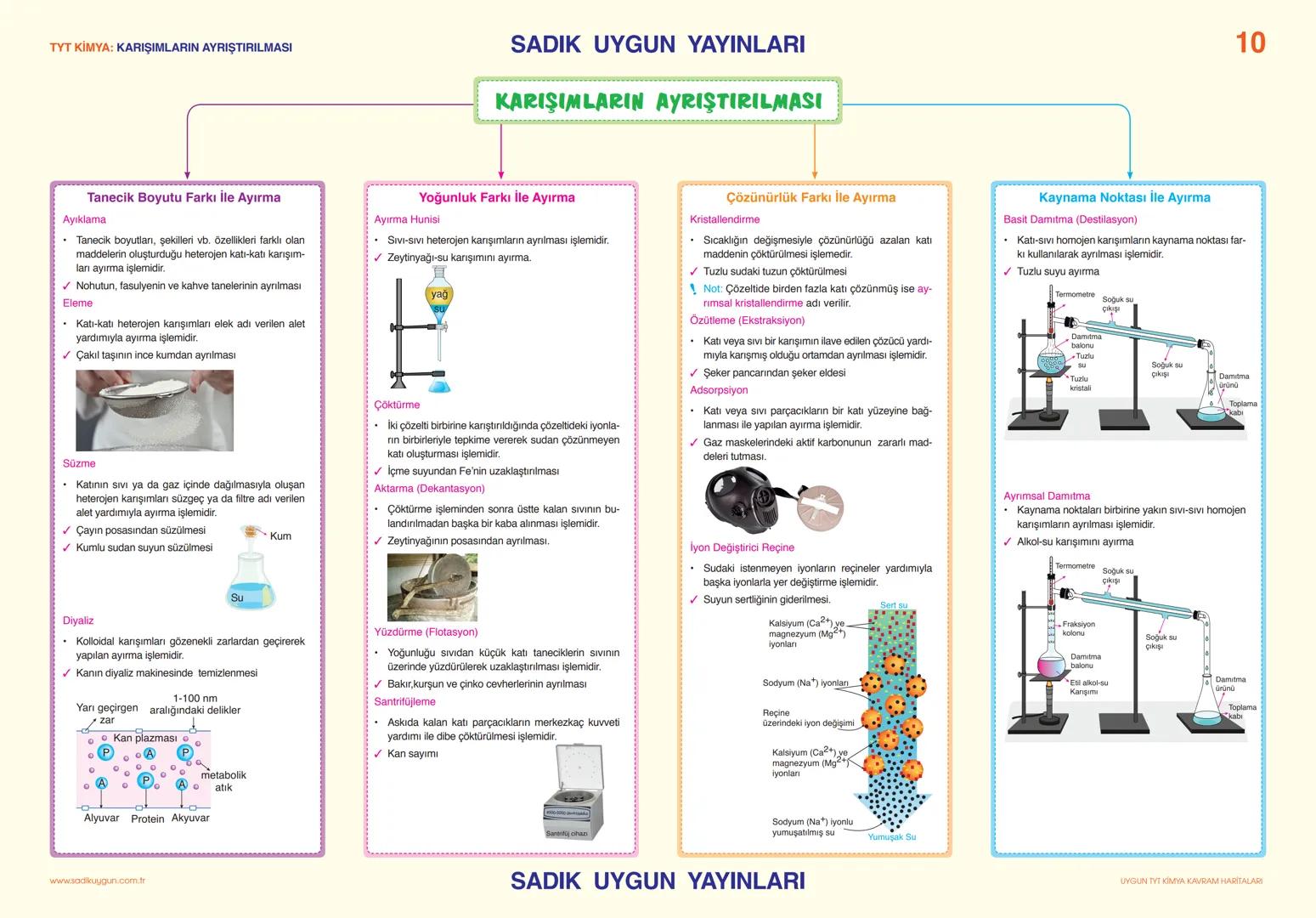
Karışımların Ayrıştırılması
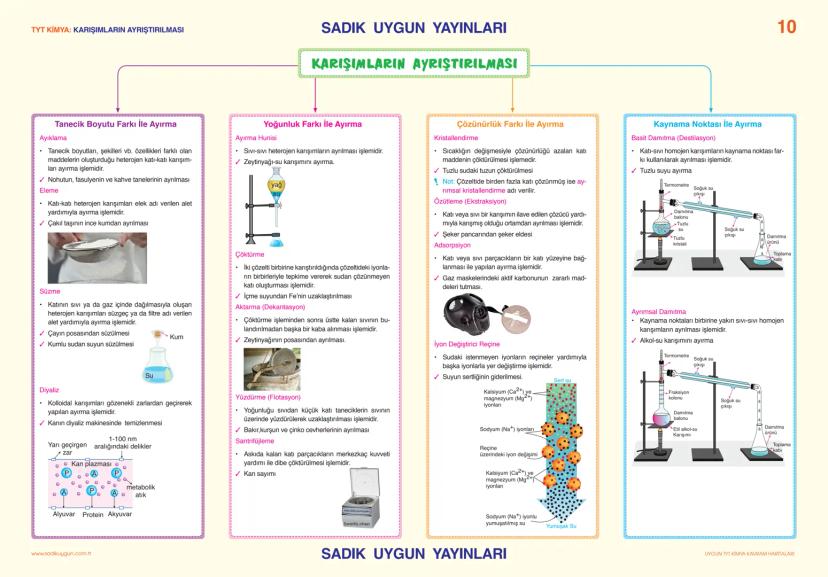
Karışımların ayrıştırılması fiziksel özellik farklarına dayanır. Tanecik boyutu farkıyla ayıklama, eleme, süzme yapılır. Çay posasından çayın süzülmesi en bilinen örnektir.
Yoğunluk farkı kullanılarak ayırma hunisi, çöktürme, dekantasyon yapılır. Çözünürlük farkı ile kristallendirme, özütleme, adsorpsiyon, iyon değiştirici reçine kullanılır. Su arıtma tesislerinde bu yöntemler kullanılır.
Kaynama noktası farkı ile basit damıtma ve ayrımsal damıtma yapılır. Tuzlu sudan tuz-su ayrımı basit damıtma, alkol-su karışımını ayırma ayrımsal damıtma örneğidir. Diyaliz kan temizliğinde, santrifüjleme kan sayımında kullanılır.
Pratik Bilgi: Hangi karışım türü için hangi ayırma yöntemi kullanılacağını öğren. Bu sınavda çok pratik sorularla çıkıyor!
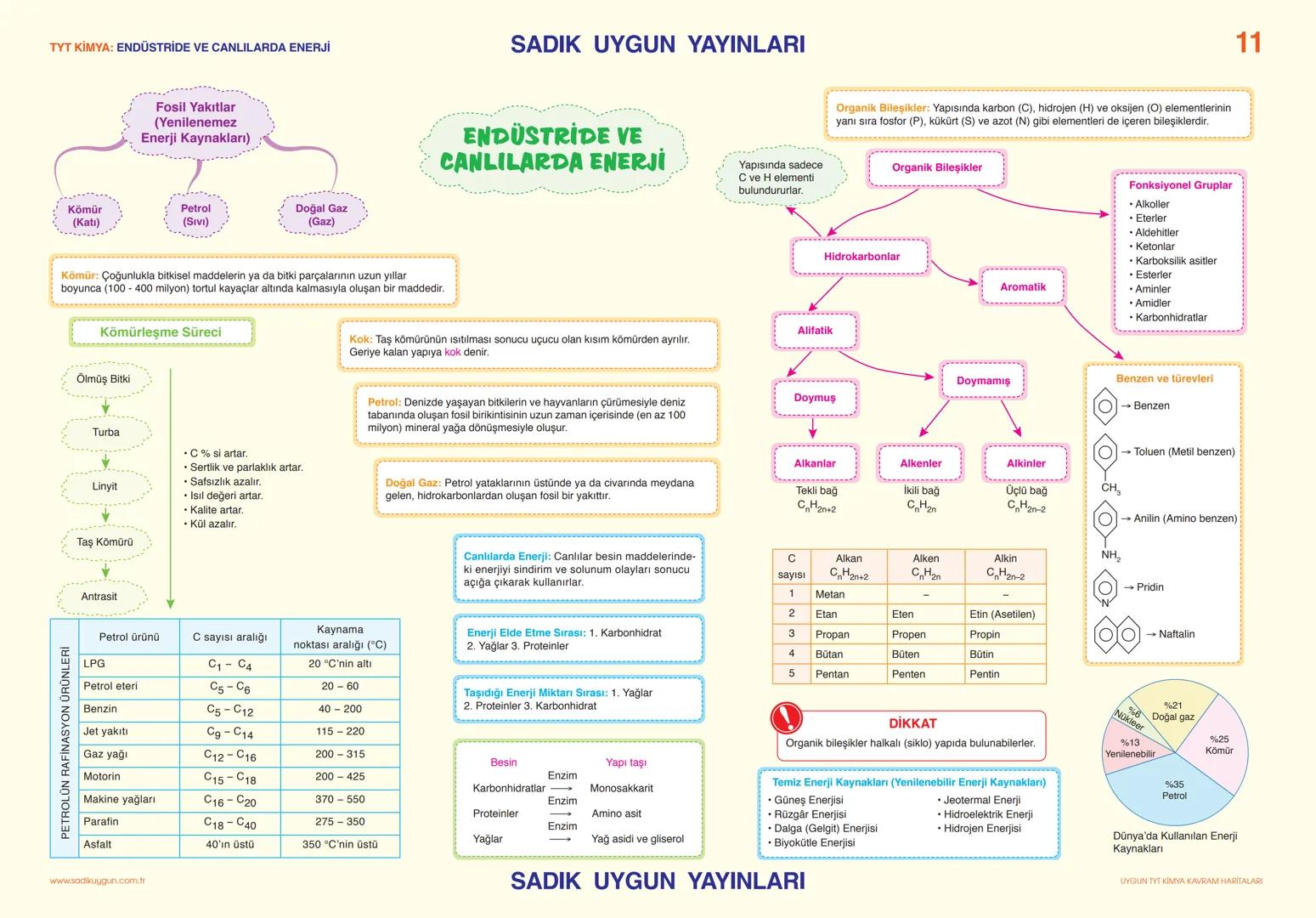
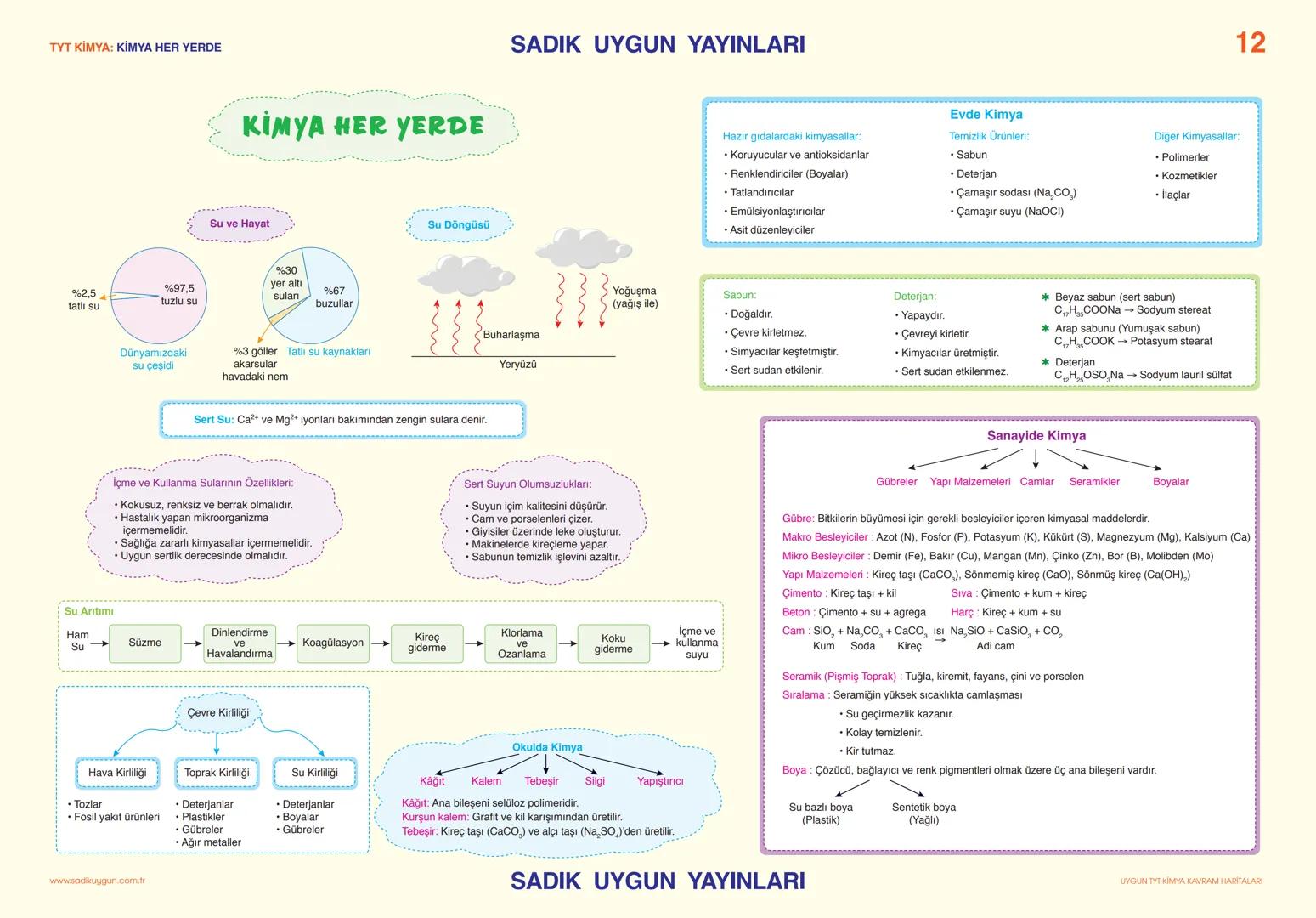
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Nanoparticles
2Kimya dersinin en popüler içerikleri
9Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
TYT Kimya Tekrar ve Özet 2024
Aktifzeka Yayınları
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
TYT Kimya Konuları
TYT Kimya, kimya biliminin temellerinden atom yapısına, periyodik sistemden kimyasal bağlara kadar pek çok konuyu kapsıyor. Bu özet, sınavda karşılaşacağın tüm temel kavramları pratik bir şekilde öğrenmeni sağlayacak.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Kimya Bilimi
Kimya tarihi aslında simyadan başlıyor ve İbn-i Sina, Ebu Bekir El-Razi gibi Türk-İslam bilginleri bu alanda önemli çalışmalar yapmış. Simyacılar cam, sabun, barut üretimi gibi günümüzde hala kullandığımız pek çok tekniği geliştirmiş.
Modern kimyanın gelişiminde Antoine Lavoisier yanma olayını açıklayarak, Van Helmont teraziyi kullanarak, Robert Boyle element tanımını yaparak önemli katkılar sağlamış. Bu bilginler sayesinde bugün kimyanın dört ana dalı var: organik kimya, anorganik kimya, fizikokimya ve biyokimya.
Elementlerin sembollerini J.J. Berzelius önermiş ve bugün hala kullanıyoruz. Örneğin H (hidrojen), O (oksijen), Na (sodyum) gibi. Kimyasal piktogramlar da güvenlik için çok önemli - radyoaktif, toksik, yanıcı madde işaretlerini mutlaka bilmelisin.
Dikkat: Geleneksel adlar sınavda çıkabilir. Kıbrıs taşı (FeSO₄.7H₂O), göz taşı (CuSO₄.5H₂O), şap gibi isimleri unutma!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Atom ve Yapısı
Atom teorisi 1803'te John Dalton ile başlayıp günümüzde modern atom teorisine kadar gelmiş. Her bilgin atomun farklı bir yönünü keşfetmiş: Thomson elektronu, Rutherford çekirdeği, Bohr enerji düzeylerini bulmuş.
Atomun yapısında proton (+), elektron (-) ve nötron (yüksüz) var. Atom numarası (Z) proton sayısına eşit. Kütle numarası (A) ise proton + nötron sayısının toplamı. Bu formülleri ezberle: Z = proton sayısı, A = proton + nötron, iyon yükü = proton - elektron.
İzotop, izoton, izobar kavramları sınavda çok çıkıyor. İzotoplar aynı proton sayısına sahip ama farklı nötron sayısına sahip atomlar. ¹²C ve ¹³C gibi. İzotonlar nötron sayısı aynı, izobarlar kütle numarası aynı atomlar.
İpucu: Atom modelleri tarihsel sırayla öğren - Dalton'dan modern atomya kadar. Bu kronoloji sınavda sıkça sorulur.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Periyodik Sistem
Mendeleyev elementleri atom kütlelerine göre sıralarken, Moseley atom numaralarına göre sıralamış. Bugün kullandığımız periyodik sistem Moseley'in çalışmasına dayanıyor.
Periyodik sistemde 7 periyot (yatay) ve 18 grup (düşey) var. 1A grubu alkali metaller, 2A grubu toprak alkali metaller, 7A grubu halojenler, 8A grubu soy gazlar olarak adlandırılıyor. Bu grupların özelliklerini mutlaka bil.
Periyodik özellikler şu şekilde değişir: Grupta aşağı indikçe atom yarıçapı artar, iyonlaşma enerjisi azalır, metalik özellik artar. Periyotta soldan sağa gidildikçe atom yarıçapı küçülür, iyonlaşma enerjisi artar, ametal özellik artar.
Pratik İpucu: "GASA" formülünü kullan - Grupta Aşağı, Soldan sAğa periyodik özellikler böyle değişir. Bu sınavda çok işine yarayacak!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Kimyasal Türler Arası Etkileşimler
Atomlar arası bağları Demokritos çengellerle açıklamaya çalışmışken, günümüzde Pauling kovalent bağı, London zayıf etkileşimleri açıklamış. Bu bağları iki ana grupta inceleyebiliriz: güçlü ve zayıf etkileşimler.
Güçlü etkileşimler arasında iyonik bağ (elektron alışverişi), kovalent bağ (elektron ortaklaşması) ve metalik bağ var. Zayıf etkileşimler ise Van der Waals kuvvetleri içinde dipol-dipol, London kuvvetleri ve hidrojen bağı bulunur.
Maddelerde fiziksel değişme ve kimyasal değişme var. Yoğurttan ayran eldesi fiziksel, zeytinyağından sabun eldesi kimyasal değişme. Fiziksel değişmede molekül yapısı korunur, kimyasalda değişir.
Dikkat: Hidrojen bağları sadece F, O, N atomlarıyla H arasında oluşur. Bu çok önemli bir detay!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Bileşiklerin Adlandırılması
İyonik bileşikler adlandırılırken önce katyonun adı, sonra anyonun adı söylenir. Örneğin NaCl = sodyum klorür. Değişken değerlikli metallerde değerlik Roma rakamıyla belirtilir: FeO = demir (II) oksit.
Kovalent bileşiklerde Latince sayılar kullanılır: mono, di, tri, tetra... N₂O₅ = diazot pentaoksit gibi. İlk ametalin sayısı 1 ise mono kullanılmaz.
Yükseltgenme basamakları çok önemli: 1A grubu +1, 2A grubu +2, 3A grubu +3 değerlikte. Hidrojen genellikle +1, oksijen -2 değerlikli. Bir bileşikteki tüm yükseltgenme basamakları toplamı sıfır olmalı.
Ezber İpucu: Çok kullanılan iyonların adlarını ezberle - NH₄⁺ (amonyum), SO₄²⁻ (sülfat), CO₃²⁻ (karbonat) gibi.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Kimyanin Temel Yasaları ve Kimyasal Tepkimeler
Lavoisier'in Kütlenin Korunumu Kanunu: Kimyasal tepkimelerde harcanan madde kütlesi = oluşan madde kütlesi. Bu temel prensip tüm kimyasal hesaplamalarda kullanılır.
Proust'un Sabit Oranlar Kanunu: Bir bileşiği oluşturan elementler arasında kütlece sabit oran vardır. Dalton'un Katlı Oranlar Kanunu ise iki element birden fazla bileşik oluşturuyorsa, değişen miktarları arasında tam sayı oranı olduğunu söyler.
Kimyasal tepkime çeşitleri beş ana grupta toplanır: yanma, asit-baz, çözünme-çökelme, analiz (ayrışma) ve sentez (birleşme) tepkimeleri. Her birinin karakteristik özellikleri var ve sınavda mutlaka çıkıyor.
Formül İpucu: Gay-Lussac'ın Hacim Oranları Kanunu'nu unutma - gazların birleşen hacimleri oranı, tanecik sayıları oranına eşit!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Maddenin Halleri
Katı, sıvı, gaz ve plazma olmak üzere dört hal var. Boyle Kanunu , Charles Kanunu ve Gay-Lussac Kanunu gaz yasalarının temeli.
Sıvılarda kohezyon (sıvının kendi molekülleri arası çekim) ve adhezyon kuvvetleri önemli. Su camda iç bükey, cıva dış bükey menisküs oluşturur. Kapiler etki de bu kuvvetlerle açıklanır.
Kristal katılar düzenli diziliş gösterirken, amorf katılar düzensiz. Cam, plastik amorf; tuz, metal kristal katılardır. Kristal katılar iyonik, moleküler, kovalent ve metalik olmak üzere dört türde sınıflandırılır.
Birim Dönüşümü: 1 L = 1000 mL = 1000 cm³, T(K) = t(°C) + 273 formüllerini ezberle!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Asitler, Bazlar ve Tuzlar
Asitler suda çözündüklerinde H⁺ iyonu veren maddeler. Bazlar ise OH⁻ iyonu veren maddeler (Arrhenius tanımı). pH ölçeği 0-14 arası, 7'den küçük asit, 7'den büyük baz, 7 nötr.
Nötrleşme tepkimesi: Asit + Baz → Tuz + Su. HCl + NaOH → NaCl + H₂O gibi. Tam nötrleşmede H⁺ ve OH⁻ mol sayıları eşit, kısmi nötrleşmede eşit değil.
Asitlerin kullanım alanları: H₂SO₄ (gübre, plastik), HNO₃ (patlayıcı), HCl (temizlik). Bazların kullanım alanları: NaOH (sabun, lavabo açıcı), Ca(OH)₂ (kireç, çimento). Tuzlar ise gıda, cam, deterjan sanayisinde kullanılır.
Günlük Yaşam: Limon, sirke, yoğurt asitli; sabun, deterjan, diş macunu bazlı maddelerdir!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Karışımlar
Homojen karışımlar (çözeltiler) her tarafta aynı özellik gösterir: hava, soda, tuzlu su. Heterojen karışımlar farklı özellik gösterir: kum-su, yağ-su, kan.
Çözelti derişimi kütlece yüzde , hacimce yüzde ve ppm/ppb olarak ifade edilir. Koligatif özellikler derişime bağlıdır: kaynama noktası yükselmesi, donma noktası düşmesi, osmoz.
Çözünürlük 100 ml çözücüdeki çözünen madde miktarı (gram). Sıcaklık katı-sıvılarda çözünürlüğü artırır, gazlarda azaltır. Basınç gazlarda çözünürlüğü artırır, katı-sıvılarda etkisizdir.
"Benzer benzeri çözer" Kuralı: Polar maddeler polar çözücülerde, apolar maddeler apolar çözücülerde iyi çözünür!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Karışımların Ayrıştırılması
Karışımların ayrıştırılması fiziksel özellik farklarına dayanır. Tanecik boyutu farkıyla ayıklama, eleme, süzme yapılır. Çay posasından çayın süzülmesi en bilinen örnektir.
Yoğunluk farkı kullanılarak ayırma hunisi, çöktürme, dekantasyon yapılır. Çözünürlük farkı ile kristallendirme, özütleme, adsorpsiyon, iyon değiştirici reçine kullanılır. Su arıtma tesislerinde bu yöntemler kullanılır.
Kaynama noktası farkı ile basit damıtma ve ayrımsal damıtma yapılır. Tuzlu sudan tuz-su ayrımı basit damıtma, alkol-su karışımını ayırma ayrımsal damıtma örneğidir. Diyaliz kan temizliğinde, santrifüjleme kan sayımında kullanılır.
Pratik Bilgi: Hangi karışım türü için hangi ayırma yöntemi kullanılacağını öğren. Bu sınavda çok pratik sorularla çıkıyor!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Nanoparticles
2Kimya dersinin en popüler içerikleri
9Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
11 sınıf kimyasal tepkimelerde enerji full tekrar
11 sınıf kimyasal tepkimelerde enerji full tekrar
TYT Kimya Tekrar ve Özet 2024
Aktifzeka Yayınları
En popüler içerikler
911. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
8.sınıf matematik
Tüm üniteleri içermektedir!
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
İnkılap tarihi
Beğenin
8. SINIF BASİT MAKİNELER-MAKARALAR
8. SINIF BASİT MAKİNELER-MAKARALAR
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
9.sınıf tarih ders notları
Yeni maarif modele uygundur
9. sınıf coğrafya ders notları
9. sınıf coğrafya ilk 3 ünitenin notları
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅