Kimyasal bileşikler, hayatımızın her alanında var olan temel yapı taşlarıdır.... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
534
•
Güncellendi May 4, 2026
•
⭐
@duhaliya
Kimyasal bileşikler, hayatımızın her alanında var olan temel yapı taşlarıdır.... Daha fazla göster




















Kimyasal formül, bir bileşiğin nasıl oluştuğunu gösterir. Bu formüller sayesinde bileşikteki elementlerin türünü ve her bir elementin atomlarının sayısını kolayca anlayabiliriz.
Örneğin H₂O formülü bize iki hidrojen atomu ve bir oksijen atomu içeren bir su molekülünü gösterir. Formüldeki alt indis sayıları, o elementten kaç atom bulunduğunu belirtir.
Kimyasal formüller, molekülleri adeta bir kimyasal "kısa kod" olarak gösterir ve karmaşık yapıları basitçe ifade etmemizi sağlar.
Dikkat! Formüllerdeki alt indis sayıları çok önemlidir. Örneğin H₂O₂ (hidrojen peroksit) ile H₂O (su) tamamen farklı özelliklere sahiptir!

Kimyasal bileşikleri iki ana gruba ayırabiliriz: iyonik bileşikler ve moleküler bileşikler.
İyonik bileşikler, pozitif yüklü iyonlar (katyonlar) ile negatif yüklü iyonların (anyonlar) elektrostatik çekim kuvvetleriyle bir araya gelmesiyle oluşur. Örneğin, sodyum klorür (NaCl) bir Na⁺ katyonu ve bir Cl⁻ anyonundan oluşur.
Magnezyum nitrat [Mg(NO₃)₂] gibi daha karmaşık iyonik bileşiklerde ise bir Mg²⁺ katyonu ve iki NO₃⁻ anyonu bulunur. Parantezler, nitrat iyonunun iki kez tekrarlandığını gösterir.
İpucu: İyonik bileşiklerde toplam pozitif yük, toplam negatif yüke her zaman eşittir. Yani bileşik her zaman elektriksel olarak nötrdür!

Moleküler bileşikler, atomların birbirine kovalent bağlarla bağlanarak oluşturduğu moleküllerden meydana gelir. Bu tür bileşiklerde atomlar arasında elektron paylaşımı gerçekleşir.
Su (H₂O), metan (CH₄) ve karbon dioksit (CO₂) en yaygın moleküler bileşik örnekleridir. Bu moleküllerde atomlar belirli bir düzende dizilmiştir ve her molekül ayrı bir birimdir.
Moleküler bileşikler genellikle oda sıcaklığında gaz veya sıvı halde bulunur ve düşük erime/kaynama noktalarına sahiptir. Bu özellikler, iyonik bileşiklerden farklıdır.
İyi Haber: Moleküler bileşiklerin formüllerini öğrenmek, kimyasal tepkimeleri anlamanızı kolaylaştıracak ve laboratuvar deneylerinizde size büyük avantaj sağlayacaktır!

Moleküler bileşikleri ifade etmek için üç farklı formül kullanırız: kaba formül, molekül formülü ve yapı formülü.
Her bir formül türü, bileşiğin farklı bir yönünü vurgular. Bir bileşiği tam olarak anlamak için bazen bu formül türlerinin hepsine ihtiyaç duyarız.
Bu formüller, moleküllerin kimyasal ve fiziksel özelliklerini anlamamızı sağlar ve laboratuvar çalışmalarında sıkça kullanılır.
Unutmayın: Sınavlarda genellikle bir molekülü farklı formüllerle ifade etmeniz istenebilir, bu yüzden her formül türünün ne anlattığını iyi bilmelisiniz!

Kaba formül, bir moleküldeki elementlerin türünü ve en basit (sadeleştirilmiş) oranını gösterir. Örneğin hidrazin (N₂H₄) için kaba formül NH₂'dir.
Molekül formülü, bir moleküldeki atomların gerçek sayılarını gösterir. Örneğin asetilsalisilik asit (aspirin) için molekül formülü CH₂O₄'tür.
Yapı formülü ise atomların birbirine nasıl bağlandığını gösterir. Atomlar arasındaki tek, ikili veya üçlü bağları, molekülün geometrisini ve atomların uzaydaki dizilişini anlamamızı sağlar.
Bilgi: Bazı moleküller aynı kaba formüle sahip olabilir ama farklı molekül formülleri ve yapıları olabilir. Bu farklı moleküllere "izomer" denir ve kimyasal özellikleri tamamen farklı olabilir!
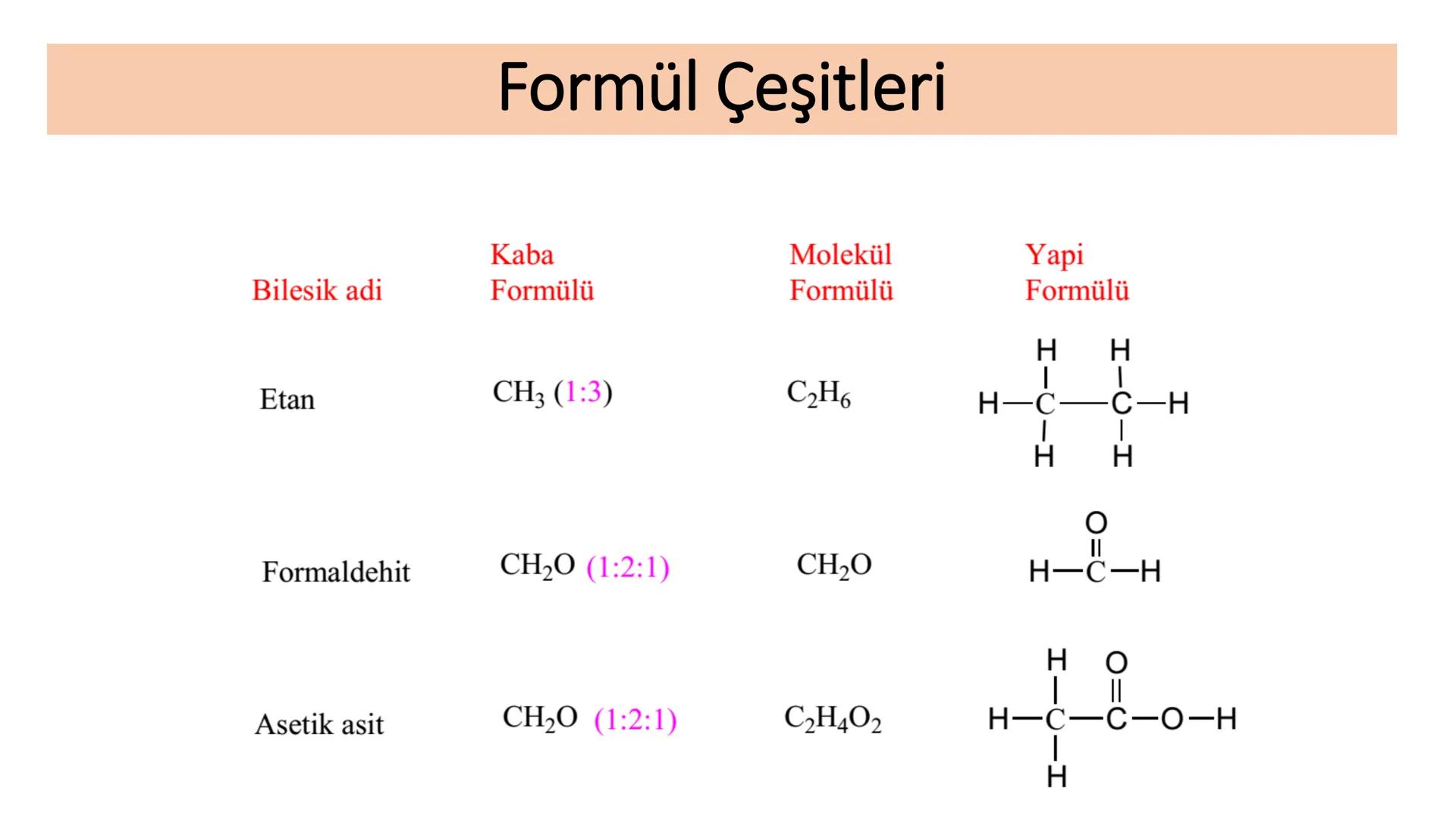
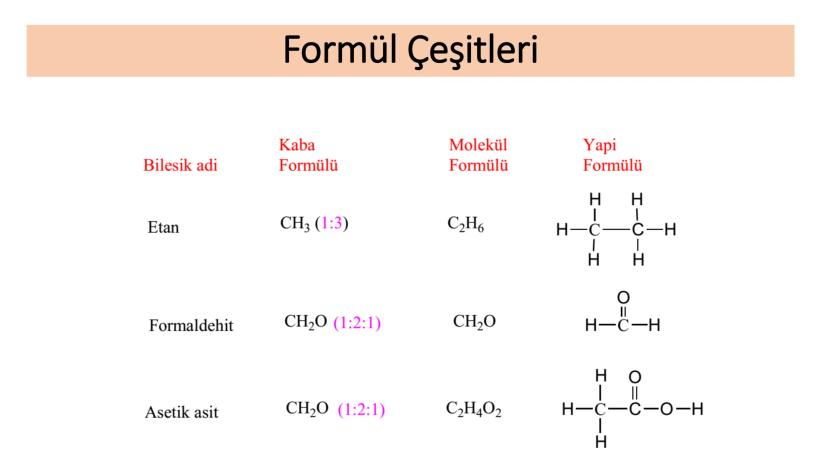
Etan molekülünün kaba formülü CH₃ (1:3 oranında karbon:hidrojen) iken, molekül formülü C₂H₆'dır. Yapı formülünde ise karbon atomları arasında tek bağ olduğunu ve her karbon atomuna üçer hidrojen bağlandığını görürüz.
Formaldehit için kaba formül CH₂O (1:2:1 oranında karbon:hidrojen:oksijen) iken, molekül formülü de aynıdır: CH₂O. Ancak yapı formülünde karbon ve oksijen arasında çift bağ olduğunu ve karbona iki hidrojen bağlandığını görürüz.
Asetik asit için kaba formül yine CH₂O iken, molekül formülü C₂H₄O₂'dir. Yapı formülünde ise daha karmaşık bir düzen görülür ve -COOH grubu (karboksil grubu) içerdiği anlaşılır.
Fark Yaratın: Aynı kaba formüle sahip formaldehit ve asetik asit tamamen farklı maddelerdir. Birincisi dezenfektan olarak kullanılırken, ikincisi sirkenin ana bileşenidir!
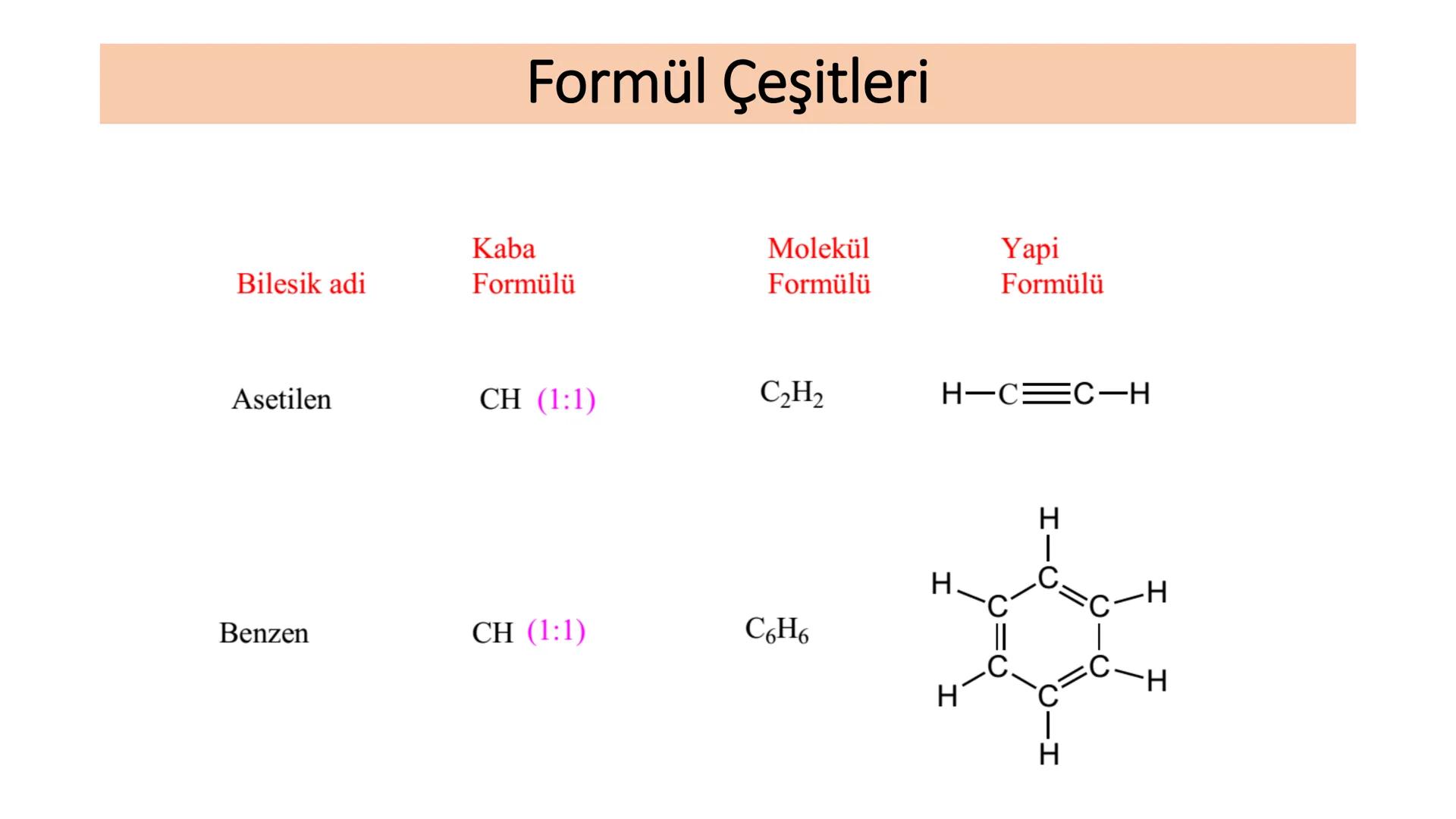
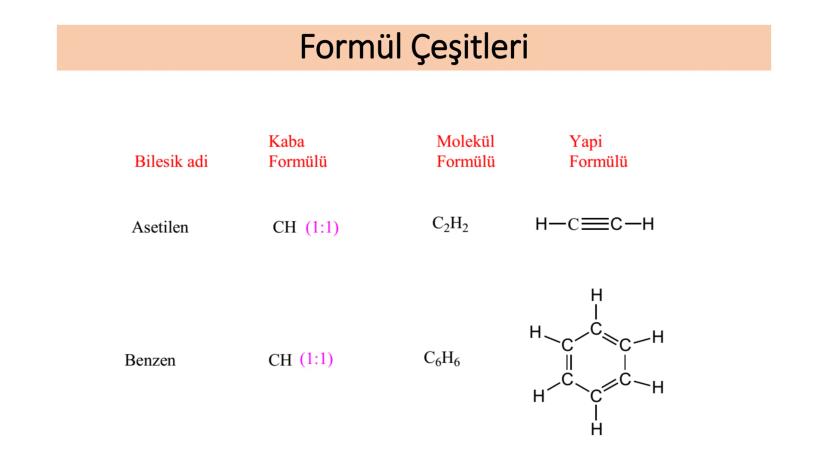
Asetilen molekülünün kaba formülü CH (1:1 oranında karbon:hidrojen) iken, molekül formülü C₂H₂'dir. Yapı formülünde ise karbon atomları arasında üçlü bağ olduğunu ve her karbon atomuna birer hidrojen bağlandığını görürüz.
Benzen için kaba formül CH (1:1 oranında karbon:hidrojen) iken, molekül formülü C₆H₆'dır. Yapı formülünde ise altı karbon atomunun halka şeklinde dizildiğini ve her karbon atomuna birer hidrojen bağlandığını görürüz.
Benzen halkası, organik kimyada çok önemli bir yapıdır ve aromatik bileşiklerin temel yapı taşıdır. Halka içindeki elektronların delokalize olması, benzene özel kararlılık kazandırır.
İlginç Bilgi: Benzenin yapısı 1865'te Friedrich August Kekulé tarafından bir rüya sonucunda bulunmuştur! Kekulé, rüyasında kendi kuyruğunu ısıran bir yılan görmüş ve bu ona benzen molekülünün halka yapısını ilham etmiştir.

Bir bileşiğin molekül kütlesi, yapısındaki her atomun molar kütlelerinin toplamına eşittir. Ma veya Mw sembolü ile gösterilir.
Hesaplama yapmak oldukça basittir: Moleküldeki her elementin atom kütlesini, o elementten kaç atom olduğuyla çarpıp toplarız. Örneğin CₓHᵧOᵣ bileşiğinin molekül kütlesi = g/mol şeklinde hesaplanır.
Asetik asit (C₂H₄O₂) için molekül kütlesi hesaplayalım: C: 2×12 = 24 g/mol H: 4×1 = 4 g/mol O: 2×16 = 32 g/mol Toplam: 60 g/mol
Pratik İpucu: Molekül kütlesi hesaplarken element sembollerinin altını çizip, karşılarına atom kütlelerini yazarak başlayın. Sonra her elementi sayısıyla çarpıp toplayın. Bu yöntem karmaşık moleküllerde bile hesaplama hatalarını önler!
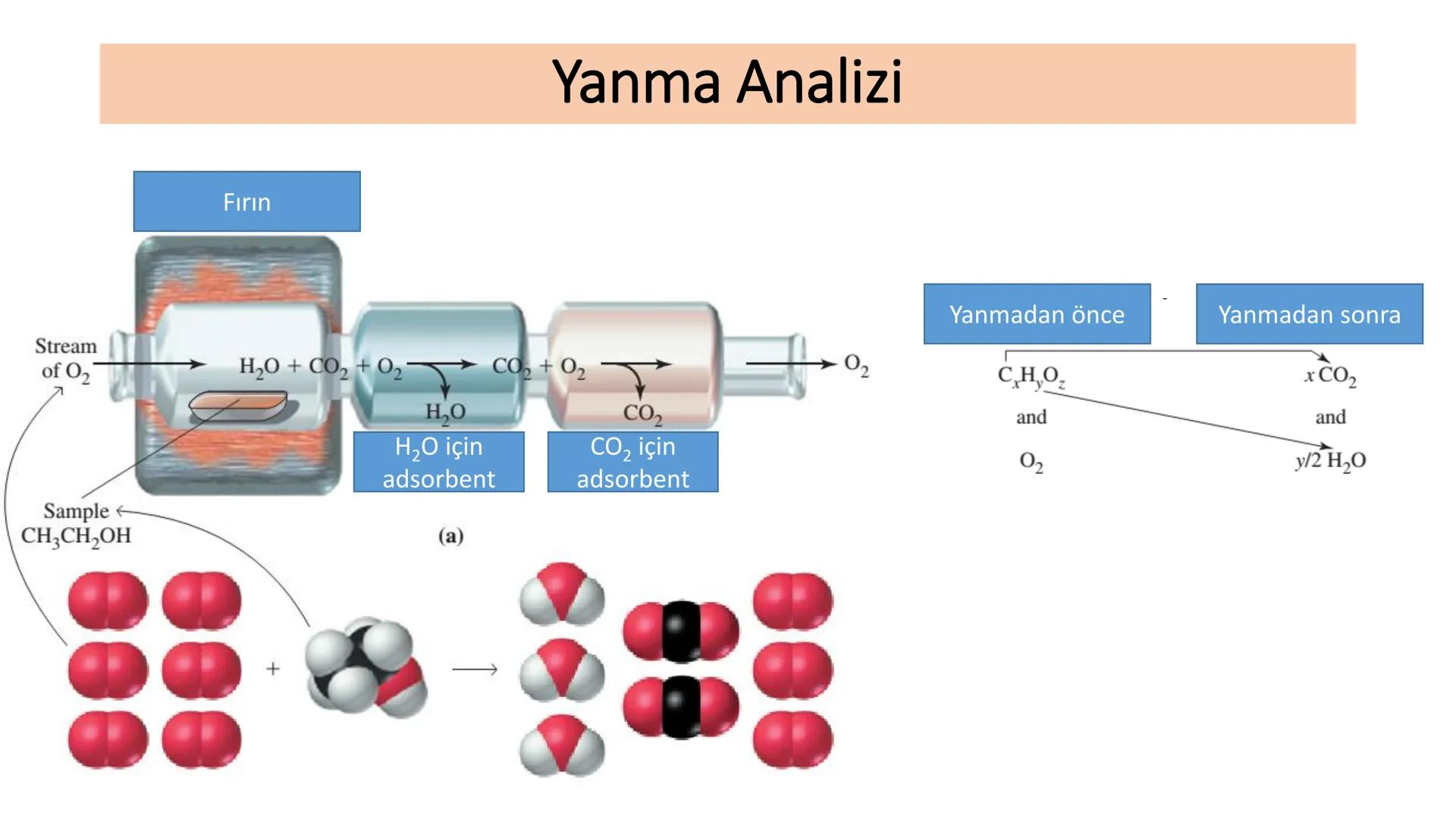
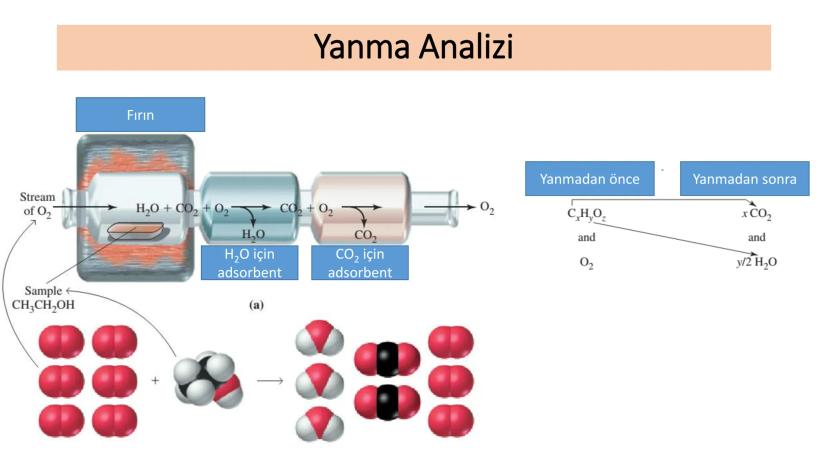
Yanma analizi, bir bileşikteki karbon, hidrojen ve oksijen miktarını belirlemek için kullanılan önemli bir tekniktir. Bu yöntemde, bileşik oksijen varlığında yakılır.
Yanma sırasında karbondan CO₂, hidrojenden H₂O oluşur. Oluşan bu ürünler özel adsorbentler tarafından tutulur ve miktarları ölçülür.
Ölçülen CO₂ ve H₂O miktarları kullanılarak, orijinal moleküldeki C ve H miktarları hesaplanabilir. Oksijen miktarı ise genellikle farktan bulunur.
Merak Edilenler: Yanma analizi, organik kimyanın gelişiminde çok önemli rol oynamıştır. Bilim insanları, bu yöntemle organik bileşiklerin yapılarını belirleyerek ilaç, kozmetik ve malzeme biliminde çığır açan keşifler yapmışlardır!

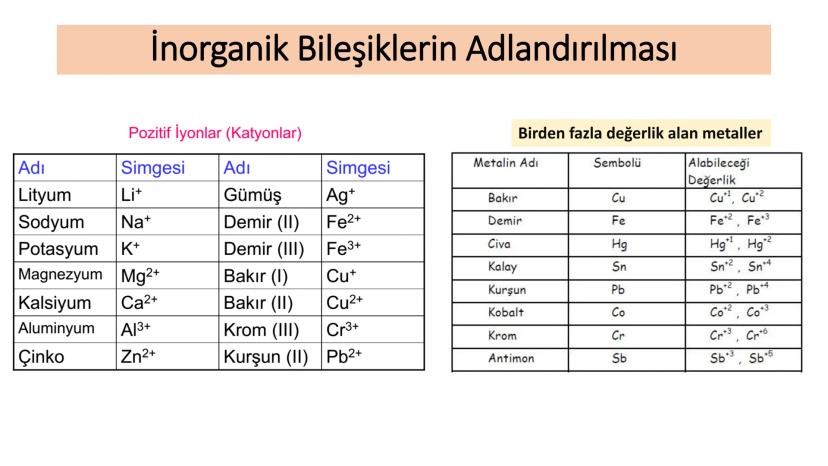
Kimyasal bileşikler, organik ve inorganik olarak iki ana gruba ayrılır. Bu ayrım, bileşiklerin yapısal özellikleri ve içerdikleri elementlere göre yapılır.
Organik bileşikler genellikle yapısında karbon (C), hidrojen (H), oksijen (O), azot (N) ve birkaç ametal atomu bulunduran bileşiklerdir. Canlı organizmalarda yaygın olarak bulunurlar.
İnorganik bileşikler ise bu tanımın dışında kalan bileşiklerdir. Metal oksitler, asitler, bazlar ve tuzlar gibi çeşitli bileşik gruplarını içerirler.
Önemli Not: Bazı karbon içeren bileşikler (CO₂, CO, karbonatlar gibi) inorganik kabul edilir. Organik-inorganik ayrımı sadece karbon varlığına değil, bileşiğin genel yapısına ve özelliklerine dayanır!












Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
⭐
@duhaliya
Kimyasal bileşikler, hayatımızın her alanında var olan temel yapı taşlarıdır. Formüllerinden adlandırılmalarına kadar kimyasal bileşiklerin nasıl tanımlandığını ve sınıflandırıldığını anlamak, kimya derslerindeki başarınız için kritik öneme sahiptir. Bu özette, kimyasal bileşik çeşitleri ve formülleri hakkında temel bilgileri bulacaksınız.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal formül, bir bileşiğin nasıl oluştuğunu gösterir. Bu formüller sayesinde bileşikteki elementlerin türünü ve her bir elementin atomlarının sayısını kolayca anlayabiliriz.
Örneğin H₂O formülü bize iki hidrojen atomu ve bir oksijen atomu içeren bir su molekülünü gösterir. Formüldeki alt indis sayıları, o elementten kaç atom bulunduğunu belirtir.
Kimyasal formüller, molekülleri adeta bir kimyasal "kısa kod" olarak gösterir ve karmaşık yapıları basitçe ifade etmemizi sağlar.
Dikkat! Formüllerdeki alt indis sayıları çok önemlidir. Örneğin H₂O₂ (hidrojen peroksit) ile H₂O (su) tamamen farklı özelliklere sahiptir!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal bileşikleri iki ana gruba ayırabiliriz: iyonik bileşikler ve moleküler bileşikler.
İyonik bileşikler, pozitif yüklü iyonlar (katyonlar) ile negatif yüklü iyonların (anyonlar) elektrostatik çekim kuvvetleriyle bir araya gelmesiyle oluşur. Örneğin, sodyum klorür (NaCl) bir Na⁺ katyonu ve bir Cl⁻ anyonundan oluşur.
Magnezyum nitrat [Mg(NO₃)₂] gibi daha karmaşık iyonik bileşiklerde ise bir Mg²⁺ katyonu ve iki NO₃⁻ anyonu bulunur. Parantezler, nitrat iyonunun iki kez tekrarlandığını gösterir.
İpucu: İyonik bileşiklerde toplam pozitif yük, toplam negatif yüke her zaman eşittir. Yani bileşik her zaman elektriksel olarak nötrdür!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Moleküler bileşikler, atomların birbirine kovalent bağlarla bağlanarak oluşturduğu moleküllerden meydana gelir. Bu tür bileşiklerde atomlar arasında elektron paylaşımı gerçekleşir.
Su (H₂O), metan (CH₄) ve karbon dioksit (CO₂) en yaygın moleküler bileşik örnekleridir. Bu moleküllerde atomlar belirli bir düzende dizilmiştir ve her molekül ayrı bir birimdir.
Moleküler bileşikler genellikle oda sıcaklığında gaz veya sıvı halde bulunur ve düşük erime/kaynama noktalarına sahiptir. Bu özellikler, iyonik bileşiklerden farklıdır.
İyi Haber: Moleküler bileşiklerin formüllerini öğrenmek, kimyasal tepkimeleri anlamanızı kolaylaştıracak ve laboratuvar deneylerinizde size büyük avantaj sağlayacaktır!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Moleküler bileşikleri ifade etmek için üç farklı formül kullanırız: kaba formül, molekül formülü ve yapı formülü.
Her bir formül türü, bileşiğin farklı bir yönünü vurgular. Bir bileşiği tam olarak anlamak için bazen bu formül türlerinin hepsine ihtiyaç duyarız.
Bu formüller, moleküllerin kimyasal ve fiziksel özelliklerini anlamamızı sağlar ve laboratuvar çalışmalarında sıkça kullanılır.
Unutmayın: Sınavlarda genellikle bir molekülü farklı formüllerle ifade etmeniz istenebilir, bu yüzden her formül türünün ne anlattığını iyi bilmelisiniz!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kaba formül, bir moleküldeki elementlerin türünü ve en basit (sadeleştirilmiş) oranını gösterir. Örneğin hidrazin (N₂H₄) için kaba formül NH₂'dir.
Molekül formülü, bir moleküldeki atomların gerçek sayılarını gösterir. Örneğin asetilsalisilik asit (aspirin) için molekül formülü CH₂O₄'tür.
Yapı formülü ise atomların birbirine nasıl bağlandığını gösterir. Atomlar arasındaki tek, ikili veya üçlü bağları, molekülün geometrisini ve atomların uzaydaki dizilişini anlamamızı sağlar.
Bilgi: Bazı moleküller aynı kaba formüle sahip olabilir ama farklı molekül formülleri ve yapıları olabilir. Bu farklı moleküllere "izomer" denir ve kimyasal özellikleri tamamen farklı olabilir!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Etan molekülünün kaba formülü CH₃ (1:3 oranında karbon:hidrojen) iken, molekül formülü C₂H₆'dır. Yapı formülünde ise karbon atomları arasında tek bağ olduğunu ve her karbon atomuna üçer hidrojen bağlandığını görürüz.
Formaldehit için kaba formül CH₂O (1:2:1 oranında karbon:hidrojen:oksijen) iken, molekül formülü de aynıdır: CH₂O. Ancak yapı formülünde karbon ve oksijen arasında çift bağ olduğunu ve karbona iki hidrojen bağlandığını görürüz.
Asetik asit için kaba formül yine CH₂O iken, molekül formülü C₂H₄O₂'dir. Yapı formülünde ise daha karmaşık bir düzen görülür ve -COOH grubu (karboksil grubu) içerdiği anlaşılır.
Fark Yaratın: Aynı kaba formüle sahip formaldehit ve asetik asit tamamen farklı maddelerdir. Birincisi dezenfektan olarak kullanılırken, ikincisi sirkenin ana bileşenidir!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Asetilen molekülünün kaba formülü CH (1:1 oranında karbon:hidrojen) iken, molekül formülü C₂H₂'dir. Yapı formülünde ise karbon atomları arasında üçlü bağ olduğunu ve her karbon atomuna birer hidrojen bağlandığını görürüz.
Benzen için kaba formül CH (1:1 oranında karbon:hidrojen) iken, molekül formülü C₆H₆'dır. Yapı formülünde ise altı karbon atomunun halka şeklinde dizildiğini ve her karbon atomuna birer hidrojen bağlandığını görürüz.
Benzen halkası, organik kimyada çok önemli bir yapıdır ve aromatik bileşiklerin temel yapı taşıdır. Halka içindeki elektronların delokalize olması, benzene özel kararlılık kazandırır.
İlginç Bilgi: Benzenin yapısı 1865'te Friedrich August Kekulé tarafından bir rüya sonucunda bulunmuştur! Kekulé, rüyasında kendi kuyruğunu ısıran bir yılan görmüş ve bu ona benzen molekülünün halka yapısını ilham etmiştir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bir bileşiğin molekül kütlesi, yapısındaki her atomun molar kütlelerinin toplamına eşittir. Ma veya Mw sembolü ile gösterilir.
Hesaplama yapmak oldukça basittir: Moleküldeki her elementin atom kütlesini, o elementten kaç atom olduğuyla çarpıp toplarız. Örneğin CₓHᵧOᵣ bileşiğinin molekül kütlesi = g/mol şeklinde hesaplanır.
Asetik asit (C₂H₄O₂) için molekül kütlesi hesaplayalım: C: 2×12 = 24 g/mol H: 4×1 = 4 g/mol O: 2×16 = 32 g/mol Toplam: 60 g/mol
Pratik İpucu: Molekül kütlesi hesaplarken element sembollerinin altını çizip, karşılarına atom kütlelerini yazarak başlayın. Sonra her elementi sayısıyla çarpıp toplayın. Bu yöntem karmaşık moleküllerde bile hesaplama hatalarını önler!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Yanma analizi, bir bileşikteki karbon, hidrojen ve oksijen miktarını belirlemek için kullanılan önemli bir tekniktir. Bu yöntemde, bileşik oksijen varlığında yakılır.
Yanma sırasında karbondan CO₂, hidrojenden H₂O oluşur. Oluşan bu ürünler özel adsorbentler tarafından tutulur ve miktarları ölçülür.
Ölçülen CO₂ ve H₂O miktarları kullanılarak, orijinal moleküldeki C ve H miktarları hesaplanabilir. Oksijen miktarı ise genellikle farktan bulunur.
Merak Edilenler: Yanma analizi, organik kimyanın gelişiminde çok önemli rol oynamıştır. Bilim insanları, bu yöntemle organik bileşiklerin yapılarını belirleyerek ilaç, kozmetik ve malzeme biliminde çığır açan keşifler yapmışlardır!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal bileşikler, organik ve inorganik olarak iki ana gruba ayrılır. Bu ayrım, bileşiklerin yapısal özellikleri ve içerdikleri elementlere göre yapılır.
Organik bileşikler genellikle yapısında karbon (C), hidrojen (H), oksijen (O), azot (N) ve birkaç ametal atomu bulunduran bileşiklerdir. Canlı organizmalarda yaygın olarak bulunurlar.
İnorganik bileşikler ise bu tanımın dışında kalan bileşiklerdir. Metal oksitler, asitler, bazlar ve tuzlar gibi çeşitli bileşik gruplarını içerirler.
Önemli Not: Bazı karbon içeren bileşikler (CO₂, CO, karbonatlar gibi) inorganik kabul edilir. Organik-inorganik ayrımı sadece karbon varlığına değil, bileşiğin genel yapısına ve özelliklerine dayanır!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
9
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı