Periyodik tablo kimyanın temelini oluşturan ve elementleri sistematik bir şekilde... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
961
•
Güncellendi May 20, 2026
•
Rukiye Türkyılmaz
@rukiyetrk_w27p0
Periyodik tablo kimyanın temelini oluşturan ve elementleri sistematik bir şekilde... Daha fazla göster















Sen de kimya dersinde neden bu kadar çok element var ve bunları nasıl ezberleyeceğin konusunda endişe duymuş olabilirsin. İşte periyodik tablo tam da bu sorunu çözmek için var! Tıpkı canlıları sınıflandırdığımız gibi, elementleri de özelliklerine göre gruplandırabiliriz.
Mendeleyev adında bir bilim insanı, elementlerin özelliklerinin belirli aralıklarla tekrarladığını fark etti. O zamanlar henüz keşfedilmemiş elementler için bile yer ayırdı ve özelliklerini tahmin etti - tahminleri de çok tuttu! Örneğin Germanyum elementinin özelliklerini 17 yıl önceden doğru olarak tahmin etmişti.
Daha sonra Henry Moseley, elementlerin asıl önemli olanının atom numarası olduğunu keşfetti. Bu yüzden günümüzde periyodik tablo elementleri artan atom numaralarına göre sıralıyor.
Pratik İpucu: Periyodik tablodaki yatay sıralar periyot (7 tane), dikey sütunlar ise grup adını alır.
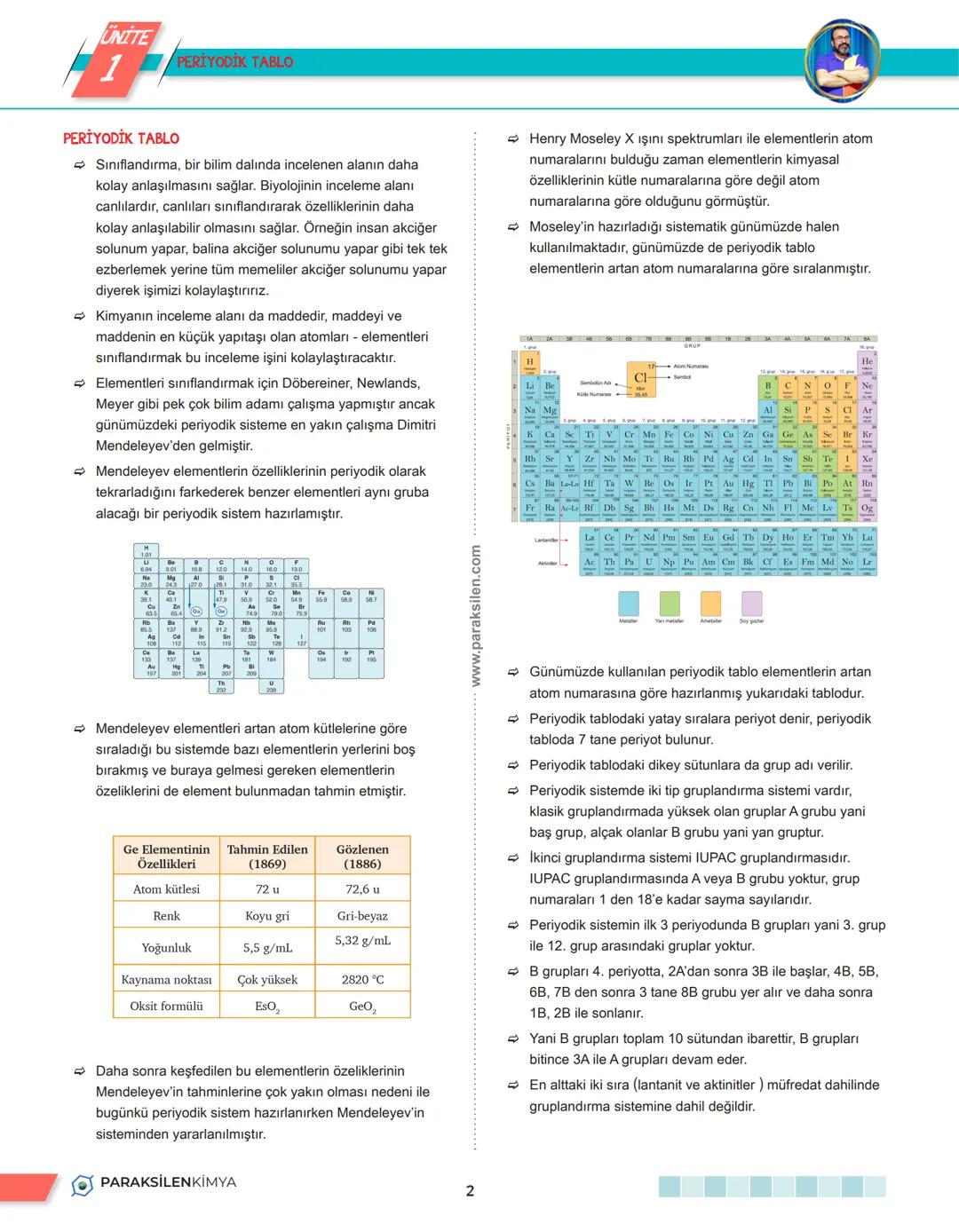
Bir elementin periyodik tablodaki yerini bulmak aslında çok basit - sadece elektron dizilimini yazman yeterli! Nötr ve temel hal elektron dizilimi yapacaksın, uyarılmış hallerle uğraşmana gerek yok.
Periyot numarası: Elektron dizilimindeki en yüksek enerji düzeyi (en büyük sayı) periyot numarasını verir. Örneğin 1s²2s²2p⁶3s² diziliminde en yüksek enerji düzeyi 3 olduğu için element 3. periyotta.
Grup numarası: Son harf s veya p ise, o orbitallerle birlikte en son s'teki elektronları topla. Örneğin 1s²2s²2p⁶3s² diziliminde grup numarası 2 (3s²'den). Son harf d ise farklı hesaplama var - B grubu elementleri için 3d'teki elektronlarla 4s'teki elektronları topla.
Önemli: s veya p ile bitenler A grubu, d ile bitenler B grubu elementleridir. Bu ayrım çok önemli çünkü özellikleri farklı!

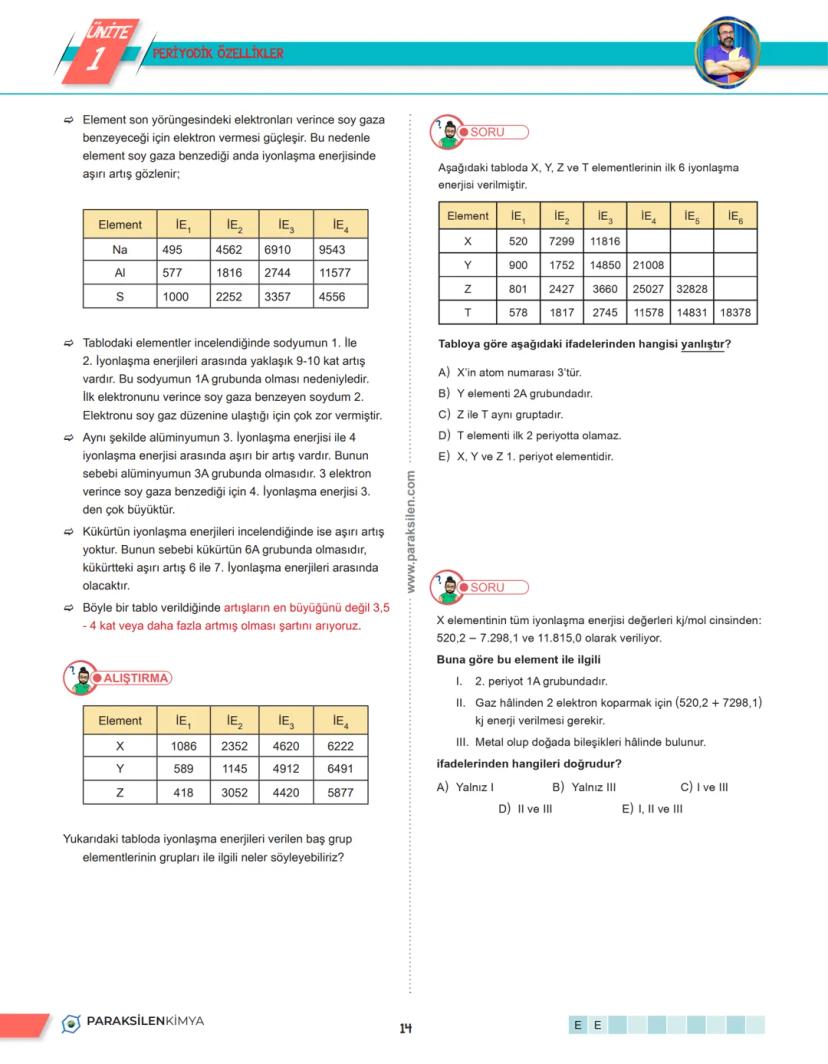
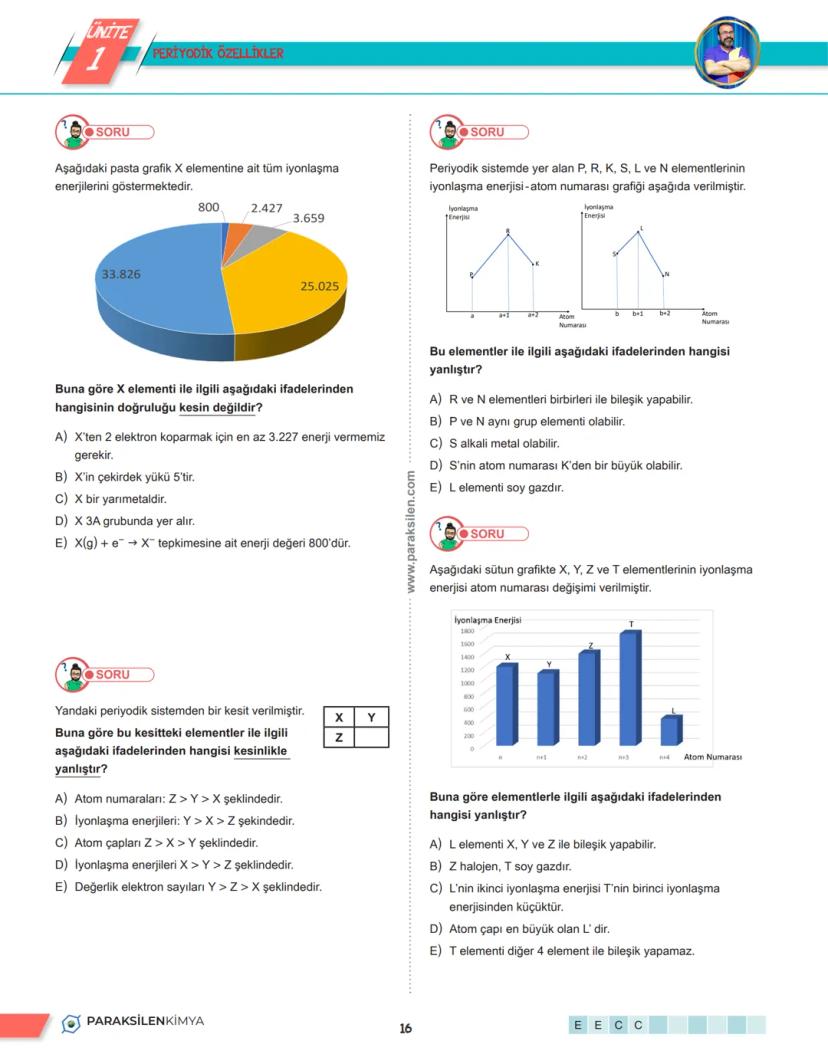
Periyodik tablodaki bazı grupların özel isimleri var ve bunları bilmen gerekiyor. Bu gruplar benzer kimyasal özellikler gösterdiği için ayrı isimler almış.
1A Grubu - Alkali Metaller: Hidrojen hariç hepsi metal ve çok aktif. Suyla tepkime verip H₂ gazı çıkarırlar - hatta bazen alev ve patlama bile olur! Tüm bileşiklerinde +1 yük alırlar.
2A Grubu - Toprak Alkali Metaller: Beryonyum hariç suyla tepkime verirler ama alkali metallerden daha az aktif. Tüm bileşiklerinde +2 yük alırlar.
7A Grubu - Halojenler: En aktif ametaller burada. F₂ ve Cl₂ gaz, Br₂ sıvı, diğerleri katı. Flor her zaman -1, diğerleri -1 ile +7 arasında değerlik alabilir.
Hatırlatma: 8A Grubu soygazlar - çok kararlı oldukları için tepkimeye girmek istemezler. He hariç hepsinin dış kabuğunda 8 elektron var.

Kimyasal olaylarda atomların çekirdeği değişmez, sadece valans elektronları (en dış kabukta bulunanlar) hareket eder. Bu elektronları verip alan atomlar iyon haline geçer.
Elektron verirse: Negatif yük dışarı çıkar, atom içinde pozitif yük fazla kalır → katyon oluşur. Örnek: Na → Na⁺ + e⁻
Elektron alırsa: Negatif yük içeri girer, atom içinde negatif yük fazla olur → anyon oluşur. Örnek: Cl + e⁻ → Cl⁻
İyon yükünü hesaplamak kolay: verdiği elektron sayısı kadar pozitif, aldığı elektron sayısı kadar negatif yük kazanır. X atomu 2 elektron verip 1 elektron alırsa, net olarak +1 yüklü olur.
Pratik Kural: İyon yükü = Verilen elektron sayısı - Alınan elektron sayısı

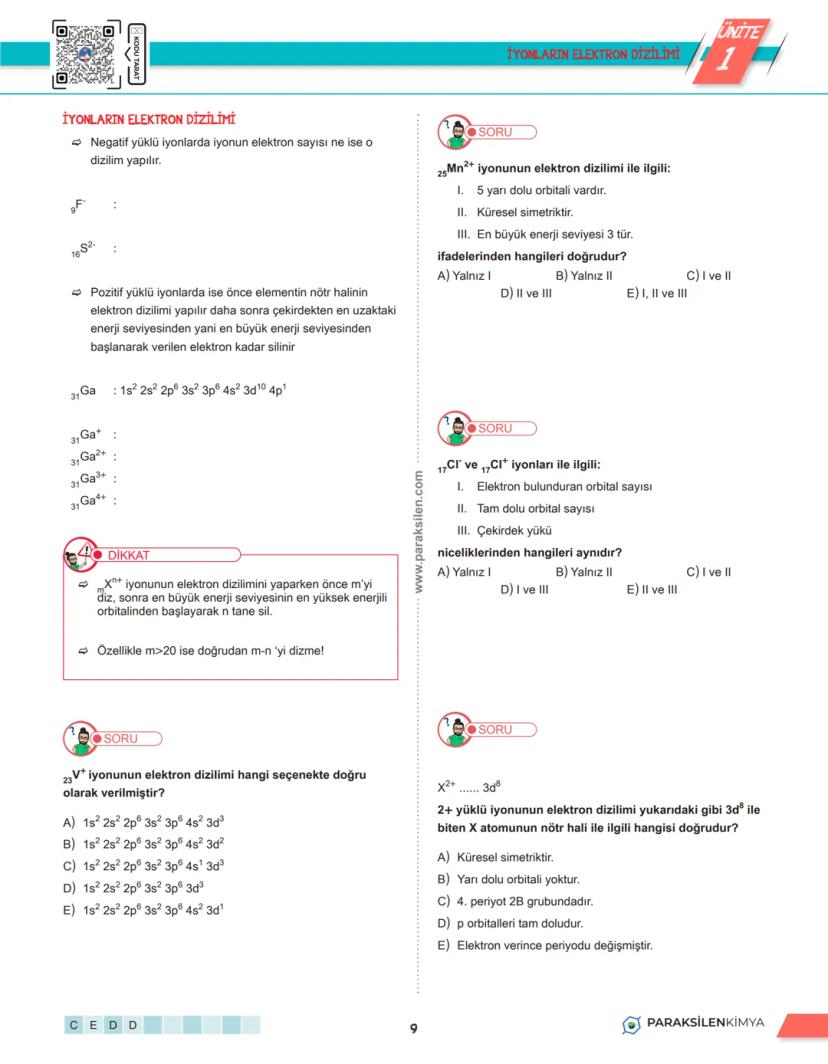
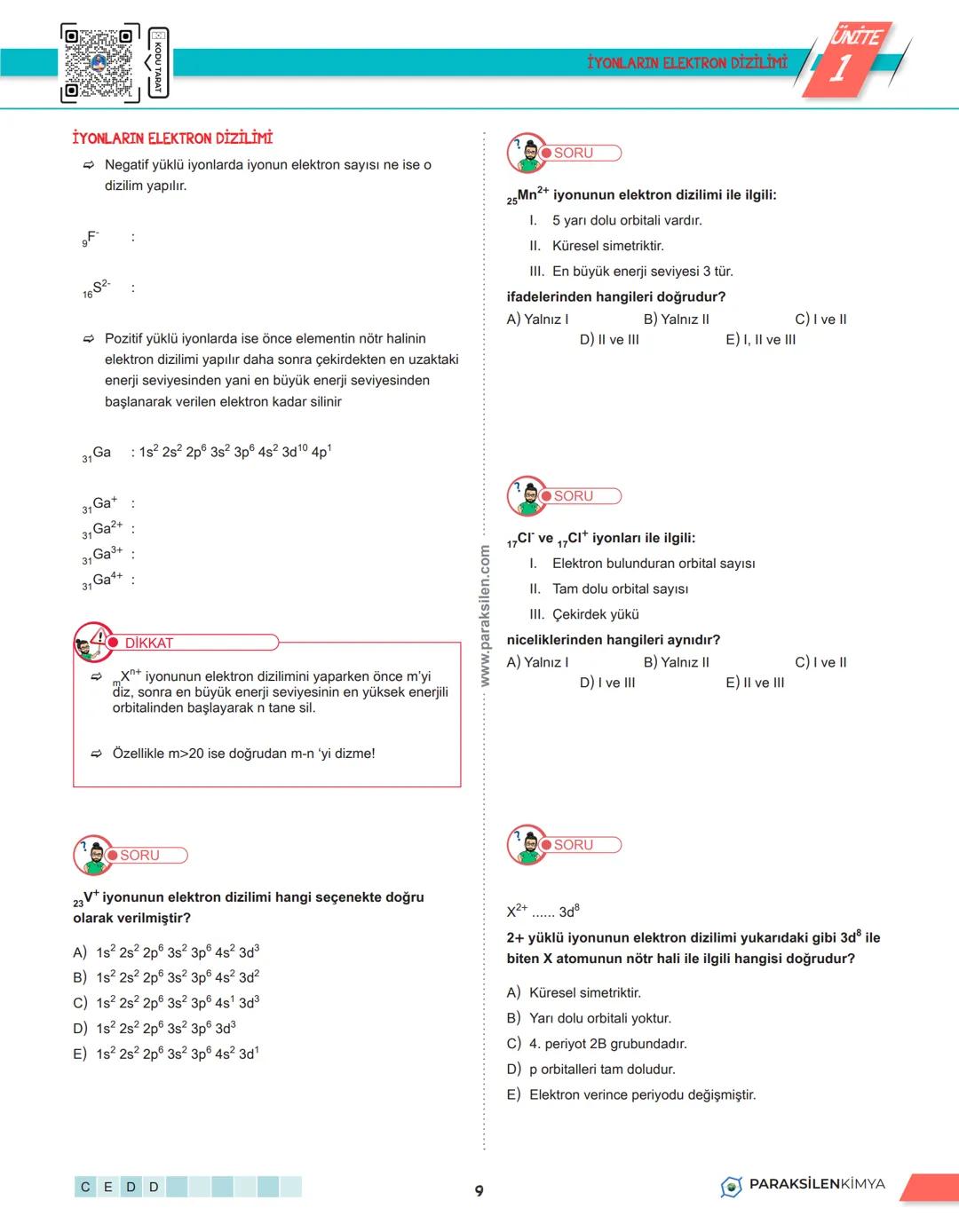
İyonların elektron dizilimini yaparken dikkatli olmalısın çünkü elektronlar belirli kurallara göre silinir ya da eklenir.
Negatif iyonlar (anyonlar): Çok basit - kaç elektronu varsa o sayı için elektron dizilimi yap. F⁻ iyonunun 10 elektronu var, 10 elektron için dizilim yap: 1s²2s²2p⁶
Pozitif iyonlar (katyonlar): Önce nötr atomun elektron dizilimini yap, sonra en büyük enerji seviyesinden başlayarak elektronları sil. Na⁺ için: Na'nın dizilimi 1s²2s²2p⁶3s¹, bir elektron silince 1s²2s²2p⁶ kalır.
Geçiş metalleri: d-bloku elementlerinde önce s orbitalinden, sonra d orbitalinden elektronlar silinir. Örneğin Fe²⁺ için önce 4s'ten 2 elektron, Fe³⁺ için 4s'ten 2, 3d'den 1 elektron silinir.
İpucu: Atom numarası 20'den büyükse doğrudan elektron sayısı için dizilim yapmaya çalışma, her zaman kuralı uygula!

İzoelektronik tanecikler elektron sayıları aynı ama proton sayıları farklı olan tanecikler. Bu taneciklerin elektron dizilimleri aynı olduğu için bazı özellikler benzerlik gösterir.
Örnek izoelektronik tanecikler: Ca²⁺, Ar, Cl⁻ - hepsinin 18 elektronu var ve elektron dizilimleri 1s²2s²2p⁶3s²2p⁶ şeklinde.
Bu tanecikleri bulmak için şu adımları izle: önce her bir tanecik için elektron sayısını hesapla (nötr atom için atom numarası, iyon için ±iyon yükü), sonra elektron sayıları aynı olanları belirle.
Önemli olan nokta: izoelektronik taneciklerin elektron dizilimleri aynı olsa da fiziksel ve kimyasal özellikleri farklıdır. Çünkü çekirdeklerindeki proton sayıları farklı!
Sınav İpucu: İzoelektronik tanecik soruları sık çıkar. Her tanecik için elektron sayısını doğru hesaplamayı mutlaka öğren.








Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Rukiye Türkyılmaz
@rukiyetrk_w27p0
Periyodik tablo kimyanın temelini oluşturan ve elementleri sistematik bir şekilde düzenleyen en önemli araçlardan biri. Elementlerin özelliklerini anlamamızı kolaylaştıran bu sistem sayesinde, yüzlerce elementin davranışını öngörebiliyor ve kimyasal olayları çok daha kolay açıklayabiliyoruz.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Sen de kimya dersinde neden bu kadar çok element var ve bunları nasıl ezberleyeceğin konusunda endişe duymuş olabilirsin. İşte periyodik tablo tam da bu sorunu çözmek için var! Tıpkı canlıları sınıflandırdığımız gibi, elementleri de özelliklerine göre gruplandırabiliriz.
Mendeleyev adında bir bilim insanı, elementlerin özelliklerinin belirli aralıklarla tekrarladığını fark etti. O zamanlar henüz keşfedilmemiş elementler için bile yer ayırdı ve özelliklerini tahmin etti - tahminleri de çok tuttu! Örneğin Germanyum elementinin özelliklerini 17 yıl önceden doğru olarak tahmin etmişti.
Daha sonra Henry Moseley, elementlerin asıl önemli olanının atom numarası olduğunu keşfetti. Bu yüzden günümüzde periyodik tablo elementleri artan atom numaralarına göre sıralıyor.
Pratik İpucu: Periyodik tablodaki yatay sıralar periyot (7 tane), dikey sütunlar ise grup adını alır.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bir elementin periyodik tablodaki yerini bulmak aslında çok basit - sadece elektron dizilimini yazman yeterli! Nötr ve temel hal elektron dizilimi yapacaksın, uyarılmış hallerle uğraşmana gerek yok.
Periyot numarası: Elektron dizilimindeki en yüksek enerji düzeyi (en büyük sayı) periyot numarasını verir. Örneğin 1s²2s²2p⁶3s² diziliminde en yüksek enerji düzeyi 3 olduğu için element 3. periyotta.
Grup numarası: Son harf s veya p ise, o orbitallerle birlikte en son s'teki elektronları topla. Örneğin 1s²2s²2p⁶3s² diziliminde grup numarası 2 (3s²'den). Son harf d ise farklı hesaplama var - B grubu elementleri için 3d'teki elektronlarla 4s'teki elektronları topla.
Önemli: s veya p ile bitenler A grubu, d ile bitenler B grubu elementleridir. Bu ayrım çok önemli çünkü özellikleri farklı!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Periyodik tablodaki bazı grupların özel isimleri var ve bunları bilmen gerekiyor. Bu gruplar benzer kimyasal özellikler gösterdiği için ayrı isimler almış.
1A Grubu - Alkali Metaller: Hidrojen hariç hepsi metal ve çok aktif. Suyla tepkime verip H₂ gazı çıkarırlar - hatta bazen alev ve patlama bile olur! Tüm bileşiklerinde +1 yük alırlar.
2A Grubu - Toprak Alkali Metaller: Beryonyum hariç suyla tepkime verirler ama alkali metallerden daha az aktif. Tüm bileşiklerinde +2 yük alırlar.
7A Grubu - Halojenler: En aktif ametaller burada. F₂ ve Cl₂ gaz, Br₂ sıvı, diğerleri katı. Flor her zaman -1, diğerleri -1 ile +7 arasında değerlik alabilir.
Hatırlatma: 8A Grubu soygazlar - çok kararlı oldukları için tepkimeye girmek istemezler. He hariç hepsinin dış kabuğunda 8 elektron var.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal olaylarda atomların çekirdeği değişmez, sadece valans elektronları (en dış kabukta bulunanlar) hareket eder. Bu elektronları verip alan atomlar iyon haline geçer.
Elektron verirse: Negatif yük dışarı çıkar, atom içinde pozitif yük fazla kalır → katyon oluşur. Örnek: Na → Na⁺ + e⁻
Elektron alırsa: Negatif yük içeri girer, atom içinde negatif yük fazla olur → anyon oluşur. Örnek: Cl + e⁻ → Cl⁻
İyon yükünü hesaplamak kolay: verdiği elektron sayısı kadar pozitif, aldığı elektron sayısı kadar negatif yük kazanır. X atomu 2 elektron verip 1 elektron alırsa, net olarak +1 yüklü olur.
Pratik Kural: İyon yükü = Verilen elektron sayısı - Alınan elektron sayısı

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
İyonların elektron dizilimini yaparken dikkatli olmalısın çünkü elektronlar belirli kurallara göre silinir ya da eklenir.
Negatif iyonlar (anyonlar): Çok basit - kaç elektronu varsa o sayı için elektron dizilimi yap. F⁻ iyonunun 10 elektronu var, 10 elektron için dizilim yap: 1s²2s²2p⁶
Pozitif iyonlar (katyonlar): Önce nötr atomun elektron dizilimini yap, sonra en büyük enerji seviyesinden başlayarak elektronları sil. Na⁺ için: Na'nın dizilimi 1s²2s²2p⁶3s¹, bir elektron silince 1s²2s²2p⁶ kalır.
Geçiş metalleri: d-bloku elementlerinde önce s orbitalinden, sonra d orbitalinden elektronlar silinir. Örneğin Fe²⁺ için önce 4s'ten 2 elektron, Fe³⁺ için 4s'ten 2, 3d'den 1 elektron silinir.
İpucu: Atom numarası 20'den büyükse doğrudan elektron sayısı için dizilim yapmaya çalışma, her zaman kuralı uygula!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
İzoelektronik tanecikler elektron sayıları aynı ama proton sayıları farklı olan tanecikler. Bu taneciklerin elektron dizilimleri aynı olduğu için bazı özellikler benzerlik gösterir.
Örnek izoelektronik tanecikler: Ca²⁺, Ar, Cl⁻ - hepsinin 18 elektronu var ve elektron dizilimleri 1s²2s²2p⁶3s²2p⁶ şeklinde.
Bu tanecikleri bulmak için şu adımları izle: önce her bir tanecik için elektron sayısını hesapla (nötr atom için atom numarası, iyon için ±iyon yükü), sonra elektron sayıları aynı olanları belirle.
Önemli olan nokta: izoelektronik taneciklerin elektron dizilimleri aynı olsa da fiziksel ve kimyasal özellikleri farklıdır. Çünkü çekirdeklerindeki proton sayıları farklı!
Sınav İpucu: İzoelektronik tanecik soruları sık çıkar. Her tanecik için elektron sayısını doğru hesaplamayı mutlaka öğren.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
4
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı