İndirgenme-yükseltgenme (redoks) tepkimeleri, elektron alışverişi sonucunda gerçekleşen kimyasal olaylardır. Bu... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
393
•
Güncellendi May 7, 2026
•
MelekCheonsa
@juliannecandy
İndirgenme-yükseltgenme (redoks) tepkimeleri, elektron alışverişi sonucunda gerçekleşen kimyasal olaylardır. Bu... Daha fazla göster


























Bir atom ya da iyonun elektron almasına indirgenme denir. İndirgenme gerçekleştiğinde taneciğin yükseltgenme basamağı (değeri) küçülür. Örneğin çinko iyonu elektron aldığında, elementel çinkoya dönüşür.
İndirgenme yarı tepkimelerine örnekler:
💡 İndirgenme olayını hatırlamanın kolay bir yolu: Elektron alan taneciğin yükü azalır, yani sayısal olarak küçülür!

Bir atom ya da iyonun elektron vermesine yükseltgenme denir. Yükseltgenme gerçekleştiğinde taneciğin yükseltgenme basamağı büyür. Örneğin hidrojen gazı elektron verdiğinde, hidrojen iyonuna dönüşür.
Yükseltgenme yarı tepkimelerine örnekler:
Günlük hayatta gördüğümüz birçok olay aslında redoks tepkimesidir. Odunun yanması, metallerin paslanması ve bileşiklerin elementlerine ayrışması bu tür tepkimelere örnektir.

İndirgenme ve yükseltgenme yarı tepkimelerinin toplamından oluşan tepkimelere indirgenme-yükseltgenme (redoks) tepkimesi denir. Bu tepkimelerde alınan ve verilen elektron sayıları daima eşittir.
"Redoks" kelimesi, "redüksiyon" (indirgenme) ve "oksidasyon" (yükseltgenme) kelimelerinin birleşiminden gelir ve elektron alışverişinin gerçekleştiği tepkimeler için kullanılır.
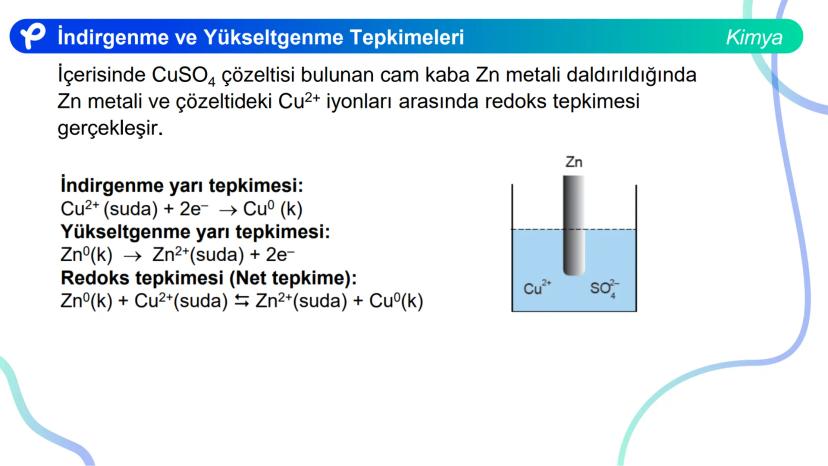
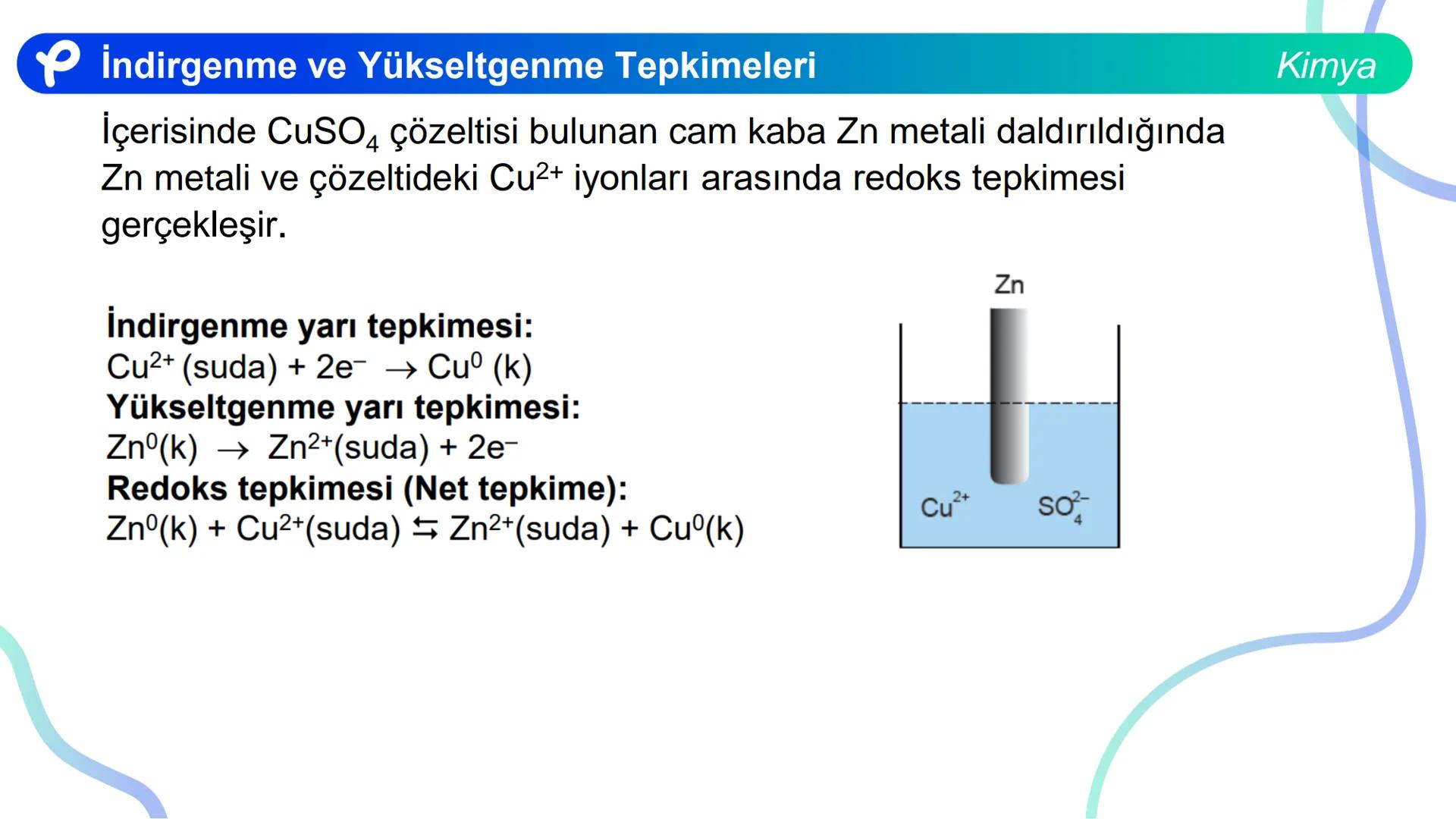
Örnek bir redoks tepkimesi: Çinko metali, bakır sülfat çözeltisine daldırıldığında gerçekleşen tepkime:
İndirgenme: Yükseltgenme: Net tepkime:

Elektron alarak indirgenen taneciklere yükseltgen, elektron vererek yükseltgenen taneciklere ise indirgen denir. Yükseltgenler bir tepkimede elektron alır ve kendileri indirgenir. İndirgenler ise elektron verir ve kendileri yükseltgenir.
O₂, KMnO₄, H₂SO₄, HNO₃ ve H₂O₂ yaygın kullanılan yükseltgenlerdir. Bu maddeler redoks tepkimelerinde elektron alarak indirgendiklerinden yükseltgen özelliği gösterir.
Örneğin:
🔑 Unutmayın: Bir redoks tepkimesinde yükseltgen madde indirgenir, indirgen madde ise yükseltgenir.

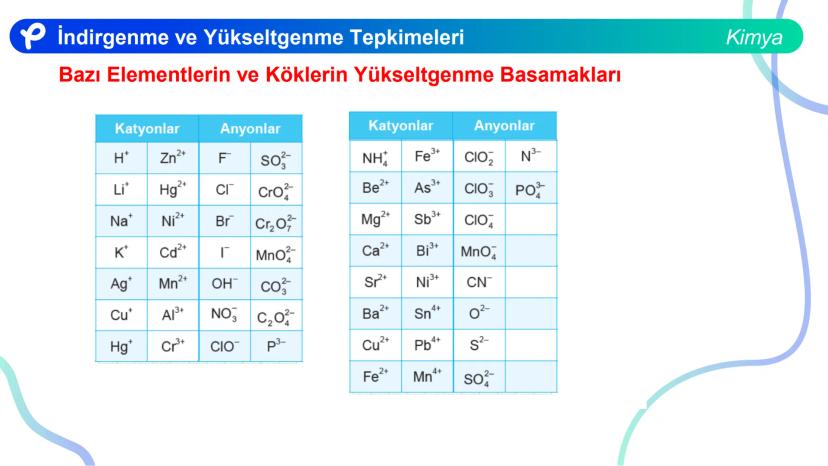
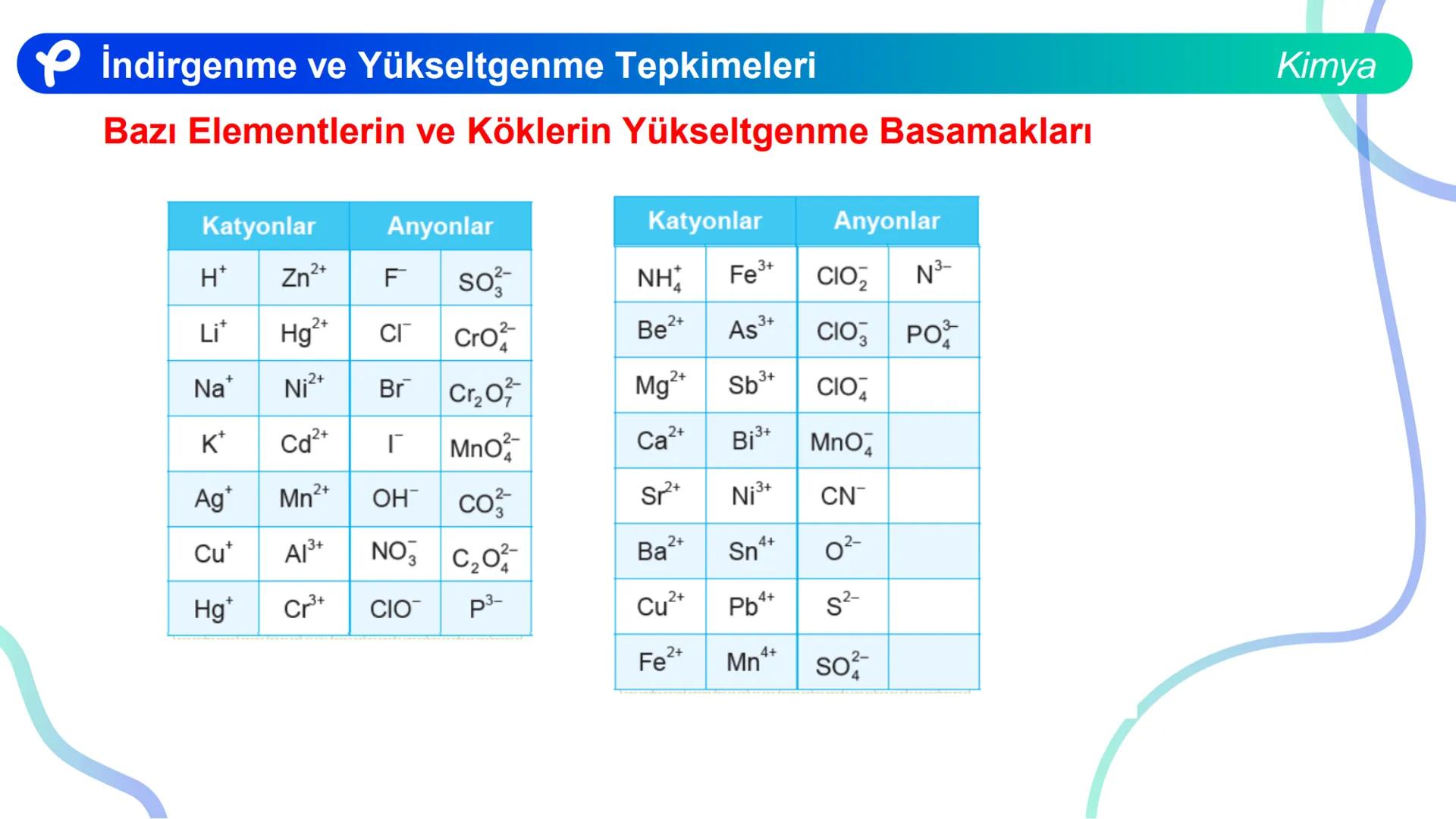
Bir atom ya da iyonun tek başına veya bileşik içerisinde sahip olduğu yüke, o taneciğin yükseltgenme basamağı denir. Bir taneciğin indirgendiği ya da yükseltgendiği, yükseltgenme basamağındaki değişime bakılarak anlaşılır.
Yükseltgenme basamaklarını belirlerken kullanılan temel kurallar:
Bir bileşikteki atomların yükseltgenme basamakları toplamı her zaman sıfıra eşittir.
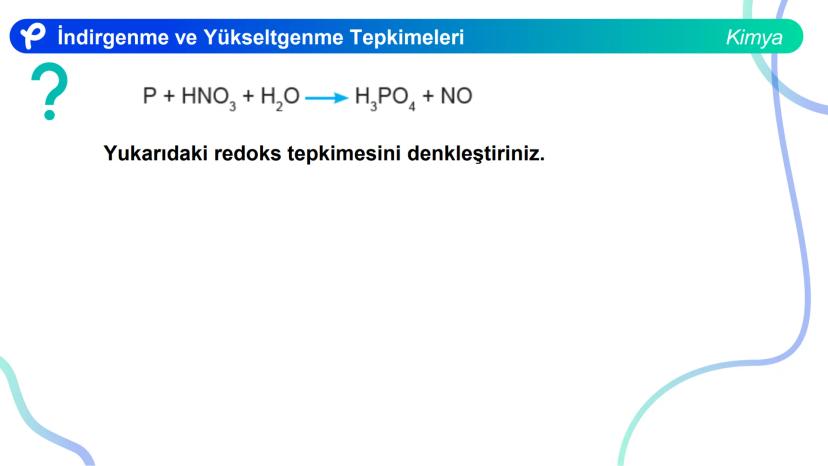
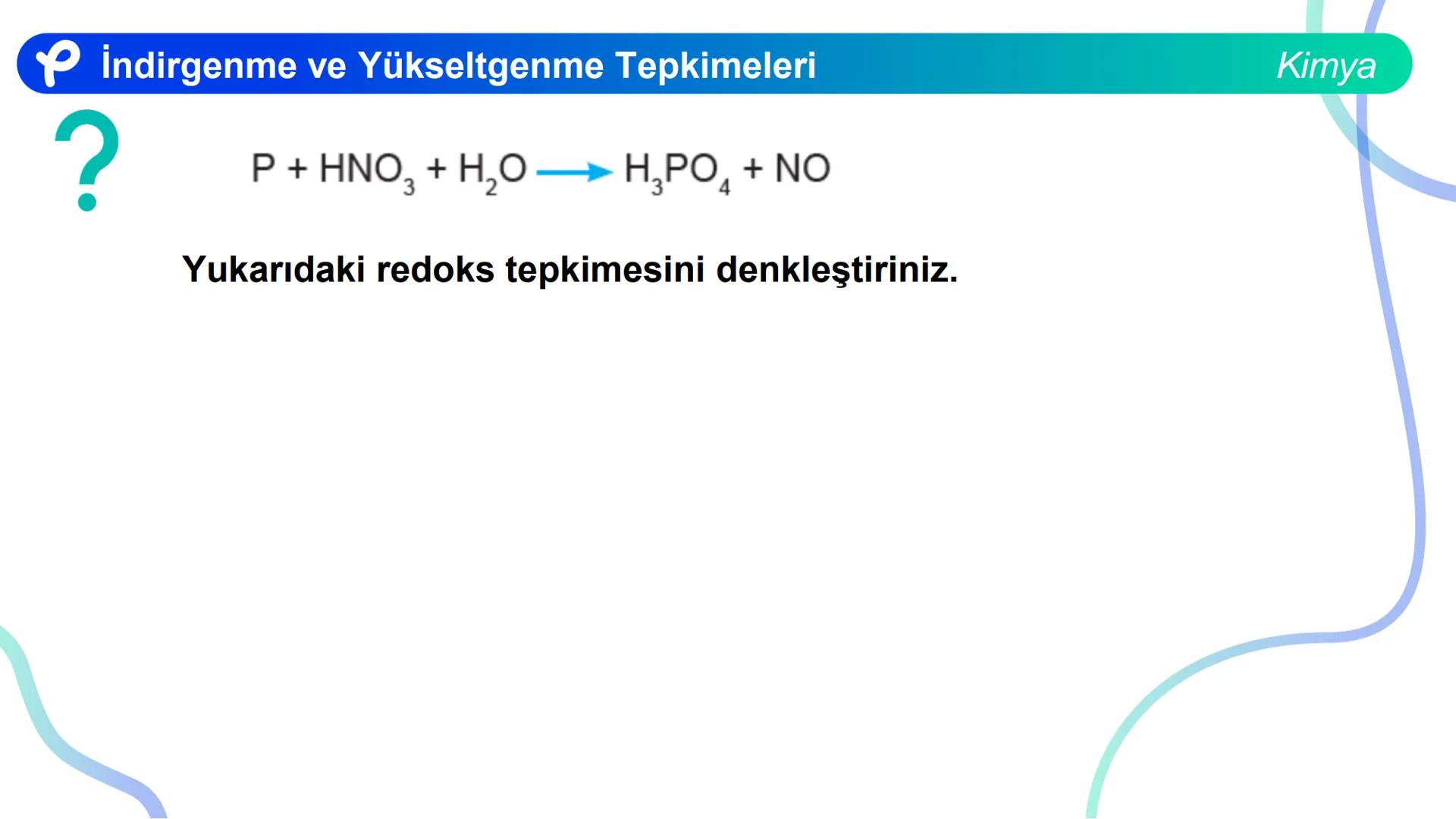
Redoks tepkimelerini denkleştirirken şu adımları izlemelisiniz:
Örnek: Cu + H₂SO₄ → CuSO₄ + SO₂ + H₂O tepkimesini denkleştirirken, önce Cu ve S elementlerinin yükseltgenme basamaklarının değiştiğini belirleyip, ardından elektron sayılarını eşitleyerek denkleştirme yapılır.
💡 Denkleştirme yaparken, atomların toplam sayısı ve yüklerin toplamı tepkimenin her iki tarafında eşit olmalıdır!

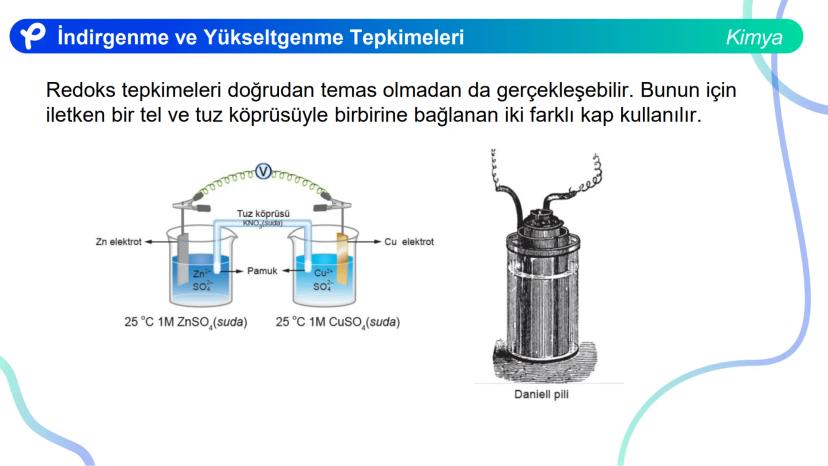
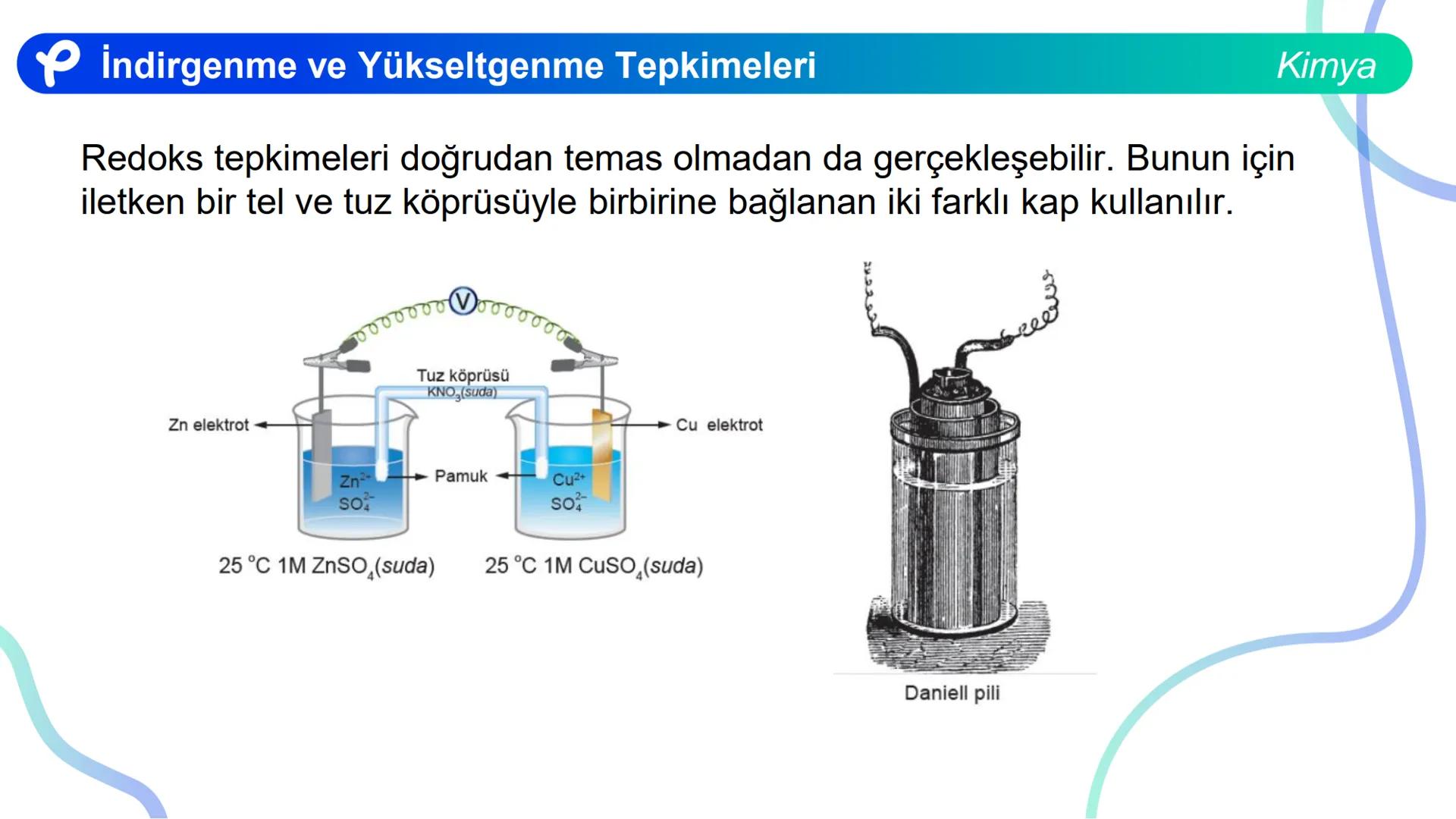
Redoks tepkimeleri doğrudan temas olmadan da gerçekleşebilir. Bunun için iletken bir tel ve tuz köprüsüyle birbirine bağlanan iki farklı kap kullanılır. Bu sisteme elektrokimyasal pil denir.
En bilinen örneği, çinko ve bakır metalleriyle oluşturulan Daniell pilidir. Bu pilde çinko elektrodu ZnSO₄ çözeltisine, bakır elektrodu ise CuSO₄ çözeltisine batırılır ve kaplar bir tuz köprüsü ile birleştirilir.
Sistemde şu redoks tepkimesi gerçekleşir: Zn(k) + Cu²⁺(suda) → Zn²⁺(suda) + Cu(k)
Bulunduğu şartlarda kendiliğinden gerçekleşen tepkimelere istemli tepkime, kendiliğinden gerçekleşmeyen tepkimelere ise istemsiz tepkime denir. Daniell pilinde gerçekleşen tepkime istemli bir tepkimedir ve elektrik enerjisi üretir.

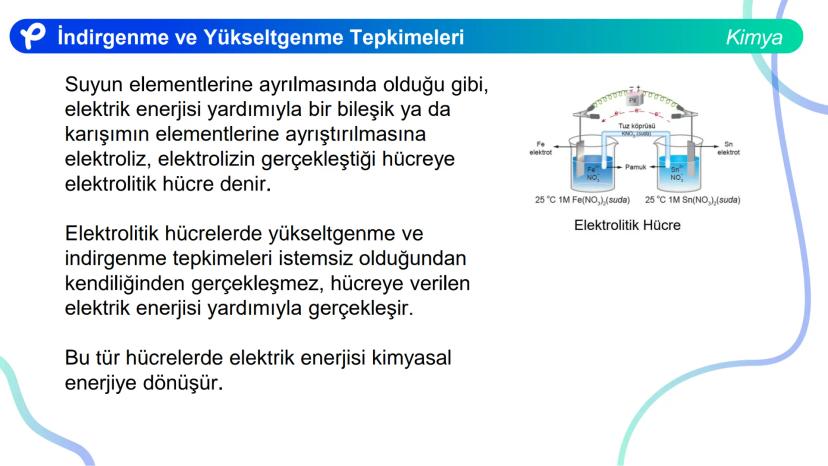
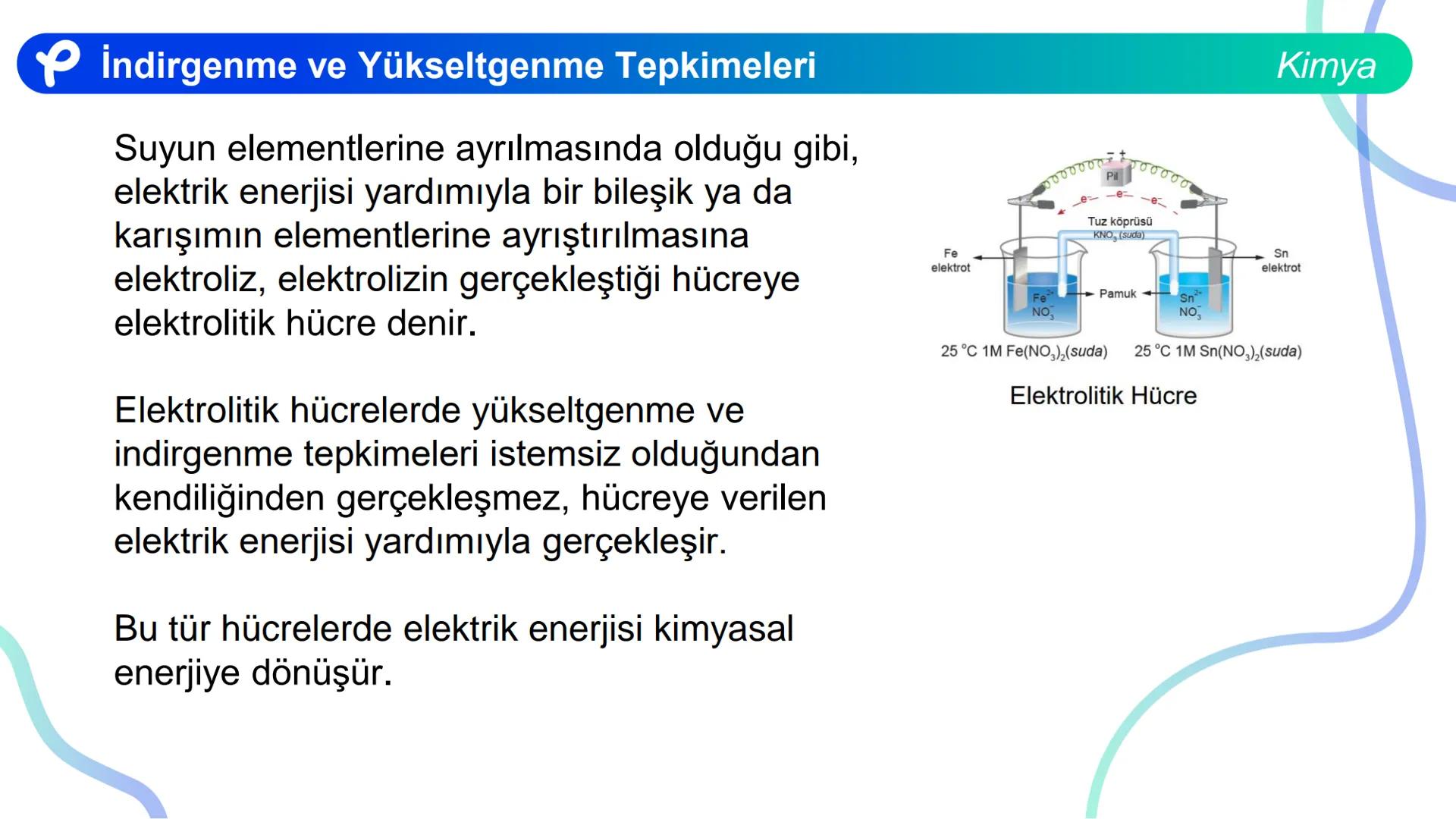
Elektrik enerjisi yardımıyla bir bileşik ya da karışımın elementlerine ayrıştırılmasına elektroliz, elektrolizin gerçekleştiği hücreye ise elektrolitik hücre denir.
Suyun elektrolizi buna iyi bir örnektir: H₂O(s) + enerji → H₂(g) + ½O₂(g)
Bu tepkime istemsizdir ve dışarıdan sürekli elektrik enerjisi verilmesi gerekir. Elektrolitik hücrelerde yükseltgenme ve indirgenme tepkimeleri kendiliğinden gerçekleşmez, hücreye verilen elektrik enerjisi yardımıyla gerçekleşir.
Elektrolitik hücrelerde, elektrik enerjisi kimyasal enerjiye dönüşür. Bu prensip, metallerin saflaştırılması, elektrokaplama ve birçok endüstriyel işlemde kullanılır.
🔍 Pil ve elektrolitik hücre arasındaki temel fark: Pil kimyasal enerjiyi elektrik enerjisine dönüştürürken, elektrolitik hücre elektrik enerjisini kimyasal enerjiye dönüştürür.


















Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
MelekCheonsa
@juliannecandy
İndirgenme-yükseltgenme (redoks) tepkimeleri, elektron alışverişi sonucunda gerçekleşen kimyasal olaylardır. Bu olaylar çevremizde yaygın olarak bulunur ve metallerin paslanmasından, odunun yanmasına kadar birçok kimyasal değişimin temelini oluşturur.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bir atom ya da iyonun elektron almasına indirgenme denir. İndirgenme gerçekleştiğinde taneciğin yükseltgenme basamağı (değeri) küçülür. Örneğin çinko iyonu elektron aldığında, elementel çinkoya dönüşür.
İndirgenme yarı tepkimelerine örnekler:
💡 İndirgenme olayını hatırlamanın kolay bir yolu: Elektron alan taneciğin yükü azalır, yani sayısal olarak küçülür!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bir atom ya da iyonun elektron vermesine yükseltgenme denir. Yükseltgenme gerçekleştiğinde taneciğin yükseltgenme basamağı büyür. Örneğin hidrojen gazı elektron verdiğinde, hidrojen iyonuna dönüşür.
Yükseltgenme yarı tepkimelerine örnekler:
Günlük hayatta gördüğümüz birçok olay aslında redoks tepkimesidir. Odunun yanması, metallerin paslanması ve bileşiklerin elementlerine ayrışması bu tür tepkimelere örnektir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
İndirgenme ve yükseltgenme yarı tepkimelerinin toplamından oluşan tepkimelere indirgenme-yükseltgenme (redoks) tepkimesi denir. Bu tepkimelerde alınan ve verilen elektron sayıları daima eşittir.
"Redoks" kelimesi, "redüksiyon" (indirgenme) ve "oksidasyon" (yükseltgenme) kelimelerinin birleşiminden gelir ve elektron alışverişinin gerçekleştiği tepkimeler için kullanılır.
Örnek bir redoks tepkimesi: Çinko metali, bakır sülfat çözeltisine daldırıldığında gerçekleşen tepkime:
İndirgenme: Yükseltgenme: Net tepkime:

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Elektron alarak indirgenen taneciklere yükseltgen, elektron vererek yükseltgenen taneciklere ise indirgen denir. Yükseltgenler bir tepkimede elektron alır ve kendileri indirgenir. İndirgenler ise elektron verir ve kendileri yükseltgenir.
O₂, KMnO₄, H₂SO₄, HNO₃ ve H₂O₂ yaygın kullanılan yükseltgenlerdir. Bu maddeler redoks tepkimelerinde elektron alarak indirgendiklerinden yükseltgen özelliği gösterir.
Örneğin:
🔑 Unutmayın: Bir redoks tepkimesinde yükseltgen madde indirgenir, indirgen madde ise yükseltgenir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bir atom ya da iyonun tek başına veya bileşik içerisinde sahip olduğu yüke, o taneciğin yükseltgenme basamağı denir. Bir taneciğin indirgendiği ya da yükseltgendiği, yükseltgenme basamağındaki değişime bakılarak anlaşılır.
Yükseltgenme basamaklarını belirlerken kullanılan temel kurallar:
Bir bileşikteki atomların yükseltgenme basamakları toplamı her zaman sıfıra eşittir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Redoks tepkimelerini denkleştirirken şu adımları izlemelisiniz:
Örnek: Cu + H₂SO₄ → CuSO₄ + SO₂ + H₂O tepkimesini denkleştirirken, önce Cu ve S elementlerinin yükseltgenme basamaklarının değiştiğini belirleyip, ardından elektron sayılarını eşitleyerek denkleştirme yapılır.
💡 Denkleştirme yaparken, atomların toplam sayısı ve yüklerin toplamı tepkimenin her iki tarafında eşit olmalıdır!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Redoks tepkimeleri doğrudan temas olmadan da gerçekleşebilir. Bunun için iletken bir tel ve tuz köprüsüyle birbirine bağlanan iki farklı kap kullanılır. Bu sisteme elektrokimyasal pil denir.
En bilinen örneği, çinko ve bakır metalleriyle oluşturulan Daniell pilidir. Bu pilde çinko elektrodu ZnSO₄ çözeltisine, bakır elektrodu ise CuSO₄ çözeltisine batırılır ve kaplar bir tuz köprüsü ile birleştirilir.
Sistemde şu redoks tepkimesi gerçekleşir: Zn(k) + Cu²⁺(suda) → Zn²⁺(suda) + Cu(k)
Bulunduğu şartlarda kendiliğinden gerçekleşen tepkimelere istemli tepkime, kendiliğinden gerçekleşmeyen tepkimelere ise istemsiz tepkime denir. Daniell pilinde gerçekleşen tepkime istemli bir tepkimedir ve elektrik enerjisi üretir.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Elektrik enerjisi yardımıyla bir bileşik ya da karışımın elementlerine ayrıştırılmasına elektroliz, elektrolizin gerçekleştiği hücreye ise elektrolitik hücre denir.
Suyun elektrolizi buna iyi bir örnektir: H₂O(s) + enerji → H₂(g) + ½O₂(g)
Bu tepkime istemsizdir ve dışarıdan sürekli elektrik enerjisi verilmesi gerekir. Elektrolitik hücrelerde yükseltgenme ve indirgenme tepkimeleri kendiliğinden gerçekleşmez, hücreye verilen elektrik enerjisi yardımıyla gerçekleşir.
Elektrolitik hücrelerde, elektrik enerjisi kimyasal enerjiye dönüşür. Bu prensip, metallerin saflaştırılması, elektrokaplama ve birçok endüstriyel işlemde kullanılır.
🔍 Pil ve elektrolitik hücre arasındaki temel fark: Pil kimyasal enerjiyi elektrik enerjisine dönüştürürken, elektrolitik hücre elektrik enerjisini kimyasal enerjiye dönüştürür.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
6
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı