Kimya, maddenin yapısını ve özelliklerini inceleyen ve günlük hayatımızın her... Daha fazla göster
9. Sınıf Kimya Ders Notları - Konu Anlatımlı ve Açıklamalı







Kimya Hayattır
Kimya etrafımızdaki her şeyi etkileyen, görünmeyen bir sihirbaz gibi çalışan bilim dalı. Maddenin yapısını, özelliklerini ve birbirleri arasındaki etkileşimi inceler.
Günlük hayatta kullandığın deterjanlardan diş macununa, telefonundaki pillerden giysilerine kadar her şey kimyayla ilgili. Fotosentez, yanma, analiz gibi olayları da kimya sayesinde anlıyoruz.
Kimya disiplinleri çok çeşitli alanlarda uzmanlaşmış:
- Analitik kimya: Maddelerin bileşenlerini ayırıp tanımlar (kan, idrar testleri gibi)
- Biyokimya: Canlıların kimyasal süreçlerini inceler (fotosentez, sindirim)
- Organik kimya: Karbon içeren bileşikleri çalışır (ilaçlar, plastikler)
- Anorganik kimya: Asitler, bazlar, tuzlar gibi organik olmayan maddeleri inceler
- Fizikokimya: Tepkime hızları ve enerji değişimlerini araştırır
Dikkat! Kimya mühendisliği, kimyager, polimer malzeme mühendisi gibi birçok kariyer fırsatı sunuyor.
Laboratuvar Güvenliği
Kimya laboratuvarında çalışmak süper eğlenceli ama güvenlik kurallarına uymak hayati önem taşıyor. Bu kurallar seni ve arkadaşlarını korumak için var!
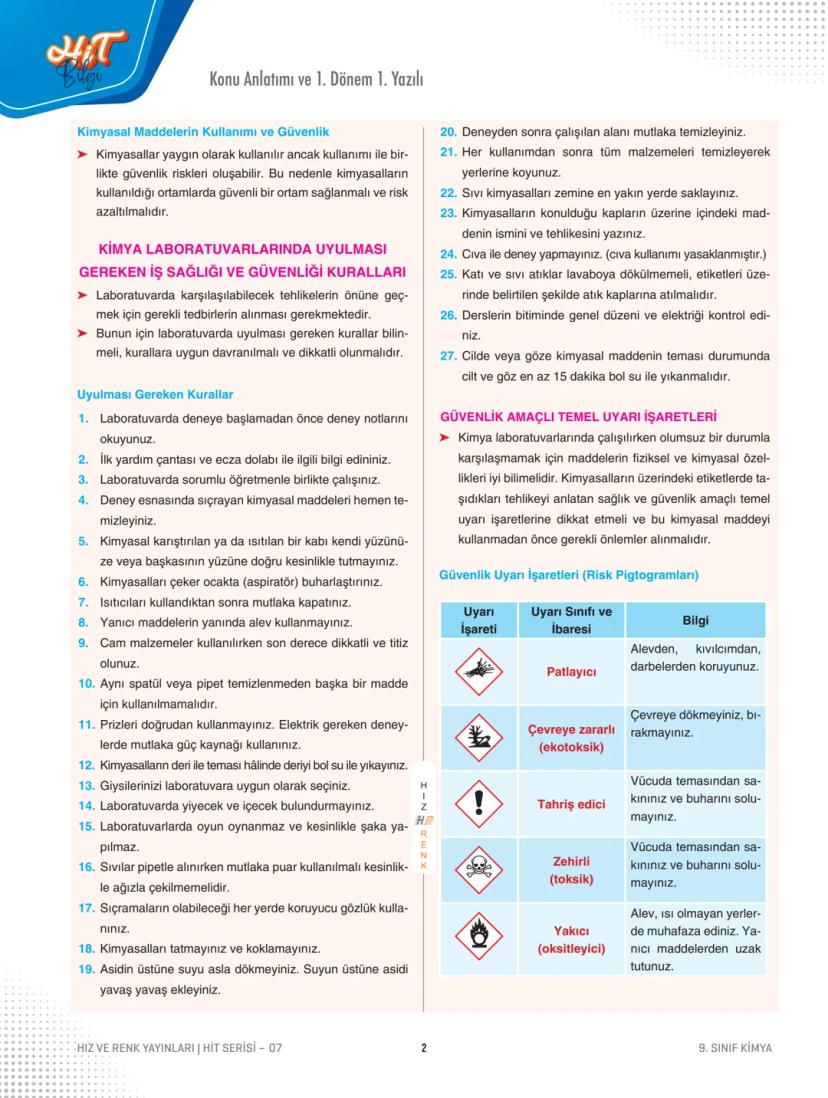
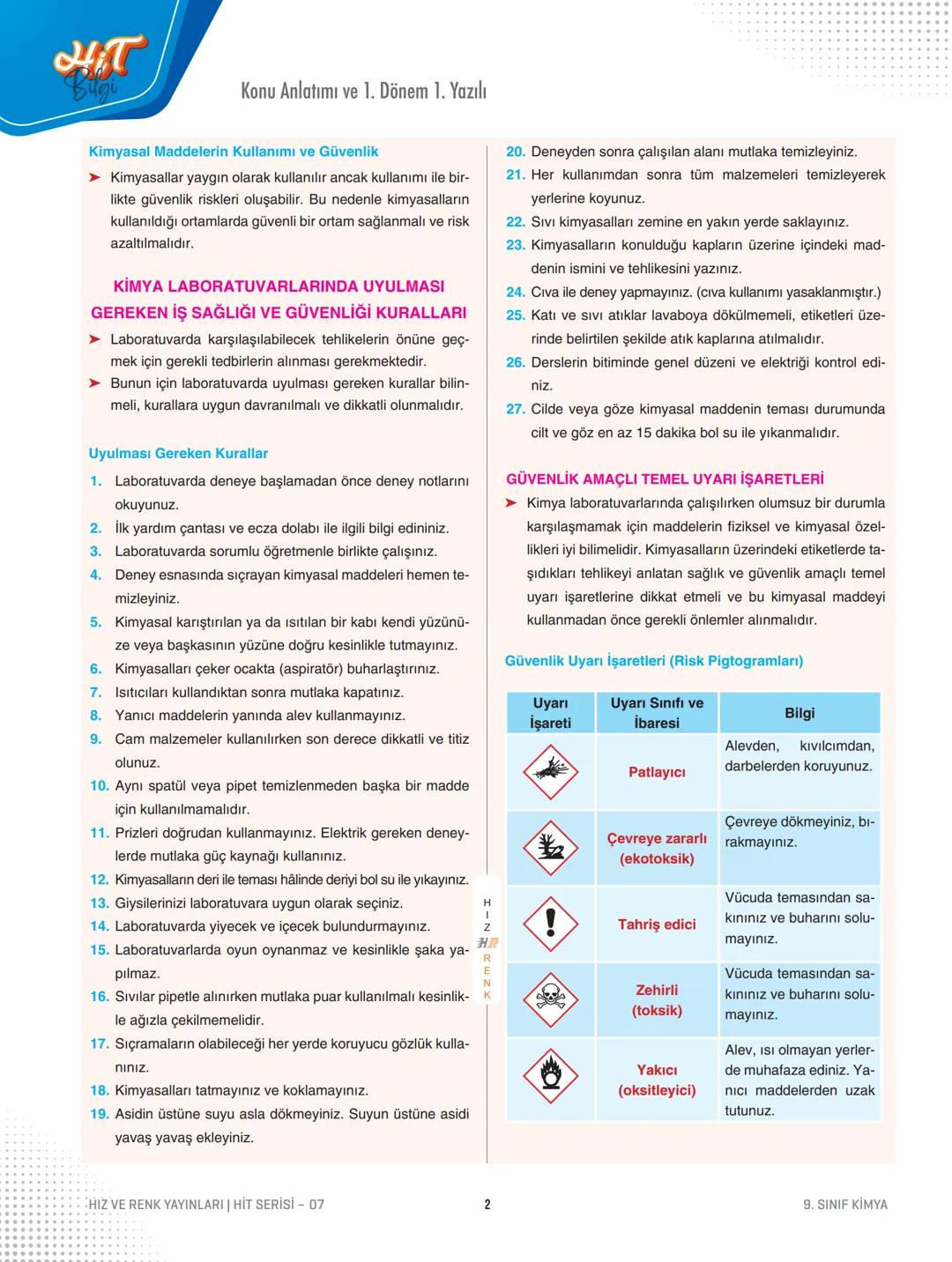
En önemli güvenlik kuralları:
- Deney öncesi notlarını oku, öğretmeninle çalış
- Koruyucu gözlük tak, kimyasalları asla tatma veya koklama
- Asidi suya ekle, suyu aside değil! Bu çok kritik
- Yanıcı maddelerin yanında alev kullanma
- Kimyasal sıçrarsa hemen 15 dakika bol suyla yıka
Güvenlik işaretleri kimyasalların ne kadar tehlikeli olduğunu gösterir. Patlayıcı, zehirli, yakıcı, tahriş edici gibi işaretleri tanımak zorundasın.
Önemli! Laboratuvarda asla şaka yapma, oyun oynama. Ciddi kazalar olabilir!
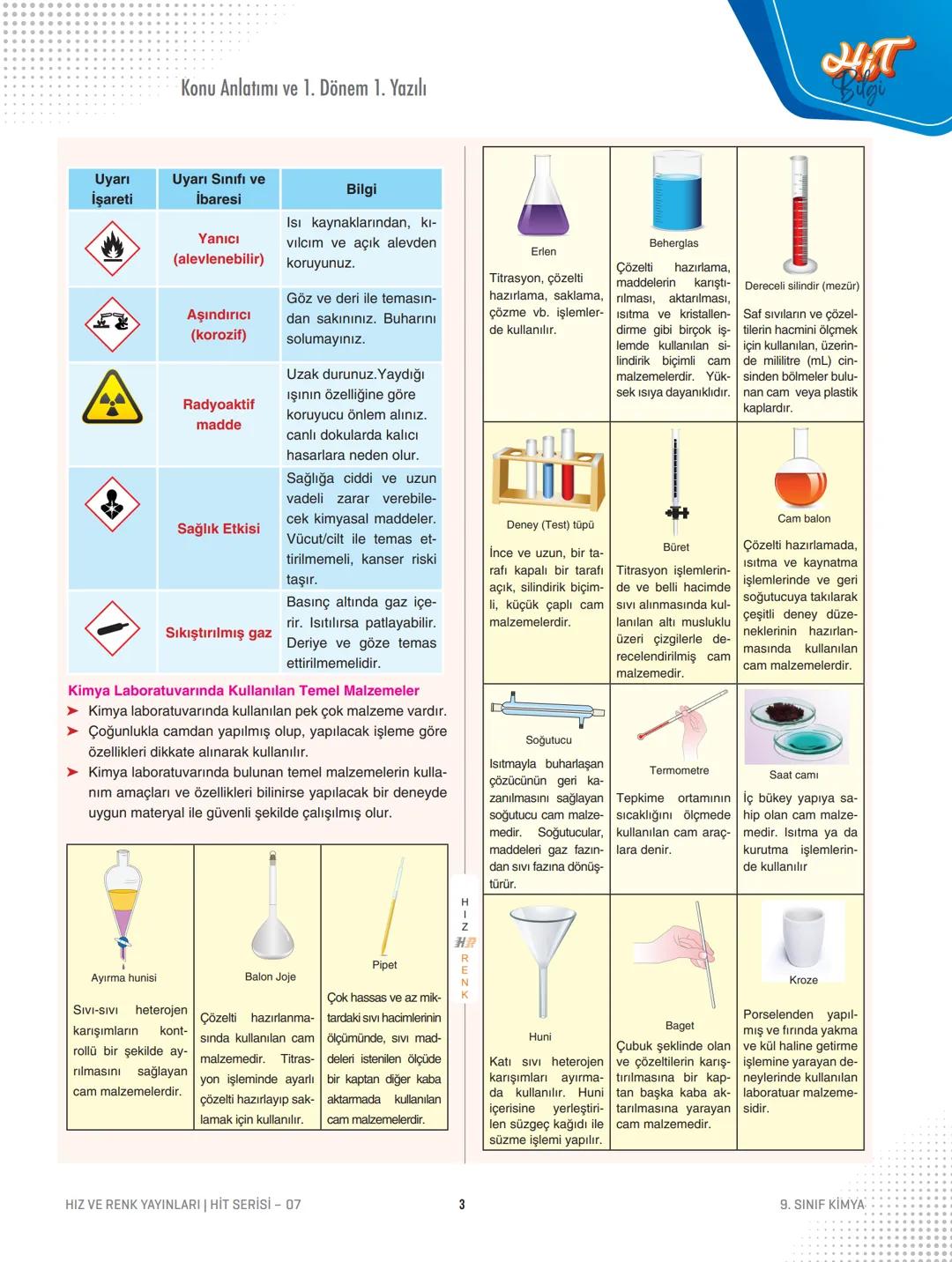
Laboratuvar Malzemeleri
Kimya laboratuvarındaki malzemeleri tanımak, deneylerini başarılı yapman için süper önemli. Çoğu cam malzemeler ve her birinin özel bir görevi var.
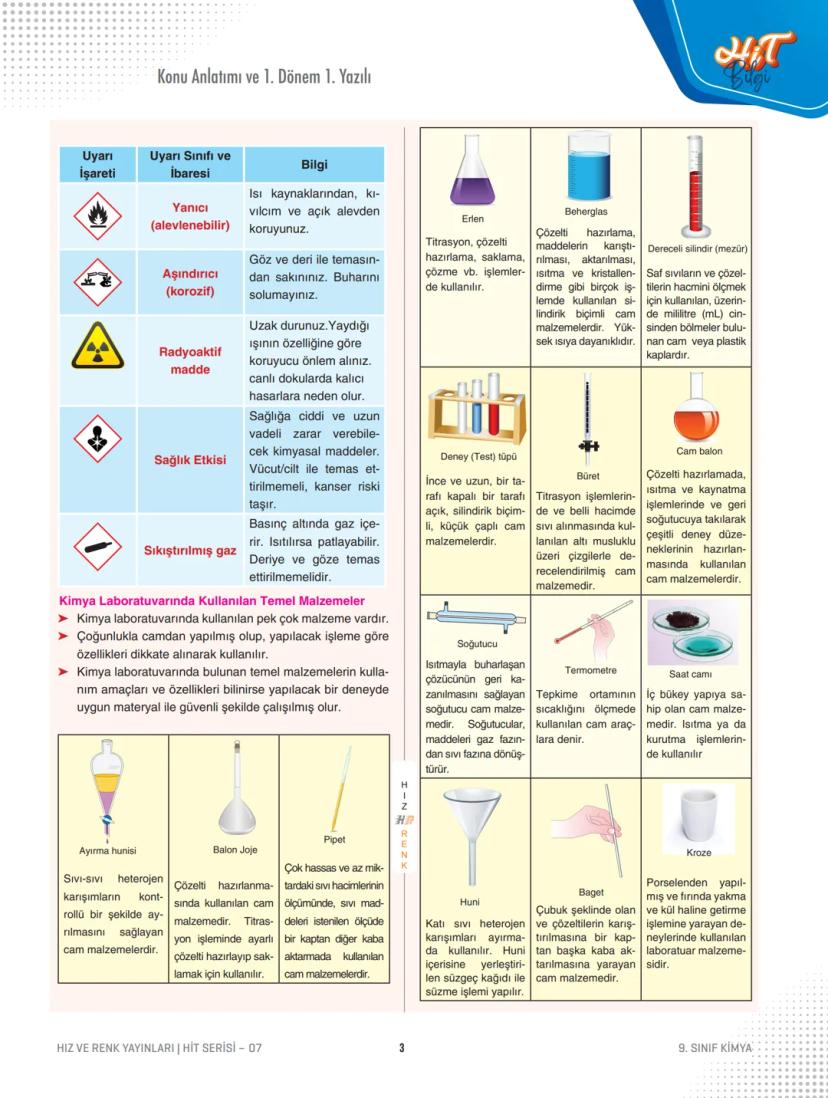
Temel laboratuvar malzemeleri:
- Erlen: Titrasyon, çözelti hazırlama, saklama işlemlerinde kullanılır
- Beherglas: Karıştırma, ısıtma, kristallendirme işlemleri için ideal
- Dereceli silindir (mezür): Sıvıların hacmini kesin olarak ölçer
- Büret: Titrasyon işlemlerinde hassas hacim ölçümü yapar
- Pipet: Çok hassas sıvı aktarımları için kullanılır
Diğer önemli araçlar arasında termometre, soğutucu, ayırma hunisi, spatül ve huni var. Her malzemenin kendine özgü kullanım alanı ve dikkat edilmesi gereken noktalar bulunuyor.
Pratik İpucu! Cam malzemeler kırılgandır. Çok dikkatli kullan ve her kullanımdan sonra temizleyip yerine koy.
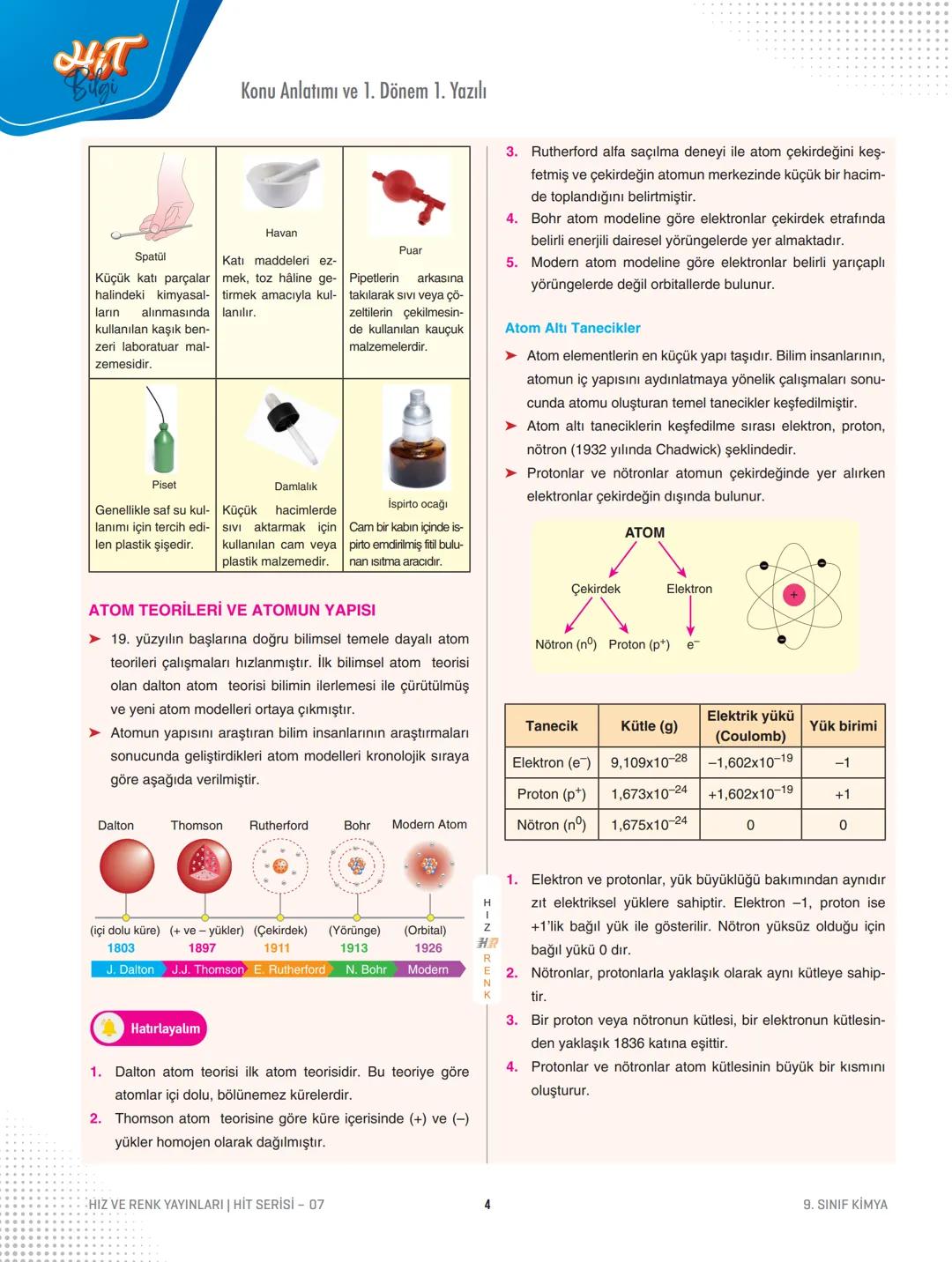
Atom Teorileri ve Atomun Yapısı
Atom teorileri zamanla gelişerek bugünkü modern anlayışımıza ulaştı. Her bilim insanı önceki teorilerin eksiklerini gidererek yeni modeller geliştirdi.
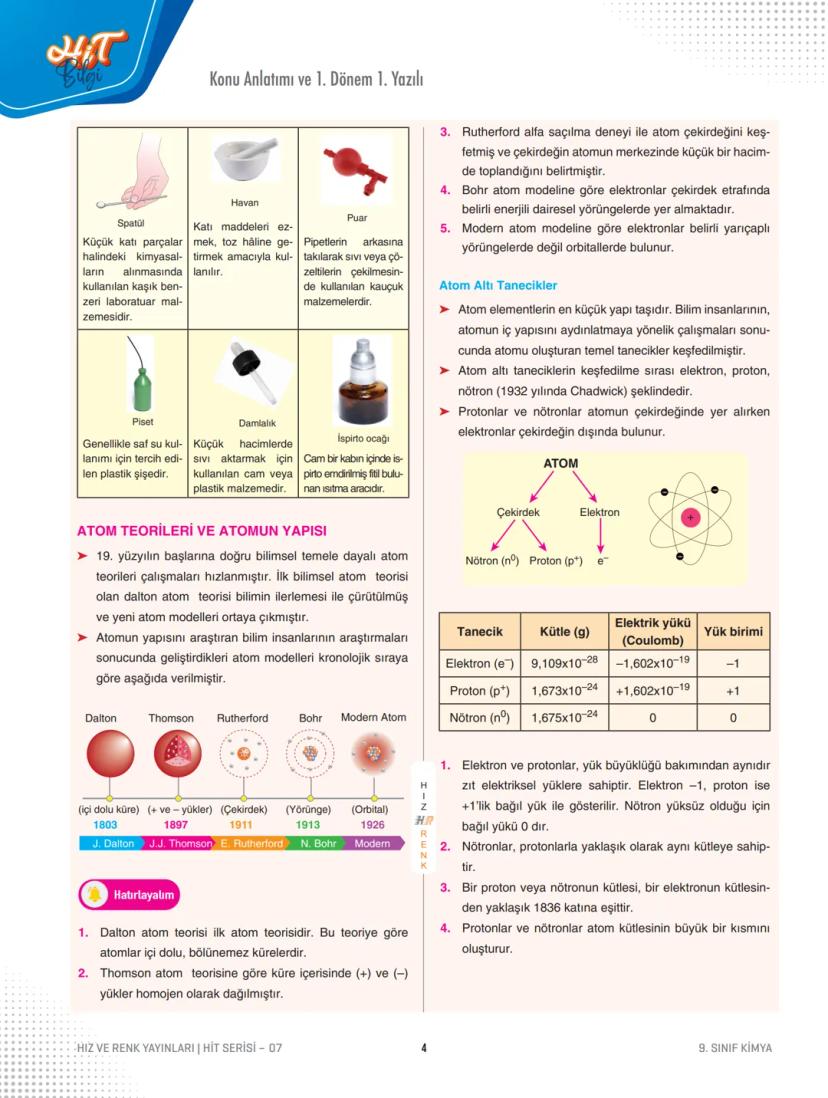
Tarihsel gelişim sırası:
- Dalton (1803): İçi dolu, bölünmez küre modeli
- Thomson (1897): Pozitif ve negatif yüklerin homojen dağıldığı model
- Rutherford (1911): Atom çekirdeğini keşfetti
- Bohr (1913): Elektronların belirli yörüngelerde döndüğü model
- Modern atom teorisi (1926): Orbital kavramını getirdi
Atom altı tanecikler üç temel parçacıktan oluşur:
- Elektron (e⁻): Negatif yüklü, çekirdek dışında bulunur
- Proton (p⁺): Pozitif yüklü, çekirdekte yer alır
- Nötron (n⁰): Yüksüz, çekirdekte bulunur
Hatırla! Atom numarası (Z) = Proton sayısı. Bu, elementin kimliğini belirler!

Bohr ve Modern Atom Teorileri
Bohr atom teorisi elektronların çekirdek etrafında belirli enerjili yörüngelerde döndüğünü söyler. Bu yörüngeler K, L, M, N veya 1, 2, 3, 4 şeklinde adlandırılır.
Elektronlar en düşük enerji seviyesinde (temel hal) bulunmak ister. Enerji aldığında yüksek seviyeye çıkar (absorpsiyon), geri inerken enerji yayar (emisyon). Bu süreç atomların renk vermesini açıklar.
Bohr modelinin eksikleri:
- Sadece tek elektronlu atomları açıklayabilir
- Elektronun dalga özelliğini göz ardı eder
- Heisenberg belirsizlik ilkesine göre elektronun yeri ve hızı aynı anda bilinemez
Modern atom teorisi bu sorunları çözer. Elektronlar artık kesin yörüngelerde değil, orbital denilen üç boyutlu uzay bölgelerinde bulunma olasılığı yüksek olan alanlarda yer alır.
Anahtar Nokta! Modern teoriye göre elektron bulutu kavramı, elektronun bulunma olasılığının en yüksek olduğu bölgeleri gösterir.




Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Laboratory Techniques
9Kimya bilimi
Kimya her yerde🔥
TYT kimya bilimi özet
Tyt kimya ders notu
9.sınıf kimya
Kimya ders notu.
9. Sınıf Kimya
Kimya notları
Tyt kimya _kimya bilimine giriş
9 sınıf kimya 1. ünite
Kimya bilimi
Kimya bilimine giriş ko
Simyadan Kimyaya
Tyt kimya, simyadan kimyaya ders notu
kimya laboratuvarında kullanılan temel malzemeler
kimya laboratuvarında kullanılan temel malzemeler görselleri ve acıklamaları ile birlikte detaylı konu anlatım notları
Kimya 1. Senertı
Kimya konu anlatımı
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Lewis Nokta Yapısı
Lewis Nokta yapısı
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
En popüler içerikler
98.sınıf matematik
Tüm üniteleri içermektedir!
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
11. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
9.sınıf tarih ders notları
Yeni maarif modele uygundur
İnkılap tarihi
Beğenin
TYT AYT TARİH
Tarih
9. Sınıf edebiyat ders notları.
9. Sınıflar için Türk Dili edebiyatı notları.
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
9. Sınıf Kimya Ders Notları - Konu Anlatımlı ve Açıklamalı
Kimya, maddenin yapısını ve özelliklerini inceleyen ve günlük hayatımızın her alanında etkili olan süper önemli bir bilim dalı. Bu derste kimya disiplinlerinden laboratuvar güvenliğine, atom teorilerinden modern kimyanın temellerine kadar her şeyi öğreneceksin!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Kimya Hayattır
Kimya etrafımızdaki her şeyi etkileyen, görünmeyen bir sihirbaz gibi çalışan bilim dalı. Maddenin yapısını, özelliklerini ve birbirleri arasındaki etkileşimi inceler.
Günlük hayatta kullandığın deterjanlardan diş macununa, telefonundaki pillerden giysilerine kadar her şey kimyayla ilgili. Fotosentez, yanma, analiz gibi olayları da kimya sayesinde anlıyoruz.
Kimya disiplinleri çok çeşitli alanlarda uzmanlaşmış:
- Analitik kimya: Maddelerin bileşenlerini ayırıp tanımlar (kan, idrar testleri gibi)
- Biyokimya: Canlıların kimyasal süreçlerini inceler (fotosentez, sindirim)
- Organik kimya: Karbon içeren bileşikleri çalışır (ilaçlar, plastikler)
- Anorganik kimya: Asitler, bazlar, tuzlar gibi organik olmayan maddeleri inceler
- Fizikokimya: Tepkime hızları ve enerji değişimlerini araştırır
Dikkat! Kimya mühendisliği, kimyager, polimer malzeme mühendisi gibi birçok kariyer fırsatı sunuyor.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Laboratuvar Güvenliği
Kimya laboratuvarında çalışmak süper eğlenceli ama güvenlik kurallarına uymak hayati önem taşıyor. Bu kurallar seni ve arkadaşlarını korumak için var!
En önemli güvenlik kuralları:
- Deney öncesi notlarını oku, öğretmeninle çalış
- Koruyucu gözlük tak, kimyasalları asla tatma veya koklama
- Asidi suya ekle, suyu aside değil! Bu çok kritik
- Yanıcı maddelerin yanında alev kullanma
- Kimyasal sıçrarsa hemen 15 dakika bol suyla yıka
Güvenlik işaretleri kimyasalların ne kadar tehlikeli olduğunu gösterir. Patlayıcı, zehirli, yakıcı, tahriş edici gibi işaretleri tanımak zorundasın.
Önemli! Laboratuvarda asla şaka yapma, oyun oynama. Ciddi kazalar olabilir!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Laboratuvar Malzemeleri
Kimya laboratuvarındaki malzemeleri tanımak, deneylerini başarılı yapman için süper önemli. Çoğu cam malzemeler ve her birinin özel bir görevi var.
Temel laboratuvar malzemeleri:
- Erlen: Titrasyon, çözelti hazırlama, saklama işlemlerinde kullanılır
- Beherglas: Karıştırma, ısıtma, kristallendirme işlemleri için ideal
- Dereceli silindir (mezür): Sıvıların hacmini kesin olarak ölçer
- Büret: Titrasyon işlemlerinde hassas hacim ölçümü yapar
- Pipet: Çok hassas sıvı aktarımları için kullanılır
Diğer önemli araçlar arasında termometre, soğutucu, ayırma hunisi, spatül ve huni var. Her malzemenin kendine özgü kullanım alanı ve dikkat edilmesi gereken noktalar bulunuyor.
Pratik İpucu! Cam malzemeler kırılgandır. Çok dikkatli kullan ve her kullanımdan sonra temizleyip yerine koy.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Atom Teorileri ve Atomun Yapısı
Atom teorileri zamanla gelişerek bugünkü modern anlayışımıza ulaştı. Her bilim insanı önceki teorilerin eksiklerini gidererek yeni modeller geliştirdi.
Tarihsel gelişim sırası:
- Dalton (1803): İçi dolu, bölünmez küre modeli
- Thomson (1897): Pozitif ve negatif yüklerin homojen dağıldığı model
- Rutherford (1911): Atom çekirdeğini keşfetti
- Bohr (1913): Elektronların belirli yörüngelerde döndüğü model
- Modern atom teorisi (1926): Orbital kavramını getirdi
Atom altı tanecikler üç temel parçacıktan oluşur:
- Elektron (e⁻): Negatif yüklü, çekirdek dışında bulunur
- Proton (p⁺): Pozitif yüklü, çekirdekte yer alır
- Nötron (n⁰): Yüksüz, çekirdekte bulunur
Hatırla! Atom numarası (Z) = Proton sayısı. Bu, elementin kimliğini belirler!

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Bohr ve Modern Atom Teorileri
Bohr atom teorisi elektronların çekirdek etrafında belirli enerjili yörüngelerde döndüğünü söyler. Bu yörüngeler K, L, M, N veya 1, 2, 3, 4 şeklinde adlandırılır.
Elektronlar en düşük enerji seviyesinde (temel hal) bulunmak ister. Enerji aldığında yüksek seviyeye çıkar (absorpsiyon), geri inerken enerji yayar (emisyon). Bu süreç atomların renk vermesini açıklar.
Bohr modelinin eksikleri:
- Sadece tek elektronlu atomları açıklayabilir
- Elektronun dalga özelliğini göz ardı eder
- Heisenberg belirsizlik ilkesine göre elektronun yeri ve hızı aynı anda bilinemez
Modern atom teorisi bu sorunları çözer. Elektronlar artık kesin yörüngelerde değil, orbital denilen üç boyutlu uzay bölgelerinde bulunma olasılığı yüksek olan alanlarda yer alır.
Anahtar Nokta! Modern teoriye göre elektron bulutu kavramı, elektronun bulunma olasılığının en yüksek olduğu bölgeleri gösterir.

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl

Ders notlarını görmek için kaydol. Ücretsiz!
- Tüm belgeleri görebilirsin
- Notlarını Yükselt
- Milyonlarca öğrenciye katıl
Hiç sormayacaksın sanmıştık...
Knowunity yapay zeka arkadaşı nedir?
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Knowunity uygulamasını nereden indirebilirim?
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity ücretsiz mi?
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
En popüler içerikler: Laboratory Techniques
9Kimya bilimi
Kimya her yerde🔥
TYT kimya bilimi özet
Tyt kimya ders notu
9.sınıf kimya
Kimya ders notu.
9. Sınıf Kimya
Kimya notları
Tyt kimya _kimya bilimine giriş
9 sınıf kimya 1. ünite
Kimya bilimi
Kimya bilimine giriş ko
Simyadan Kimyaya
Tyt kimya, simyadan kimyaya ders notu
kimya laboratuvarında kullanılan temel malzemeler
kimya laboratuvarında kullanılan temel malzemeler görselleri ve acıklamaları ile birlikte detaylı konu anlatım notları
Kimya 1. Senertı
Kimya konu anlatımı
Kimya dersinin en popüler içerikleri
9Tyt kimya
Tyt kimya özet
Kimyaa
9.sınıf KİMYASAL BAĞLAR(metalik bağ,iyonik bağ,kovalent bağ) (☆▽☆)
TYT Kimya her yıl çıkan konu notları
MEBİ TYT Kimya Özetleri
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
11 sınıf kimya 4 ünite kimyasal tepkimelerde enerji
Kimyasal Türler Arası Etkileşimler
El Yazısı Özet Bilgiler
Lewis Nokta Yapısı
Lewis Nokta yapısı
9. Sınıf Kimya 2. Dönem 1. Yazılı Notları
İyi çalışmalar🫶🏻
Kimyasal Bağlar
9.sınıf Kimya metalik bağ,iyonik bağ,kovalent bağ konusu ders notu (Kimyasal bağlar)
kimyasal türler arası etkileşimler
apolarlik polarlik yukseltgenme basamaklari zayif ve guclu etkilesimler
En popüler içerikler
98.sınıf matematik
Tüm üniteleri içermektedir!
9. Sınıf Tarih Konu Anlatımı
9. sınıf tarih tüm ünite konu anlatımı
11. sınıf biyoloji dolaşım sistemi ders notları
11. sınıf biyoloji dolaşım sistemi ders notları
Tyt biyoloji
Bio
7. Sınıf Fen Bilimleri
Tüm üniteler
9.sınıf tarih ders notları
Yeni maarif modele uygundur
İnkılap tarihi
Beğenin
TYT AYT TARİH
Tarih
9. Sınıf edebiyat ders notları.
9. Sınıflar için Türk Dili edebiyatı notları.
Aradığını bulamıyor musun? Diğer derslere göz at.
Kullanıcılarımızdan yorumlar. Onlar her şeyi çok beğendi — sen de beğeneceksin.
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅