Kimyanın temel kanunları, maddelerin nasıl davrandığını ve tepkime verdiğini anlamamızı... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Knowunity AI
Daha fazla
Dersler
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Tüm konuları göster
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Tüm konuları göster
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Tüm konuları göster
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Tüm konuları göster
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Tüm konuları göster
2,262
•
Güncellendi May 22, 2026
•
Şnt
@ntsunshine
Kimyanın temel kanunları, maddelerin nasıl davrandığını ve tepkime verdiğini anlamamızı... Daha fazla göster

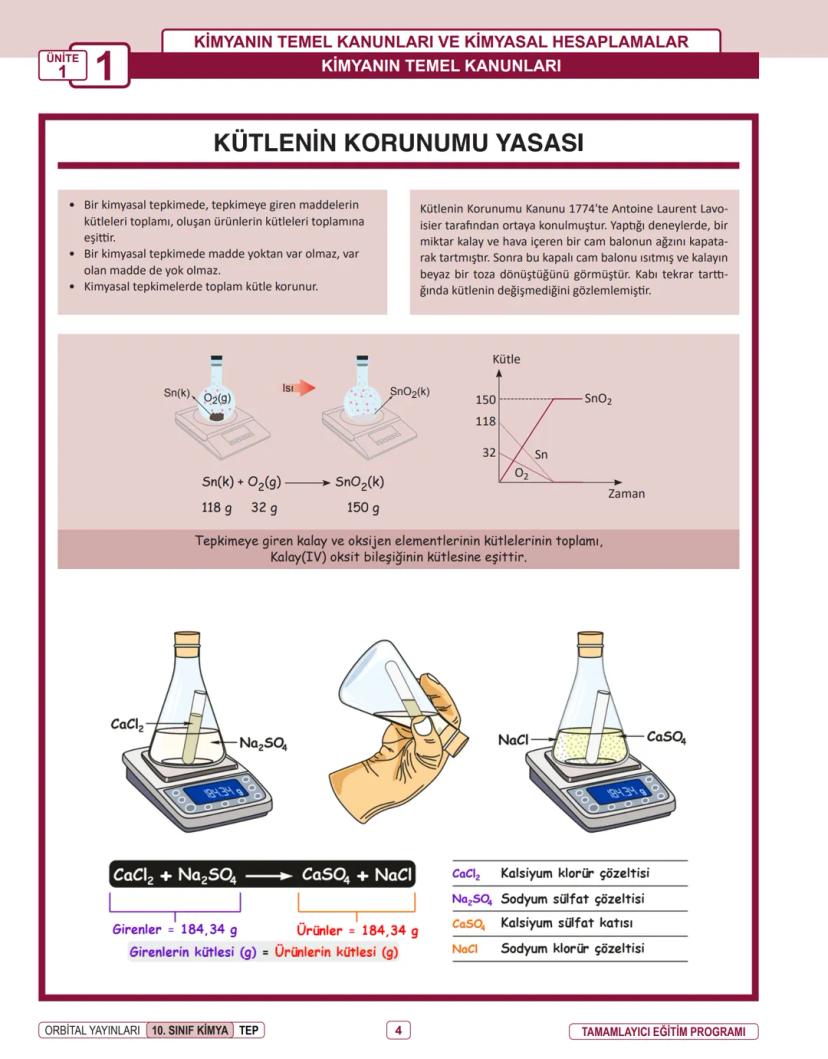










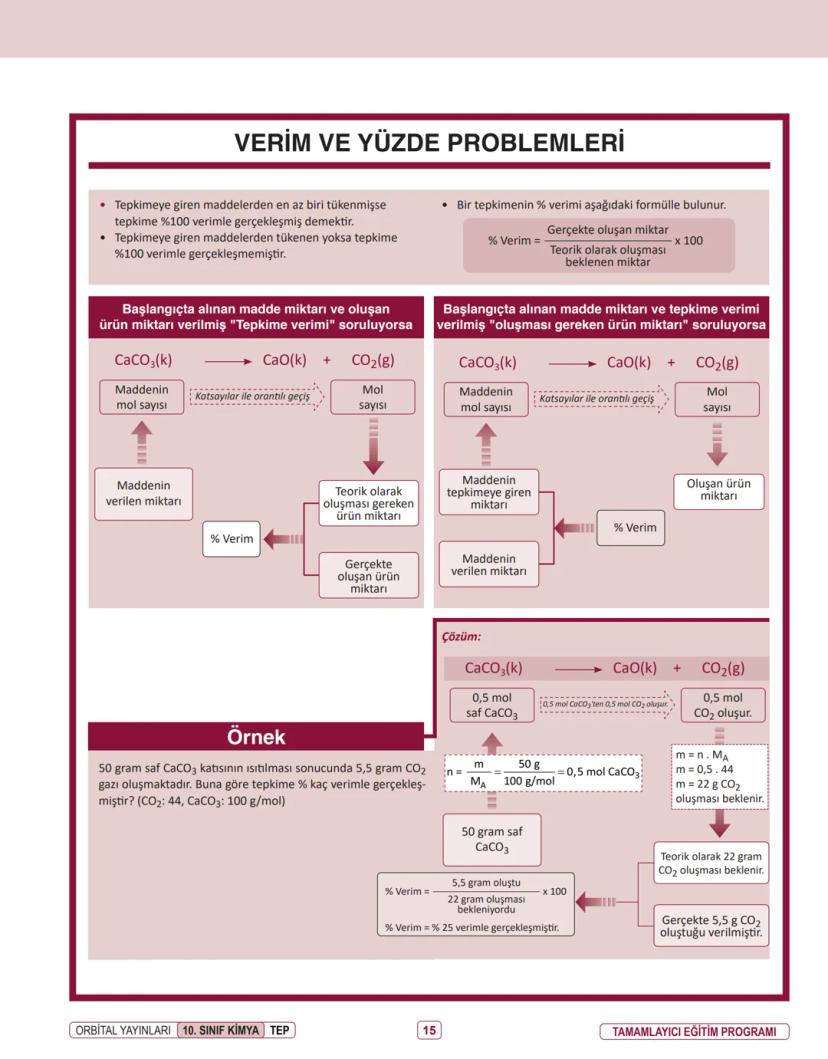










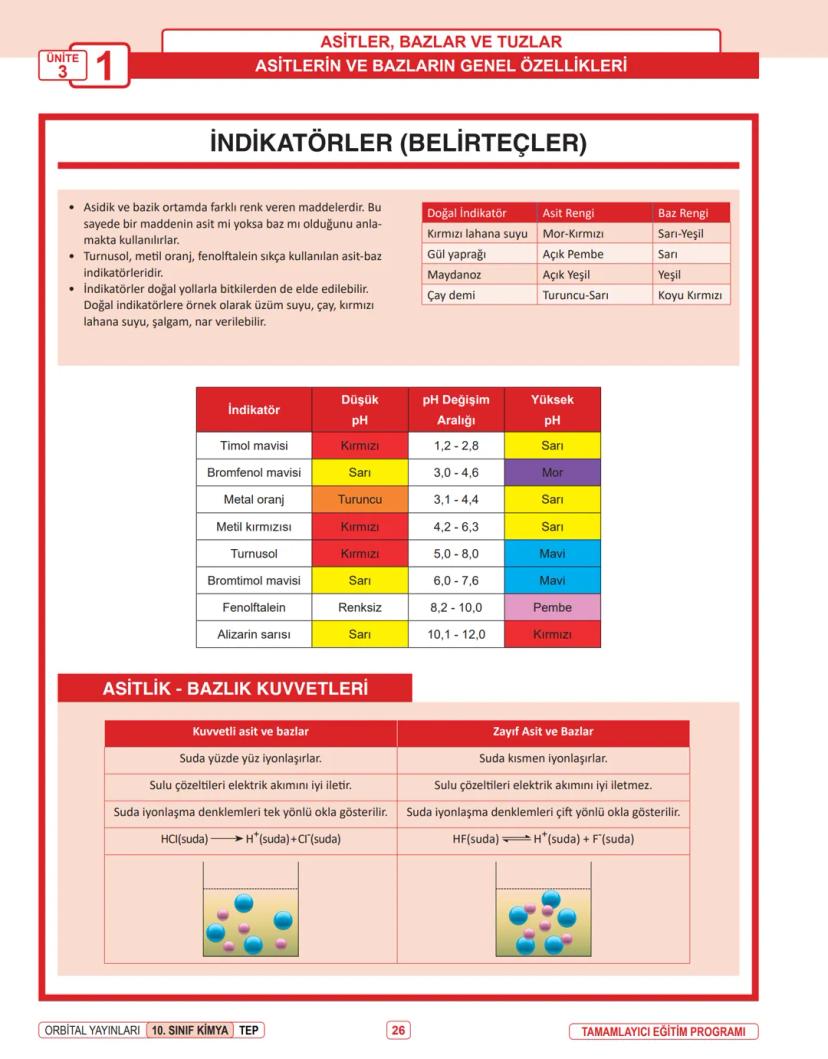
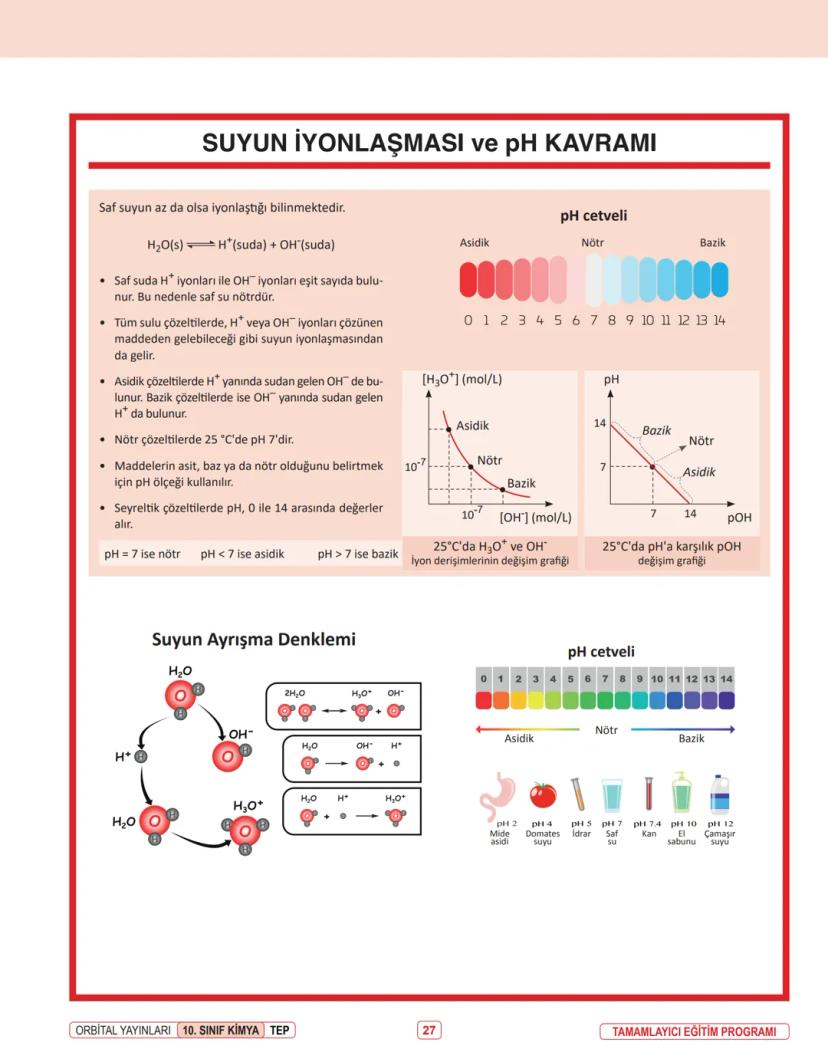









Bir kimyasal tepkimede madde yoktan var olmaz, var olan da yok olmaz. Bu basit ama güçlü kural, 1774'te Lavoisier tarafından keşfedildi.
Kütlenin korunumu yasası şunu der: Tepkimeye giren maddelerin toplam kütlesi = Oluşan ürünlerin toplam kütlesi. Yani tepkimeden önce ne kadar madde varsa, tepkimeden sonra da o kadar madde olur.
Lavoisier'nin kalay deneyi bunu kanıtladı. Kapalı bir kapta kalayı ısıttığında beyaz toz elde etti, ama kabın toplam ağırlığı hiç değişmedi. Bu, kütlenin korunduğunu gösteriyordu.
Hatırla: Kimyasal tepkimelerde toplam kütle her zaman korunur!

Bir bileşikteki elementler daima aynı oranlarda birleşirler. Bu Joseph Proust'un 1799'daki keşfi!
Sabit oranlar yasasına göre, CO₂'de karbon ve oksijenin kütlece birleşme oranı her zaman 3:8'dir. Ne kadar CO₂ yaparsın yap, bu oran değişmez.
MgO örneğinde bunu görebiliriz: Mg ve O'nin kütlece birleşme oranı hep 3:2'dir. 3g Mg ile 2g O tepkimeye girip 5g MgO oluşturur. 6g Mg ile 4g O tepkimeye girip 10g MgO oluşturur. Oran değişmez!
Not: Elementler sabit oran dışında kullanılırsa, fazla olan madde artar ve tepkimede yer almaz.

Mol, çok küçük tanecikler için kullandığımız bir grup ismi. Tıpkı 1 düzine = 12 tane gibi, 1 mol = 6,02×10²³ tane demek.
Bu devasa sayı Avogadro sayısı olarak bilinir ve Nₐ ile gösterilir. 1 mol demir = 6,02×10²³ demir atomu, 1 mol su = 6,02×10²³ su molekülü demektir.
Mol sayısı ile tanecik sayısı arasındaki formül: n = N/Nₐ . Bu formülle istediğin zaman mol sayısından tanecik sayısına, ya da tersine geçiş yapabilirsin.
Unutma: 1 mol her zaman 6,02×10²³ tanedir, maddenin türü önemli değil!

Herhangi bir elementin 1 mol atomunun gram cinsinden kütlesi, o elementin mol kütlesidir. Helyum için 4 g/mol, oksijen için 16 g/mol gibi.
Mol sayısı ile kütle arasındaki formül: n = m/Mₐ . Bu formülle kütleden mol sayısını bulabilirsin.
Bağıl atom kütlesi ise atomların kütlesini karşılaştırmak için kullanılır. ¹²C izotopunun 1/12'si referans alınır ve bu 1 atomik kütle birimi (1 akb) olur. 1 gram = 6,02×10²³ akb'dir.
İpucu: Atom kütleleri soru sonunda verilir, ezberlemene gerek yok!

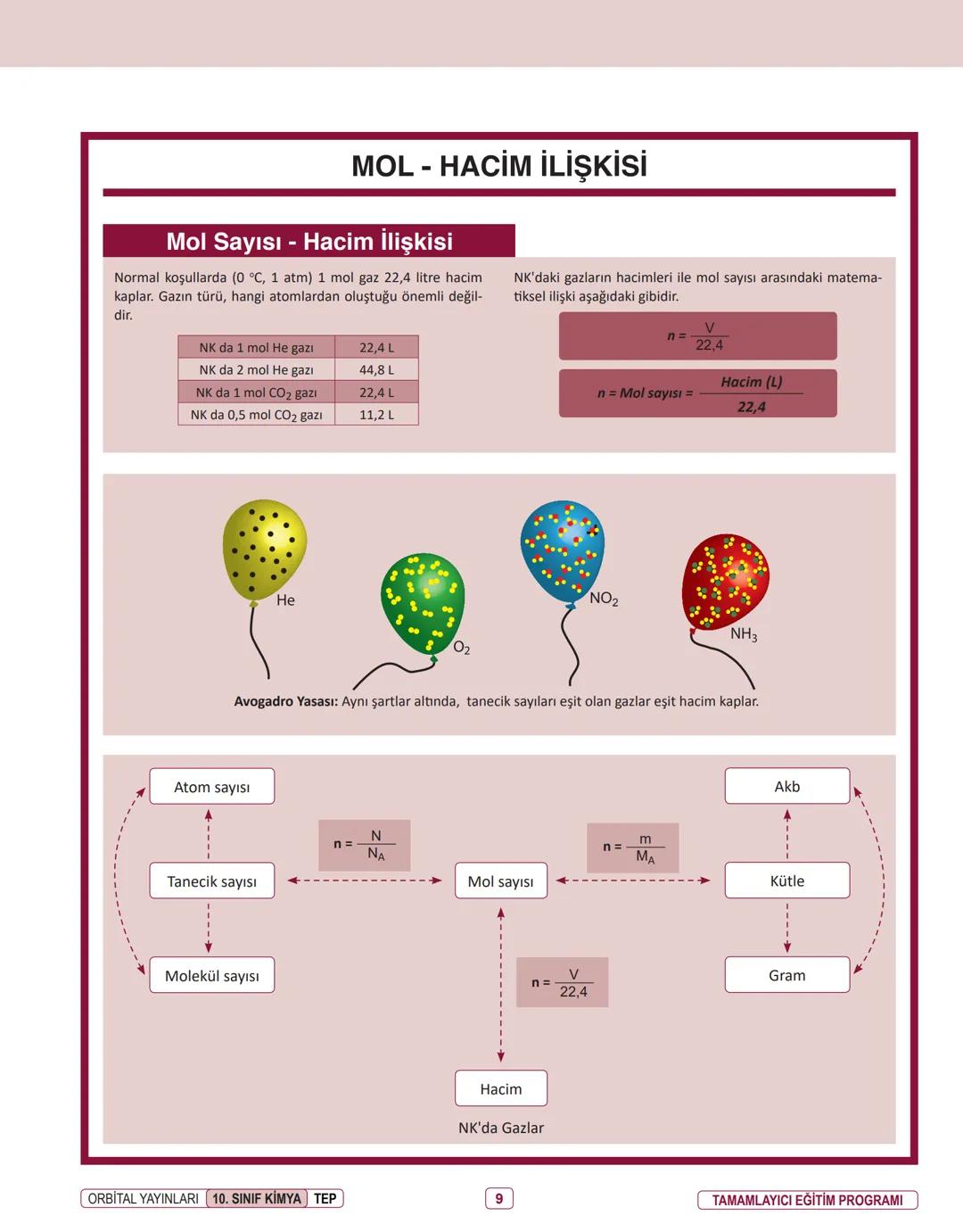
Normal koşullarda (0°C, 1 atm) 1 mol gaz 22,4 litre hacim kaplar. Gazın türü önemli değil - ister helyum, ister karbondioksit olsun.
NK'da mol sayısı ile hacim arasındaki formül: n = V/22,4 . Bu formülle hacimden mol sayısını bulabilirsin.
Avogadro yasası şunu der: Aynı koşullarda, eşit sayıda tanecik içeren gazlar eşit hacim kaplar. Bu yüzden 1 mol herhangi bir gaz NK'da hep 22,4 L yer alır.
Formül özeti: Tanecik sayısı için n=N/Nₐ, kütle için n=m/Mₐ, NK'da hacim için n=V/22,4

Kimyasal tepkimeler maddelerin başka maddelere dönüştüğü olaylardır ve her zaman enerji değişimi vardır. Tepkimelerde toplam atom sayısı ve kütle korunur.
Sentez tepkimeleri: İki veya daha fazla madde birleşerek yeni bileşik oluşturur . Demir ile oksijenin birleşip demir oksit oluşturması gibi.
Ayrışma tepkimeleri: Bir bileşik parçalanarak daha basit maddelere dönüşür . Sentezin tersi işlemdir. KClO₃'ün ısıtıldığında KCl ve O₂'ye ayrışması gibi.
Denkleştirme: En çok atom içeren bileşiğin katsayısı 1 kabul edilir, diğerleri buna göre bulunur.
Yanma tepkimeleri: Maddelerin oksijen ile tepkimesidir. Yanma için oksijen, yanacak madde ve tutuşma sıcaklığı gerekir. Çoğu yanma tepkimesi ısı verir (ekzotermik).
Asit-baz tepkimeleri: Asitten gelen H⁺ iyonu ile bazdan gelen OH⁻ iyonu tepkime verir. Genel denklem: Asit + Baz → Tuz + Su şeklindedir.
Çözünme-çökelme tepkimeleri: İki tuz çözeltisi karıştırıldığında çözünmeyen yeni bir tuz oluşabilir. AgNO₃ ile NaCl karıştırılınca beyaz AgCl çökeltisi oluşması gibi. Net iyon denkleminde sadece çöken iyonlar yazılır.
Yanma şartları: Oksijen + Yanacak madde + Tutuşma sıcaklığı = Yanma tepkimesi

Kimyasal tepkimelerde bir maddenin miktarı verildiğinde, denklem katsayılarını kullanarak diğer maddelerin miktarını bulabiliriz.
İşlem sırası şöyle: Verilen miktarı mol sayısına çevir → Denklem katsayıları ile orantı kur → İstenen maddenin mol sayısını bul → İstenen birime çevir.
N₂ + 3H₂ → 2NH₃ tepkimesinde 56g N₂ verilirse: 56g ÷ 28g/mol = 2 mol N₂. Denklemden 1 mol N₂'den 2 mol NH₃ oluşur, o halde 2 mol N₂'den 4 mol NH₃ oluşur. 4 mol × 17g/mol = 68g NH₃.
Önemli: Önce mol sayısına çevir, sonra denklem katsayıları ile orantı kur!

Birden fazla madde miktarı verildiğinde sınırlayıcı bileşen kavramı devreye girer. Biri tükenir, diğeri artar.
Çözüm yöntemi: Verilen miktarları mol sayısına çevir → Mol sayılarını denklem katsayılarına böl → Küçük oranı seç → Bu oranla çarparak harcanan ve oluşan miktarları bul.
6 mol N₂ ve 6 mol H₂ örneğinde: N₂ için 6÷1 = 6, H₂ için 6÷3 = 2. Küçük oran 2'dir. 2 katla çarpınca: 2 mol N₂ harcanır (4 mol artar), 6 mol H₂ tükenir, 4 mol NH₃ oluşur. H₂ sınırlayıcıdır.
Sınırlayıcı bileşen: Oranı en küçük olan madde tükenir ve tepkimeyi sınırlar.




















Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Şnt
@ntsunshine
Kimyanın temel kanunları, maddelerin nasıl davrandığını ve tepkime verdiğini anlamamızı sağlayan en önemli kurallardır. Bu kanunlar sayesinde kimyasal hesaplamalar yapabilir ve tepkimelerin sonucunu önceden tahmin edebiliriz.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bir kimyasal tepkimede madde yoktan var olmaz, var olan da yok olmaz. Bu basit ama güçlü kural, 1774'te Lavoisier tarafından keşfedildi.
Kütlenin korunumu yasası şunu der: Tepkimeye giren maddelerin toplam kütlesi = Oluşan ürünlerin toplam kütlesi. Yani tepkimeden önce ne kadar madde varsa, tepkimeden sonra da o kadar madde olur.
Lavoisier'nin kalay deneyi bunu kanıtladı. Kapalı bir kapta kalayı ısıttığında beyaz toz elde etti, ama kabın toplam ağırlığı hiç değişmedi. Bu, kütlenin korunduğunu gösteriyordu.
Hatırla: Kimyasal tepkimelerde toplam kütle her zaman korunur!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Bir bileşikteki elementler daima aynı oranlarda birleşirler. Bu Joseph Proust'un 1799'daki keşfi!
Sabit oranlar yasasına göre, CO₂'de karbon ve oksijenin kütlece birleşme oranı her zaman 3:8'dir. Ne kadar CO₂ yaparsın yap, bu oran değişmez.
MgO örneğinde bunu görebiliriz: Mg ve O'nin kütlece birleşme oranı hep 3:2'dir. 3g Mg ile 2g O tepkimeye girip 5g MgO oluşturur. 6g Mg ile 4g O tepkimeye girip 10g MgO oluşturur. Oran değişmez!
Not: Elementler sabit oran dışında kullanılırsa, fazla olan madde artar ve tepkimede yer almaz.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Mol, çok küçük tanecikler için kullandığımız bir grup ismi. Tıpkı 1 düzine = 12 tane gibi, 1 mol = 6,02×10²³ tane demek.
Bu devasa sayı Avogadro sayısı olarak bilinir ve Nₐ ile gösterilir. 1 mol demir = 6,02×10²³ demir atomu, 1 mol su = 6,02×10²³ su molekülü demektir.
Mol sayısı ile tanecik sayısı arasındaki formül: n = N/Nₐ . Bu formülle istediğin zaman mol sayısından tanecik sayısına, ya da tersine geçiş yapabilirsin.
Unutma: 1 mol her zaman 6,02×10²³ tanedir, maddenin türü önemli değil!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Herhangi bir elementin 1 mol atomunun gram cinsinden kütlesi, o elementin mol kütlesidir. Helyum için 4 g/mol, oksijen için 16 g/mol gibi.
Mol sayısı ile kütle arasındaki formül: n = m/Mₐ . Bu formülle kütleden mol sayısını bulabilirsin.
Bağıl atom kütlesi ise atomların kütlesini karşılaştırmak için kullanılır. ¹²C izotopunun 1/12'si referans alınır ve bu 1 atomik kütle birimi (1 akb) olur. 1 gram = 6,02×10²³ akb'dir.
İpucu: Atom kütleleri soru sonunda verilir, ezberlemene gerek yok!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Normal koşullarda (0°C, 1 atm) 1 mol gaz 22,4 litre hacim kaplar. Gazın türü önemli değil - ister helyum, ister karbondioksit olsun.
NK'da mol sayısı ile hacim arasındaki formül: n = V/22,4 . Bu formülle hacimden mol sayısını bulabilirsin.
Avogadro yasası şunu der: Aynı koşullarda, eşit sayıda tanecik içeren gazlar eşit hacim kaplar. Bu yüzden 1 mol herhangi bir gaz NK'da hep 22,4 L yer alır.
Formül özeti: Tanecik sayısı için n=N/Nₐ, kütle için n=m/Mₐ, NK'da hacim için n=V/22,4

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal tepkimeler maddelerin başka maddelere dönüştüğü olaylardır ve her zaman enerji değişimi vardır. Tepkimelerde toplam atom sayısı ve kütle korunur.
Sentez tepkimeleri: İki veya daha fazla madde birleşerek yeni bileşik oluşturur . Demir ile oksijenin birleşip demir oksit oluşturması gibi.
Ayrışma tepkimeleri: Bir bileşik parçalanarak daha basit maddelere dönüşür . Sentezin tersi işlemdir. KClO₃'ün ısıtıldığında KCl ve O₂'ye ayrışması gibi.
Denkleştirme: En çok atom içeren bileşiğin katsayısı 1 kabul edilir, diğerleri buna göre bulunur.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Yanma tepkimeleri: Maddelerin oksijen ile tepkimesidir. Yanma için oksijen, yanacak madde ve tutuşma sıcaklığı gerekir. Çoğu yanma tepkimesi ısı verir (ekzotermik).
Asit-baz tepkimeleri: Asitten gelen H⁺ iyonu ile bazdan gelen OH⁻ iyonu tepkime verir. Genel denklem: Asit + Baz → Tuz + Su şeklindedir.
Çözünme-çökelme tepkimeleri: İki tuz çözeltisi karıştırıldığında çözünmeyen yeni bir tuz oluşabilir. AgNO₃ ile NaCl karıştırılınca beyaz AgCl çökeltisi oluşması gibi. Net iyon denkleminde sadece çöken iyonlar yazılır.
Yanma şartları: Oksijen + Yanacak madde + Tutuşma sıcaklığı = Yanma tepkimesi

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kimyasal tepkimelerde bir maddenin miktarı verildiğinde, denklem katsayılarını kullanarak diğer maddelerin miktarını bulabiliriz.
İşlem sırası şöyle: Verilen miktarı mol sayısına çevir → Denklem katsayıları ile orantı kur → İstenen maddenin mol sayısını bul → İstenen birime çevir.
N₂ + 3H₂ → 2NH₃ tepkimesinde 56g N₂ verilirse: 56g ÷ 28g/mol = 2 mol N₂. Denklemden 1 mol N₂'den 2 mol NH₃ oluşur, o halde 2 mol N₂'den 4 mol NH₃ oluşur. 4 mol × 17g/mol = 68g NH₃.
Önemli: Önce mol sayısına çevir, sonra denklem katsayıları ile orantı kur!

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Birden fazla madde miktarı verildiğinde sınırlayıcı bileşen kavramı devreye girer. Biri tükenir, diğeri artar.
Çözüm yöntemi: Verilen miktarları mol sayısına çevir → Mol sayılarını denklem katsayılarına böl → Küçük oranı seç → Bu oranla çarparak harcanan ve oluşan miktarları bul.
6 mol N₂ ve 6 mol H₂ örneğinde: N₂ için 6÷1 = 6, H₂ için 6÷3 = 2. Küçük oran 2'dir. 2 katla çarpınca: 2 mol N₂ harcanır (4 mol artar), 6 mol H₂ tükenir, 4 mol NH₃ oluşur. H₂ sınırlayıcıdır.
Sınırlayıcı bileşen: Oranı en küçük olan madde tükenir ve tepkimeyi sınırlar.

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl

Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Yapay zeka arkadaşımız öğrencilerin ihtiyaçlarına göre özel olarak tasarlanmıştır. Platformda bulunan milyonlarca içeriğe dayanarak öğrencilere gerçekten anlamlı ve ilgili yanıtlar verebiliyoruz. Ancak mesele sadece cevaplar değil, refakatçi aynı zamanda kişiselleştirilmiş öğrenme planları, sınavlar veya sohbet içerikleri ve öğrencilerin becerilerine ve gelişimlerine dayalı %100 kişiselleştirme ile öğrencilere günlük öğrenme zorluklarında rehberlik ediyor.
Uygulamayı Google Play Store ve Apple App Store'dan indirebilirsiniz.
Knowunity uygulaması ücretsiz! Uygulamamız çok yakında indirmeye hazır olacak, bekle bizi. 💙
40
Akıllı Araçlar YENİ
Bu notu şunlara dönüştür: ✓ 50+ Alıştırma Sorusu ✓ Etkileşimli Flash Kartları ✓ Tam Deneme Sınavı ✓ Kompozisyon Taslakları
App Store
Google Play
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı
Uygulama çok kolay kullanılıyor ve güzel tasarlanmış. Şu ana kadar aradığım her şeyi buldum ve sunumlardan çok şey öğrendim! Kesinlikle ödevlerim için hep kullanacağım!
A.S.
iOS kullanıcısı
Uygulama çok iyi. Çok fazla ders notu ve yardımlaşma var. Örneğin benim problem yaşadığım bir ders Geometriydi ve ANINDA yardım ettiler beraber hem sorularımı çözdük hem konu anlatımı buldum. Herkese tavsiye ederim.
S.L.
Android kullanıcısı
BEN ŞOK. Reklamını sık sık gördüğüm için uygulamayı denedim ve gerçekten hayran kaldım. Bu uygulama okul için tam ihtiyacım olan şey. Anında ödev yardımı, konu anlatımı, örnek sınavlar, flaşkartlar hepsi hepsi var, şiddetle tavsiye ederim ✅
A.
iOS kullanıcısı
Knowunity'yi keşfedinceye kadar ödevlerimi zamanında tamamlamakta zorlanıyordum, Knowunity sadece kendi ders notlarımı yüklemeyi kolaylaştırmakla kalmıyor, aynı zamanda çalışmamı daha hızlı ve verimli hale getiren harika özetler de sunuyor.
Thomas R
iOS kullanıcısı
Ödevlerim için önemli bilgilerin tümünü bulmak her zaman bir zorluktu - Knowunity'yi kullanmaya başladığımdan beri, ders notlarımı kolayca yükleyebilir ve başkalarının özetlerinden faydalanabilirim, bu da organizasyon konusunda bana çok yardımcı oluyor.
Lisa M
Android kullanıcısı
Ders çalışırken genellikle yeterince genel bakışa sahip olmadığımı hissederdim, ama Knowunity'yi kullanmaya başladığımdan beri bu artık sorun değil - ders notlarımı yüklüyorum ve platformda her zaman yardımcı özetler buluyorum, bu da öğrenmemi çok daha kolaylaştırıyor.
David K
iOS kullanıcısı
Uygulama acayip iyi! Konuyu yazıyorum hemen yanıt alıyorum. Bi şeyi anlamak için 10 tane youtube videosu izlemem gerekmiyor. Kesssinlikle tavsiye ederim!
Sudenaz Ocak
Android kullanıcısı
Matematikte baya kötüydüm ama bu uygulama sayesinde şimdi daha iyiyim. Uygulamayı yapanlara için çok teşekkürler!
G.B.
Android kullanıcısı
Sunumlarım için tüm bilgileri toplamak gerçekten zordu. Ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyorum ve başkalarından harika özetler buluyorum - bu da çalışmamı çok daha verimli hale getiriyor!
Julia S
Android kullanıcısı
Tüm çalışma materyalleriyle sürekli stres altındaydım, ama Knowunity'yi kullanmaya başladığımdan beri, notlarımı yüklüyor ve başkalarının harika özetlerine bakıyorum - her şeyi daha iyi yönetmemi sağlıyor ve çok daha az stresli.
Marco B
iOS kullanıcısı
QUİZLER VE FLASHCARDLAR ÇOK FAYDALI VE Knowunity AI'I ÇOK SEVİYORUM. AYRICA TAM OLARAK CHATGPT GİBİ AMA DAHA AKILLI!! RİMEL SORUNLARIMDA DA YARDIM ETTİ!! GERÇEK DERSLERİMDE DE TABII Kİ! DUHHH 😍😁😲🤑💗✨🎀😮
Sarah L
Android kullanıcısı
Eskiden okul materyallerini Google'da aramakla saatler harcardım, ama şimdi sadece notlarımı Knowunity'ye yüklüyorum ve başkalarının faydalı özetlerine bakıyorum - sınavlara hazırlanırken kendimi çok daha güvende hissediyorum.
Paul T
iOS kullanıcısı