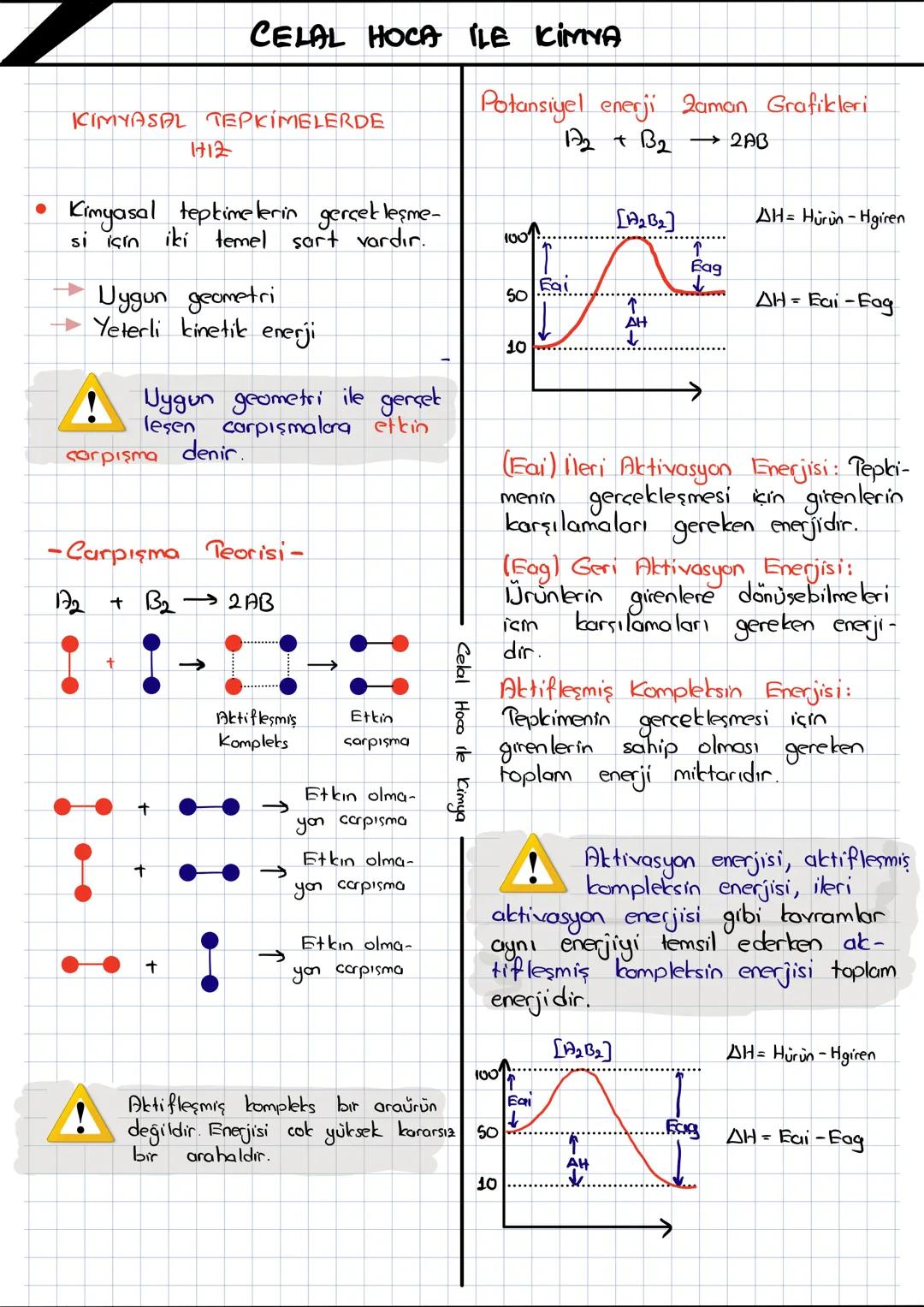
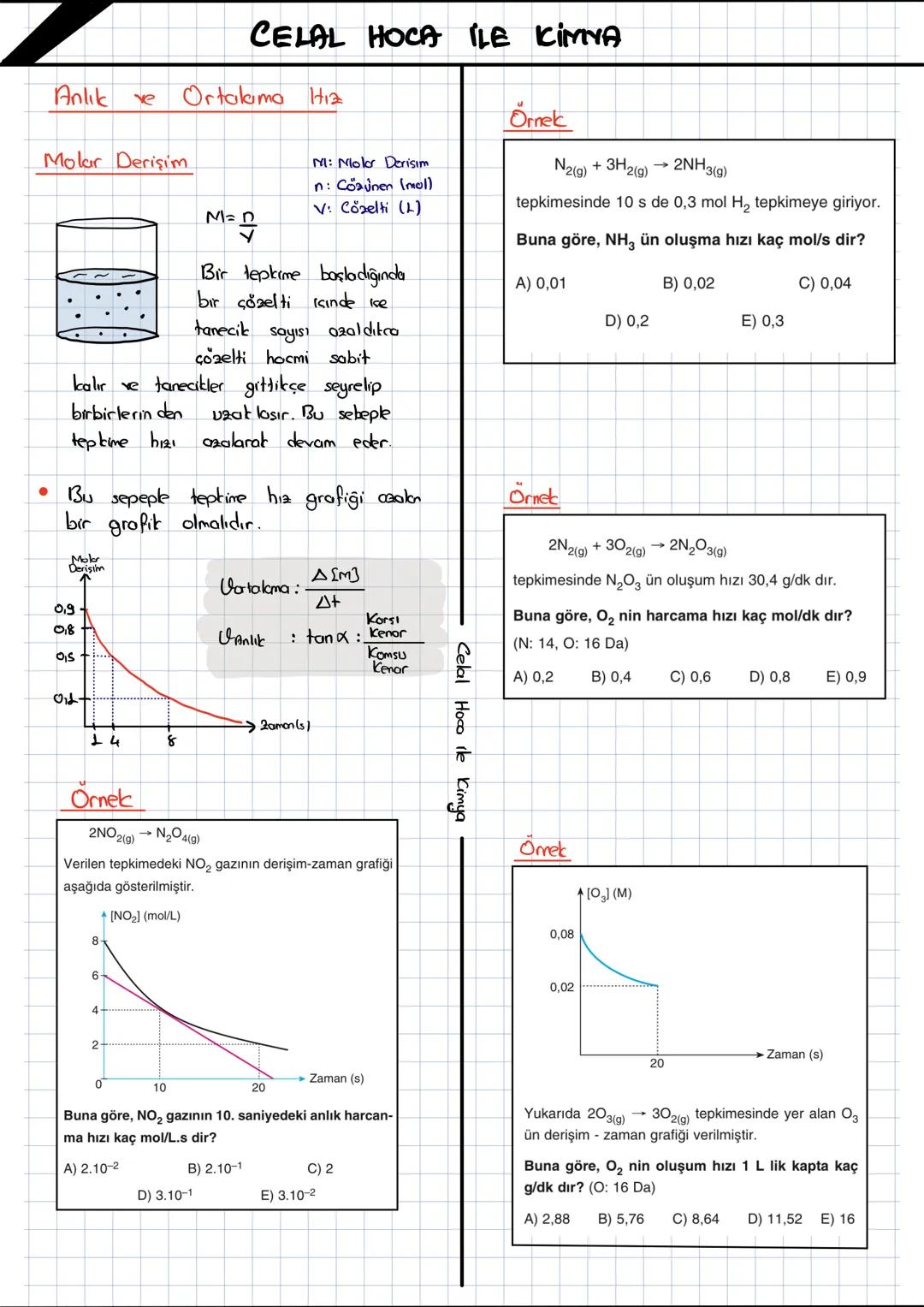
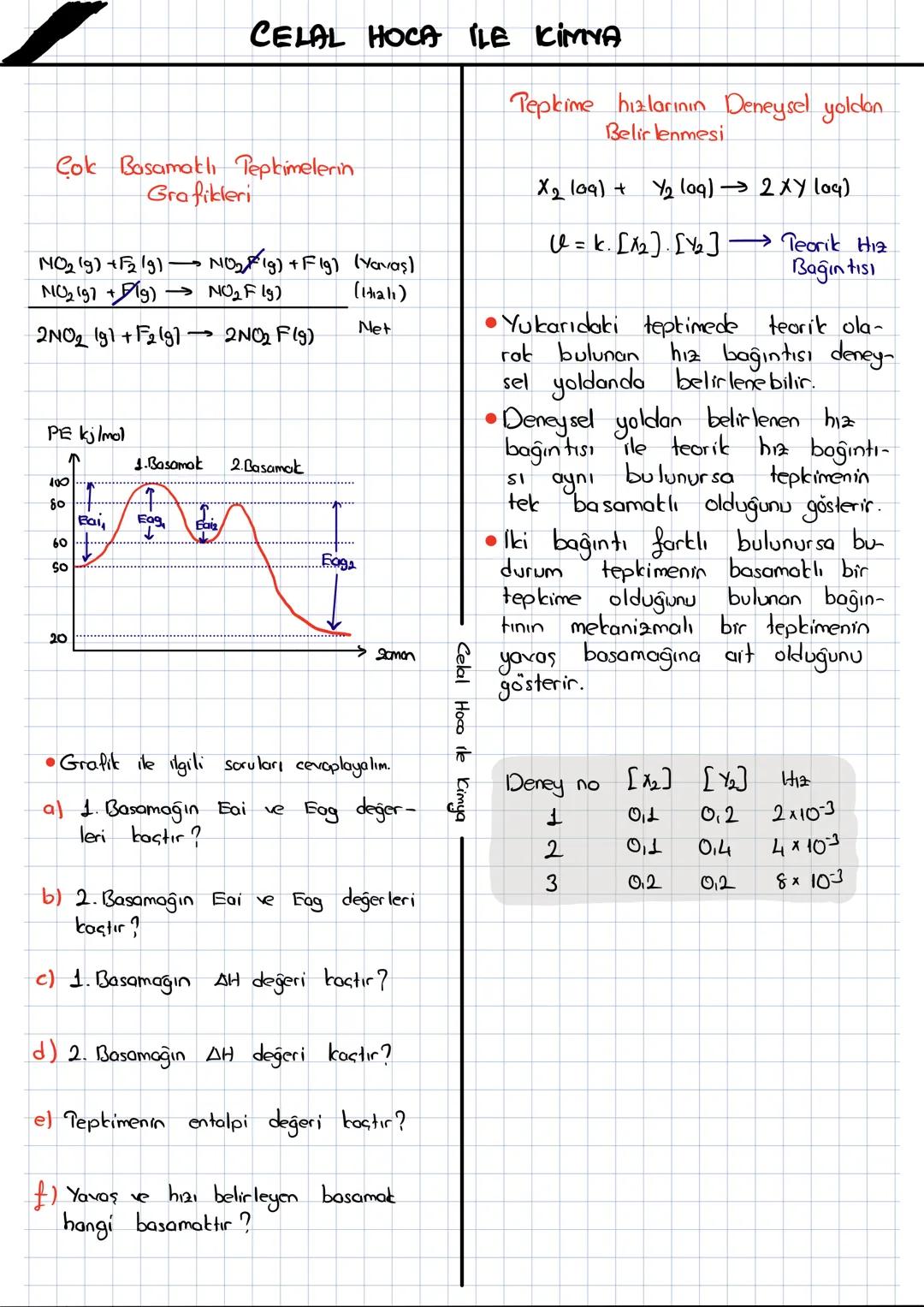
Kimyasal tepkimelerin nasıl gerçekleştiğini ve hızlarını etkileyen faktörleri anlamak, kimyanın temellerini kavramak için kritik öneme sahip. Bu konuda... Daha fazla göster
Ders notlarını görmek için kaydolÜcretsiz!
Tüm belgeleri görebilirsin
Notlarını Yükselt
Milyonlarca öğrenciye katıl
Kaydolduğunda Hizmet Şartları ve Gizlilik Politikasını kabul etmiş olursun